油田土壤石油烴類污染物氧化降解性能研究
董健 代紅波 寇恒治
1中石化石油工程設計有限公司
2中國石油大學(華東)化工學院
3中石油新疆油田公司陸梁油田作業區
土壤修復技術的研究起源于20 世紀70 年代后期。19 世紀90 年代中期,國外就開始了有機污染土壤的化學氧化修復研究,而直至20 世紀90 年代中期,石油污染土壤的化學氧化修復技術才得以現場應用[1]。目前,許多國家都在大力開展土壤修復技術的研究,土壤修復技術得到迅速發展,積累了豐富的技術和經驗。我國土壤修復技術起步較晚,在“十五”期間才列入高技術研究規劃發展計劃[2]。近年來,隨著我國土壤修復技術研究的開展,土壤修復學已經成為一門新興的環境分支學科,即將發展成為一門新興的土壤分支學科。目前,化學氧化法在國內已經應用于一些石油化工類污染土壤的修復,但與國外仍有很大的差距。例如,過硫酸鈉氧化降解油土在國外應用廣泛,而我國還處于實驗室研究階段[3]。當前的研究顯示,土壤修復技術將更趨向于多種技術聯合使用[4]。利用化學氧化對油土進行預處理,使難降解的有機污染物轉化為易被生物降解的組分,再聯合生物法進行土壤修復,可以達到高效低耗的土壤修復效果。為解決油田石油烴污染土壤的問題,本文考察了兩種化學氧化方法對石油污染土壤的修復效果。在30 ℃環境下模擬油田土壤原位修復,選出去除率高、操作簡便、修復效果較好的氧化劑及氧化方案,為油田污染土壤的修復處理提供理論支撐。
1 實驗
1.1 儀器與試劑
油浴鍋(HH-S 數顯),金壇市醫療儀器廠;真空干燥箱(ZK-82B),上海市試驗儀器廠;電子天平(BS22-S),北京賽多利斯儀器系統有限公司。
過氧化氫(H2O2)、硫酸亞鐵(FeSO4·7H2O)、過硫酸鈉(Na2S2O8)、二氯甲烷(CH2Cl2)。油土中油品性質見表1。

表1 模擬石油污染土壤中油品成分Tab.1 Oil properties in simulate oil-contaminated soil質量分數/%
1.2 實驗方法
選取芬頓體系、過硫酸鈉+亞鐵離子體系對模擬石油污染土壤進行氧化處理研究。參考已知文獻,確定適合烴類污染物氧化的氧化劑及使用條件[5]并測試評價各氧化劑氧化降解效果。通過實驗,探究不同因素對氧化效果的影響(包括初始烴含量、氧化劑投加量、添加順序、土壤介質pH 值等),確定最佳反應條件。
1.2.1 土壤中石油烴含量的測定
利用索式抽提裝置,對經烘干處理后的含油土壤進行油品與土壤分離處理,將土壤中石油烴組分提取出來。取一定量油土m1,以二氯甲烷為萃取劑,在索式抽提器內抽提至無色,蒸出溶劑二氯甲烷,并在105 ℃左右烘干,冷卻后稱重m2,則:石油烴含量=。
1.2.2 石油烴去除率的計算
計算出氧化前后的土壤中石油烴的含量,由公式(1)得到反應去除率,評價氧化降解效果。

2 結果與討論
2.1 芬頓氧化體系的影響因素
2.1.1 初始烴含量
分別配制初始烴含量為0.04、0.055、0.07、0.085(質量分數)的模擬石油污染土壤各25 g,分別加入pH 值為3、濃度為2 mol/L的硫酸亞鐵溶液6.12 mL,飽和浸漬后烘干。烘干后各加入7.344 mL 濃度10 mol/L 的H2O2并攪拌均勻,在35 ℃下反應2 h,計算石油烴去除率。考察初始烴的含量與去除率的關系,實驗結果見圖1。
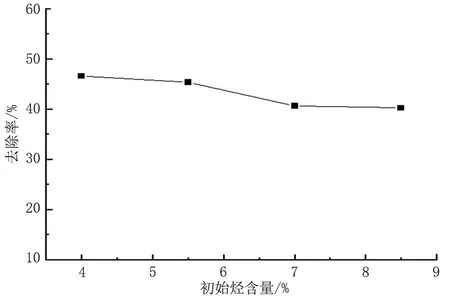
圖1 芬頓氧化體系中初始烴含量與去除率的關系Fig.1 Relationship between initial hydrocarbon content and the removal rate in Fenton oxidation system
由圖1可以看出,在相同反應條件下,芬頓體系中去除率隨土壤中初始烴含量的增加而降低,初始烴含量為0.04時石油烴去除率最高,為46.57%。文獻[6]中發現在低污染水平時需要大量的氧化劑,而本實驗結果與之有一定的差別,原因可能是因為實驗室配制的油土混合物中沒有強烈的土壤基體-油的相互作用,即石油污染物與土壤之間的結合不緊密,從而導致含油量越少去除率越高。
2.1.2 H2O2/Fe2+物質的量比例
配制初始烴含量0.04的模擬油土125 g,將其分成5份,分別加入濃度為2、1.5、1.2、1、0.857 mol/L,pH值為3的6.12 mL硫酸亞鐵溶液并混合均勻,烘干各加入7.344 mL 的H2O2溶液。在反應溫度為35 ℃,反應時間為2 h條件下,考察H2O2與Fe2+的質量之比與去除率的關系,實驗結果見圖2。
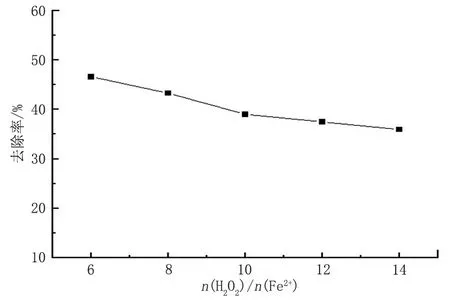
圖2 芬頓氧化體系中n(H2O2)/n(Fe2+)與去除率的關系Fig.2 Relationship between n(H2O2)/n(Fe2+)and the removal rate in Fenton oxidation system
由圖2 可知:在固定H2O2為7.344 mL、初始烴含量為0.04、體系pH 值為3、反應時間2 h 的情況下,在n(H2O2)/n(Fe2+)=6時石油烴去除效果最好,為46.57%,隨著n(H2O2)/n(Fe2+)的增加,亞鐵離子減少,去除率呈降低趨勢,這是因為Fe2+濃度過低,活化劑的量不足,沒有足夠的羥基自由基參與反應,導致去除率降低[7]。
2.1.3 反應時間
配制25 g 初始烴含量為0.04 的模擬油土并烘干,加入濃度為1.5 mol/L,pH值為3的硫酸亞鐵溶液6.12 mL,飽和浸漬,烘干。加入7.344 mL 的H2O2溶液攪拌均勻后,在35 ℃下反應,間隔1 h取樣一次測去除率,考察反應時間與去除率的關系,實驗結果見圖3。
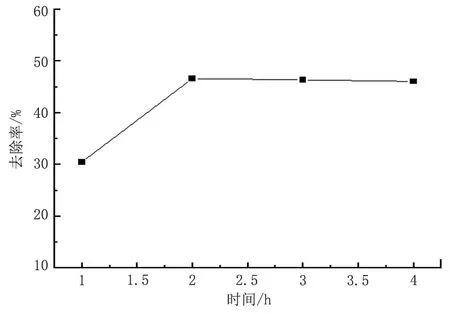
圖3 芬頓氧化體系中反應時間與去除率關系Fig.3 Relationship between reaction time and the removal rate in Fenton oxidation system
由圖3可知:隨著反應時間的延長,去除率在2 h時達到最大,后趨于平緩,最佳反應時間為2 h。反應初期,Fe2+活化H2O2生成的羥基自由基增多,加速有機污染物的氧化降解;隨著時間的推移,H2O2被消耗,羥基自由基減少,反應緩慢,直至H2O2被消耗完全,去除率不再增大。
2.2 過硫酸鈉氧化體系的影響因素
2.2.1 添加量及添加順序
在該體系中,考察了體系中氧化劑(Na2S2O8)和催化劑(Fe2+)的添加順序對烴類污染物去除率的影響[8]。
(1)先加入過硫酸鈉。先將24.48 mL的濃度為1 mol/L 過硫酸鈉與100 g 的模擬油土混合均勻,分成四等份,調節Fe2+與Na2S2O8物質的量之比,考察去除率與n(Fe2+)/n(Na2S2O8)加入量的關系,結果如圖4所示。
由圖4 數據可知:在過硫酸鈉足量的情況下,n(Fe2+)/n(Na2S2O8)=0.25時效果最好,且隨著Fe2+量的增加,去除率呈現減小的趨勢,這是由于Fe2+具有還原性,對硫酸根自由基產生了競爭,發生了如下副反應[8]:
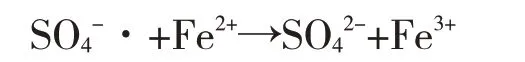
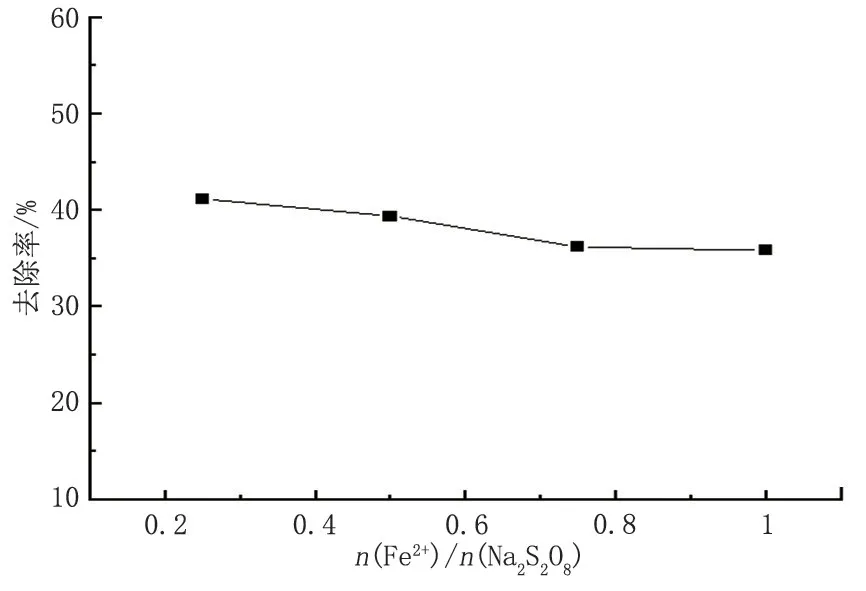
圖4 過硫酸鈉氧化體系中n(Fe2+)添加量與去除率關系Fig.4 Relationship between n(Fe2+)addition and the removal rate in sodium persulfate oxidation system
這使得參與氧化反應的硫酸根自由基數量減少,有機物分子的氧化降解受到抑制,導致去除率降低。
(2)先加入亞鐵離子。先將24.48 mL的硫酸亞鐵與100 g 的模擬油土混合均勻,分成4 等份,調節過硫酸鈉與Fe2+物質的量之比,考察去除率與n(Fe2+)/n(Na2S2O8)加入量的關系,結果如圖5所示。
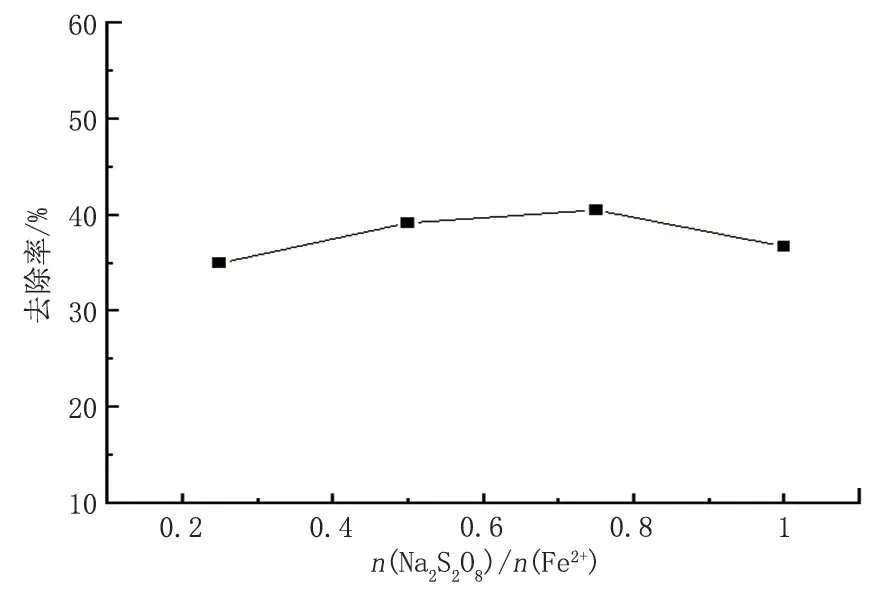
圖5 過硫酸鈉氧化體系中n(Na2S2O8)/n(Fe2+)添加量與去除率關系Fig.5 Relationship between the addition amount of n(Na2S2O8)/n(Fe2+)and the removal rate in sodium persulfate oxidation system
由圖5可知:在Fe2+足量的情況下,n(Na2S2O8)/n(Fe2+)=0.75時石油烴去除效果最好,石油烴去除率隨Na2S2O8量的增加先增大后減小,原因是反應初期Na2S2O8不足,硫酸根自由基的產生受到限制,去除率較低;隨著Na2S2O8的增加,硫酸根自由基的量隨之增加,從而促進氧化反應的進行,去除率增大[9];Na2S2O8濃度過高時,則會將Fe2+氧化為Fe3+,從而消耗掉Na2S2O8而導致硫酸根自由基量不足,進而使去除率下降[10]。
催化劑和氧化劑不同添加順序的兩個實驗方案結果均表明,Fe2+與Na2S2O8均適量時,會促進有機污染物的氧化降解,過量則反而會降低去除率。在過硫酸鈉氧化體系中,最佳反應條件為先加Fe2+且n(Na2S2O8)/n(Fe2+)比例為0.75,此條件下石油烴去除率為40.48%。
2.2.2 pH值
在上述方案的基礎上,選擇最佳條件,(先加入Fe2+且n(Na2S2O8)/n(Fe2+)比例為0.75),考察pH 值對去除率的影響,不同pH 值用硫酸來調節,結果如圖6所示。
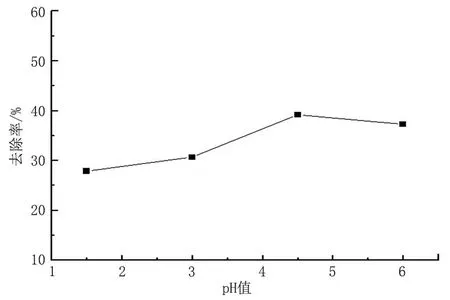
圖6 過硫酸鈉氧化體系中pH值與除率的關系Fig.6 Relationship between pH valve and the removal rate in sodium persulfate oxidation system
由圖6 可以看出,隨著體系pH 值的增大,去除率先增加后略微降低,在pH 值為4.5 處達到最大,之后隨pH 值的增加略有降低,但仍比強酸條件時去除率高。這說明強酸性環境并不利于過硫酸鈉體系對有機污染物的氧化降解,在pH 值為4-5左右時,可以最大程度地發揮氧化劑的氧化作用。
2.2.3 反應時間
在上述方案的基礎上,選擇最優體系(先加Fe2+,n(Na2S2O8)/n(Fe2+)=0.75,pH 為4.5)在35 ℃下反應,間隔1 h 取樣一次測去除率,考察時間對石油烴去除率的影響,結果如圖7所示。
由圖7 的數據可以看出,隨著反應時間的延長,去除率在0.5~1 h 左右時快速增大,之后雖有所增大但很緩慢。反應初期,Fe2+活化Na2S2O8生成的硫酸根自由基增多,加速了有機污染物的氧化降解[11]。隨著時間的推移,Na2S2O8被消耗,硫酸根自由基減少,反應緩慢。相比于芬頓反應,適當延長時間能有效提高過硫酸鈉氧化體系的去除率,這是由于硫酸根自由基的半衰期較長(4 s,40 ℃),能更充分地氧化降解有機污染物分子。
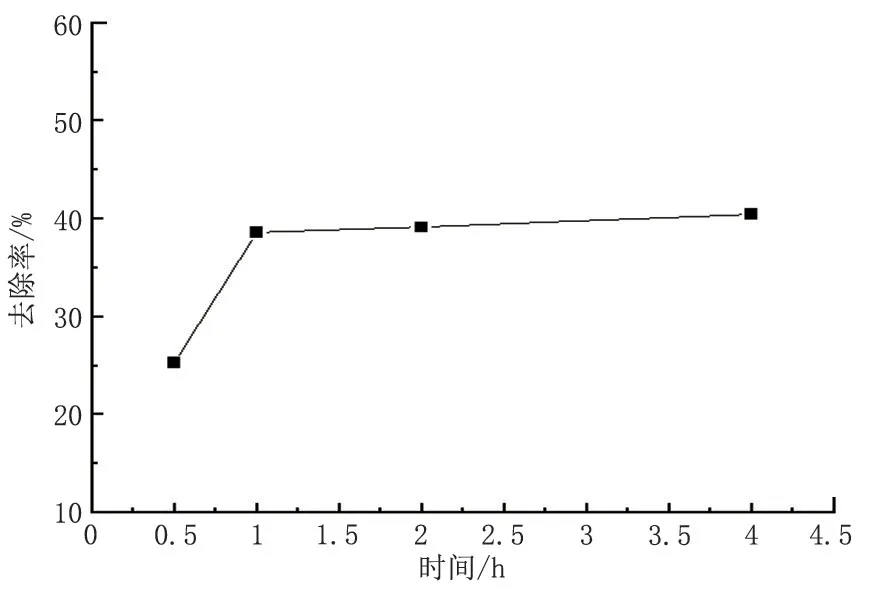
圖7 過硫酸鈉氧化體系中反應時間對去除率的影響Fig.7 Effect of the reaction time on the removal rate in sodium persulfate oxidation system
2.3 兩種氧化體系效果對比
研究結果表明,芬頓氧化體系的最佳條件為pH=3、n(H2O2)/n(Fe2+)=6、H2O2投加量為29.3 mL/100 g,此時石油烴去除率為46%;過硫酸鈉氧化體系的最佳條件為pH=4.5、n(Na2S2O8)/n(Fe2+)=0.75、Na2S2O8投加量為18.36 mL/100 g,此時石油烴去除率為40.48%。芬頓氧化體系的石油烴去除率大于過硫酸鈉氧化體系,處理方法更加成熟,應優先選用芬頓氧化體系。
3 結論
研究了芬頓體系和過硫酸鈉兩種氧化劑體系對模擬油土氧化降解情況,考察了不同的實驗條件下(包括pH值、氧化劑添加量、添加順序、添加方式等)對模擬油土中污染物去除率的影響,得到以下結論:
(1)土壤中含油量越大,氧化降解效果越差。
(2)在兩種氧化體系中,芬頓氧化降解的效果要優于過硫酸鈉氧化體系。
(3)在pH=3、n(H2O2)/n(Fe2+)=6 的條件下,芬頓氧化對石油污染土壤中石油烴去除率最高可達46%。在pH=4.5、n(H2O2)/n(Fe2+)=0.75 的條件下,過硫酸鈉氧化體系對石油烴去除率可達40.48%。

