常見精神疾病的大、小鼠遺傳模型研究進展
羅卓慧龐 碩張連峰
(1.中國醫學科學院醫學實驗動物研究所,北京協和醫學院比較醫學中心,國家衛生健康委員會人類疾病比較醫學重點實驗室,北京 100021;2.中國醫學科學院神經科學中心,北京 100730)
精神疾病是指在各種生物學、心理學以及社會環境因素影響下,由大腦功能失調導致認知、情感、意志和行為等精神活動出現不同程度障礙為臨床表現的疾病[1],包括抑郁癥、雙相情感障礙、精神分裂癥、其它精神病、癡呆癥、智力殘疾和自閉癥在內的發育障礙[2]。我國的各種精神疾病中,焦慮癥(7.6%)和情緒障礙(7.4%)發病率最高[3]。
目前有超過50%的神經科學實驗使用嚙齒類動物模型,作為嚙齒類動物的代表,大鼠易于構建模型并且不易受外界環境的干擾,小鼠的基因修飾模型資源豐富,在遺傳學等方面具有使用優勢[4]。隨著大鼠基因編輯的開展,大鼠基因修飾模型資源日漸豐富,或將成為研究情感行為和精神類疾病的首要模型[5]。常見的大鼠和小鼠精神疾病模型主要包括誘導模型和遺傳模型兩類,誘導模型與自然產生的疾病相比存在差異,誘導難度高;而遺傳模型有助于了解基因相關的病理生理學信息[6]。現總結常見精神疾病的大、小鼠遺傳模型及適用的行為學評估方法,見表1。
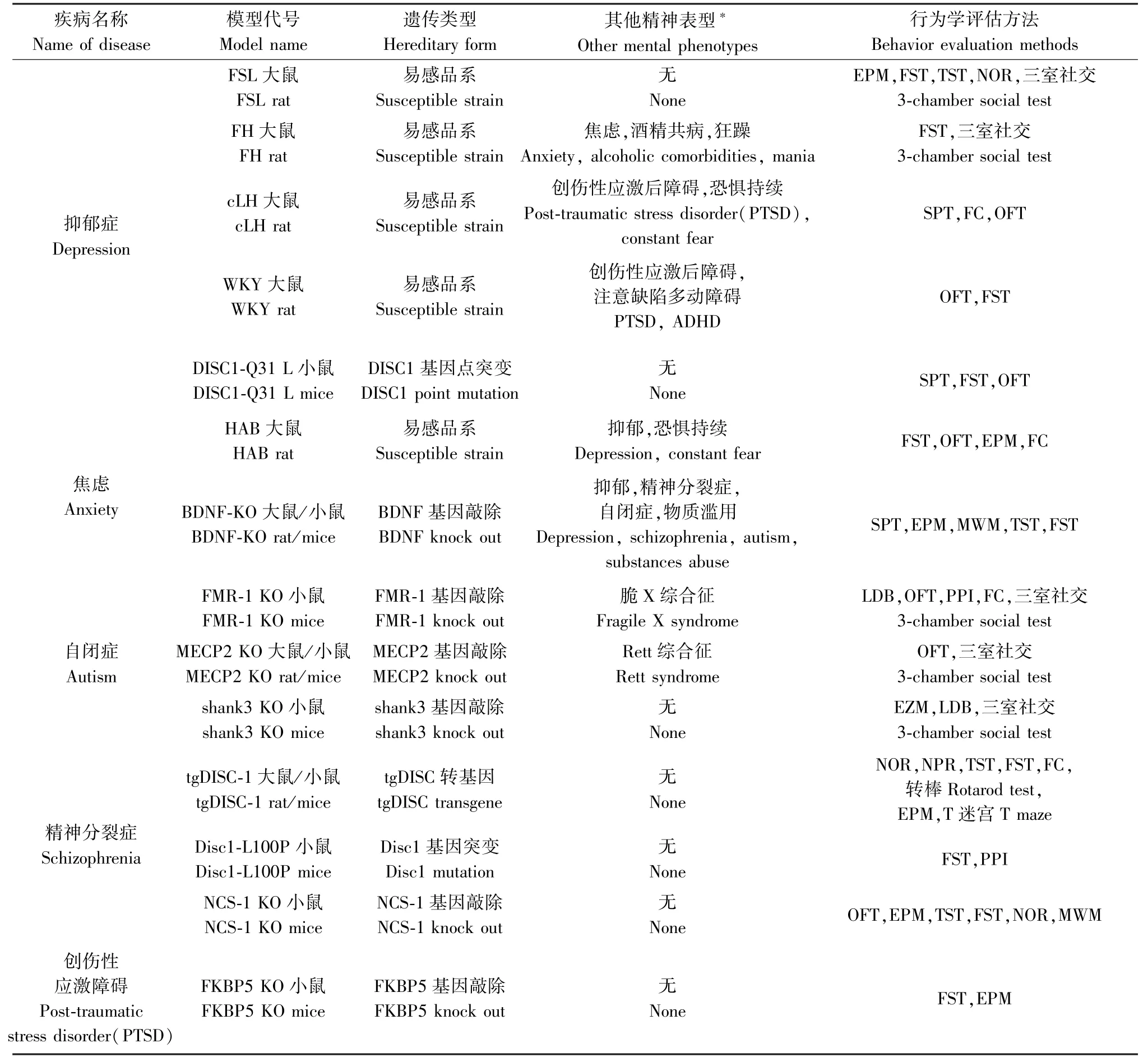
表1 常見精神疾病的大、小鼠遺傳模型及行為學評估方法Table 1 Rat and mice models of common mental disorders
1 抑郁模型
常見的抑郁癥遺傳模型包括4種選擇性繁育大鼠和1種基因突變小鼠。常見的抑郁癥行為學評估方法分為兩類,以行為絕望為代表的評估方法包括FST、TST和LH以及以快感缺乏為代表的評估方法SPT[6]。FSL大鼠、FH大鼠和WKY大鼠適合評估行為絕望,而cLH大鼠適合評估快感缺乏,DISC1-Q31 L小鼠兩類評估方法均適用。
1.1 FSL大鼠系(Flinders Sensitive rat Line)
FSL大鼠是Sprague-Dawley(SD)背景的選擇性繁育大鼠,原作為一種對抗膽堿酯酶反應增強的動物模型[6],表現出與抑郁患者的相似的快動眼睡眠增加[7]及嗅覺受損[8]。FSL大鼠的行為學表型包括在FST中靜止時間增加,活動性減少;在SPT實驗中FSL快感缺乏的表型不明顯,不適合用SPT進行評估[7],三室社交實驗中FSL不愿意與不熟悉動物社交,可作為重度抑郁(MDD)疾病模型[8]。在月齡方面2~3月齡的FSL在EPM和FST中抑郁癥狀不穩定,6~7月齡后在NOR和FST中分別體現的認知缺陷及抑郁癥狀不明顯,評估時應選擇合適的月齡[9]。除抑郁外,FSL大鼠還表現出明顯的認知缺陷及活動障礙,生理結構上表現為海馬皮質5-羥基吲哚乙酸和去甲腎上腺素紊亂,海馬區脂質過氧化增加[10]。
FSL現常作為自發抑郁癥模型,由于FSL的抑郁表型可由藥物治療逆轉,適用于長期和急性抗抑郁藥物治療效果評價[10-11],對五羥色胺選擇性再攝取抑制劑類和去甲腎上腺素轉運抑制劑三環類抗抑郁藥評估中效果較好[12]。
1.2 FH大鼠(Fawn Hooded rat)
FH大鼠原為選擇性繁育的高血壓大鼠[7],表現出與精神病患者相似的酒精攝入增加[13]。FH大鼠的行為學表型包括在FST中靜止時間明顯增加[13],在三室社交實驗中總社交時間和攻擊行為均減少[14]。在生理結構上FH大鼠的五羥色胺系統異常[15]。不同背景的的FH大鼠表型存在差異,其中ACI/N品系酒精偏好不明顯[13],FH/HamSlc品系具有特異性的狂躁行為,表現為刺激依賴的高活動性抑制和單胺功能失調,具有雙向情感障礙造模潛力[15]。
FH大鼠是常用的抑郁和焦慮模型,研究發現LH大鼠的焦慮和酗酒在一定聯系,可作為抗酗酒藥物篩選及抑郁-酒精共病模型[13],或將成為社交恐懼癥及其他社交行為受損的焦慮模型[14]
1.3 cLH大鼠(congenitally learned helpless rat)
cLH大鼠是選擇性繁育的先天習得性無助大鼠[16],雌性cLH大鼠表現出明顯的酒精剝奪效應及先天類抑郁[17]。cLH大鼠的行為學表型包括在MWM中空間記憶正常,在SPT中快感缺乏表型明顯,適合評估抑郁癥的快感缺乏癥狀[18],在OFT中新環境的探索增加[19],在獎賞實驗中對獎賞偏好反應的切換速度減慢[20],在FC中僵直時間增加,與PTSD患者癥狀相似,cLH大鼠更傾向于形成及維持恐懼相關記憶[19]。cLH的先天性習得性無助行為能夠通過增加環境豐富度在14周時得到改善,28周徹底逆轉[21]。在生理結構上cLH大鼠mGlu5表達升高[22]。cLH大鼠常作為長期抑郁模型[22],或將成為PTSD疾病模型。
1.4 WKY大鼠系(Wistar-Kyoto rat Line)
WKY大鼠原為選擇性繁育的自發性高血壓大鼠,同時出現焦慮和抑郁表型。類似抑郁患者,WKY大鼠的快動眼睡眠增加[6-7]。WKY的行為學表型包括在OFT中心區停留時間減少,FST中靜止時間增加[23]。此外,WKY出現精神運動遲緩,習得性無助,精神抑制,社交互動減少等表型[24]。在生理結構上WKY的海馬神經元先天受損,腦內糖酵解強度降低,線粒體功能損傷,甲狀腺功能減退[25]。
WKY是最常見的抑郁模型,可用作難治性抑郁模型,重度抑郁模型,產后抑郁模型和兒童抑郁癥動物模型[6]。研究發現WKY對危險和安全信號的處理與野生大鼠不同,將WKY作為PTSD模型[26],還有研究將WKY作為注意力缺陷多動癥障礙(ADHD)模型[27]。
1.5 DISC1-Q31 L小鼠
DISC-1基因與情緒障礙和精神分裂癥密切相關[28]。現有的DISC-1基因相關動物模型包括過表達DISC-1的轉基因大鼠和轉基因小鼠,Disc1-L100P小鼠和DISC1-Q31 L小鼠,其中DISC1-Q31 L小鼠是C57/BL6背景,DISC-1基因外顯子2區發生127A/T顛換[29]。DISC1-Q31 L小鼠的行為學表型包括在SPT快感缺乏明顯,FST中靜止時間長,OFT中水平活動性增加[29]。生理結構上DISC1-Q31 L小鼠伏隔核多巴胺,血清素和去甲腎上腺素的含量降低[30],腦容量減少6%[29]。
DISC1-Q31 L小鼠是常見的抑郁模型,常用于抗抑郁藥物篩選,評估藥物對社交障礙及快感缺乏癥狀的改善作用[30]。
2 焦慮模型
常見的焦慮行為學評估方法包括OFT、EPM和LDB[6]。常見的遺傳性焦慮模型因具有明顯的抑郁表型,常作為抑郁模型或焦慮-抑郁共病模型。
2.1 HAB大鼠(high anxiety behaviour rat Line)
HAB是Wistar背景的先天焦慮及抑郁大鼠,表現出與抑郁患者相似的晝夜節律紊亂[6]。HAB的行為學表型包括在FST中靜止時間增加,OFT中心區探索減少[31],EPM中開放臂中停留時間和穿梭次數增加,低頭行為的持續時間和次數明顯增加,焦慮程度高[32],在FC中恐懼階段的心率和恐懼反應增加,僵直時間仍高于對照組,表現為恐懼消退缺陷[33]。哺乳期的HAB拱背護理和幼崽回收行為的次數增加,母性攻擊增強[34]。生理結構上HAB的多個腦區鞘脂代謝相關酶的活性增加[35]。
HAB常用于構建焦慮,抑郁及焦慮-抑郁共病模型,常用于機制,治療措施和藥物篩選[33]。
2.2 BDNF+/-大鼠/小鼠(BDNF敲除大鼠/小鼠)
BDNF+/-大鼠為SD背景[36]。BDNF+/-大鼠和小鼠均表現出乙醇濫用表型。和重度抑郁患者相似,BDNF+/-大鼠和小鼠快感缺乏[37]。BDNF+/-大鼠的行為學表型包括在SPT和EPM中表現出明顯的快感缺乏和焦慮,在MWM中空間記憶缺陷并不明顯和TST中分別表現出的和行為絕望現象并不明顯[37]。在生理結構上BDNF+/-大鼠的腦和血漿中BDNF含量減少,前額葉皮質中糖皮質激素受體,神經調節蛋白1和神經分裂癥干擾因子1上調[37]。
BDNF+/-大鼠和小鼠是常用的焦慮和抑郁模型[38],常用于精神分裂癥,自閉癥和物質濫用研究[39]。目前有利用BDNF-KO雜合小鼠研究青春期激素暴露對成年期的影響[40]。除精神疾病外,BDNF-KO雜合小鼠模型也被用于認知研究中[36]。關于BDNF+/-小鼠作為焦慮易感模型的穩定性現仍存在爭議,有研究發現BDNF+/-小鼠在OFT,FST,安逸敏感度等評估中行為學表型并不明顯[41]。
3 自閉癥模型
常見的自閉癥遺傳模型有3種,均適用于以三室社交為代表的行為學評估方法,同時具有焦慮和抑郁表型。
3.1 FMR-1+/-小鼠(FMR-1敲除小鼠)
FMR1是自閉癥最常見的單基因病因,FMR-1+/-小鼠是C57/BL6背景,雌性出現與患者類似的自閉樣行為和聽源性癲癇[42],腦成熟后睡眠異常[43]。FMR-1+/-小鼠的行為學表型包括在LDB中穿梭次數增加,被動回避受損[42],在OFT中活動性升高,外周區停留時間增加,焦慮程度高[44],在FC中條件性恐懼反應異常,PPI中脈沖前抑制缺陷[42],在三室社交實驗中社交障礙明顯。超聲波檢測發現FMR-1+/-小鼠的社交次數自青春期明顯減少,而社交新穎性回避,高活動性和情景恐懼等表型主要在成年期出現[45]。在生理結構上FMR-1+/-小鼠的杏仁核,聽覺皮層及海馬CA2區的神經元網絡密度降低[46]。
FMR-1+/-小鼠常作為脆X綜合征和自閉癥模型[42],常用于自閉癥機制研究和藥物篩選[47]。
3.2 MECP2+/-大鼠/小鼠(MECP2敲除大鼠/小鼠)
自閉癥患者MECP2基因啟動子異常甲基化,大腦內MECP2表達缺陷[48]。MECP2+/-小鼠是C57/BL6背景,大鼠是SD背景,由cre-loxP技術構建[49-50]。MECP2+/-小鼠的行為學表型包括在OFT中中央區停留時間減少,探索的方格數目減少,直立次數增加,靜止時間增加,焦慮程度高[49]。在三室社交實驗中社交障礙明顯[51],MECP2+/-小鼠和腦選擇性敲除的小鼠出生時正常,3~4周齡表現出輕微的步態異常[49],16周齡步態不協調,運動缺陷明顯[51]。MECP2+/-小鼠后肢抱合,偶發癲癇及震顫,呼吸不規律,學習和記憶障礙,牙齒磨損嚴重,下頜錯位[49]。半數MECP2+/-小鼠會在8~12周齡死亡[48]。雄性MECP2+/-小鼠個體的雄激素水平降低,雄性特征減少,行為學表型包括居住入侵測試中攻擊性降低,三室社交測試中社交行為增加[52]。MECP2+/-大鼠表現出與MECP2敲除小鼠類似的下頜錯位、生長遲緩、運動減少、呼吸無規律及社交缺陷等表型,前肢握力降低,藍斑神經元過度放電,未見后肢抱合,半數個體在2月齡死亡[50]。
MECP2+/-大鼠和小鼠常作為自閉癥和Rett綜合征模型,現有研究利用MECP2+/-大鼠和小鼠用于研究自閉癥患者體感功能障礙和觸覺障礙[51]及Rett綜合征與肥胖的關系[53]。
3.3 shank3 KO小鼠(shank3敲除小鼠)
目前使用較多的是shank3B-/-小鼠和shank3αβ KO小鼠。shank3B-/-小鼠的行為學表型包括在EZM開放臂停留時間減少,LDB中進入明室的潛伏期增加,三室社交實驗中社交新穎性減少,OFT中成對的shank3B-/-小鼠互嗅鼻子、肛門及生殖器的次數減少。shank3B-/-小鼠偶發癲癇,3~6月齡出現過度梳理和自殘行為,一般交配群體中35%的個體皮膚損傷,大體解剖和組織學無明顯異常,紋狀體功能障礙[54]。shank3αβ KO小鼠的腸道微生物群顯著改變,糞便中的細菌主要為厚壁菌與放線菌,生理結構上表現為小腸絨毛長度減少,肝中脂多糖含量升高,IL-6含量升高,星形膠質細胞激活[55]。目前shank3 KO小鼠常作為自閉癥模型用于機制研究[56]。
4 精神分裂癥模型
常見的3種精神分裂癥遺傳模型中,Disc1-L100P小鼠適合以PPI為代表的精神分裂癥行為學評估,tgDISC-1大鼠和小鼠及NCS-1 KO小鼠表現出一定程度的抑郁、焦慮和認知缺陷。
4.1 tgDISC-1大鼠/小鼠(DISC-1轉基因大鼠/小鼠)
tgDISC-1大鼠和小鼠是轉基因模型。tgDISC-1小鼠的載體由人類DISC-1基因片段,αCaMKII啟動子和pMM403構建,導入C57/BL6小鼠的卵母細胞中獲得[28]。tgDISC-1大鼠的行為學表型包括在NOR和NPR中表現出超探索行為及對新物體和新位置的明顯偏好,在轉棒實驗中旋轉缺陷明顯[57],在EPM中運動距離和開放臂停留時間均減少,焦慮程度升高,在T迷宮中自發交替次數減少,短期工作記憶損傷[58]。tgDISC-1小鼠的行為學表型包括在TST和FST中靜止時間增加,FC中恐懼抑制受損[59]。生理結構上tgDISC-1大鼠背側紋狀體突觸嚴重失調[60],tgDISC-1小鼠側腦室增大,大腦皮層減少,胼胝體發育不全,海馬和內側前額葉皮層的多巴胺能神經元減少,背外側額葉皮層移位,神經突變短變少[59]。tgDISC-1小鼠晝夜節律正常,僅清醒時間長于野生組[28]。目前tgDISC-1大鼠和小鼠常用作精神分裂癥模型。
4.2 Disc1-L100P小鼠(Disc1突變小鼠)
Disc1-L100P小鼠為C57/BL6背景,DISC1基因外顯子2區334 T/C顛換[29]。Disc1-L100P小鼠在FST中表現為可由抗抑郁藥物安非他酮逆轉的靜止時間增加[29],在PPI中表現出可由抗精神病藥物逆轉的脈沖前抑制和后抑制障礙[61。Disc1-L100P小鼠多動,聲驚跳反應減少等精神分裂表型在12周齡時出現[61]。在生理結構上,Disc1-L100P小鼠的腦容量減少13%[29]。
Disc1-L100P小鼠常作為精神分裂癥模型,常用于多巴胺相關精神分裂癥研究及藥物篩選,目前Disc1-L100P和DISC1-Q31 L在行為表型的穩定性存在爭議[62]。
4.3 NCS-1 KO小鼠(NCS-1敲除小鼠)
NCS-1基因與自閉癥,雙向情感障礙和精神分裂癥均相關,NCS-1 KO小鼠為C57/BL6背景,通過基因打靶技術獲得[63]。NCS-1+/-和NCS-1-/-小鼠的行為學表型包括在OFT中探索減少;NCS-1-/-在EPM開放臂停留時間減少,在Large-OFT中邊緣區停留時間明顯降低,在TST,FST中靜止時間增加,表現出明顯的焦慮和抑郁,在NOR中長期記憶受損[64],在MWM中表現空間學習記憶缺陷[63]。食物工作的意愿降低,在三室社交,社會交互和居住入侵實驗中社交活動減少[65]。在生理結構方面,NCS-1-/-小鼠腦內的BDNF和多巴胺含量下降[66],NCS-1-/-成年鼠體重增加,高脂食物喂養后易演化為2型糖尿病,可能提供精神疾病與肥胖的潛在聯系[63]。NCS-1-/-小鼠常作為精神分裂模型用于機制研究和藥物篩選。研究發現NCS-1通過直接或間接增加BDNF含量調節空間學習和記憶,多巴胺受體相關蛋白可以與與NCS-1相互作用,D2R/NCS-1互作模型或將成為抗精神病藥新靶標[67]。
5 PTSD模型
PTSD的結構和功能障礙與FKBP5密切相關[68]。FKBP5 KO小 鼠 是C57/BL6背 景[69]。FKBP5 KO小鼠目前研究較少,行為學表型包括在FST中的游泳時間增加,在EPM中開放臂停留時間減少,對新的急性刺激反應減弱,恢復增強[70],并表現出并非由味覺和酒精代謝差異引起的酒精消耗量增加[71]。在生理結構方面,FKBP5 KO小鼠的體重和腎上腺重量均減少,皮質酮水平下降。在同樣的壓力條件下,FKBP5 KO小鼠在生理結構上軸突發育相關基因的表達下降[72]。
FKBP5 KO小鼠可作為PTSD模型。FKBP5或將成為PTSD生理學研究潛在靶點[72]。
6 小結
本文主要分析了常見的14種常見的精神疾病大鼠和小鼠遺傳模型及適用的的行為學評估方法,其中FH大鼠、cLH大鼠、WKY大鼠、HAB大鼠、BDNF-KO大鼠/小鼠具有多種精神表型,適用于評估多種精神疾病。FMR-1 KO小鼠、MECP2 KO大鼠/小鼠作為有精神疾病表型的遺傳病模型,主要用于遺傳病研究,對特定精神狀態評估特異性不強。BDNF+/-小鼠、Disc1-L100P小鼠和DISC1-Q31 L小鼠行為學表型的穩定性存在爭議。研究者在實驗時需注意這些模型的特點和適用范圍,結合評估方法,根據實際需要做出選擇。未來的精神疾病動物模型或將體現出遺傳與環境的交互作用,向著可靠、特異的方向發展。

