銅綠假單胞菌對乳制品中沙門氏菌檢測的干擾作用評價
◎ 燕如娟,劉芳玉
(飛鶴(甘南)乳品有限公司,黑龍江 齊齊哈爾 162100)
沙門氏菌屬腸桿菌科,革蘭氏陰性腸道桿菌,無芽孢,無莢膜,周身鞭毛,在自然界中分布廣泛,是一種最為常見的食源性致病菌。在世界各國的細菌性食物中毒中,有沙門氏菌引起的食源性食物中毒往往高居首位[1-2],在我國有高達80%的食物中毒是由沙門氏菌所引起[3],國內外的很多食品安全相關標準中都有明確規定各類食品中均不得檢出沙門氏菌。因此,沙門氏菌的正確檢出對于保障居民飲食衛生安全具有極其重要的現實意義。
現行的沙門氏菌標準檢測方法為傳統培養法,主要包括前增菌、選擇性增菌、選擇性平板分離、生化實驗和血清學分離鑒定5大步驟[4]。然而食品中往往存在大量雜菌影響沙門氏菌在選擇性平板的分離與鑒定。近年來對于沙門氏菌分離與鑒定過程中干擾菌的研究多聚焦于弗氏檸檬酸桿菌和奇異變形桿菌[5],然而本實驗室在進行沙門氏菌檢出能力測試時發現銅綠假單胞桿菌對沙門氏菌的檢驗效果同樣可以產生極大干擾。在本實驗中,將銅綠假單胞菌作為干擾菌株,分別評價不同的前增菌時間下各品牌增菌液對沙門氏菌檢出效果的影響,為提高食品中沙門氏菌檢測結果的準確性提供可靠依據。
1 材料與方法
1.1 菌種
鼠傷寒沙門氏菌(ATCC 14028)、銅綠假單胞菌(ATCC 9027),均購自美國菌種保藏中心。
1.2 設備與材料
36.0 ℃恒溫培養箱,購自上海一恒科學儀器有限公司;42.0 ℃恒溫培養箱,購自德國Memmert;2~8 ℃冰箱,購自青島海爾集團;臺式振蕩器,購自哈爾濱市東聯電子設備有限公司;電子天平(感量0.1 g),購自梅特勒托利多儀器(上海)有限公司;無菌試管,購自黑龍江立高儀器設備有限公司;一次性移液管,1 mL(具0.01刻度),10 mL(具0.1刻度),購自NEST;無菌培養皿,購自廣東華粵集團;一次性定量接種環,購自廣東環凱生物技術有限公司;微量移液器,購自北京大龍興創實驗儀器股份公司;生物安全柜,購自哈爾濱市東聯電子設備有限公司;全自動微生物生化鑒定藥敏分析儀,購自美國BD公司。
1.3 培養基及試劑
緩沖蛋白胨水(BPW),分別購自品牌A、品牌B、某品牌C,四硫磺酸鈉煌綠(TTB)增菌液、亞硒酸鹽胱氨酸(SC)增菌液、腦心浸液肉湯(BHI)培養基、營養肉湯(NA)瓊脂、亞硫酸鉍(BS)瓊脂和沙門氏菌屬顯色培養基,所用培養基和試劑均按操作說明書進行,使用前均通過GB 4789.28—2013規定的質控測試。
1.4 實驗方法
1.4.1 菌液制備
將凍存的鼠傷寒沙門氏菌和銅綠假單胞菌分別接種于10 mL BHI培養基中,36.0 ℃靜置培養24 h后,用無菌生理鹽水將復蘇后的菌液梯度稀釋至10-7,分別吸取1 mL菌懸液涂布于NA平板和沙門氏菌顯色平板,36.0 ℃培養24 h后進行細菌計數。
1.4.2 樣本制備
各稱取25 g奶粉溶于225 mL不同品牌的BPW增菌液中,按表1所示分別向每份奶粉樣品中人工污染相應劑量的沙門氏菌和銅綠假單胞菌,充分混勻。

表1 人工污染奶粉樣本沙門氏菌及銅綠假單胞菌接種量表
1.4.3 前增菌及選擇性增菌
將人工污染后的樣本置于36 ℃靜置培養10 h和18 h,分別吸取1 mL增菌液接種于10 mL TTB內,于42.0 ℃培養24 h。同時,另取1 mL增菌液轉種于10 mL SC內,36.0 ℃靜置培養24 h,進行選擇性增菌。
1.4.4 選擇性平板分離
將使用不同品牌增菌液前增菌10 h和18 h的沙門氏菌污染樣本對應的TTB、SC二次增菌液分別用直徑3 mm的接種環劃線接種于沙門氏菌顯色平板36.0 ℃培養24 h和BS平板,36 ℃培養48 h,進行沙門氏菌的選擇性分離,同時觀察菌落形態。
1.4.5 生化鑒定
參照GB 4789.4-2016沙門氏菌檢測的食品安全國家標準挑取沙門氏菌顯色平板及BS平板上的典型特征菌落進行生化鑒定。
2 結果與分析
2.1 沙門氏菌及銅綠假單胞菌在不同平板上生長特性比較
分別將復蘇后沙門氏菌及銅綠假單胞菌稀釋并涂布于NA平板和沙門氏菌顯色平板,進行細菌計數,結果如表2所示。結果證實銅綠假單胞菌在沙門氏菌顯色平板的回收效率顯著降低。

表2 沙門氏菌及銅綠假單胞菌在不同平板上生長特性比較表(單位:CFU)
2.2 不同品牌BPW增菌后,分離平板菌落形態及顏色對比
應用不同品牌增菌液進行前增菌并進行選擇性增菌后,分離平板菌落形態無顯著差異,分離平板菌落形態及顏色有差異。應用不同品牌的BPW,分別進行10 h和18 h增菌,分離平板上的菌落也有所差異,見表3。

表3 樣本中沙門氏菌顯色平板菌落形態及顏色表
2.3 生化鑒定結果
將使用不同品牌增菌液前增菌10 h和18 h的沙門氏菌污染樣本對應的TTB、SC二次增菌液分別劃線接種于沙門氏菌顯色平板及BS平板,待長出單菌落后挑取特征性菌落劃線接種于NA平板,36 ℃培養24 h后上機鑒定,鑒定結果見表4。
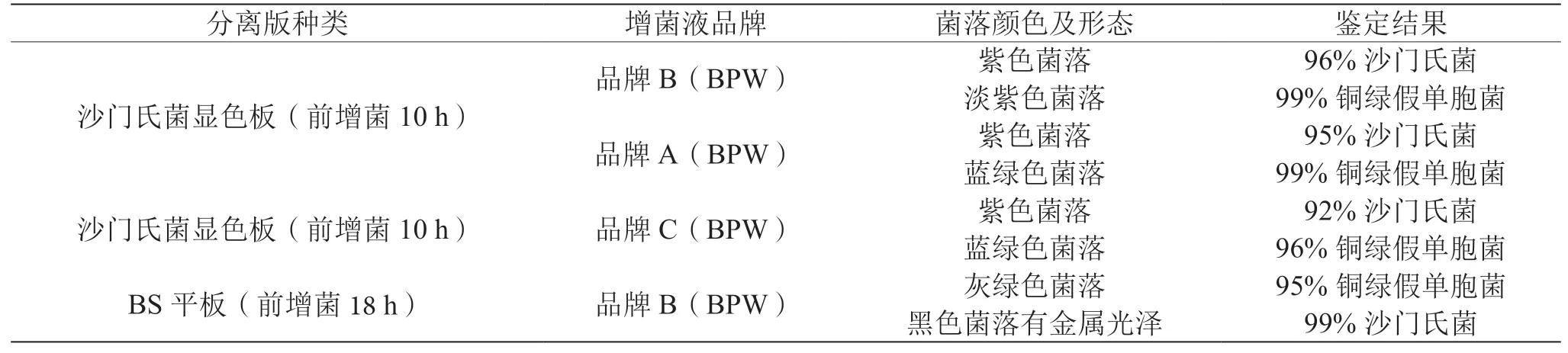
表4 樣本中沙門氏菌及銅綠假單胞菌生化鑒定結果表
2.4 沙門氏菌和銅綠假單胞菌在沙門氏菌選擇性平板上菌落形態比較
沙門氏菌和銅綠假單胞菌在沙門氏菌顯色選擇性平板上有些菌落雖具有相似的顯色情況,但銅綠假單胞菌菌落紫色較淡,菌落邊緣為淡色,多成無定形長。在BS平板上菌落形態具有明顯差異,詳見表5。

表5 沙門氏菌和銅綠假單胞菌在沙門氏菌選擇性平板上菌落形態比較表
3 結論與討論
本實驗參照《食品安全國家標準 食品微生物學檢驗 沙門氏菌檢驗》(GB 4789.4—2016)對人工污染不同濃度沙門氏菌及銅綠假單胞菌的無菌奶粉樣本進行檢驗,使用NA平板和沙門氏菌顯色平板進行細菌計數,結果證實銅綠假單胞菌在沙門氏菌顯色平板的回收效率顯著降低。通過應用不同品牌BPW對樣本進行前增菌,探究了銅綠假單胞菌作為干擾菌株對沙門氏菌檢出效果的影響。結果表明應用不同品牌的增菌液進行前增菌,菌落形態無明顯差異,增菌效果略有不同,但均能夠檢出沙門氏菌陽性樣本。此外應用品牌A增菌液進行前增菌后,沙門氏菌顯色平板有顯著的藍綠色銅綠假單胞菌典型菌落長出,應用品牌A增菌液與品牌C增菌液前增菌時間從10 h延長至18 h,分離后沙門氏菌平板上藍綠色菌落增多,兩者出現典型菌落的比例明顯降低,BPW為非選擇性培養基,當干擾菌的含量明顯高于目標菌時,這種放大效應就會更明顯。研究表明前增菌時間過長會使沙門氏菌的分離效果下降,對沙門氏菌的檢出效果有一定的影響。相比于使用品牌A和品牌C增菌液進行前增菌,使用品牌B增菌液進行前增菌,最終沙門氏菌的檢出率更高。因此為保證沙門氏菌檢測的準確性和提高檢出效率,在檢驗過程中,應根據對樣品污染程度的估計,結合檢驗標準的規定,合理選擇前增菌時間。

