太赫茲波生物效應*
彭曉昱 周歡
1) (中國科學院重慶綠色智能技術研究院,太赫茲技術研究中心,重慶 400714)
2) (中國科學院大學重慶學院,重慶 400714)
3) (重慶大學,重慶 400044)
太赫茲波能被生物組織中的水強烈吸收,能與生物組織中生物大分子和這些分子間的弱相互作用產生共振,因而太赫茲波在生物醫學中有許多潛在的應用.盡管單個太赫茲光子能量很低,對生物組織沒有電離損傷作用,但是隨著強度增大,太赫茲波會對生物細胞和組織產生一系列生物效應.由于太赫茲波參數和受輻照生物材料等輻照條件不同,將導致不同的生物學效應,包括以熱效應為主和以非熱效應為主導致的生物學效應.本文討論了這兩種效應的物理機理,介紹了適合用于生物效應研究的現今主要的強太赫茲輻射源種類,綜述了典型的太赫茲波的生物效應具體表現和已有的研究進展,展望了太赫茲波生物效應的潛在應用以及面臨的挑戰.
1 引言
太赫茲波通常是指頻率范圍在0.1—10 THz,波長在3—0.03 mm 之間的電磁波.太赫茲波在生物醫學中有許多潛在的應用,主要由于其具有以下獨特性質:1)能被生物組織中的水強烈吸收;2)生物組織中蛋白質、DNA、RNA、脂類、糖類等生物大分子骨架振動、轉動以及分子之間弱的相互作用(氫鍵、范德瓦耳斯力等)正好位于 THz 頻段范圍內,太赫茲波與這些生物大分子作用可以產生共振,因此其特征共振吸收峰可用于檢測物質結構和成分的微小變化,為分析細胞結構和醫學診斷提供了新方法;3)太赫茲光子能量低(1 THz-4.1 meV),不會直接對生物組織產生電離損傷,因而波束強度較低時可安全用于人體和其他生物材料的檢測和成像.目前,基于較低能量的太赫茲波的光譜探測技術已用于生物分子的表征和獲取生物分子的信息[1]或者用于生物組織中某種成份的測定[2],以及通過太赫茲成像技術用于腫瘤細胞和腫瘤組織的診斷[3].
盡管單個太赫茲光子對生物組織沒有類似于X 射線那樣的直接電離損傷作用,但是隨著波束強度的增大,太赫茲波會對生物細胞和組織產生一系列生物效應,包括熱效應和非熱效應導致的二次效應,如導致組織溫度升高,影響基因表達,促使細胞增殖,導致腫瘤抑制因子和細胞周期調節蛋白表達明顯升高,影響細胞的形態和細胞膜的通透性,引起生物大分子構象和功能發生變化或損傷生物大分子,甚至可能導致細胞凋亡和壞死而損傷生物組織等.
本文包含以下6 個部分:第1 節引言中一般性介紹太赫茲波的獨特性質及其產生的生物效應;第2 節描述太赫茲波與生物材料相互作用產生生物效應的基本物理機理;第3 節回顧可用于太赫茲波生物效應研究的主要強太赫茲輻射源種類;第4 節為重點內容,從個體、組織、細胞、分子等4 個層面綜述太赫茲波生物效應的研究現狀和典型成果;第5 節介紹了太赫茲波生物效應的潛在應用;最后一部分即第6 節總結和展望太赫茲波生物效應研究面臨的挑戰和機遇.
2 太赫茲波生物效應的物理機理
跟其他電磁波一樣,太赫茲波遇到生物介質時會發生反射、折射、散射、衍射等現象,折射進入生物介質后會與生物介質發生作用而被吸收.由于太赫茲波長相對于生物介質的組成部分(如細胞、細胞器、生物大分子等)來說要大好幾個數量級,因此太赫茲波的散射非常弱,太赫茲波與生物介質的相互作用中的衰減主要來自生物介質對太赫茲波的吸收作用.
從物理角度來看,太赫茲波輻照生物材料導致的生物效應本質上來源于太赫茲波的熱效應和非熱效應.熱效應主要來自生物體內大量的水分子對太赫茲波的強烈吸收,而非熱效應主要來自生物大分子受太赫茲波激發所產生的非線性共振作用.
2.1 太赫茲波產生的熱效應
2.1.1 生物介質中的水對太赫茲波的強烈吸收
構成生物體的成分含量最多的是水,如哺乳動物身體中含有約65%的水分,尤其是代謝旺盛的組織器官,如人的心臟和大腦分別高達79%和84%.人類皮膚中表皮含水量約有10%—35%,而越往里層含水量越髙,真皮含水量可達80%.因此,當太赫茲波與生物組織發生作用時,不可避免地要跟其中大量的水發生相互作用.由于水分子間氫鍵的拉伸和彎曲振動模式都落在太赫茲頻域內(最強共振頻率分別為5.6 和1.5 THz)[4-6],當生物組織或細胞受太赫茲波輻照時,其中的水分子間氫鍵的上述振動模式被激發從而引發共振,導致水對太赫茲波產生強烈的吸收,被吸收的太赫茲波能量轉化成水分子自身無規則運動的動能,相互碰撞的頻率增加,即產生熱能[7].如果沒有發生其他的能量轉換過程,隨著熱的不斷積累將會直接導致生物組織溫度的上升.高功率連續波或高重頻脈沖太赫茲波輻照生物組織時,由于其中的水吸收太赫茲波的過程中轉化的熱能來不及及時向外輻射、傳導或對流,因此這類太赫茲輻射更可能對生物組織產生熱效應.
2.1.2 生物大分子受太赫茲波激發產生共振吸收
由于DNA/RNA 堿基、氨基酸、糖類、脂類等生物大分子的許多轉動、擺動、扭動等能級剛好在太赫茲波段,因此一定頻率的太赫茲波對這些生物大分子作用可激發相應的共振.圖1 所示為本課題組測量的DNA/RNA 堿基在整個太赫茲頻段內的吸收光譜[8].可以看出,在整個太赫茲波段內都分布有這些生物大分子的吸收峰.從理論上說太赫茲波激發生物大分子發生線性共振會對生物組織吸收太赫茲波有貢獻,也會產生一部分熱(早期也有人稱之為微熱效應),不過由于水在細胞中的含量遠大于這些生物大分子,是生物組織中在太赫茲頻段的主要發色團[9],因此水在生物介質中對太赫茲波的吸收占絕對主導地位,由此產生的熱效應主要是水的貢獻,所以這些生物大分子因共振產生的熱可忽略不計.尤其是對于單頻的連續太赫茲波或窄頻的長脈沖太赫茲波,只能對某些生物大分子的少數振動模式有貢獻,其產生的熱效應更是微乎其微.
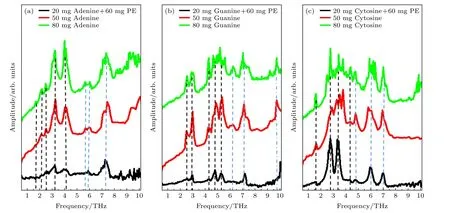
圖1 DNA/RNA 其中3 種堿基的太赫茲波吸收光譜[8] (a) 腺嘌呤;(b)鳥嘌呤 ;(c) 胞嘧啶Fig.1.Absorption spectra of three DNA/RNA nucleobases [8]:(a) Adenine;(b) Guanine;(c) Cytosine.
生物組織中通過水對太赫茲波的強烈吸收,增加了游離水分子的動能,可能改變水分子的極化特性,甚至影響結合水的特性,導致含有這些結合水的生物大分子結構的變化,進而影響一系列與生物有關的活動,如導致蛋白質結構的變化,影響酶的活性,導致膜的功能變化.因此,太赫茲波的熱效應導致的生物效應是通過生物介質內大量的水分子的作用來實現的.
2.2 太赫茲波產生的非熱效應
前面提到生物大分子的許多轉動、擺動、扭動等能級剛好在太赫茲波段,因此太赫茲波對這些生物大分子作用可激發相應的共振.當太赫茲波不是很強時,對某些細胞來說這種共振是一種線性共振,有可能對細胞有激活作用甚至是增殖作用,可能對人體組織和器官有理療作用.當太赫茲波強度不斷增大,太赫茲波可直接與生物分子耦合誘導相干激發[10]以產生非熱效應,即激發生物大分子的非線性共振效應,從而引起生物大分子的構象或構型變化,這些變化消耗了吸收的太赫茲波能量,劇烈的振蕩最終導致生物鍵斷裂.比如太赫茲輻射與生物分子中的氫鍵相互作用[11],引起低頻分子內振動從而導致蛋白質構象改變[12],甚至將分子間的氫鍵振斷,從而影響生物大分子和細胞的功能[11],更嚴重的情況可以導致細胞凋亡[13].
除了上述生物大分子的非線性共振作用外,還存在著非共振激發的非熱效應.細胞膜的靜態電場強度約為105V/cm,如果強場太赫茲波的峰值電場接近甚至超過這個場強值,太赫茲波將顯著影響細胞膜的通透性[14].太赫茲輻射單個光子能量很低,不會直接產生電離作用,但輻照生物介質的太赫茲波束足夠強(強場)時,可發生能量遠大于太赫茲光子能量的激發,如碰撞電離[15]或場電離,從而對生物組織產生電離損傷作用.這種電離作用跟可見光波段的激光類似,當光強很弱時,單個光子并沒有電離作用,但激光強度增加到一定閾值時即可發生碰撞電離,再增加激光強度甚至可以發生場電離,即激光電場直接把原子外的電子剝離出去.強場太赫茲波可直接激發半導體材料產生熒光[16],甚至已用于加速電子[17],由此可見強場太赫茲波的這些非共振激發的非熱效應將會嚴重影響細胞和生物組織的功能,甚至直接殺死細胞和電離灼傷生物組織.
3 用于研究太赫茲波生物效應的太赫茲輻射源種類
由于太赫茲輻射光子能量低(無電離損傷作用),低劑量輻照條件下,即太赫茲波強度較弱、輻照時間較短時,這些輻射源還不足以對人類生物細胞和組織產生明顯的生物效應[18],因而低功率連續波和低能量脈沖太赫茲輻射源通常被認為是安全的.如果要觀察到明顯的生物效應,需要加大輻照劑量,即加大太赫茲波功率或能量,延長輻照時間.如果要在較短時間內觀察到顯著的生物效應,需要強太赫茲輻射源.所謂的“強太赫茲輻射源”須具有高的平均功率或者大的脈沖能量或者強的峰值電場,只有這3 種太赫茲輻射源或者兼而有之的輻射源能產生明顯的生物效應.下面主要介紹這3 類強太赫茲輻射源.
3.1 高平均功率太赫茲輻射源
這類輻射源特點是平均功率高,主要有連續波或高重復頻率太赫茲輻射源,如二氧化碳激光泵浦的太赫茲激光器、自由電子激光器、行波管、返波管、電子回旋管(連續波)等.日本福井大學的電子回旋管連續波太赫茲輻射源裝置(FU CW1)[19],工作頻率為0.3 THz,輸出功率為2.3 kW.國內電子科技大學劉盛綱院士課題組[20]也有類似的電子回旋管連續波太赫茲輻射源,工作頻率在0.5 THz,輸出功率為389 W.這類輻射源輻照生物細胞和組織時,吸收的太赫茲波能量主要轉換為細胞和組織的熱能,致使溫度升高,即產生明顯的熱效應,并由此帶來一系列生物學效應.因此,使用這類太赫茲輻射源直接輻照生物材料時,會產生主要是熱效應為主的生物效應.
除了上述一類高平均功率的連續波太赫茲輻射源外,還有一類高重頻大功率脈沖太赫茲輻射源.這類輻射源雖然不是連續波,單脈沖能量也不是很高,但重復頻率很高,有很高的平均功率.主要有基于傳統電子加速器的太赫茲輻射源,如自由電子激光器太赫茲輻射源[21,22].在國內,中國工程物理研究院研制的自由電子激光裝置CTEFL,頻率調節范圍為0.7—4.2 THz,平均功率達到10 W,峰值功率大于0.5 MW,倍頻光頻率調節范圍為4—8 THz.基頻和倍頻太赫茲波束均為高度線偏振,偏振度大于99%.目前為止已有多個國內研究小組使用這臺太赫茲輻射源用于輻照細胞和腫瘤的生物效應的研究并取得了不少成果.
3.2 高能量長脈沖太赫茲輻射源
這類源的特點是脈沖能量很高,至少大于幾十個毫焦,甚至可達幾百毫焦,脈寬通常為微秒量級,如脈沖式電子回旋管太赫茲輻射源.由于脈寬較長,這類太赫茲輻射脈沖的峰值場強并不高.俄國一個小組研制的脈沖式電子回旋管[23],脈沖磁場強度為40 T,工作頻率在1 THz,脈寬50 μs,脈沖能量為75 mJ,功率為1.5 kW.
3.3 強場太赫茲輻射源
這類輻射源特點是頻譜較寬,甚至超過幾十個太赫茲的超寬頻譜,低重復頻率,輸出能量不是特別強,通常為幾個微焦至幾個毫焦之間,但因脈寬短,具有很強的峰值電場(約1 MV/cm)和磁場(約0.3 T),通常被稱為強場太赫茲輻射源.如基于傳統電子加速器的相干渡越輻射太赫茲源、基于傾斜激光波前泵浦的光整流太赫茲輻射源、基于飛秒激光等離子體相互作用的太赫茲輻射源等.
斯坦福大學直線相干光源自由電子激光器中的電子束通過鈹膜時產生的相干渡越輻射太赫茲輻射源[24],重復頻率為10 Hz,脈沖能量為140 μJ,峰值場強高達62 MV/cm.不過基于傳統加速器的相干渡越輻射太赫茲源因為加速器復雜且體積龐大,造價高.
光整流太赫茲輻射源頻譜通常在3 THz 以下.利用傾斜激光波前泵浦鈮酸鋰晶體的光整流太赫茲輻射源,使用100 mJ 激光能量,可產生脈沖能量為373 μJ、峰值場強約為9.1 MV/cm 的太赫茲輻射[25].目前光整流太赫茲輻射源的最強記錄為太赫茲脈沖輻射能量為1.4 mJ,重復頻率為10 Hz,中心頻率為0.4 THz,峰值場強為6.3 MV/cm[26].
雙色飛秒激光場產生的氣體等離子體太赫茲輻射通常為可以調控的超寬頻譜[27],超過10 THz以上.這種方法產生的太赫茲脈沖能量可達幾十個微焦,在優化各項條件后預計脈沖能量可以達到300 μJ[28].更強的激光等離子體太赫茲輻射源來自強激光與固體薄膜靶的相互作用[16],脈沖能量可達幾個甚至幾十個毫焦量級.
光整流太赫茲輻射源和激光等離子體太赫茲輻射源都是由超短脈沖強激光泵浦產生的,屬于臺式太赫茲輻射源,他們的重復頻率通常在1 Hz—1 kHz 之間,取決于激光器的重復頻率.
4 太赫茲波生物效應的具體表現
太赫茲波的生物效應取決于輻照條件(如太赫茲輻射源的特性,太赫茲波的頻率、功率或能量,輻照時間等因素)和受輻照生物材料的特性.由于所使用的太赫茲輻射源種類較多和各種生物材料(如不同細胞、不同組織、不同個體等)對太赫茲波的敏感性和反應不同,所產生的生物效應會有很大差異.生物材料受太赫茲波輻照一定劑量后產生包括熱效應和非熱效應的生物效應,根據輻照劑量不同,生物材料不同,將導致從生物體、組織、細胞到生物分子的不同層次和水平的生物效應.這些效應互為關聯,主要包括影響生物體的行為和生理狀態、組織凝固或炎癥、細胞死亡,細胞內的應激反應,細胞器功能受到干擾,生物大分子受損等[29].至于是太赫茲波的熱效應還是非熱效應為主導致的生物效應,目前主要還是通過輻照過程中的生物材料溫度是否有明顯上升來判斷.通常連續波太赫茲輻射源、高重頻脈沖太赫茲輻射源以及長脈沖太赫茲輻射源輻照生物材料時溫度都會上升,一般認為產生的是熱效應為主的生物效應.下面從宏觀到微觀,即從生物個體、組織、細胞、生物大分子的順序,總結一些典型的太赫茲波的生物效應,對于那些沒有明顯效應的案例,本文不再贅述.
4.1 太赫茲波對生物體行為和生理狀態的影響
已有的實驗表明,一定劑量的太赫茲波輻照動物個體后,會對它們的學習記憶、心理行為和生物節律等產生一定的影響,甚至影響發育和生殖等其他重要生理過程.
4.1.1 太赫茲波對動物行為的影響
Bondar 等[30]研究了太赫茲激光器3.6 THz的太赫茲波對雄性小鼠的行為效應,輻照功率為15 mW.結果表明:在輻照15 min 后,小鼠能感知到太赫茲波且太赫茲波對小鼠直接接觸激光的影響最大;在輻照30 min 后的第二天,觀察到受太赫茲波輻照的雄性小鼠的焦慮程度增加.Kirichuk等[31]使用NO 頻率范圍(150.176—150.664 GHz)的大功率太赫茲波對應激性運動功能減退的大鼠輻照30 min 后,發現大鼠的運動功能得以部分或全部恢復.該研究小組還研究了該太赫茲波輻照應激誘導的雄性白化病大鼠血小板聚集及行為反應的影響[32],實驗中太赫茲波功率密度3 mW/cm2,輻照時間為15,30 及60 min.實驗結果表明,太赫茲輻射60 min 能夠誘導大鼠抑郁情緒和行為改變.
4.1.2 太赫茲波對動物生理活動的影響
一定劑量的太赫茲波輻照動物可調節其生理活動,并產生一些有益的效應.Kirichuk 等[32]一系列的實驗表明,太赫茲波可以活化血小板的凝血功能.Ostrovskiy 等[33]使用頻率為0.15 THz、強度為 0.03 mW/cm2的太赫茲波對淺度和深度燒傷的患者每次輻照15 min,每天進行7—10 次輻照,發現太赫茲波輻照可通過加速上皮化進程促進局部燒傷創面的修復.
太赫茲波可影響昆蟲的生命周期.Weisman等[34]研究了太赫茲輻射對黑腹果蠅存活率和壽命的影響,將240 只果蠅暴露在寬帶脈沖太赫茲輻射下30 min,頻率為0.1—2.2 THz,脈沖持續時間為1 ps,脈沖功率為8.5 mW,脈沖重復頻率為76 MHz.實驗結果顯示,雄性果蠅對太赫茲輻射不是很敏感,而受太赫茲波輻照的雌性果蠅的存活率在生命的后半段顯著增加.照射對果蠅的平均壽命和最大壽命值沒有顯著影響,但雄性和雌性果蠅平均壽命值之間的差距增加了.他們認為太赫茲輻射對存活率和壽命的影響機制可能與細胞膜、基因表達和信號通路的變化有關,是通過對果蠅壽命相關基因和信號通路的間接調節作用實現的[34].
4.2 太赫茲波對生物組織的生物效應
足夠劑量的太赫茲波輻照將導致生物組織升溫、急性炎癥反應或腫瘤消融等生物效應.
4.2.1 太赫茲波導致組織升溫和炎癥反應
連續太赫茲波或高重頻脈沖太赫茲波輻照生物組織產生的熱效應會導致組織升溫,如果過熱將導致以下二次效應[35]:1)激發急性炎癥反應(如疼痛、發熱、發紅、腫脹).2)組織脫水和壞死(當溫度提高到80—100 ℃幾秒鐘就會出現).3) 50—70 ℃溫度下幾分鐘細胞蛋白質即可發生不可逆結構變性.膠原蛋白會失去雙折射特性,導致組織變白.
Bottauscio 等[36]通過應用Pennes 生物傳熱方程和高斯分布推斷在組織空間分布的熱功率沉積以模擬聚焦太赫茲波束的影響,以此研究聚焦太赫茲波束輻射下人體組織的熱效應.研究結果顯示,低強度的0.025—1 THz 頻率太赫茲輻照人體皮膚的熱效應不明顯,但隨著入射太赫茲波強度的增加,溫度呈線性上升.Dalzell 等[37]使用杰佛遜實驗室的自由電子激光器高功率太赫茲源(頻率0.1—1 THz,輻照強度2—14 W/cm2,脈沖持續時間為350 ps,光斑大小為0.452 cm2,輻照時間為2 s)研究太赫茲輻射輻照麋鹿皮膚組織的損傷閾值,結果顯示寬帶(0.1—1 THz)太赫茲波的組織損傷閾值為7.16 W/cm2,這個值與計算模型預測的5.0 W/cm2非常接近.隨著輻照強度增加,受輻照組織的溫度不斷上升,當照射強度為7.16 W/cm2時,組織溫度升高31.72 ℃.在國內,陸軍軍醫大學的余爭平教授團隊[38]使用不同強度的0.22 THz 的行波管連續波太赫茲輻射源輻照小鼠皮膚組織,發現當太赫茲波強度為50 mW/cm2時輻照5 min 后,皮膚平均溫度迅速升高超過2 ℃,并且導致出現上皮脫落及出血等病理損傷特征.該團隊還繼續增大輻照強度至160 mW/cm2以及輻照時間延長至10 min,發現可導致小鼠皮膚氧化應激反應,并引起皮膚組織內IL-1β,IL-6 和PGE2 含量升高[39].
脈沖太赫茲波輻照生物組織的非熱效應也可導致炎癥反應.Hwang 等[40]使用脈沖太赫茲波輻照小鼠皮膚,太赫茲波頻率為2.7 THz,脈寬為4 μs,脈沖能量為61.4 μJ,重復頻率為3 Hz,平均功率為260 mW/cm2.實驗中采用聚焦太赫茲波照射裝置,照射30 min.由于重復頻率低,雖然脈寬較長,但紅外相機沒有觀察到耳朵皮膚表面的溫度變化,說明沒有產生明顯的熱效應.然而,6 h 后受太赫茲波輻照皮膚區域觀察到新浸潤的中性粒細胞的大量募集,表明脈沖太赫茲波輻照通過非熱效應在皮膚上誘導了急性炎癥反應.
4.2.2 太赫茲波腫瘤消融
太赫茲波的熱效應可以用來殺死腫瘤細胞.日本福井大學使用電子回旋管連續波太赫茲輻射源(0.203 和0.107 THz)產生的熱效應即熱療法來消融白鼠的腫瘤[19].經過波導會聚在腫瘤上的太赫茲波能量密度為4.67 kJ/cm2,輻照10 min,溫度上升到熱療所需的溫度(43 ± 1) ℃,并通過控制電子回旋管輸出功率和波導與老鼠的距離來保持這個溫度再輻照10 min.與該老鼠身上另外一個同等大小的腫瘤作為對照,每天測量受輻照腫瘤和對照腫瘤的大小.結果發現,受太赫茲波輻照的腫瘤逐漸減小,15 天后消失,而未受輻照的對照腫瘤體積卻越來越大,圖2(a)和圖2(b)所示分別為受0.203 和0.107 THz 太赫茲波輻照后的腫瘤與對照腫瘤的生長曲線圖.兩種頻率的太赫茲波通過熱療法都有消融腫瘤的作用,但后者在21 天后腫瘤略有長大,于是,該團隊又將太赫茲波的熱療法與光動力療法相結合,取得了更好的消融效果[19].
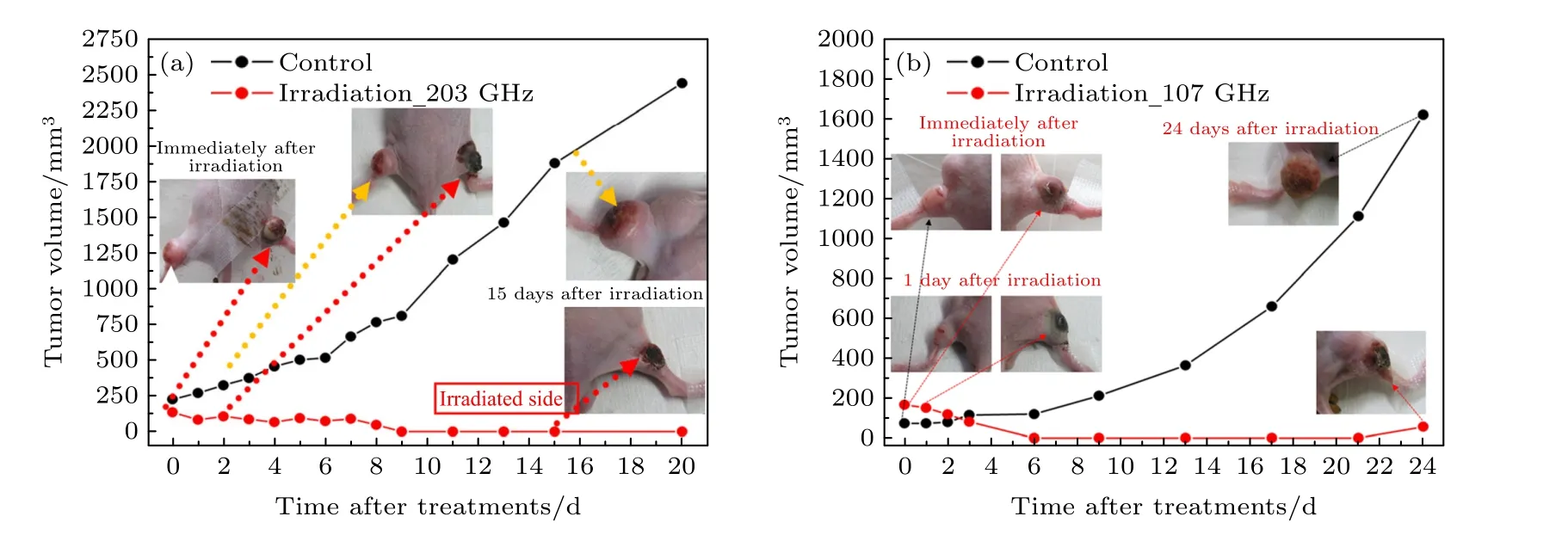
圖2 腫瘤分別受頻率為(a) 0.203 THz 和(b) 0.107 THz 的太赫茲波輻照后與對照腫瘤的生長曲線圖[19]Fig.2.Growth curves of the tumors after the irradiation at (a) 0.203 THz and (b) 0.107 THz compared with that of the control tumors,respectively [19].
國內電子科技大學周俊教授團隊[41,42]利用中國工程物理研究院的自由電子激光裝置(CTEFL)產生的太赫茲輻射源(2.5 THz)研究了非熱效應方法來消融腫瘤.為了在輻照過程溫度不上升,即不產生熱效應,將太赫茲波重復頻率控制在1 Hz,觀察到受輻照腫瘤在22 天以前體積略有增大,22 天后逐漸變小,而對照腫瘤體積卻增長很快.實驗結果表明強場脈沖太赫茲波可實現非熱消融腫瘤.
由此可見,無論是太赫茲波的熱效應還是非熱效應,都有可能用于未來的腫瘤治療.
4.3 太赫茲波對細胞的生物效應
大量的實驗表明,細胞受一定劑量的太赫茲波輻照后,其形態、膜的通透性、活性、周期、功能等都可能受到影響.
4.3.1 太赫茲波導致細胞形態變化
細胞受到一定劑量的太赫茲波輻照后,其形態會發生某種程度的變化.Alexandrov 等[43]分別使用來自氣體激光等離子體的寬帶(1—30 THz)太赫茲波(中心頻率為10 THz,強度1.2 mW/cm2,重復頻率為1 kHz)和來自CO2氣體太赫茲波激光器的單頻(2.52 THz)連續太赫茲波(3 mW/cm2)輻照小鼠干細胞,與對照組相比,兩種太赫茲源輻照2 h 后,小鼠干細胞的形態都發生了改變,如圖3所示.使用寬帶太赫茲波輻照9 h 后,還可以觀察到細胞中含有大量的脂滴包含物.
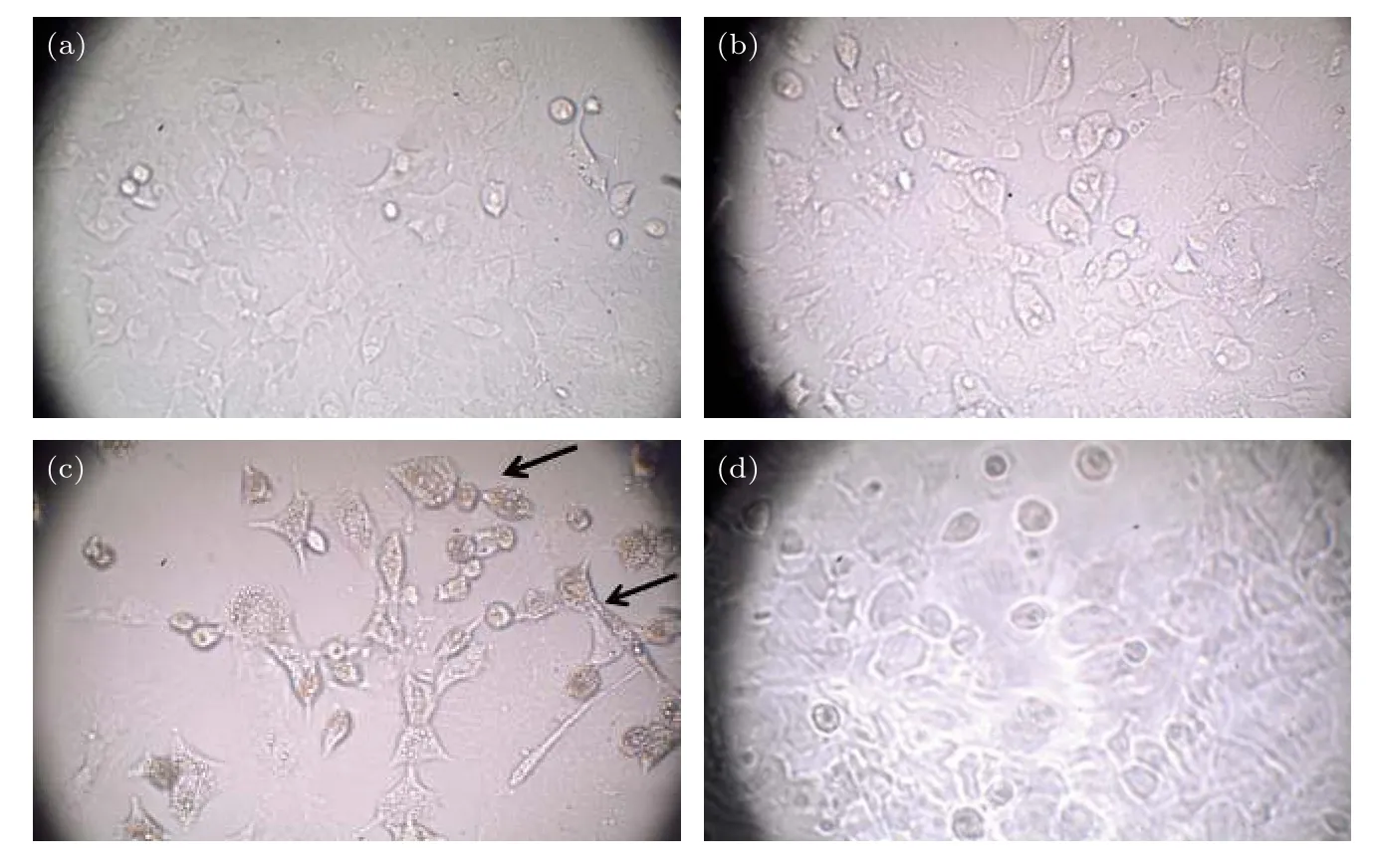
圖3 小鼠干細胞受太赫茲輻照后發生形態變化的顯微鏡照片 (a)對照組;(b) 寬帶太赫茲波輻照2 h;(c) 寬帶太赫茲波輻照9 h;(d) 單頻連續波太赫茲波輻照2 h;圖(c)中的箭頭表示細胞中含有大量的脂滴包涵含物 [43]Fig.3.Light microscopy image:(a) Control cultures;mouse stem cells after (b) 2 h and (c) 9 hours of pulsed broad-band irradiation;(d) mouse stem cells after 2 h of irradiation from the CW laser source.The arrows in panel (c) indicate cells with an elevated number of lipid droplets inclusions [43].
陸軍軍醫大學的馬秦龍等[44]研究了太赫茲波輻射對Neuro-2a 細胞突出生長的變化情況,發現太赫茲波輻照引起Neuro-2a 細胞突出長度和分支數目顯著減少,突出生長及功能相關的基因Tubb3 和Syp 表達顯著下調,且具有劑量依賴效應.Perera等[14]利用同步輻射源0.3—19.5 THz 的太赫茲輻射源輻照類似于神經元細胞的嗜鉻細胞瘤細胞PC12,通過掃描電子顯微鏡觀察到在PC12 細胞表面形成了直徑高達1 μm 的異常大的氣泡.
4.3.2 太赫茲波影響細胞膜的通透性
Ramundo-Orlando 等[45]研究了由自由電子激光器產生的0.13 THz 的太赫茲脈沖輻射對脂質體膜通透性的影響,太赫茲強度為1—18 mW/cm2,結果表明頻率太赫茲輻射在低重復頻率(5,7 或10 Hz)脈沖下可以增強含陽離子脂質體的通透性.該小組后續的實驗還表明脂質體膜的通透性隨太赫茲峰值電場強度增大而增強[46].Fedorov 等[47]研究了太赫茲輻射對人類紅細胞和淋巴細胞的影響,實驗中太赫茲波強度為20 mW/cm2,輻照時間30—90 min,結果顯示人類紅細胞和淋巴細胞的細胞膜通透性得到了增強.
2019 年,Perera 等[14]利用同步輻射源0.3—19.5 THz 的太赫茲輻射,研究了類似于神經元細胞的嗜鉻細胞瘤細胞PC12 對太赫茲輻射反應.發現在(25.2 ± 0.4) ℃溫度下輻照10 min,由于誘發了細胞膜通透性暫時增加,通過共聚焦顯微鏡和高分辨率的透射電子顯微鏡都證實二氧化硅納米球(直徑d=(23.5 ± 0.2) nm)及其團簇(d=63 nm)得以進入PC12 細胞內.圖4 所示為共聚焦顯微鏡下的受太赫茲輻照PC12 細胞和未受輻照的細胞對比圖,可清楚看見前者有二氧化硅納米球攝入細胞質中,而對照組則沒有任何納米球進入細胞中.長時間內,受太赫茲波輻照的PC12 細胞與對照組比較,雖然代謝活動無重大差異,但卻有更多數量的受輻照細胞PC12 對神經生長因子NGF 有響應.這些發現表明,由于太赫茲輻射能促進細胞吸納納米顆粒而不引起細胞凋亡、壞死或生理損傷,有可能發展基于納米顆粒介導的藥物傳遞和基因治療技術[14].

圖4 PC12 細胞受太赫茲波輻照10 min 后納米球的攝入情況.共聚焦激光掃描顯微圖像顯示受太赫茲波輻照的細胞中攝入了納米球,而未受輻照的對照組細胞沒有攝入任何納米球[14]Fig.4.Nanosphere internalization of PC12 cells following a 10 min exposure of THz radiation.Confocal laser scanning microscopy (CLSM) images illustrate the uptake of silica nanospheres by the THz treated cells whereas the untreated control does not exhibit any nanosphere uptake[14].
4.3.3 太赫茲波影響細胞周期和活性
足夠劑量的太赫茲波輻照會影響細胞增殖、分化、細胞周期.Olshevskaya 等[48]研究了太赫茲波輻射對神經元系統的影響,實驗采用0.7,2.49 和3.69 THz 這3 種太赫茲頻率,強度為0.3—30 mW/cm2,輻照時間為1 min.結果顯示神經元的增殖能力、細胞黏附能力、細胞膜的形態、胞內結構的損傷以及神經元細胞的靜息電位均受到了不同程度的影響.Hintzsche 小組[49]研究了太赫茲輻射對人倉鼠雜交細胞紡錘體的影響.實驗使用頻率為0.106 THz、強度為0.043—7.3 mW/cm2的連續太赫茲波輻照人-倉鼠雜交細胞 0.5 h,發現太赫茲波會干擾有絲分裂房垂體的形成,會引起細胞分裂后期和末期的染色體紊亂.
對于某類細胞,一定劑量的太赫茲波輻照也可能產生正面的效應.Wei 等[50]使用頻率為0.1—3 THz、功率60 μW/cm2的太赫茲波輻照精子,發現輻照時間超過5 min 時能顯著提高精子的活力和胞內鈣濃度(如圖5 所示),但其DNA 的完整性沒有變化.

圖5 太赫茲波輻照效應對精子細胞內鈣濃度的影響[50]Fig.5.Effect of terahertz irradiation on the intracellular calcium concentration in sperm[50].
4.3.4 太赫茲波導致細胞凋亡和壞死
足夠強的太赫茲輻射源可導致細胞凋亡甚至直接壞死.Wimink 等[51]研究了暴露在強太赫茲輻射時細胞死亡的閾值和細胞特異性的基因表達情況.太赫茲波頻率為2.52 THz,強度為227 mW/cm2,暴露持續時間為5—40 min.結果顯示,Jurkat 細胞在輻照20 min 后表現出了明顯的凋亡及壞死,同時細胞的凋亡率及死亡率隨著暴露時間的延長呈指數增長(圖6).熒光顯微成像術結果表明,強太赫茲波輻照增強了人皮膚成纖維細胞細胞膜的通透性,且離太赫茲輻射源照射的中心位置越近,細胞膜通透性越高.基因芯片分析顯示,部分細胞應激反應通路被激活,少數特異性的基因呈現上調.Borovkova 等[13]研究了頻率為0.12—0.18 THz、強度為3.2 mW/cm2的連續太赫茲波對大鼠膠質細胞的影響,發現太赫茲波照射大鼠膠質細胞1 min 后,細胞凋亡相對數量增加了1.5 倍,照射5 min 后增加了2.4 倍,隨著照射時間的延長細胞凋亡越發嚴重.
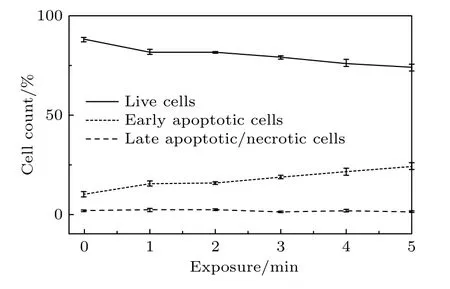
圖6 樣品中存活細胞、早凋亡細胞、晚凋亡細胞與太赫茲波輻照時間的關系[13]Fig.6.Number of live cells and cells at early and late stages of apoptosis in the sample in relation of the THz radiation exposure time[13].
不同細胞在同一輻照條件下可能出現相反的反應.Federov 等[47]使用相同輻照條件(頻率為3.68 THz,強度為20 mW/cm2,輻照時間為30—90 min,溫度為25℃)的太赫茲波輻照人類紅細胞和淋巴細胞,發現有38%的淋巴細胞死亡增殖受到顯著抑制,而紅細胞則表現出增強的細胞增殖能力和細胞膜通透性.
4.4 太赫茲波對生物大分子層面的生物效應
太赫茲波輻照生物組織時,將與細胞內的各種生物大分子發生作用,會影響這些分子結構的穩定性和功能,甚至損傷生物大分子,或者影響基因的表達.
4.4.1 太赫茲波對生物大分子的結構穩定性和功能的影響
20 世紀90 年代Govorun 等就發現太赫茲輻射可以改變白蛋白的二級結構,如α-螺旋[52].Cherkasova 等[12]研究了太赫茲輻射對白蛋白(BSA)光譜特性和功能特性的影響,實驗中采用太赫茲頻率3.6 THz,波束強度為10 mW/cm2,照射60 min.實驗結果顯示太赫茲輻射可以顯著改變BSA 的光譜,同時這種變化是有劑量依賴性的,這表明太赫茲輻射會影響蛋白質分子的構象及其功能特征.除了高功率連續太赫茲波的熱效應會導致蛋白質變性[37],Lundholm 等[53]發現脈沖太赫茲輻射也會引起蛋白質晶體的非熱結構變化.
Alexandrov 等[10]從理論上模擬研究了DNA的配對-非配對動力學,結果顯示太赫茲輻射可能顯著干擾雙鏈DNA 自然發生的局部鏈分離動力學,從而影響DNA 的功能,太赫茲輻射的主要效應是共振影響dsDNA 系統的動力學穩定性.在國內,電子科技大學宮玉彬教授團隊[54]基于密度泛函理論和薛定諤方程,通過理論模擬研究了亞皮秒強場太赫茲輻射誘導的DNA 堿基對氫鍵中質子轉移過程的完整量子模型,發現在特定極化方向上電場強度高達10 GV/m 的太赫茲波可以精確地控制堿基對氫鍵中的質子轉移過程.
Korenstein-Ilan 等[55]使用頻率為0.1 THz、強度為0.031 mW/ cm2的連續太赫茲波輻照淋巴細胞1,2 和24 h,用熒光原位雜交技術(FISH)檢測1,10,11 和17 號染色體數的變化及其中心粒復制時間的變化.結果發現11 號染色體和17 號染色體最為脆弱(暴露2 和24 h 后非整倍體增加約30%),而1 號染色體和10 號染色體未受影響.還觀察到11,17 和1 的著絲點在暴露2 h 后異步復制模式發生了40%的變化,4 個著絲點在暴露24 h 后異步復制模式發生了50%的變化.推測這些效應是由輻射誘導的蛋白質和DNA 的低頻集體振動模式引起的.上述實驗結果表明,體外暴露在0.1 THz低功率密度輻射下的淋巴細胞會導致基因組不穩定.
Homenko 等[56]研究了太赫茲輻射對堿性磷酸酶活性和抗原抗體相互作用的影響,太赫茲輻射頻率為100 GHz,輻射強度為0.08 mW/cm2,輻照時間30—120 min.在該輻照條件下研究了堿性磷酸酶與底物對硝基苯磷酸的相互作用,結果顯示液態堿性磷酸酶受太赫茲波照射會導致酶活性略微減少,但統計上有明顯降低,輻照時間越長,導致催化能力越弱.在對抗原抗體相互作用的影響實驗中顯示太赫茲波輻照可降低抗原-抗體復合物的穩定性.
4.4.2 太赫茲波對基因表達的影響
有許多實驗表明,強太赫茲波會顯著影響基因表達的水平.Alexandrov 等[43]研究了太赫茲輻射對小鼠間充質干細胞的非熱效應,實驗采用了脈沖寬帶(1—30 THz)激光等離子體氣體太赫茲輻射源以及一個光泵浦的分子氣體連續波太赫茲激光源(2.52 THz)輻照小鼠間充質干細胞培養物.為盡量減少熱對基因活性的影響,溫度保持在26—27 ℃,連續波太赫茲輻射平均強度控制在1—3 mW/cm2.研究結果表明連續波太赫茲輻射對熱休克蛋白(HSP105,HSP90 以及CRP)的表達沒有影響,而寬頻脈沖太赫茲波輻照細胞9 h,某些基因(Adiponectin,GLUT4,以及PPARG)則產生了明顯的上調.
Titova 等[57]發現,強太赫茲脈沖會影響與人類非黑色素瘤皮膚癌、牛皮癬、特應性皮炎有關的人類皮膚組織大量基因的表達水平.如圖7 所示,能量為1 μJ、頻率為0.2—2.5 THz 的太赫茲脈沖輻照皮膚組織10 min,發現有422 個基因的表達水平發生變化;即使能量降低10 倍,即為0.1 μJ,仍然有397 個基因表達水平被改變.受強太赫茲脈沖影響的基因包括近一半的表皮分化復合體(EDC)成員.EDC 基因定位于人類染色體1q21 區域,編碼參與表皮分化的蛋白質,在銀屑病和皮膚癌等疾病中經常過度表達.在幾乎所有因暴露于強太赫茲脈沖而表達不同的基因中,轉錄水平的變化與疾病相關的變化相反.強太赫茲脈沖能夠引起與炎癥性皮膚病和皮膚癌相關的多個基因表達的協同有利變化,這表明強太赫茲脈沖具有潛在的治療應用價值.
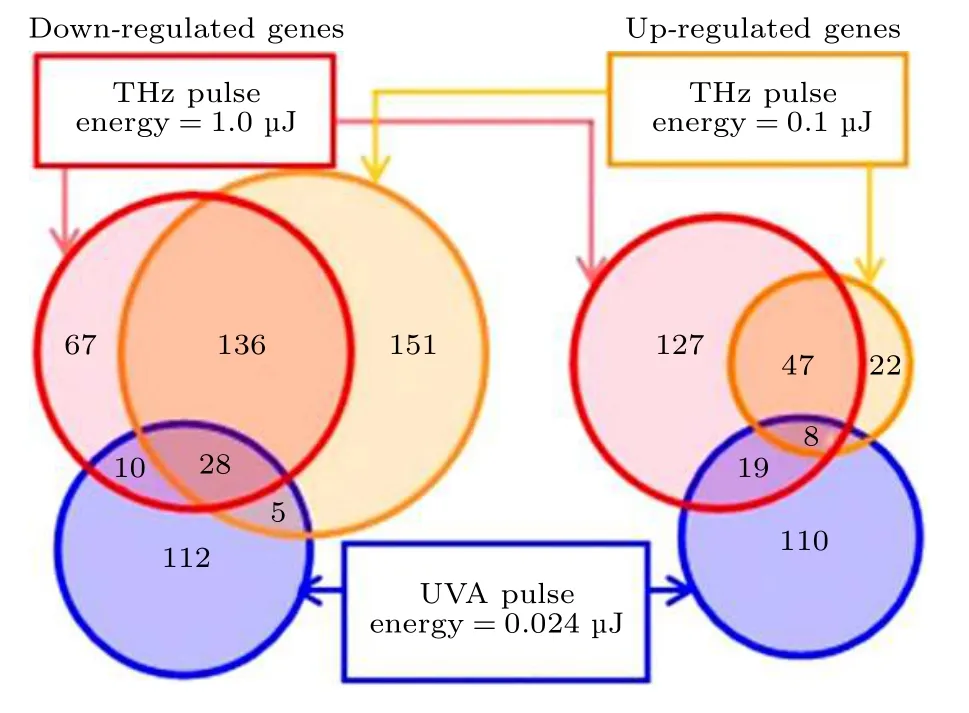
圖7 強太赫茲脈沖誘導的人類皮膚的基因表達.維恩圖概括了EpiDermFT 組織受1.0 μJ 或者0.1 μJ 太赫茲脈沖輻照后基因表達的變化[57]Fig.7.Intense THz-pulse-induced gene expression in human skin.Venn diagrams summarizing differentially-expressed genes in EpiDermFT tissues exposed to either 1.0 μJ or 0.1 μJ THz pulses[57].
Echchgadda 等[58]研究了不同太赫茲頻率的太赫茲輻射對人角質形成細胞基因表達的影響.實驗中選用了3 種太赫茲頻率,分別是1.4,2.52 和3.11 THz,輻照強度為44.2 mW/cm2,輻照時間20 min.結果顯示每種頻率的太赫茲波觸發了特定的基因和代謝信號通路,這提示不同頻率的太赫茲輻射可能引起不同的生化和細胞反應,他們指出要把太赫茲輻射作為刺激特定細胞表型特性(如形態、生物化學或生理特征)的潛在工具時,需要仔細選擇太赫茲波的頻率,旨在調節其反應或者條件行為.
在國內,天津大學何明霞團隊[59]研究了光整流太赫茲輻射對3 種不同人眼細胞基因的影響,通過轉錄組測序發現,使用上述寬頻太赫茲輻射源輻照6 h 后導致了基因表達的改變以及與這些基因相關的生物功能的變化.他們的實驗結果還表明,太赫茲輻射對基因表達的影響能持續超過15 h 且依賴于細胞的種類.最近,西安交通大學的盧曉云團隊[60]使用轉錄組基因測試技術,研究了頻率為0.1 THz 的太赫茲波對神經細胞DNA 分子中基因表達的影響和這種作用的分子機制,發現有111 個基因表達上調,54 個基因表達下調.這些結果表明,太赫茲輻射可能影響轉錄因子和DNA 的相互作用,并導致基因表達的改變.
4.4.3 強太赫茲波對生物大分子的損傷作用
高功率連續太赫茲波的熱效應會損傷生物大分子.例如Korenstein-Ilan 等[55]使用頻率為1.89 THz、強度為189.92 mW/cm2的連續波太赫茲輻射輻照新鮮豬鼻子、豬腿、豬耳朵60 min,觀察到組織溫度升高15—18 ℃,雖然未觀察到明顯的組織損傷跡象,然而一些樣品顯示出可見的蛋白凝固,于是做了后續的蛋白實驗,發現溫度升高10—12 ℃,有一些蛋白出現了凝固的現象,即這些蛋白質分子受到損傷而變性.
強場太赫茲波也會損傷生物大分子.Titova等[61]從實驗上研究了脈沖太赫茲輻射對人體皮膚組織的生物學效應,使用傾斜波前激光泵浦鈮酸鋰晶體的光整流寬帶脈沖太赫茲輻射源,脈沖能量可達1 μJ,重復頻率1 kHz,光斑直徑1.5 mm,最高強度為57 mW/cm2.實驗結果顯示,暴露10 min會導致H2AX 的顯著磷酸化,DNA 雙鏈斷裂造成DNA 損傷.同時,幾種負責細胞周期調控和腫瘤抑制的蛋白質水平增加,表明DNA 損傷修復機制被快速激活.
如果使用可引起非線性共振效應的某些特定頻率的強場太赫茲波,去針對性對癌細胞DNA 分子作用,則有可能抑制癌細胞.DNA 甲基化可調控基因表達的關鍵的DNA 表觀遺傳修飾,血癌細胞DNA 分子甲基化程度對應特征共振頻率大致為1.7 THz.Cheon 等[62]使用頻率為1.7 THz的強場太赫茲波輻照上述血癌細胞,引發非線性共振效應,可導致甲基-DNA 鍵斷裂,去甲基化程度高達70%.該團隊還使用強場太赫茲波輻照黑色素瘤細胞[63]以評估太赫茲波去甲基化在細胞水平上的影響,并驗證太赫茲波對DNA 的損傷.結果顯示,40 μW 的太赫茲波輻照30 min 后,黑色素瘤細胞內DNA 甲基化程度降低了約10%—15%.圖8為黑色素瘤細胞內DNA 去甲基化程度隨太赫茲波輻照時間的變化曲線.上述結果表明,使用強場太赫茲波可以操控DNA 基因組甲基化,即強太赫茲輻射具有誘導DNA 去甲基化的能力,因此可作為表觀遺傳抑制劑,可能在癌癥治療中有潛在的應用價值.
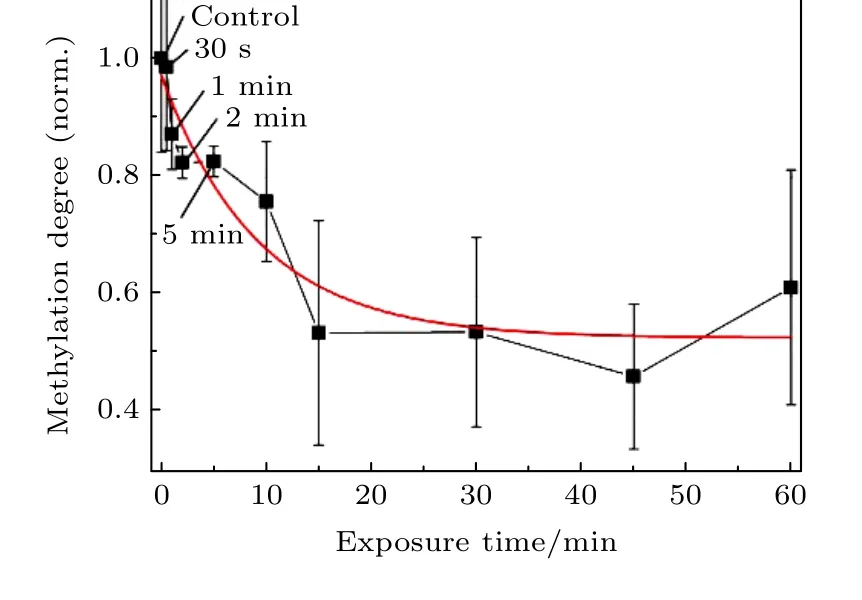
圖8 黑色素瘤細胞內DNA 去甲基化程度隨太赫茲波輻照時間的變化曲線[63]Fig.8.THz demethylation dependence on exposure time in M-293T DNA[63].
5 太赫茲波生物效應的潛在應用
已有的太赫茲波生物效應的研究成果顯示有許多潛在的應用,如可用于制定行業安全防護標準,或可能用于人類某些疾病的治療.
5.1 用于制定行業安全防護標準
從目前已有實驗結果來看,當太赫茲波輻照劑量(即一定頻率的太赫茲輻射源強度和輻照時間)達到某個閾值時,將對生物組織和細胞帶來永久性的傷害.如頻率0.1—1 THz 的自由電子激光器太赫茲輻射源輻照生物組織時,其損傷閾值[40]為7.16 W/cm2.使用頻率為2.52 THz、強度為227 mW/cm2的光學泵浦分子氣體太赫茲源輻照Jurkat 細胞的數據顯示,60%的Jurkat 細胞在30 min 的太赫茲暴露中存活,而只有20%的細胞在40 min 的暴露中存活[13].這些結果提醒人們必須考慮太赫茲波的安全性.近年來隨著太赫茲技術更加廣泛和更深入的應用,使用高功率的太赫茲輻射源的場景越來越多,風險也越來越大[64].目前針對太赫茲生物效應的研究尚不夠充分,不同種類不同頻率太赫茲輻射源的損傷閾值數據仍然很有限,因此,針對太赫茲輻射損傷閾值的研究對于制定太赫茲行業安全防護標準以確保潛在暴露人群的安全性至關重要.此外,還有必要研究長期暴露在太赫茲輻射環境下對人體基因和遺傳的慢性影響,這是長期安全使用太赫茲技術的前提和基礎.國內陸軍軍醫大學的余爭平教授團隊開展了多年的相關研究并在近期取得了許多研究進展[38,39].
5.2 用于某些疾病的治療
從目前已有的太赫茲波生物效應研究結果看,太赫茲波潛在的治療作用主要表現在以下6 方面:
1)某些疾病的輔助治療.對某類組織或細胞,較低劑量的太赫茲輻照有一些良性作用,如細胞活性增加,促進血液循環,有可能用于理療,如關節炎、肩周炎等一些慢性疾病局部輔助治療.此外,太赫茲波還有可能用于燒傷創面的治療[33].
2)用于皮膚病治療.強太赫茲脈沖能夠引起與炎癥性皮膚病和皮膚癌相關的多個基因表達的協同有利變化[57],這表明強太赫茲脈沖具有潛在的治療應用價值,有可能發展人類皮膚病的太赫茲波治療新技術.但有關各種皮膚病的太赫茲波生物效應研究目前還較少有相關結果報道,還需要做大量的前期研究工作.
3)用于白血病的治療.對于受強太赫茲波輻照導致的骨髓間質干細胞增殖現象,有可能將來用于白血病的治療.或者利用強場太赫茲波誘導DNA去甲基化治療血癌[63].
4)強太赫茲輻射具有誘導DNA 去甲基化的能力[62],因此可作為表觀遺傳抑制劑,可能在癌癥治療中有潛在的應用價值.
5)用于腫瘤的直接物理治療.目前有關太赫茲波導致癌細胞凋亡[13]或癌組織消融[19]的實驗表明,無論是利用太赫茲波的熱效應還是其非熱效應,都有可能殺死癌細胞或消融癌組織,但最有前途的是有望利用其非熱效應發展太赫茲波無炎癥腫瘤物理治療的新技術,因為不會產生疤痕,尤其適合對美觀度要求較高的部位如面部或身體其他暴露部位的腫瘤以及乳腺癌的治療.當然,對于不同種類的腫瘤,因損傷閾值不同,或者對于同一種類的腫瘤,不同的強太赫茲輻射源對其的損傷閾值也不一樣,所以還需要做大量的前期離體腫瘤細胞凋亡實驗和動物模型實驗,才能用于臨床試驗.
6)太赫茲技術與其他技術相結合的癌癥綜合治療技術.強場太赫波可以增加細胞膜的通透性[14],促進細胞吸納納米顆粒而不引起細胞凋亡、壞死或生理損傷,有可能發展太赫茲波和藥物傳遞綜合治療新技術,用于腫瘤或其他基因疾病的治療.
6 總結和展望
太赫茲波與生物材料的作用可以產生熱效應和非熱效應或者二者兼而有之的生物效應.一般認為熱效應主要來自生物組織或細胞內水分子對太赫茲波的強烈吸收,而非熱效應主要來自于生物大分子的非線性共振效應.究竟是哪種效應占主導地位,依賴于所使用的太赫茲輻射源的特性和指標,如連續波還是脈沖波、脈沖寬度、頻率范圍、單位面積上的輻照能量或輻照功率等因素(即輻照強度或功率密度)、輻照時間以及受輻照的生物材料特性等.無論是熱效應還是非熱效應,如果輻照劑量足夠大,都可能發生在從生物大分子、細胞器、細胞、組織和生物個體的多個層次上,這些不同層次的作用大多相互關聯.從微觀到宏觀來看,太赫茲波對生物大分子的作用通過各種通路和機制最終體現在細胞和組織的結構和功能變化上,以及對生物個體的生理和行為的影響上.
對某類細胞或組織而言,一定輻照劑量的太赫茲波可促進其生長,因而有可能作為某些慢性疾病的理療手段或者某些疾病的綜合治療方案中的輔助治療手段.更強的太赫茲波則是一把雙刃劍,一方面可能會導致細胞凋亡或壞死而損傷正常細胞,提醒人們必須考慮其對操作人員的安全性,基于不同太赫茲波的損傷閾值數據制定相應的安全防護標準.另一方面,可以利用強太赫茲波誘導腫瘤細胞凋亡,或者利用強場太赫茲波增加細胞膜的通透性來介導納米顆粒藥物,讓這些藥物更容易進入靶細胞,從而提高治療效果,縮短治療周期,因而在某些疾病的治療尤其是惡性腫瘤的物理治療等方面可能有巨大的潛在應用價值.
本文歸納了能夠產生太赫茲生物效應的強太赫茲輻射源種類,介紹了兩類生物效應的物理機理,重點綜述了從宏觀到微觀的生物效應的研究成果和進展,最后預測了這些生物效應研究成果可能的潛在應用,全文的邏輯結構如圖9 所示.太赫茲波的生物效應研究也面臨一些挑戰.由于各種太赫茲輻射源的參數不同和生物組織、細胞等生物材料不同,導致實驗結果千差萬別,不同太赫輻射源對不同生物材料產生生物效應的量效關系數據還很有限,到目前為止用于生物效應實驗的生物材料種類還不是很多,實用、經濟的緊湊型強太赫茲輻射源還很缺乏,因此,有關太赫茲波生物效應的研究還需要做大量的工作,尤其是對于太赫茲波對生物材料的量效關系、作用機制和信號通路等還需要更充分和更深入的研究.可以相信,隨著太赫茲技術的不斷進步,越來越多的太赫茲波生物效應的研究成果必將造福于人類生命健康.
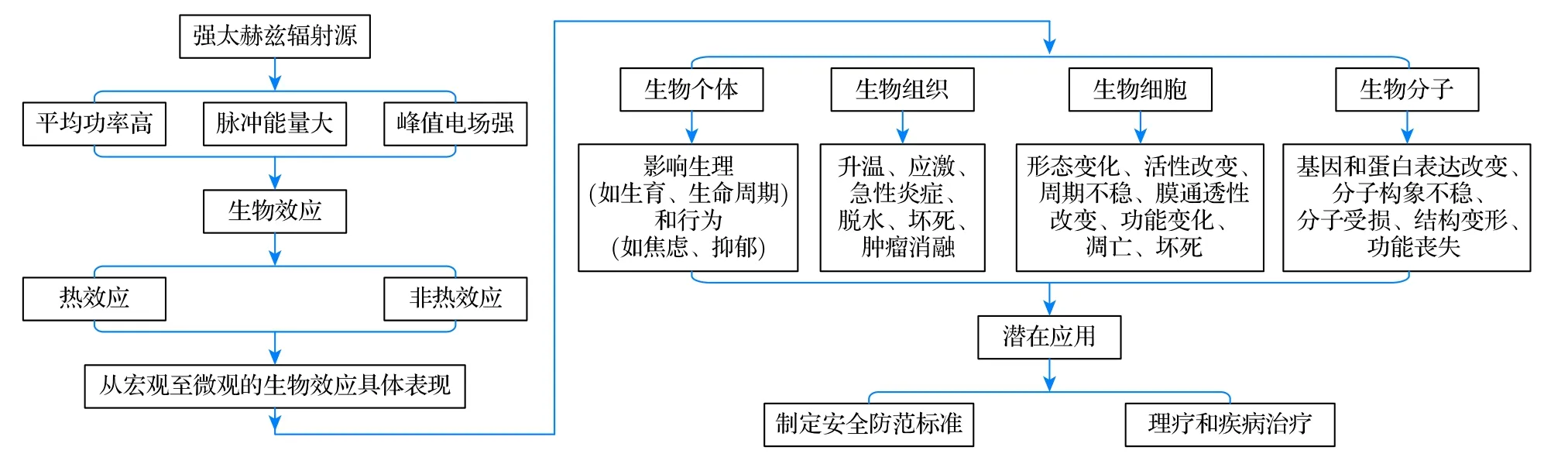
圖9 包括太赫茲波主要生物效應的本文邏輯結構圖Fig.9.Logical structure diagram including the main bio-effects of THz waves summarized in this paper.

