長焰煤低溫干餾失重動力學實驗研究
張學梅,李東,馬青華,郝靜遠
長焰煤低溫干餾失重動力學實驗研究
張學梅1,李東1,馬青華1,郝靜遠2
(1. 西安思源學院 能源及化工大數據應用教學研究中心,陜西 西安 710038;2. 西安交通大學 化工學院,陜西 西安 710038)
用鄂爾多斯盆地東勝長焰煤,在定型的低溫干餾爐中制備20個有不同干餾程度的蘭炭樣品。這些樣品的區別在于是否經過恒速升溫干燥脫水階段、或恒速升溫到達哪個輕微熱解溫度、或在特定恒溫強烈熱解時間的長短。通過恒溫熱解動力學方程先計算3個溫度下強烈熱解階段的失重速率常數后,再計算強烈熱解階段的指前因子和活化能。通過恒速升溫熱解動力學方程分別直接計算脫水階段和輕微熱解階段的指前因子和活化能。結果表明:在460~510 ℃區間的恒溫強烈熱解階段的失重活化能為149.1 kJ·mol-1,失重率最小;從室溫到245 ℃區間的恒速升溫干燥脫水階段的失重活化能為32.3 kJ·mol-1,失重率次之;而從245 ℃開始的恒速升溫輕微熱解階段的失重活化能為19.1 kJ·mol-1,失重率最大。
低溫干餾熱解;溫度時間取樣路線圖;恒速升溫;恒溫熱解;失重動力學
我國的煤階分布是以包括褐煤和長焰煤在內的低階煤為主。長焰煤低溫干餾熱解就是一種針對低階煤高水分、高揮發分和低熱值之不足以改善煤質提高加工利用適用性而采用的提質工藝[1-2]。根據熱解溫度的不同,長焰煤在300~600 ℃的熱解被定義為低溫熱解。在這樣溫度區間,煤的大分子結構開始解聚并分解,生成氣態的熱解氣體、液態的焦油和固態的半焦。我國陜北地區的半焦(蘭炭)生產廠的工藝過程和設備就是基于對長焰煤的低溫干餾原理而設計和操作運行的,所以進一步研究低階煤熱解動力學就具有重要實際意義。因為等溫法和非等溫法的熱重分析技術能夠獲得質量隨時間或/和溫度的變化曲線,所以是研究低階煤熱解動力學的重要手段。有用非等溫熱重分析方法研究了不同粒徑、熱解終溫和升溫速率條件下長焰煤的熱解過程和機理[3-6],針對不同煤種,如超精煤[7]、東勝煤[8]、混煤[9]、蔚州長焰煤[10]、準東煤[11]、新疆煙煤[12],在固定床反應器上研究了N2氣氛中,不同壓力和溫度下的唐山煙煤熱解反應[13]。還有采用熱重-紅 外-質譜聯用技術對4種不同煤種在氮氣氣氛進行熱解特性研究[14];也有研究專門比較煤熱解的單一反應模型和分布活化能[15-16]。雖然等溫法或非等溫法熱重分析有操作周期短、測量精確和獲得信息量多的優點,但卻沒有從初始樣到終止樣之間的固態中間樣。為此本文將根據我國陜北地區的半焦(蘭炭)生產廠的工藝過程和能夠進行熱解動力學數據處理的恒速升溫熱解和恒溫熱解的方式進行實驗。實驗制備一系列具有可比性但卻有不同干餾程度的蘭炭樣品,然后分析初始樣、終止樣和一系列中間樣的熱解失重率,之后進行動力學探討。
1 熱解實驗
本實驗采用相同起始樣加3個階段(干燥脫水階段,輕微熱解階段,460 、485、510 ℃ 3個溫度的強烈熱解階段)19個樣品的溫度時間取樣路線圖。采用HYLZ-2型鋁甑低溫干餾爐制備一系列具有可比性但卻有不同干餾程度的提質煤樣品。
1.1 起始樣
將3 kg產于鄂爾多斯盆地神府-東勝煤田的長焰煤在粉碎機中破碎到1 mm過篩,然后放入60 ℃烘箱中烘烤2 h取出,在空氣中冷卻裝入塑封袋并放入干燥皿中作為起始樣備用,編號“0”。
1.2 干燥脫水樣
將70.0 g起始樣按5 ℃·min-1恒速升溫45 min,從20 ℃升至245 ℃后終止反應,取樣稱重作為干燥脫水階段樣,編號“00”。
1.3 輕微熱解樣
將70.0 g起始樣經過干燥脫水階段和在245 ℃停留5 min后,再以5 ℃·min-1恒速升溫,從245 ℃升至3個不同溫度(460、485、510 ℃,編號分別為“1-1”、“2-1”、“3-1”)后終止反應,取樣稱重,為輕微熱解階段樣。
1.4 強烈熱解樣
強烈熱解樣是在3個不同溫度下5個不同恒溫時間(20、60、120、200、320 min)取的樣。編號“1-2”至“1-6”、“2-2”至“2-6”、“3-2” 至 “3-6”。5個樣分別是在460、485、510 ℃時恒溫不同時間的強烈熱解樣。
在每次新實驗開始時,加入HYLZ-2型低溫干餾爐不銹鋼甑中的起始樣均為70.0克。表1為19次實驗后產物的重量及失重量,溫度時間失重變化見圖1。

表1 20個實驗的產物重量及失重量
從圖1可以看出,以5 ℃·min-1升溫從245 ℃升至3個不同溫度(460、485、510 ℃)的輕微熱解階段單位時間失重量最大;從20 ℃升至245 ℃的干燥脫水階段單位時間失重量其次;而3個不同溫度下不同恒溫時間的強烈熱解階段單位時間失重量最小。同時還可以看出,在恒溫強烈熱解階段,溫度高的單位時間失重量大于溫度低的單位時間失重量。
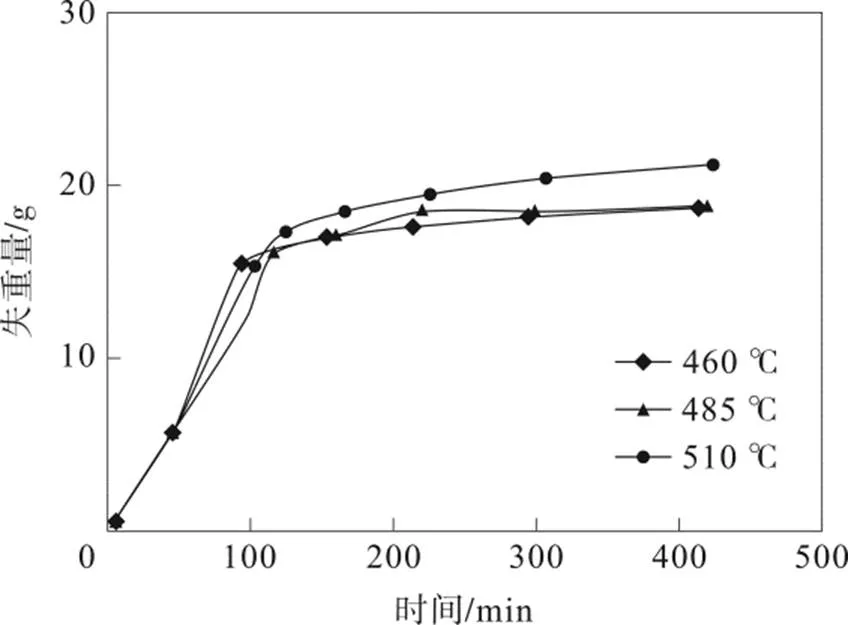
圖1 溫度時間失重圖
2 動力學計算及討論
氣固多相化學反應的反應機理很復雜,通常用于表示反應速率和轉化率之間關系如式(1)所示:

式中:—速度常數,量綱與反應級數有關;
—反應級數;
—轉化率,%。
如果用失重率來代替轉化率,則有式(2):

式中:0—試樣原始量,70.0 g;
—試樣在某一時刻的量,g;
f—試樣終點時殘余量,g。
2.1 恒溫熱解
當=1、恒溫熱解時,失重率只與恒溫的時間有關,即:

根據方程(3),在某一特定溫度下恒溫熱解時,-ln(1-)與時間成直線關系。該直線的斜率為速度常數,截距為積分常數。
Arrhenius equation(式4)是適用于基元和非基元化學反應的速度常數與溫度之間的經驗關系式。

式中:—活化能,kJ·mol-1;
—絕對溫度,K;
—指前因子,min-1;
—氣體常數,8.314 J·mol-1·K-1。
通過式(1)至式(4)計算恒溫熱解樣的失重率及相應數據,結果如表2所示。

表2 恒溫熱解樣品失重率及相應計算數據
根據表2數據,按方程(3)作圖得3個不同溫度下ln(1-)與的關系圖,如圖2所示。

圖2 3個不同溫度下ln(1-α)與t的關系圖
由圖2得到在460、485、510 ℃ 3個溫度下的強烈熱解階段的速度常數和積分常數,如表3所示。

表3 3個溫度下強烈熱解階段的速度常數k和積分常數C
根據表3的數據,按方程(4)作3個不同溫度下lnk與1/的關系圖,如圖3所示。
由圖3可以求得強烈熱解階段的活化能=149.1 kJ·mol-1,指前因子的自然對數ln=18.303。

圖3 3個不同溫度下lnki與1/T的關系圖
2.2 恒速升溫熱解
恒速升溫熱解表示溫度和時間都是變量,但溫度是以恒定速率上升,升溫速率見式(5):

當溫度變化不大時可視為定值。由式(1)、式(4)和式(5)可得:

當=1時,設定初始條件為=0時=0,對方程(6)進行積分得:

方程(7)的右邊為:

根據Doyle近似積分:

結合Doyle近似積分和方程(7)和方程(8)得:
。(10)
根據方程(10)左邊對1/作圖得一直線。該直線的斜率和截距可求指前因子和活化能。恒速升溫熱解階段的活化能和指前因子見表4。

表4 不同階段的活化能和指前因子
從表4可以看出,從245 ℃升至3個不同溫度的輕微熱解活化能在15.38~21.11 kJ·mol-1之間,其平均值是19.13 kJ·mol-1。指前因子則在17.2~6.2之間,其平均值是13.368。大的活化能就跟隨大的指前因子。
按預定溫度時間取樣路線圖從相同起始樣加恒速升溫干燥脫水階段、恒速升溫輕微熱解階段和3個恒溫熱解強烈熱解階段所得20個樣品的失重率可以分別通過恒溫熱解動力學方程計算3個溫度下強烈熱解階段的失重速率常數后,再計算強烈熱解階段的指前因子和活化能;通過恒速升溫熱解動力學方程分別計算脫水階段和輕微熱解階段的指前因子和活化能。表5列出低溫干餾所經歷的3個階段的指前因子和活化能。將3個階段的活化能與相對應3個階段的單位時間失重量進行比較。

表5 3個階段的指前因子和活化能
從表5可以看出,恒溫強烈熱解階段的活化能最大,所以單位時間失重量最小;恒速升溫干燥脫水階段的活化能其次,所以單位時間失重量處于中間;而恒速升溫輕微熱解階段的活化能最小,所以單位時間失重量最大則是必然的。
3 結 論
1)使用定型的低溫干餾爐按相同起始樣加恒速升溫干燥脫水階段、恒速升溫輕微熱解階段和3個溫度的恒溫強烈熱解階段的溫度時間取樣路線圖制備一系列具有可比性但卻有不同干餾程度的蘭炭樣品的方法是可行的。
2)恒溫熱解和恒速升溫熱解是兩個有明確動力學方程的工藝操作。通過恒溫熱解動力學方程計算3個溫度下強烈熱解階段的失重速率常數后,再計算強烈熱解階段的指前因子和活化能。通過恒速升溫熱解動力學方程分別計算脫水階段和輕微熱解階段的指前因子和活化能。
3)在460~510 ℃區間的恒溫強烈熱解階段的失重活化能最大,為149.1 kJ·mol-1;從室溫到 245 ℃區間的恒速升溫干燥脫水階段的失重活化能其次,為32.3 kJ·mol-1;而從245 ℃開始的恒速升溫輕微熱解階段的失重活化能最小,為19.1 kJ·mol-1。
[1] 萬象明,邢國棟,王玉彬.低階煤低溫干餾技術發展分析[J].干燥技術與設備,2015,13(2):1-6.
[2] 翟偉,張紅麗,王榮,等.神府低變質煤的低溫干餾工藝研究[J].煤炭加工與綜合利用,2014(10):78-80.
[3] 李文軍,陳姍姍,陳艷鵬,等 .基于熱重的煤熱解反應動力學試驗研究[J]. 中國煤炭,2020,46(3):84-89.
[4] 李愛蓉,吳道洪,王其成,等.非等溫熱重分析長焰煤熱解過程與動力學特征[J].燃料與化工,2013,44(6):7-11.
[5] 張翠珍,衣曉青,劉亮.煤熱解特性及熱解反應動力學研究[J].熱力發電,2006(4):17-20.
[6] 閔凡飛,張明旭.熱分析在煤燃燒和熱解及氣化動力學研究中的應用[J].煤炭轉化,2004(1):9-12.
[7] 郭龍飛,左海濱,趙駿,等.超精煤熱解行為及動力學研究[J].潔凈煤技術,2018,24(2):40-45.
[8] 鄭明東,白大勇.東勝煤非等溫熱解特性與動力學參數確定[J].煤化工,2006(2):13-16.
[9] 郭延紅,程帆.混煤熱解動力學模型適應性分析[J].燃燒科學與技術,2019,25(6):509-518.
[10] 王子兵,康潤寧,劉玉寶,等.蔚州長焰煤熱解特性及熱解動力學研究[J].煤炭技術,2017,36(1):308-310.
[11] 錢琳,張拯政,馮鵬,等.基于熱重法的準東煤熱解特性研究[J].節能技術,2019,37(3):226-230.
[12] 吳凡,王敏輝.新疆煙煤熱解特性及動力學研究[J].中國煤炭,2019,45(2):84-90.
[13] 吳潔,狄佐星,羅明生,等.N2氣氛下溫度和壓力對煤熱解的影響[J].化工進展,2019,38(S1):116-121.
[14] 劉欽甫,徐占杰,崔曉南,等.不同煤化程度煤的熱解及氮的釋放行為[J].煤炭學報,2015,40(2):450-455.
[15] 楊景標,張彥文,蔡寧生.煤熱解動力學的單一反應模型和分布活化能模型比較[J].熱能動力工程,2010,25(3):301-305.
[16] 趙巖,邱朋華,謝興,等.煤熱解動力學分布活化能模型適用性分析[J].煤炭轉化,2017,40(1):13-18.
[17] 劉鵬華,王紹清,郭強,等.不同煤級均質鏡質體的AFM研究[J].煤炭技術,2019,38(12):88-91.
[18] 尹振勇,許浩,湯達禎,等.不同煤階煤熱解過程中孔隙結構變化規律研究[J].煤炭科學技術,2019,47(9):74-79.
[19] 梁鼎成,解強,黨鉀濤,等.不同煤階煤中溫熱解半焦微觀結構及形貌研究[J].中國礦業大學學 報,2016,45(4):799-806.
Experimental Study on the Weight Loss Dynamics of Low Temperature Long Flame Coal Carbonization
1,1,1,2
(1. Energy & Chemical Engineering Research Center, Xi’an Siyuan University, Xi’an Shannxi 710038, China;2. School of Chemical Engineering, Xi'an Jiaotong University, Xi’an Shannxi 710038, China)
Using the Dongsheng long flame coal of Ordos Basin, 20 samples of semi-coke with different degrees of carbonization were prepared in a retort. The difference between these samples was whether they went through a constant heating of dehydration, or to what temperature of slightly carbonization was reached by constant heating, or to keep how long of intense carbonization isothermally. After calculating the weight loss rate constant of the intense carbonization at three temperatures, the pre-exponential factor and the activation energy were calculated. The pre-exponential factor and the activation energy of both phases of the dehydration and the slightly carbonization were calculated directly. The results showed that, the weight loss activation energy for the intense carbonization was 149.1 kJ·mol-1, for the dehydration was 32.3 kJ·mol-1, and for the slightly carbonization was 19.1 kJ·mol-1.
Low temperature coal carbonization; Temperature-time-sampling road map; Constant heating; Iso-thermal pyrolysis; Weight loss dynamics
陜西省教育廳2020年一般專項科學研究計劃(項目編號:20JK0858)。
2021-05-24
張學梅(1987-),女,陜西省榆林市人,講師,碩士,2012年畢業于鄭州大學化學工程專業,研究方向:煤炭資源高效清潔利用。
TQ523.2
A
1004-0935(2021)12-1753-05

