邯鄲市婦女空氣污染暴露對妊娠期高血壓的影響
曹 蕾,王 婷,王麗君,刁瑞萍,于麗敬,崔小麗,毛洪鈞*
邯鄲市婦女空氣污染暴露對妊娠期高血壓的影響
曹 蕾1,2,王 婷1,2,王麗君1,2,刁瑞萍3,于麗敬3,崔小麗3,毛洪鈞1,2*
(1.南開大學環境科學與工程學院,天津市城市交通污染防治研究中心重點實驗室,天津 300071;2.國家環境保護城市空氣顆粒物污染防治重點實驗室,天津 300350;3.邯鄲市婦幼保健院,河北 邯鄲 056001)
選擇河北省邯鄲市某醫院孕婦數據,探討了6項空氣污染物暴露對孕婦患妊娠期高血壓(GH)的影響和不同人群的效應差異,采用傳統Logistic回歸模型評估了各項污染物的效應,采用主成分改進的Logistic回歸模型評估了各項污染物在額外調整其它污染物后的效應.結果顯示,單污染物模型中,妊娠期前26周每20μg/m3增量的O3暴露與患病風險呈顯著正相關關系(OR=1.211,95%CI:1.094~1.340),且在妊娠前期的效應大于在妊娠中期的效應.多污染物模型中,孕前3個月每20μg/m3增量的PM2.5和PM10暴露顯著增加了患病的風險,OR值分別為1.021(95%CI:1.004~1.038)和1.016(95%CI:1.002~1.031);妊娠期前26周每20μg/m3增量的O3暴露也對患病風險有顯著效應(OR=1.026,95%CI:1.002~1.050).亞組分析結果顯示,25~30歲或初次妊娠的孕婦孕前3個月對PM2.5、PM10、NO2和CO的暴露較為敏感,>35歲或學歷為大學以下的孕婦妊娠期前26周受O3暴露的影響更易患病.總的來說,邯鄲市空氣污染對孕婦患GH存在顯著的影響,孕婦應在孕前和妊娠期間做好防護,降低空氣污染暴露造成的不利影響.
妊娠期高血壓;空氣污染;懷孕;隊列研究
空氣污染是造成全球疾病負擔的一個重要環境風險因素,暴露于空氣污染與多種疾病相關[1-3].作為人口中脆弱的一個亞群體,孕婦及其胎兒因空氣污染而承受更大的疾病負擔[4-7].妊娠期高血壓(GH)是一種妊娠并發癥,對母嬰健康有著極大的危害[6].有研究表明,暴露于空氣污染與全身炎癥和氧化應激有關,這可能與妊娠期間血管重塑和全身功能改變發生相互作用[6].部分流行病學研究發現空氣污染會增加孕婦患GH的風險[8-10],但也有一部分研究并沒有發現二者之間顯著的聯系[7,11],關于空氣污染暴露與GH的關系尚缺乏確鑿的流行病學證據.以往關于孕婦空氣污染暴露與GH關系的研究主要關注妊娠期間的單污染物暴露,往往忽略了孕前暴露的效應.最新的證據表明,孕前3個月可能也是一個關鍵的時間窗口,孕前暴露可能會增加母體的系統性氧化應激或炎癥[12-13].
目前,國內開展的相關研究僅限于深圳、武漢、呼和浩特和蘭州這些大城市或城市群[14-17],然而中小型城市的大氣污染形勢不容忽視[18],其居民健康也值得被關注.邯鄲市是中國北方典型的煤炭重工業城市,除了特殊地形與區域大氣環流的疊加影響外,以煤炭、鋼鐵為主的產業結構導致其空氣質量污染嚴重,秋冬季重污染天氣頻發[19-21].為此,本研究選擇邯鄲市某醫院孕婦數據,利用Logistic回歸模型來分別評估包括可吸入顆粒物(PM10)、可入肺顆粒物(PM2.5)、二氧化硫(SO2)、二氧化氮(NO2)、一氧化碳(CO)和臭氧(O3)在內的各項空氣污染物的孕前暴露和妊娠期暴露對孕婦患GH的影響.由于實際空氣環境中多污染物共存,且污染物之間存在相互作用,本研究進一步將6種污染物同時納入模型,利用主成分改進的Logistic回歸評估了各項空氣污染物在調整其余5項污染物后的效應,旨在探究共暴露環境下單個污染物的效應.此外,對孕婦進行亞組分析以探究空氣污染對不同特征人群的效應差異,為有針對性地保障公眾健康提供參考.
1 資料與方法
1.1 研究區域
本研究隊列人群所在區域為河北省邯鄲市.邯鄲市位于河北省南部,西部為太行山區,東部為華北平原,屬暖溫帶大陸性季風氣候,四季分明,轄6區、11縣和1個縣級市,總面積1.2萬km2,戶籍總人口1057萬,常住人口955萬,人口出生率為11.80%[22].
1.2 研究對象
本研究為一項回顧性隊列研究,研究對象為2018年2月~2020年7月在河北省邯鄲市婦幼保健院住院分娩的婦女.邯鄲市婦幼保健院每年接收邯鄲市超過一半的孕婦分娩,病例數據覆蓋全市范圍,醫院的記錄詳細介紹了產婦和胎兒的特征以及懷孕和分娩的臨床數據.
1.3 疾病診斷標準
GH:收縮壓/舒張壓3140/90mmHg (間隔6h,至少2次),無蛋白尿,妊娠20周后首次出現,血壓于產后12周恢復正常.如伴有其他表現,如頭痛、視物不清、上腹不適或血小板減少等應高度懷疑子癇前期.
1.4 空氣污染物暴露評估
從邯鄲市生態環境局獲取44個監測站點(包括國控站點和省控站點)2017~2020年的6項污染物濃度數據.孕婦和監測站點的分布情況如圖1所示.由于監測站點數量足夠多,且空間覆蓋率較好,因此本研究采用目前公共衛生領域常用的近鄰模型來評估個體暴露水平.近鄰模型是根據空氣污染源與研究對象之間距離的遠近估算研究對象的暴露水平,直接將個體住宅最近監測站點的暴露水平賦值給個體[23].該方法不僅簡單易行,且提供了較高的時間分辨率.根據每位孕婦的孕周和分娩日期計算了以下幾個窗口的平均暴露情況:(1)孕前3個月(孕前13周,Pre_T);(2)妊娠早期(第1~13孕周,T1);(3)妊娠中期(第14~26孕周,T2);(4)妊娠期前26周(T).為了確保暴露在結果之前,沒有考慮妊娠26周之后的暴露.
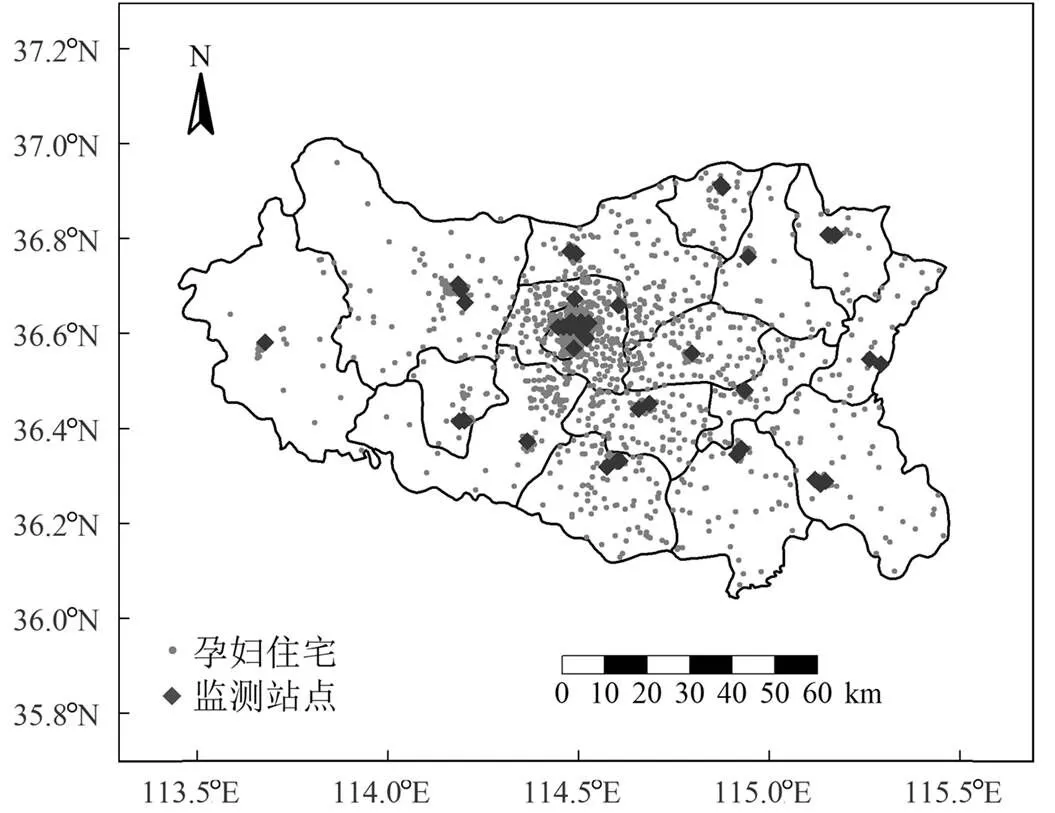
圖1 孕婦的住宅和監測站點分布
1.5 統計學分析
由于所選受試人群的特征皆為分類變量,用2檢驗比較了患GH的孕婦和不患GH的孕婦在所選特征上的差異.另外,不同暴露窗口的污染物平均暴露濃度之間的相關性通過Spearman相關系數展示.


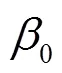



為了便于結果討論及與其他文獻數據作對比,將污染物濃度作為連續變量來表示研究結果,分別計算了各暴露窗口PM和O3每20μg/m3、SO2和NO2每10μg/m3、CO每0.5mg/m3的增量與患GH風險的OR和95%CI.研究結果分為調整和未調整混雜變量的效應,混雜變量包括年齡(<25,25~30,30~35,>35歲)、教育程度(大學以下、大學及以上)、醫保類型(自費、職工醫保、城鄉醫保)、孕次(初次、非初次)、懷孕年份(2017,2018,2019年)、懷孕季節(春、夏、秋、冬)和不良孕產史(有、無).未調整混雜變量的單污染物模型的自變量僅包含一種污染物,調整混雜變量的單污染物模型的自變量包括一種污染物和所有混雜變量.
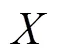
研究結果分為調整和未調整混雜變量的效應,未調整混雜變量的多污染物模型的自變量包含6種污染物的主成分變量,調整混雜變量的多污染物模型的自變量包括6種污染物和所有混雜變量的主成分變量.
此外,根據孕婦的年齡、孕次、不良孕產史和教育程度劃分人群,分別用單污染物模型和多污染物模型進行亞組分析,亞組分析調整了除分組因素外所有的混雜因素.以上所有的統計學分析采用R軟件(版本3.5.3)完成,采用雙側檢驗,檢驗水準=0.05.
2 結果與分析
2.1 邯鄲市空氣污染情況
2017~2020年邯鄲市空氣污染物的年均濃度如表1所示.污染物的年均濃度是全年365d (2020年366d)日均濃度的平均值,污染物的日均濃度是當日所有監測站點數據的算術平均值,監測點收集數據完整性和一致性均符合國家環境空氣質量監測規范要求,其中O3濃度為日最大8h均值,其他項均為24h均值.研究期間,邯鄲市PM2.5和PM10的年均污染水平遠高于《環境空氣質量標準》(GB 3095-2012)的二級濃度限值[27],SO2的年均污染水平遠低于二級標準.邯鄲市2017年NO2的年均污染水平略高于二級標準,2019~2020年NO2的年均污染水平均低于二級標準.2017~2020年CO和O3的年均污染水平遠未達到二級標準中的日24h均值或日最大8h均值標準.

表1 2017~2020年邯鄲市空氣污染物的年均濃度
2.2 孕婦信息描述性分析
2018年2月~2020年7月在河北省邯鄲市婦幼保健院住院分娩的孕婦信息的統計學描述如表2所示.本研究在排除了多胎分娩、胎齡<20周、妊娠前患慢性高血壓和信息缺失的孕婦后,最終將9820位孕婦納入研究.其中患GH的孕婦占比7.89%;孕婦年齡主要集中在25~35歲之間,約占總人群的74.24%;超過一半的孕婦學歷在大學及以上;約21.22%的孕婦無醫保;一半多的孕婦有妊娠經歷;約30.48%的孕婦有不良孕產史.

表2 孕婦信息的統計學描述

表3 不同暴露窗口的污染物平均濃度的相關性分析
2檢驗的結果顯示,除懷孕年份和懷孕季節外,患病與未患病的孕婦在其余特征上有著顯著的差異.與未患GH的孕婦相比,患GH的孕婦普遍年齡偏大(>30歲)、教育程度偏高(學歷為大學及以上),而且,初次懷孕和有不良孕產史的孕婦患GH的幾率較大.
2.3 孕婦空氣污染暴露情況
表3為孕婦不同暴露窗口的污染物平均濃度的Spearman相關性分析.根據Spearman相關系數,各窗口污染物之間的相關性較強,因此無法將任意兩種污染物直接同時納入Logistic回歸模型.
2.4 空氣污染物與GH發病率之間的關系
2.4.1 單污染物模型 表4顯示了單污染物Logistic回歸模型中各污染物未調整和調整混雜變量的OR和95%CI.在未調整混雜變量的單因素回歸模型中,Pre_T時期的CO暴露每增加0.5mg/m3,GH的患病風險就會增加8.4% (OR=1.084, 95% CI: 1.006~1.169).在調整了混雜變量的模型中,T時期每20μg/m3增量的O3暴露與GH風險呈顯著正相關關系(OR=1.211, 95% CI: 1.094~1.340),且O3暴露在T1時期的效應要高于在T2時期的效應,OR值分別為1.128 (95% CI: 1.046~1.218)和1.093 (95% CI: 1.015~1.177).
圖2A展示了單污染物模型調整混雜變量后空氣污染對不同年齡段孕婦的效應.對于25~30歲的孕婦,Pre_T時期的PM2.5、PM10、NO2和CO暴露顯著增加了其患GH的風險,OR值分別為1.316 (95% CI: 1.094~1.583)、1.189 (95% CI: 1.060~1.334)、1.249 (95% CI: 1.056~1.479)和1.261 (95% CI: 1.056~1.506);T時期尤其T2時期的O3暴露也對其患GH有顯著效應(OR=1.223, 95% CI: 1.074~1.393).對于>35歲的孕婦,T時期尤其T1時期的O3暴露每增加20μg/m3,其患GH的風險就會增加39% (OR=1.390, 95% CI: 1.158~1.670).
圖2B展示了單污染物模型調整混雜變量后空氣污染對不同孕次孕婦的效應.對于初次妊娠的孕婦, Pre_T時期的PM2.5、PM10和CO暴露顯著增加了其患GH的風險,OR值分別為1.219 (95% CI: 1.051~1.414)、1.122 (95% CI: 1.022~1.231)和1.195 (95% CI: 1.033~1.382).T時期每20μg/m3增量的O3暴露對初次妊娠和非初次妊娠的孕婦患GH的風險都有顯著效應,但初次妊娠孕婦的效應值更大(OR=1.241, 95% CI: 1.074~1.433).

表4 單污染物模型中各污染物的效應
注:a表示模型還調整了年齡、教育程度、醫保類型、孕次、懷孕年份、懷孕季節和不良孕產史,*表示<0.05,加粗表示污染物為危險因素.
圖2C展示了單污染物模型調整混雜變量后空氣污染對是否有不良孕產史孕婦的效應.對于無不良孕產史的孕婦,T時期尤其T1時期的O3暴露每增加20μg/m3,其患GH的風險就會增加15.3% (OR= 1.153, 95% CI: 1.054~1.262).
圖2D展示了單污染物模型調整混雜變量后空氣污染對不同教育程度孕婦的效應.與大學及以上學歷的孕婦相比,大學以下學歷的孕婦在T時期受O3暴露的影響更大,每20μg/m3增量的O3暴露增加其26.6%患GH的風險(OR=1.266, 95% CI: 1.092~1.467).

*表示<0.05
2.4.2 多污染物模型 表5展示了多污染物Logistic回歸模型中各污染物未調整和調整混雜變量的OR和95% CI.在未調整其余混雜變量的模型中,污染物暴露對孕婦患GH風險無顯著效應.當模型調整了混雜變量后,Pre_T時期每20μg/m3增量的PM2.5、PM10和每10μg/m3增量的NO2暴露對孕婦患GH風險有顯著效應,OR值分別為1.021 (95% CI: 1.004~1.038)、1.016 (95% CI: 1.002~1.031)和1.018 (95% CI: 1.000~1.037);T1時期的PM2.5暴露也顯著增加了孕婦患GH的風險(OR=1.011, 95% CI: 1.000~1.024);T時期的O3暴露每增加10μg/m3,孕婦患GH的風險增加2.6% (OR=1.026, 95% CI: 1.002~ 1.050).
圖3A~D分別展示了多污染物模型調整混雜變量后空氣污染對不同年齡段、不同孕次、是否有不良孕產史和不同教育程度的孕婦的效應.對于>35歲的的孕婦,T時期的O3每增加20μg/m3,孕婦患GH的風險增加9.5% (OR=1.095, 95% CI: 1.033~1.162).對于初次妊娠的孕婦,Pre_T時期每10μg/m3的NO2增量會增加其患GH的風險,OR值為1.034 (95% CI: 1.001~1.068).多污染物模型中,各污染物對不同教育水平的孕婦患GH無顯著效應.對于有不良孕產史的孕婦,T時期每20μg/m3增量的PM2.5、PM10和Pre_T時期每10μg/m3增量的NO2對其患GH有顯著效應,OR值分別為1.059 (95% CI: 1.011~1.109)、1.038 (95% CI: 1.010~1.066)和1.047 (95% CI: 1.004~1.092).對于無不良孕產史的孕婦,T1時期的O3每增加20μg/m3,孕婦患GH的風險增加2.3% (OR=1.023, 95% CI: 1.004~1.042).各污染物對不同教育程度的孕婦患GH的效應無顯著差異.
3 討論
作為一個污染嚴重、人口眾多的城市,邯鄲的數據具有一定的代表性和普遍性.本研究用Logistic回歸模型評估了邯鄲市各項空氣污染物對某醫院孕婦患GH的效應.研究結果包括調整和未調整混雜變量的效應,實際上這些混雜因素是影響孕婦患GH的主要原因[28-30],因此在探究空氣污染物對孕婦患GH的影響時,調整混雜變量的模型結果更接近實際效應.調整混雜變量的單污染物模型結果顯示,T時期除O3外其余污染物對孕婦患GH風險增加均無顯著的統計學意義.先前的研究已經證明GH和暴露于空氣污染物可能有很強的關聯[8-10],例如,兩項美國的研究得出妊娠期PM2.5和NO2暴露與GH風險呈正相關關系[9,31],另一項荷蘭的研究發現暴露于PM10和CO與GH風險增加有關[32].由于研究人群、研究環境、研究設計方案和暴露評估方法等因素的不同,研究結果在各個研究中并不一致,未來需要更多的研究來支持這一發現.另外,結果顯示O3暴露在T1時期的效應要高于在T2時期的效應.因此,妊娠早期可能是發生GH的關鍵易感窗口,這可能是因為這一時期的空氣污染會干擾母體血管重塑過程[10,33].一項來自美國的研究也發現與妊娠中期相比,妊娠早期的O3暴露對孕婦患GH的影響更大(ORT1=1.04, 95% CI: 1.03~1.06; ORT2=1.03, 95% CI: 1.02~1.04)[34].

表5 多污染物模型中各污染物的效應
注:a表示模型還調整了年齡、教育程度、醫保類型、孕次、懷孕年份、懷孕季節和不良孕產史,*表示<0.05,加粗表示污染物為危險因素.

*表示<0.05
調整混雜變量的多污染物模型結果顯示,Pre_T時期的PM2.5和PM10暴露對孕婦患GH風險有顯著效應,這說明孕前暴露也是一個關鍵的暴露窗口.之前有研究調查了孕前空氣污染暴露與孕婦患子癇前期和妊娠期糖尿病的關系[12-13,35-37],結果顯示出顯著的正相關關系,本研究結果也佐證了孕前暴露于空氣污染對孕婦患產科并發癥的不良影響.另外,與單污染物模型相比,多污染物模型中T時期的O3暴露對孕婦患GH的效應偏低,這說明T時期其余污染物的共暴露也是影響孕婦患GH的危險因素,在未調整其余污染物的單污染物模型高估了O3暴露的效應.幾項國外的研究顯示,單污染物模型中的污染物效應要高于雙污染物模型中的污染物效應[9,13,38-40],一項北京的研究也發現在多污染物模型中,分別引入SO2或(和)NO2后,PM10與全人群系統疾病門診人數的關聯減弱[41].由于污染物彼此間較強的相關性,以往研究為了避免模型中出現多重共線性問題,只調整了與被研究污染物相關性相對較弱的污染物.實際環境種各空氣污染物共存,各污染物對孕婦患GH可能存在協同/拮抗效應,因此需要調整目標污染物外的其余污染物的影響,使用包含多個污染物的多污染物模型,更能反映共暴露環境下單污染物的效應.
在依據孕婦年齡進行的亞組分析中,Pre_T時期的PM2.5、PM10、NO2和CO暴露顯著增加了25~30歲的孕婦患GH的風險.一方面,邯鄲市PM2.5、PM10、NO2和CO主要來源于交通源和工業源排放[19], 25~30歲的孕婦大部分為上班族,通常由于工作、生活等原因每天有固定的時間接受交通和環境中空氣污染的暴露.另一方面,從暴露窗口來看,備孕階段防護意識薄弱可能也是25~30歲的孕婦成為敏感人群的一個重要原因.另外,結果還表明>35歲的孕婦為T時期O3暴露的敏感人群,這與Choe等[39]的研究結果一致,其發現與25~29歲的孕婦相比,30歲以上的孕婦在妊娠期間受空氣污染影響患妊娠期糖尿病的風險隨著年齡增加而增大.這可能是因為高齡孕婦的脂代謝能力較差,受空氣污染影響更易誘發或加重動脈粥樣硬化等疾病的發生[42].
就孕次分層結果而言,Pre_T時期的PM2.5、PM10、NO2和CO暴露顯著增加了初次妊娠的孕婦患GH的風險.一項武漢的研究結果也顯示初產孕婦為空氣污染的敏感人群,每10μg/m3增量的NO2對初產孕婦患妊娠期糖尿病的OR值為1.40 (95% CI: 1.14~1.72)[43].有研究認為初次妊娠本身是孕婦患GH的一個高危因素,胎兒來源的絨毛初次暴露,母體對其免疫應答異常導致GH發生[44-45],而母體暴露于空氣污染可能會加重這種免疫反應.另外,初次妊娠的孕婦由于缺乏經驗和備孕意識,更容易發生意外懷孕,缺失孕前的準備和防護,成為孕前空氣污染暴露的敏感人群.
本研究還發現不良孕產史在空氣污染與孕婦患GH之間的中介作用,但亞組人群對于空氣污染暴露的敏感程度因污染物而異.王偉業[43]的研究表明無流產史的孕婦和有糖尿病史的孕婦受NO2污染暴露更易患妊娠期糖尿病.不良孕產史病因復雜,主要歸因于遺傳因素、解剖因素、內分泌因素、免疫因素和感染因素[46].由于本文的原始信息缺少不良孕產史孕婦的詳細病因,譬如是否先前患妊娠期高血壓類疾病導致了不良孕產結局,或者是否先前妊娠期空氣污染暴露是不良孕產結局的原因之一,因此無法得出結論,有/無不良孕產史的孕婦是空氣污染的敏感人群,需要進一步的研究來確定這一結果.
在單污染物模型調整混雜變量后依據孕婦教育程度進行的亞組分析中,大學以下學歷的孕婦對于妊娠期間的空氣污染暴露更加敏感.這與之前的研究結果一致,張曉彤[47]在武漢的研究和Choe等[39]在紐約的研究都顯示受教育年限小于9a的孕婦受空氣污染影響更易發生早產或患妊娠期糖尿病.這可能是因為未受高等教育年的孕婦大部分社會經濟地位較低,妊娠期接受室外空氣污染暴露的總時長較長,或由于圍產期保健知識和防護意識的匱乏導致忽略了對空氣污染的防護[48].另外,是否受高等教育的孕婦在基礎健康狀態也可能存在差異.
綜上所述,孕前和妊娠期間的空氣污染物高暴露濃度對孕婦患GH的風險存在不良效應,且這種效應在不同人群中存在一定差異.2017~2020年邯鄲市CO和O3的年均污染水平遠未達到環境空氣質量二級標準中8h均值標準,NO2的年均污染水平除2017年外也基本未超標(表1).由于發展水平和對環境質量重視程度存在一定差距,各個國家制定的環境空氣質量標準有所不同.與其他國家相比,我國NO2二級標準(40μg/m3)已處于國際領先水平,但略低于韓國和澳大利亞(30μg/m3),O3二級標準(160μg/m3)還有很大的修訂空間,CO濃度限值在國際上已經比較嚴格[49-51].本研究中,單污染物模型結果顯示CO是一個顯著的危險因素,這可能是因為其余污染物的共暴露也是影響孕婦患GH的危險因素,在未調整其余污染物的單污染物模型高估了CO暴露的效應;排除其余污染物影響的多污染物模型結果顯示,NO2與O3為孕婦患GH的危險因素,在污染水平相近的其他地區,如美國、丹麥和日本,研究人員也發現NO2[7,23,38]和O3[12,33-34]會增加孕婦患GH的風險,因此可能需要評估和反思我國現行NO2與O3限值標準的科學性,今后的標準既要參考發達國家,也要依據國民自身情況進行進一步的嚴格控制.
本研究是首個評估常規空氣污染物在調整了其余污染物之后的效應的研究,巧妙地利用主成分改進的Logistic回歸模型解決了納入模型的污染物之間的共線性問題,使得結果更接近實際暴露情況.另一個優點是,本研究將孕前3個月作為一個可能的暴露窗口,探究了其間空氣污染暴露對孕婦患GH的效應.同時,本研究也存在一些不足之處,由于原始數據中信息的缺失,沒能調整一些可能重要的混雜變量,包括孕婦體重指數、孕婦飲酒、孕婦壓力和噪音暴露等.其次,由于所獲得數據的局限性,沒有關于懷孕期間孕婦流動性的信息,單純將住宅地址的暴露賦值給孕婦,無法細致地評估孕婦在工作地點的暴露情況,這在未來有待進一步研究.
4 結論
4.1 單污染物模型中,妊娠期前26周每20μg/m3增量的O3暴露與GH風險呈顯著正相關關系,且在妊娠早期的效應要高于在妊娠中期的效應,妊娠早期可能是發生GH的關鍵易感窗口.
4.2 多污染物模型中,孕前每20μg/m3增量的PM2.5和PM10暴露與孕婦患GH呈顯著正相關關系,孕前3個月也是一個關鍵的暴露窗口;妊娠期前26周的O3暴露對孕婦患GH風險也有顯著效應,且與單污染物模型的結果相比效應偏低,空氣污染物共暴露對孕婦患GH的風險可能存在協同效應.
4.3 亞組分析結果顯示,25~30歲或初次妊娠的孕婦為孕前3個月PM2.5、PM10、NO2和CO暴露的易感人群;>35歲或大學以下學歷的孕婦受妊娠期前26周O3暴露的影響更易患GH.
[1] Fan S J, Heinrich J, Bloom M S, et al. Ambient air pollution and depression: A systematic review with meta-analysis up to 2019 [J]. Science of the Total Environment, 2020,701:134721.
[2] Nardone A, Neophytou A M, Balmes J, et al. Ambient air pollution and asthma-related outcomes in children of color of the USA: A scoping review of literature published between 2013 and 2017 [J]. Current Allergy and Asthma Reports, 2018,18(5):29.
[3] Rajagopalan S, Al-Kindi S G, Brook R D. Air pollution and cardiovascular disease JACC state-of-the-art review [J]. Journal of the American College of Cardiology, 2018,72(17):2054-2070.
[4] Murray C J L, Aravkin A Y, Zheng P, et al. Global burden of 87 risk factors in 204 countries and territories, 1990~2019: A systematic analysis for the global burden of disease study 2019 [J]. The Lancet, 2020,396(10258):1223-1249.
[5] Jacobs M, Zhang G C, Chen S, et al. The association between ambient air pollution and selected adverse pregnancy outcomes in China: A systematic review [J]. Science of the Total Environment, 2017,579: 1179-1192.
[6] Madsen C, Haberg S E, Aamodt G, et al. Preeclampsia and hypertension during pregnancy in areas with relatively low levels of traffic air pollution [J]. Maternal and Child Health Journal, 2018, 22(4):512-519.
[7] Pedersen M, Halldorsson T I, Olsen S F, et al. Impact of road traffic pollution on pre-eclampsia and pregnancy-induced hypertensive disorders [J]. Epidemiology, 2017,28(1):99-106.
[8] Zhu Y, Zhang C, Liu D, et al. Ambient air pollution and risk of gestational hypertension [J]. American Journal of Epidemiology, 2017,186(3):334-343.
[9] Savitz D A, Elston B, Bobb J F, et al. Ambient fine particulate matter, nitrogen dioxide, and hypertensive disorders of pregnancy in New York City [J]. Epidemiology, 2015,26(5):748-757.
[10] Lee P C, Roberts J M, Catov J M, et al. First trimester exposure to ambient air pollution, pregnancy complications and adverse birth outcomes in Allegheny County, PA [J]. Maternal and Child Health Journal, 2013,17(3):545-555.
[11] Choe S A, Kauderer S, Eliot M N, et al. Air pollution, land use, and complications of pregnancy [J]. Science of the Total Environment, 2018,645:1057-1064.
[12] Mendola P, Wallace M, Liu D, et al. Air pollution exposure and preeclampsia among US women with and without asthma [J]. Environmental Research, 2016,148:248-255.
[13] Jo H, Eckel S P, Chen J C, et al. Associations of gestational diabetes mellitus with residential air pollution exposure in a large Southern California pregnancy cohort [J]. Environment International, 2019, 130:104933.
[14] Wang Q, Zhang H, Liang Q, et al. Effects of prenatal exposure to air pollution on preeclampsia in Shenzhen, China [J]. Environmental Pollution, 2018,237:18-27.
[15] 楊明翰.大氣細顆粒物暴露與孕婦妊娠期血壓變化的關聯 [D]. 武漢:華中科技大學, 2019.
Yang M H. Association between atmospheric fine particle exposure and blood pressure changes in pregnant women during pregnancy [D]. Wuhan: Huazhong University of Science and Technology, 2019.
[16] 趙伯毅.呼和浩特市空氣污染與妊娠疾病及不良出生結局關系研究 [D]. 呼和浩特:內蒙古大學, 2020.
Zhao B Y. The association between air pollution exposure and pregnancy diseases and adverse birth outcomes in Hohhot [D]. Hohhot: Inner Mongolia University, 2020.
[17] Huang X, Qiu J, Zhang Y, et al. Ambient air pollutant PM10and risk of pregnancy-induced hypertension in urban China [J]. Environmental Research Letters, 2015,10(8):084025.
[18] 許亞宣,李小敏,于華通,等.邯鄲市大氣復合污染特征的監測研究 [J]. 環境科學學報, 2015,35(9):2710-2722.
Xu Y X, Li X M, Yu H T, et al. Characteristics of air pollution complex in Handan [J]. Acta Scientiae Circumstantiae, 2015,35(9): 2710-2722.
[19] 李福燕,李許明,付 沖,等.邯鄲市區空氣污染現狀及其防治措施 [J]. 環境衛生學雜志, 2015,5(4):357-360.
Li F Y, Li X M, Fu C, et al. Air pollution and prevention measures in Handan [J]. Journal of Environmental Hygiene, 2015,5(4):357-360.
[20] 彭 玏,趙媛媛,趙吉麟,等.京津冀大氣污染傳輸通道區大氣污染時空格局研究 [J]. 中國環境科學, 2019,39(2):449-458.
Peng L, Zhao Y Y, Zhao J L, et al. Spatiotemporal patterns of air pollution in air pollution transmission channel of Beijing-Tianjin- Hebei from 2000 to 2015 [J]. China Environmental Science, 2019, 39(2):449-458.
[21] 伯 鑫,徐 峻,杜曉惠,等.京津冀地區鋼鐵企業大氣污染影響評估 [J]. 中國環境科學, 2017,37(5):1684-1692.
Bo X, Xu J, Du X H, et al. Impacts assessment of steel plants on air quality over Beijing-Tianjin-Hebei area [J]. China Environmental Science, 2017,37(5):1684-1692.
[22] 邯鄲市人民政府.邯鄲市綜合概況[EB/OL]. http://www.hd.gov.cn/ zjhd/hdgk/zhgk/202103/t20210324_1435054.html, 2021-04-27.
Handan Municipal People's Government. Comprehensive overview of Handan City [EB/OL]. http://www.hd.gov.cn/zjhd/hdgk/zhgk/202103/ t20210324_1435054.html, 2021-04-27.
[23] Xu X, Hu H, Ha S, et al. Ambient air pollution and hypertensive disorder of pregnancy [J]. Journal of Epidemiology and Community Health, 2014,68(1):13-20.
[24] 行岳真,祁 瑞,李金梅,等.主成分Logistic回歸在篩選冠心病危險因素中的應用 [J]. 實用預防醫學, 2012,19(8):1138-1140.
Xing Y Z, Qi R, Li J M, et al. Application of logistic regression based on principal component analysis in the screening of risk factors of coronary heart disease [J]. Practical Preventive Medicine, 2012,19(8): 1138-1140.
[25] 裘炯良,鄭劍寧,張 揚.主成分改進的Logistic回歸模型方法在流行病學分析中的應用 [J]. 中國熱帶醫學, 2005,5(2):207-209.
Qiu J L, Zheng J N, Zhang Y. Application of modified logistic regression model in the analysis of epidemiology [J]. China Tropical Medicine, 2005,5(2):207-209.
[26] 王 丹,潘曉平.主成分logistic回歸在篩選妊娠期糖尿病危險因素中的應用 [J]. 現代預防醫學, 2008,35(5):826-827,830.
Wang D, Pan X P. Application of logistic regression based on principal component analysis on risk factors of women with gestational diabetes mellitus [J]. Modern Preventive Medicine, 2008,35(5):826-827,830.
[27] GB 3095-2012 環境空氣質量標準 [S].
GB 3095-2012 Ambient air quality standards [S].
[28] 顧 穎,馮亞玲,許 倩.妊娠期高血壓疾病的相關危險因素分析 [J]. 中國衛生統計, 2017,34(4):618-619,624.
Gu Y, Feng Y L, Xu Q. Risk factors of hypertension in pregnancy [J]. Chinese Journal of Health Statistics, 2017,34(4):618-619,624.
[29] 林 彤,陳麗紅,胡繼芬,等.妊娠期高血壓的危險因素 [J]. 中華高血壓雜志, 2015,23(1):83-85.
Lin T, Chen L H, Hu J F, et al. Risk factors for hypertension during pregnancy [J]. Chinese Journal of Hypertension, 2015,23(1):83-85.
[30] 張秀蘭,袁碧波,李增彥.妊娠期高血壓疾病發生的危險因素及預防措施分析[J]. 中國婦幼保健, 2017,32(17):4052-4054.
Zhang X L, Yuan B B, Li Z Y. Analysis of risk factors and preventive measures of hypertensive diseases during pregnancy [J]. Maternal and Child Health Care of China, 2017,32(17):4052-4054.
[31] Nobles C J, Williams A, Ouidir M, et al. Differential effect of ambient air pollution exposure on risk of gestational hypertension and preeclampsia [J]. Hypertension, 2019,74(2):384-390.
[32] van den Hooven E H, de Kluizenaar Y, Pierik F H, et al. Air pollution, blood pressure, and the risk of hypertensive complications during pregnancy: The generation R study [J]. Hypertension, 2011,57(3): 406-412.
[33] Mobasher Z, Salam M T, Goodwin T M, et al. Associations between ambient air pollution and Hypertensive Disorders of Pregnancy [J]. Environmental Research, 2013,123:9-16.
[34] Hu H, Ha S, Xu X. Ozone and hypertensive disorders of pregnancy in Florida: Identifying critical windows of exposure [J]. Environmental Research, 2017,153:120-125.
[35] Rudra C B, Williams M A, Sheppard L, et al. Ambient carbon monoxide and fine particulate matter in relation to preeclampsia and preterm delivery in western Washington State [J]. Environmental Health Perspectives, 2011,119(6):886-892.
[36] Najafi M L, Zarei M, Gohari A, et al. Preconception air pollution exposure and glucose tolerance in healthy pregnant women in a middle-income country [J]. Environmental Health, 2020,19(1):131.
[37] Robledo C A, Mendola P, Yeung E, et al. Preconception and early pregnancy air pollution exposures and risk of gestational diabetes mellitus [J]. Environmental Research, 2015,137:316-322.
[38] Michikawa T, Morokuma S, Fukushima K, et al. A register-based study of the association between air pollutants and hypertensive disorders in pregnancy among the Japanese population [J]. Environmental Research, 2015,142:644-650.
[39] Choe S A, Eliot M N, Savitz D A, et al. Ambient air pollution during pregnancy and risk of gestational diabetes in New York City [J]. Environmental Research, 2019,175:414-420.
[40] Pan S C, Huang C C, Lin S J, et al. Gestational diabetes mellitus was related to ambient air pollutant nitric oxide during early gestation [J]. Environmental Research, 2017,158:318-323.
[41] 張 瑩,邵 毅,王式功,等.北京市空氣污染物對呼吸系統疾病門診人數的影響 [J]. 中國環境科學, 2014,34(9):2401-2407.
Zhang Y, Shao Y, Wang S G, et al. Relationship between air pollutant and respiratory diseases hospital outpatient visits in Beijing [J]. China Environmental Science, 2014,34(9):2401-2407.
[42] 劉 情,王笑笑,張英奎,等.河北省2016年婦女妊娠期高血壓疾病與年齡的相關性分析 [J]. 中華流行病學雜志, 2018,39(9):1270-1273.
Liu Q, Wang X X, Zhang Y K, et al. Correlation analysis of hypertensive disease during pregnancy and age in Hebei Province in 2016 [J]. Chinese Journal of Epidemiology, 2018,39(9):1270-1273.
[43] 王偉業.武漢市孕婦孕期NO2暴露與胎兒生長及妊娠期糖尿病關系研究 [D]. 武漢:華中科技大學, 2017.
Wang W Y. Gestational diabetes mellitus and fetal growth in association with maternal NO2exposure during pregnancy in Wuhan city [D]. Wuhan: Huazhong University of Science and Technology, 2017.
[44] Shiozaki A, Matsuda Y, Satoh S, et al. Comparison of risk factors for gestational hypertension and preeclampsia in Japanese singleton pregnancies [J]. Journal of Obstetrics and Gynaecology Research, 2013,39(2):492-499.
[45] Li X, Tan H Z, Huang X, et al. Similarities and differences between the risk factors for gestational hypertension and preeclampsia: A population based cohort study in south China [J]. Pregnancy Hypertension-an International Journal of Womens Cardiovascular Health, 2016,6(1):66-71.
[46] Lao T T, Hui A S Y, Law L W, et al. Prior abortion history and pregnancy hypertensive disorders in primiparous gravidae [J]. Pregnancy Hypertens, 2018,14:168-173.
[47] 張曉彤.武漢市孕婦孕期空氣細顆粒物暴露與早產的關聯性研究 [D]. 武漢:武漢大學, 2020.
Zhang X T. The association between maternal PM2.5exposure and preterm birth in Wuhan [D]. Wuhan: Wuhan University, 2020.
[48] Ng C, Malig B, Hasheminassab S, et al. Source apportionment of fine particulate matter and risk of term low birth weight in California: Exploring modification by region and maternal characteristics [J]. Science of the Total Environment, 2017,605-606:647-654.
[49] 董 潔,李夢茹,孫若丹,等.我國空氣質量標準執行現狀及與國外標準比較研究 [J]. 環境與可持續發展, 2015,40(5):87-92.
Dong J, Li M R, Sun R D, et al. Study on the air quality standards of china and comparative with foreign standards [J]. Environment and Sustainable Development, 2015,40(5):87-92.
[50] 郭 超,郜 志.關于國內外臭氧限值濃度標準的探究 [J]. 建筑科學, 2020,36(2):163-170,199.
Guo C, Gao Z. Research on ozone limit concentration standards at home and abroad [J]. Building Science, 2020,36(2):163-170,199.
[51] 王宗爽,武 婷,車 飛,等.中外環境空氣質量標準比較 [J]. 環境科學研究, 2010,23(3):253-260.
Wang Z S, Wu T, Che F, et al. Comparison between domestic and international ambient air quality standards [J]. Research of Environmental Sciences, 2010,23(3):253-260.
Maternal exposure to ambient air pollution and gestational hypertension in Handan.
CAO Lei1,2, WANG Ting1,2, WANG Li-jun1,2, DIAO Rui-ping3, YU Li-jing3, CUI Xiao-li3, MAO Hong-jun1,2*
(1.Tianjin Key Laboratory of Urban Transport Emission Research, College of Environmental Science and Engineering, Nankai University, Tianjin 300071, China;2.State Environmental Protection Key Laboratory of Urban Ambient Air Particulate Matter Pollution Prevention and Control, Tianjin 300350, China;3.Handan Maternal and Child Health Hospital, Hebei 056001, China)., 2022,42(1):444~455
The traditional logistic regression model was used to evaluate the effects of exposure to various pollutants on GH, and the logistic regression model based on principal component analysis was used to evaluate the effects on GH by additionally adjusting parameters of other pollutants. Results of single-pollutant model showed that each 20μg/m3increment of O3was significantly positively correlated with the increased risk of GH (OR=1.211, 95%CI: 1.094~1.340) during the first 26 weeks of gestation, and the effect in the first trimester was greater than that in the second trimester. In multi-pollutant model, each 20μg/m3increment of PM2.5and PM10exposure significantly increased the GH risk of pregnant women in the three months before pregnancy, with OR values of 1.021 (95%CI: 1.004~1.038) for PM2.5and 1.016 (95%CI: 1.002~1.031) for PM10. Consistent with the results of single-pollutant model, each 20μg/m3increment of O3exposure also had a significant effect on the risk of GH (OR=1.026, 95%CI: 1.002~1.050) during the first 26 weeks of gestation in multi-pollutant model. The results of subgroup analysis showed that pregnant women aged 25~30 years or those in the first pregnancy were susceptible to PM2.5, PM10, NO2and CO exposure before pregnancy, while pregnant women over 35 years old or without college degrees were more likely to develop GH due to O3exposure during pregnancy. In summary, air pollution in Handan has significant impacts on pregnant women inducing suffering from GH. To mitigate the negative impacts of exposure to air pollution, more attention should be paid to the enhancement of air pollution protection awareness for pregnant women before and during pregnancy.
gestational hypertension;air pollution;pregnancy;cohort study
X703.5
A
1000-6923(2022)01-0444-12
曹 蕾(1997-),女,山西長治人,南開大學碩士研究生,主要從事大氣污染與人體健康研究.
2021-06-05
中央高校基本科研業務費(63211075)
* 責任作者, 教授, hongjun_mao@hotmail.com

