小鼠骨髓間質干細胞來源的胞外囊泡對尼古丁誘導的小鼠生精細胞損傷的修復作用
劉子瑤,黃玥,王超,李濤,王晶哲,藺博涵,王子璇,孫曉春,陳華標
(1.江蘇大學醫學院,江蘇 鎮江 212013;2.上海市東方醫院馬歇爾消化道疾病國際診療中心實驗室,上海 200120;3.哈佛醫學院麻省總醫院疫苗和免疫治療中心,馬薩諸塞州 波士頓 02114)
吸煙不僅對肺部損傷嚴重,對于男性精液的危害更為嚴重,長期吸煙者精子的各項質量指標都會降低[1]。尼古丁是煙草中主要的活性成分,又名煙堿,吸入并沉積于機體內會使機體生理功能紊亂,導致多組織、器官慢性損傷,引發肺癌、動脈粥樣硬化、冠心病等多種疾病發生[2]。
當前我國不孕不育人數約占人口比例15%,其中,約50%由男性不育引起[3],已證實吸煙可致精子氧化損傷、DNA加合物、DNA鏈斷裂、染色體畸變和遺傳突變[4]。尼古丁可通過多種途徑影響生殖細胞功能,最終致使機體出現生精障礙[5]、不育[6-7]。間質干細胞通過釋放胞外囊泡和其他介質發揮旁分泌作用,經證實小鼠骨髓間質干細胞來源的胞外囊泡(mBMMSCs-EVs)和介質攜帶有細胞保護的相關信號[8]。此外,mBMMSCs-EVs包含的DNA、mRNA和蛋白質在細胞信號轉導中起重要作用[9]。mBMMSCs-EVs在小鼠DBA/1模型中具有抗炎作用[10];同時,其對組織損傷具有修復作用[11],但mBMMSCs-EVs對尼古丁誘導的生精細胞損傷的影響尚不清楚。因此,本研究擬以生精細胞GC-1為研究對象,探討mBMMSCs-EVs對尼古丁誘導的生精細胞損傷的影響。
1 材料與方法
1.1 細胞系、主要試劑及儀器
4~6周齡雄性BALB/c小鼠12只,購于江蘇大學實驗動物中心,合格證號:No.201926222;小鼠GC-1生精細胞株(廣州吉妮歐生物科技有限公司);L-DMEM、RPMI-1640、胰酶、胎牛血清均為美國Gibco公司產品;MTT試劑(美國Amrgsco公司);二甲基亞砜溶液(上海生工公司);Transwell小室(美國Corning公司);雙抗、BCA蛋白濃度檢測試劑盒均購自上海碧云天公司;Annexin-V-FITC細胞凋亡檢測試劑盒(南京福麥斯公司);成骨成脂誘導分化培養基試劑盒(美國Cyagen公司);CD9兔抗小鼠單克隆抗體、CD63兔抗小鼠單克隆抗體(英國Abcam公司);HRP標記羊抗兔IgG(上海愛必信公司)。CO2細胞培養箱(美國Thermo公司);倒置顯微鏡(日本Olympus公司);酶標儀(美國Biotek公司)。
1.2 細胞培養
用含10 %胎牛血清、100 U/mL 鏈霉素和100 U/mL青霉素的L-DMEM,于37 ℃、5% CO2細胞培養箱中培養原代小鼠骨髓間質干細胞(mBMMSCs),用于收集培養上清液及提取mBMMSCs-EVs。
用含10%胎牛血清、100 U/mL鏈霉素和100 U/mL青霉素的RPMI-1640,于37 ℃、5% CO2細胞培養箱中培養GC-1生精細胞。
1.3 mBMMSCs提取及鑒定
1.3.1 mBMMSCs提取 脫頸處理BALB/c小鼠,快速放至75%乙醇的燒杯內浸泡備用,取股骨和脛骨,沖出骨髓,將沖洗出來的細胞懸液收集于離心管中;在20 ℃條件下,600 r/min離心5 min;棄上清液,重懸細胞懸液并接種于培養瓶;置于37 ℃、5% CO2培養箱中按“1.2”方法培養。
1.3.2 mBMMSCs鑒定 利用流式細胞儀對mBMMSCs表面的CD29、CD44、Sca-1和CD117蛋白進行鑒定。使用成骨誘導分化培養基培養誘導成骨分化3周;PBS沖洗;4%中性甲醛溶液固定30 min;PBS沖洗;茜素紅染色5 min。使用成脂誘導分化培養基和維持培養基交替培養誘導成脂分化2周;PBS沖洗;4%中性甲醛溶液固定30 min;PBS沖洗;油紅O染料工作液染色30 min(工作液配制方法:油紅O貯存液∶蒸餾水=3∶2)。
1.4 mBMMSCs-EVs提取及鑒定
1.4.1 mBMMSCs-EVs提取 待mBMMSCs生長至80%~90%融合度時,用無血清培養基培養48 h,收集上清液;于4 ℃行2 000×g離心20 min;4 ℃行100 000×g超速離心1 h;棄上清液;用PBS重懸沉淀,100 000×g再次超速離心1 h。
1.4.2 mBMMSCs-EVs形態觀察及粒徑檢測 取10 μL mBMMSCs-EVs,充分混懸后滴加至銅網上,室溫靜置1 min,用濾紙吸去邊緣液體;取醋酸雙氧鈾10 μL滴加于銅網上,室溫靜置1 min,用濾紙吸去邊緣液體;干燥后置于透射電鏡下觀察mBMMSCs-EVs形態。取10 μL mBMMSCs-EVs用雙蒸水稀釋至30 μL;用標準品進行粒徑分析儀器性能檢測,合格后行mBMMSCs-EVs上樣,進行梯度稀釋避免樣本堵塞進樣針;對合適濃度的處于布朗運動中的mBMMSCs-EVs 進行捕捉和分析,即可獲得mBMMSCs-EVs的粒徑和濃度信息。
1.4.3 蛋白質印跡法檢測mBMMSCs-EVs分子標志物CD9和CD63表達 取100 μL純化后的mBMMSCs-EVs,與RIPA 裂解液等體積混勻,放置冰上10 min,振蕩 1 min,重復操作3次;完全裂解后4 ℃、15 000×g離心15 min,取上清液,用 BCA 法測定其蛋白濃度。加入蛋白上樣緩沖液,煮沸 8 min;緩慢加樣行SDS-PAGE(150 V,45 min);350 A恒流2 h,將蛋白轉移至PVDF膜;脫脂奶粉封閉 2 h;分別加入CD9和CD63(1∶500)一抗孵育過夜;TBST 洗膜;加入HPR標記的山羊抗兔二抗(1∶2 000)室溫孵育2 h;TBST洗膜3次;ECL 曝光顯影。
1.5 MTT實驗檢測GC-1生精細胞增殖能力
生精細胞GC-1分別用含0、8、16、32 μg/mL尼古丁的RPMI-1640處理24 h;收集細胞,以2×103個/孔細胞密度接種于96孔板,設置4個時間點(0、24、48和72 h),每組設5個復孔;分別按照所設時間點,每孔加入20 μL MTT試劑(5 mg/mL);4 h后加入150 μL二甲基亞砜溶液,置于搖床上低速振蕩10 min,以確保結晶充分溶解;酶標儀測定490 nm波長處各孔光密度(D)值,并計算細胞活力。細胞增殖率(%)=(實驗組D值-空白組D值)/(對照孔D值-空白組D值)×100%。另外,生精細胞GC-1用32 μg/mL 尼古丁預處理24、48、72 h后,分別用0、50、100、200 μg/mL 胞外囊泡處理24 h,步驟同上。篩選最適濃度的尼古丁和胞外囊泡進行后續實驗。
1.6 GC-1生精細胞遷移及凋亡實驗
1.6.1 細胞分組 將GC-1生精細胞分為對照組、尼古丁組和尼古丁+胞外囊泡組。對照組:常規培養;尼古丁組:32 μg/mL尼古丁預處理24 h后常規培養24 h;尼古丁+胞外囊泡組:32 μg/mL尼古丁預處理24 h后加入200 μg/mL 的mBMMSCs-EVs處理細胞24 h。
1.6.2 Transwell遷移實驗檢測GC-1生精細胞遷移能力 收集各組細胞,計數,先于下室中加入600 μL含10%胎牛血清的營養液,再以1×105/孔細胞重懸于200 μL無血清培養基中;將細胞懸液滴加于Transwell小室上室中,于37 ℃、5% CO2孵箱內培養8 h;吸干上室內液體,用棉簽除去上室中未遷移細胞;PBS洗3~4遍;將小室于4%多聚甲醛中固定30 min;PBS洗3~4遍;結晶紫染色30 min;PBS洗3~4遍;隨機選擇3個視野,計算每個視野內的細胞遷移數并進行統計。
1.6.3 流式細胞儀檢測GC-1生精細胞凋亡情況 收集各組細胞,用PBS洗滌2次,避光條件下用AnnexinV-FITC和PI染色30 min。用BD Accuri C6流式細胞儀(美國Becton Dickinson公司)對染色細胞進行流式細胞術分析。
1.7 統計學分析
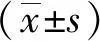
2 結果
2.1 mBMMSCs的鑒定
通過流式細胞儀檢測第3代處于對數生長期的mBMMSCs(圖1A),此時標志物CD29、CD44和Sca-1呈陽性(>95%),CD117則呈陰性(<5%)。
經成骨誘導3周后,細胞慢慢由長梭形轉變成不規則的多邊形,茜素紅染色后可以在鏡下觀察到胞質呈紅色(圖1B)。成脂誘導2周后,細胞逐漸轉變成橢圓形,通過油紅O染色可以觀察到細胞胞質中布滿橘紅色的脂滴,脂滴具有較強的折光性(圖1C)。由此說明,提取的細胞即為mBMMSCs。
2.2 mBMMSCs-EVs的觀察和鑒定
由圖2可見,通過透射電鏡觀察顯示,mBMMSCs-EVs形態呈典型的“杯盤”狀,粒徑分布在30~200 nm,主要集中在110 nm附近。蛋白印跡法檢測顯示mBMMSCs-EVs表達CD9和CD63,由此提示成功分離mBMMSCs-EVs。

A:流式細胞術檢測細胞標志物;B:成骨誘導分化(100×);C:成脂誘導分化(200×)圖1 小鼠骨髓間質干細胞的鑒定

A:透射電子顯微鏡觀察mBMMSCs-EVs形態;B:納米顆粒跟蹤分析mBMMSCs-EVs粒徑分布;C:蛋白質印跡檢測mBMMSCs-EVs表面標志圖2 小鼠間質干細胞來源的胞外囊泡的鑒定
2.3 mBMMSCs-EVs對尼古丁誘導損傷GC-1生精細胞增殖能力的影響
MTT實驗結果顯示(圖3),與0 μg/mL尼古丁相比,32 μg/mL尼古丁作用24、48、72 h時GC-1生精細胞增殖能力明顯降低(P<0.05或<0.01),8、16 μg/mL尼古丁作用24、48、72 h時組間差異無統計意義。由此確定24 h,32 μg/mL尼古丁作為最適作用時間和濃度。
由圖3可見,與0 μg/mL胞外囊泡組相比,24、48、72 h時,200 μg/mL胞外囊泡組細胞增殖能力明顯增加(P<0.05或<0.01);48、72 h時,100 μg/mL胞外囊泡組細胞增殖能力增加,50、100 μg/mL胞外囊泡作用24 h及50 μg/mL胞外囊泡作用48、72 h時組間差異無統計學意義。由此說明,mBMMSCs-EVs可以逆轉尼古丁對GC-1生精細胞增殖能力的抑制。因此,選擇24 h,200 μg/mL mBMMSCs-EVs作為胞外囊泡修復尼古丁損傷GC-1生精細胞最適作用時間和濃度。

a:P<0.05,b:P<0.01,與同時間點0 μg/mL尼古丁組比較;c:P<0.05,d:P<0.01,與同時間點0 μg/mL胞外囊泡組比較圖3 MTT實驗檢測各組處理不同時間后GC-1生精細胞的增殖能力
2.4 mBMMSCs-EVs對尼古丁誘導損傷GC-1細胞遷移能力的影響
Transwell遷移結果顯示,與對照組相比,尼古丁組GC-1生精細胞遷移數明顯減少(t=3.405,P<0.01);尼古丁+胞外囊泡組的生精細胞遷移數量較尼古丁組明顯增多(t=3.625,P<0.05),見圖4。由此說明mBMMSCs-EVs可以部分逆轉尼古丁對生精細胞遷移的抑制。

a:P<0.01,與對照組相比;b:P<0.05,與尼古丁組相比圖4 Transwell遷移實驗檢測不同組GC-1生精細胞遷移能力(×100)
2.5 mBMMSCs-EVs對尼古丁誘導損傷GC-1細胞凋亡能力的影響
結果顯示,與對照組相比,尼古丁組GC-1生精細胞凋亡率明顯增高(t=13.010,P<0.01);與尼古丁組相比,尼古丁+胞外囊泡組細胞凋亡率明顯降低(t=5.889,P<0.01)。見圖5。由此表明,mBMMSCs-EVs可以逆轉尼古丁引起的GC-1生精細胞凋亡。

a:P<0.01,與對照組相比;b:P<0.01,與尼古丁組相比圖5 流式細胞術檢測各組GC-1生精細胞凋亡率
3 討論
本研究采用生精細胞GC-1作為尼古丁誘導損傷生精模型;32 μg/mL尼古丁作用24 h時,GC-1細胞增殖率明顯降低,200 μg/mL胞外囊泡作用尼古丁誘導損傷細胞24 h時,細胞增殖率明顯增高。由此表明,mBMMSCs-EVs可以逆轉尼古丁對GC-1生精細胞增殖能力的抑制。
本研究中,與尼古丁組相比,尼古丁+胞外囊泡組的細胞遷移數量明顯增加、細胞凋亡數量明顯減少,說明mBMMSCs-EVs可逆轉尼古丁對GC-1生精細胞的遷移抑制和凋亡促進,可一定程度修復尼古丁對GC-1生精細胞的損傷。有研究表明,間充質干細胞可以促使心臟修復[12],促進燒傷創面再生[13]。mBMMSCs-EVs相較于間充質干細胞更利于制造儲存,更具有生物活性[14],在受損的組織或細胞中,mBMMSCs-EVs可以替代間充質干細胞用于治療并且更加優化[15]。例如,mBMMSCs-EVs治療可修復受損的腎上腺組織,并使其功能得到較大程度的恢復[16],治療人角膜內皮細胞可促使傷口愈合速度加快[17],本實驗結果與其相一致。此外,有研究表明,人臍帶間充質干細胞來源的胞外囊泡可促進施萬細胞增殖和遷移,有助于受損的周圍神經修復[18],這表明除mBMMSCs-EVs之外,其他來源的胞外囊泡也具有修復能力。
綜上所述,本研究分離的mBMMSCs-EVs對尼古丁誘導的GC-1生精細胞損傷有一定的修復作用。目前關于mBMMSCs-EVs修復尼古丁誘導的生精細胞損傷的體內實驗和潛在機制研究并不完善,有待后續進一步研究。