土壤改良基質對土壤性狀及微生物群落的影響
吳昊,歐陽俊峰,宋時麗,陸曉林,張振華,管永祥,張勇,戴傳超*
(1.南京師范大學生命科學學院,江蘇省微生物資源產業化工程技術研究中心,江蘇省微生物與功能基因組學重點實驗室,南京 210023;2.江蘇省農業科學院資源與環境研究所,南京 210014;3.江蘇省農業技術推廣總站,南京 210036;4.江蘇省句容藍天碧水生物科技有限公司,江蘇 句容 212402)
土壤有機質和微生物與作物產量及土壤質量關系密切[1]。隨著人口數量的增加和生活水平的提高,糧食需求量也日益增長,尤其是在糧食低產和中產地區這種矛盾尤為突出。我國人均耕地有限,大多數地區的耕地貧瘠且產量較低[2]。因此提高耕地產量以滿足食物需求對我國具有重要意義。
各類有機添加物(如豆科植物、糞肥和有機肥等)被用于農業生產以提高耕地產量[3-6],但這些有機添加劑對提升土壤肥力的效果有限。例如:種植豆科作物改良土壤時,需要很長時間來供植物吸收固氮,因此對土壤質量的改良見效較慢[7];植物殘體和糞肥的使用有引入病原菌和提高土壤重金屬含量的風險[3-4,8-9]。此外,商業化有機改良劑的生產還受到原料來源和成本的限制。因此,尋找可以快速培肥且成本低廉的土壤改良劑成為了一個重要的研究領域。
秸稈作為一種重要的農業廢棄物,直接還田會伴隨病原菌的侵染和對養分的爭奪[10]。因此,本研究使用發酵和分解的秸稈作為土壤改良劑,即土壤改良培肥基質(SM)。基質的有機質含量超過55%,活菌數超過2×108cfu·g-1,原料廉價易得,密度低且便于運輸。
為驗證該基質對土壤酶、土壤微生物和作物產量的影響,本課題組在我國小麥-玉米的典型低產區進行了不同施用量的田間試驗。研究分析了基質對土壤理化性質和生物學性質的影響,土壤性質對土壤微生物群落和多樣性的影響,以及不同投入量的基質對小麥產量的影響。
1 材料與方法
1.1 試驗地點與試驗設計
試驗區位于中國江蘇省濱海縣黃河灣農場(34°08'N,119°53'E),農場每年實行小麥-玉米輪作制。該地屬溫帶季風氣候,年平均氣溫14.1 ℃,年平均降水量949.5 mm。土壤類型為潮土,有機質含量為6.55 g·kg-1,全氮含量為0.55 g·kg-1,有效氮含量為8.67 mg·kg-1,有效磷含量為8.47 mg·kg-1,有效鉀含量為65.54 mg·kg-1,容重為1.35 g·cm-3,pH 值為8.50(土水比為1∶2.5)。
田間試驗設置5 個處理:(1)化肥(CK,無土壤改良基質);(2)3 000 kg·hm-2的土壤改良基質(SM1);(3)6 000 kg·hm-2的土壤改良基質(SM2);(4)9 000 kg·hm-2的土壤改良基質(SM3);(5)12 000 kg·hm-2的土壤改良基質(SM4)。所有處理的化肥用量與CK 相同。土壤改良基質理化性質見表1。5 個處理的總N、總P和總K含量見表2。

表1 土壤改良基質的物理和化學指標Table 1 Physical and chemical indexes of the soil amended substrate medium

表2 對照和不同處理的營養成分(kg·hm-2)Table 2 Nutrient contents of the applied chemical fertilizer and soil amended substrate medium(kg·hm-2)
每個試驗區均為15 m×10 m,每種處理3個重復,共15 個試驗裂區,各裂區采用完全隨機分配。按當地耕作習慣,在上季作物收獲后,將殘留秸稈粉碎還田。土壤改良基質于2017年7月,小麥種植前作基肥施用,小麥于2017 年10 月30 日種植。在小麥生長期內,各處理均有養分含量共計270 kg·hm-2N、150 kg·hm-2P2O5和75 kg·hm-2K2O的化肥施用到田間。本課題組開發的土壤改良培肥基質使用水稻秸稈和小麥秸稈作為原材料,秸稈干燥后濕度控制在65%以下作為堆肥材料,堆肥過程中加入枯草芽孢桿菌和黑曲霉促進發酵(成品中均能檢測到兩種微生物的存在)。每堆堆肥的原材料重達3 t,長、寬、高分別為18、1.5、1.5 m。根據堆體溫度的變化,每10~15 d 翻堆一次,加入硅鎂土促進黏合和成型。該基質完全由本課題組研發,并由句容藍天碧水生物科技有限公司商業化生產。
1.2 樣品采集
在2017 年10 月小麥種植前(S0)、2018 年3 月小麥返青期(S1)、2018 年4 月小麥拔節期(S2)和2018年6 月小麥成熟期(S3)采集土壤樣本,Zadoks 編號分別為z00、z24、z37和z92[11]。在每個樣地中隨機采集5個直徑38 mm、深度5~15 cm的土芯,同一地塊的土壤混合成一個樣本。將采集的新鮮土壤樣品分為兩個子樣本,一個子樣本儲存在-20 ℃用于DNA 提取,另一個子樣本立即分析土壤性質和土壤酶活性。
在每個地塊對角線位置設置3 個等距采樣點用于成熟期植物樣品采集,每個采樣點1 m2且距離地塊邊緣至少2 m。收獲采樣點內所有的小麥并記錄穗數。小麥烘干后取20 株穗用于谷粒計數,計算每株穗的平均谷粒數和每1 000粒谷粒的質量。作物產量(kg·hm-2)=每平方米穗數×每穗平均谷粒數×每1 000粒谷粒質量(g)/100。
1.3 土壤物理、化學和生物分析
制備土水比為1∶2.5(m/V)的干土懸浮液,測定土壤pH值。采用1∶5(m/V)的土壤水混合物測定土壤電導率(EC)。采用重鉻酸鉀氧化法測定土壤有機質(SOM)。采用凱氏定氮法測定全氮(TN)。采用NaHCO3萃取-鉬藍比色法測定有效磷(AP)。采用醋酸銨浸提-火焰光度法測定有效鉀(AK)。采用堿擴散法測定有效氮(AN)。體積密度(BD)由給定體積土壤的質量計算。根據《土壤農化分析》[12]對上述土壤性質進行分析。采用氯仿熏蒸提取法測定微生物生物量碳(MBC)和微生物生物量氮(MBN)[13-14]。
土壤中轉化酶和纖維素酶的活性用3,5-二硝基水楊酸比色法測定[15-16],脲酶的活性用吲哚酚比色法測定[15]。
1.4 細菌和真菌群落的定量分析
采用Step1 實時熒光定量PCR 系統對試驗前、小麥拔節期和小麥成熟期土壤中的細菌和真菌進行定量分析。根據CéBRON 等[17]的方法,采用SYBRGreen 實 時PCR 法,測定 土壤總DNA 中16S rDNA 和18S rDNA 的拷貝數。將枯草芽孢桿菌16S rDNA 和雜色曲霉18S rDNA 插入p-easy blunt 載體中,將連接產物轉化入DH5α。16S rDNA 通用引物為338f/518r,18S rDNA 通用引物為Fung5F/FF390R[18]。篩選Amp+平板進行陽性克隆轉化和測序。提取質粒作為定量分析的標準。用10 倍梯度稀釋質粒獲得定量標準曲線,用于SYBR-Green 實時PCR 擴增。用無菌水代替模板DNA 作為陰性對照。通過與標準曲線比較,計算每個樣本的Ct值,獲得拷貝數。
1.5 變性梯度凝膠電泳(DGGE)分析
用PCR-DGGE法對各處理成熟期土壤的16S rDNA和18S rDNA 片段進行細菌和真菌的擴增。使用的引物為357F-GC/517R 和NS1/GC-Fung[19]。擴增反應重復3 次,PCR 產物經1%EB 瓊脂糖凝膠電泳驗證。用定量軟件分析DGGE上觀察到的條帶。
1.6 統計分析
采用SPSS 20.0 統計軟件對同一時期不同處理或同一處理不同時期下的產量、土壤性質和土壤微生物群落進行統計分析,采用Duncan 法進行多重比較。基于DGGE 譜帶,利用軟件計算Shannon 多樣性指數(H)、均勻度指數(E)和Chao-1 指數。利用Gelcompar Ⅱ軟件包對DGGE 譜帶進行識別和聚類。利用Canoco 5 軟件進行典型相關分析(CCA),揭示土壤性狀與細菌和真菌群落組成的關系。
2 結果與分析
2.1 土壤特性和作物產量的變化
在本季試驗之后,各試驗裂區的SOM 含量總體隨著土壤中加入土壤改良培肥基質含量的增加而增加(表3)。SM3 和SM4 處理各時期SOM 含量均顯著高于CK(P<0.05)。在小麥拔節期,SM4 的平均SOM含量比CK 高出79.1%(表3)。TN 含量在基質處理與CK間無顯著差異,然而基質處理的各階段AN含量均低于CK,且4 個基質處理之間AN 含量均無顯著差異。在小麥整個生育期內,AP 含量隨著生長期的變化呈現先升高后降低的趨勢,AP 含量在返青期達到最高,在成熟期降低至與播種前同一水平。在整個生育期,所有基質處理的AK 水平都高于CK。土壤EC值在基質處理與CK 間差異顯著(表3),4個基質處理的EC值均顯著低于CK,特別是拔節期和成熟期。
MBC 和MBN 在拔節期含量較高,在成熟期時略有下降(表3)。在各個時期處理組的MBC 和MBN 均高于CK,MBC 含量隨著基質用量的增加而增加,且SM4處理顯著高于CK。MBN在返青期和拔節期均是基質處理顯著高于CK,然而在成熟期各處理與CK間差異減弱,沒有達到顯著水平。

表3 小麥生長期內土壤理化性質Table 3 Soil physicochemical properties of wheat
土壤改良培肥基質處理的小麥產量高于CK(表4)。SM4 處理的小麥產量最高,是CK 的1.32 倍。而SM2 處理的小麥產量低于SM1,這可能是由田間地形、水文等因素造成的。

表4 小麥產量Table 4 The yield of wheat
2.2 土壤酶活性的變化
在各個處理中,蔗糖酶活性在不同時期間存在差異。總體而言,同一處理的土壤蔗糖酶活性呈現先增加(拔節期)后減少(成熟期)的趨勢(圖1a)。在同一階段,不同基質處理的蔗糖酶活性均顯著高于CK,且在拔節期這種差異最為顯著,拔節期SM4處理的蔗糖酶活性最高,比CK 高60.4%。總體而言,在返青期與拔節期,蔗糖酶活性的變化趨勢與基質的用量呈正相關,而在成熟期基質增加對蔗糖酶活性沒有產生顯著影響。
在返青期,SM2~SM4 處理的脲酶活性顯著增加(圖1b)。拔節期各處理的脲酶活性均較高,可能與期間追肥有關,其中SM3 和SM4 處理的脲酶活性顯著高于CK。在成熟期,不同基質施加量處理的脲酶活性無顯著差異。
同一處理的土壤纖維素酶活性在3 個生長階段逐漸增加(圖1c)。在3個生長階段中,成熟期基質處理組的纖維素酶活均顯著高于CK,其中SM4 處理的纖維素酶活最高,比CK高出65.1%。

圖1 土壤蔗糖酶、脲酶和纖維素酶的活性Figure 1 The activities of invertase,urease and cellulase
2.3 土壤微生物群落豐度及多樣性
土壤中細菌和真菌的豐度隨著土壤改良培肥基質施用量的增加而顯著增加(表5)。小麥拔節期,SM4 處理的真菌豐度最大,是CK 的15.8 倍。在成熟期,各處理真菌豐度均下降,但除SM1外,其余處理仍顯著高于CK。總體而言,土壤細菌豐度是隨基質的增加而增加,各處理組中細菌豐度在拔節期的SM3處理中達到最高,是CK的7.8倍(表5)。

表5 土壤細菌和真菌豐度Table 5 The abundance of bacteria and fungi in soil
與細菌DGGE 指紋圖譜(圖2a)相比,真菌DGGE指紋圖譜(圖3a)在小麥成熟期不同處理之間顯示出更大的差異性。主成分分析結果顯示,各處理間真菌微生物群落分區明顯(圖3b)。與CK 和SM1 處理相比,SM3和SM4處理的土壤真菌群落有顯著差異。細菌DGGE 圖譜檢測到的條帶數比真菌的更多,但是各個處理在主成分分析結果中區分不明顯。

圖2 小麥成熟期不同處理細菌16S rRNA基因片段的DGGE圖譜(a)和主成分分析(b)Figure 2 Comparison of the DGGE profiles(a)and principal component analysis(b)of bacterial 16S rRNA genes fragments from the different treatments at the wheat ripening stage

圖3 小麥成熟期不同處理真菌18S rRNA基因片段的DGGE圖譜(a)和主成分分析(b)Figure 3 Comparison of the DGGE profiles(a)and principal component analysis(b)of fungal 18S rRNA genes fragments from the different treatments at the wheat ripening stage
各處理組真菌群落Shannon 指數和Chao-1 指數高于CK,且在SM2 和SM3 兩個基質處理中達到顯著差異(表6)。而各處理間均勻度指數差異均不顯著。有機質的提高進一步提高了Shannon 和Chao-1指數,SM3 處理的Shannon 和Chao-1指數達到最高值。然而,在SM4 處理中,Shannon 和Chao-1 指數顯著低于SM3 和SM2 處理。細菌群落的各項指數中,只有SM2處理的均勻度指數顯著高于CK(表7),SM2處理的Shannon 和均勻度指數最大,SM3的Chao-1指數最大。
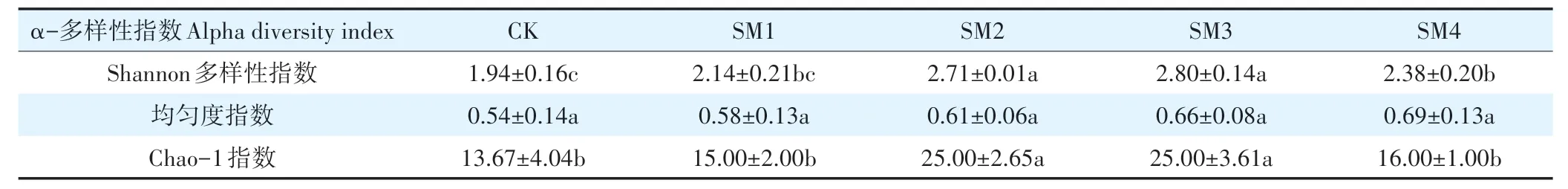
表6 成熟期不同處理的真菌群落的α多樣性指數Table 6 Alpha-diversity index of fungal communities treated with different treatments at ripening stage

表7 成熟期不同處理的細菌群落的α多樣性指數Table 7 Alpha-diversity index of bacterial communities treated with different treatments at ripening stage
2.4 土壤真菌、細菌群落組成與土壤性質的相關性分析
采用典型相關分析法(CCA)分析了成熟期土壤真菌群落結構與土壤性質(SOM、pH、TN、AN、AP、AK、BD、EC、MBC、MBN)的關系(圖4),總變異系數為4.36,解釋變量占73.8%。真菌CCA 排序結果的前兩軸特征值分別為0.573 7 和0.473 9,說明排序結果是合理的。CCA 結果表明,MBC 對真菌多樣性和群落結構有顯著影響,其次是SOM、TN、AN、AP 和BD(貢獻率>10%)。但上述環境因子對細菌群落的變化無顯著影響(P>0.05)。MBC 是影響真菌群落的主要因子(P<0.05)。SOM 是對細菌群落影響最大的環境因素,但是細菌的CCA 結果各處理之間沒有很好區分(圖5)。

圖4 小麥成熟期不同處理真菌群落組成與土壤性質的典型相關分析(CCA)Figure 4 Canonical correlation analysis of the fungal community compositions and soil properties from the different treatments at the wheat ripening stage

圖5 小麥成熟期不同處理細菌群落組成與土壤性質的典型相關分析(CCA)Figure 5 Canonical correlation analysis of the bacterial community compositions and soil properties from the different treatments at the wheat ripening stage
3 討論
3.1 增施基質對小麥產量的影響
本研究結果顯示增施基質提高了小麥產量,特別是SM4 處理的小麥產量與CK 相比提升幅度達到顯著水平。研究發現,無機肥料和有機物料(SM)聯合配施可以維持甚至提高作物產量。已有的研究發現,大多數有機物料的投入對產量有正面影響,但也有一些有機物料(如綠肥和秸稈)的投入對產量有負面影響[20-21]。總體來說,與CHEN等[22]在我國廣泛進行的3種農業措施(傳統農業實踐、改進實踐、高產系統)相比,本研究SM4 處理的最大產量為8 276.40 kg·hm-2,達到了CHEN 等研究中改進實踐的產量(8.3 Mg·hm-2),說明施用SM 是一種快速有效的施肥措施。使用有機材料時,化肥是維持生產所必需的[3-4,21]。雖然本研究在所有處理中都施用了相同數量的肥料,但在今后保持作物產量的同時減少SM處理中的化肥施用量是可行的。SM 的施用并不是為了替代化肥,而是增加退化土壤的生產率。
SOM 是影響作物生產力和土壤質量的關鍵因素[1,6]。試驗區(黃河故道)SOM 含量普遍低于江蘇省平均水平(22 g·kg-1)[23],因此利用有機投入維持并提高該地區土壤肥力具有重要意義。與研究開始前的未處理土壤相比,經SM3 和SM4 處理的土壤中的SOM 分別增加了2.66 g·kg-1和2.92 g·kg-1。同樣,BEI等[3]在華北平原農田有機投入連續4 a,結果顯示秸稈處理的農田SOM 增加了4.05 g·kg-1,有機肥處理增加了4.04 g·kg-1,秸稈還田加有機肥處理增加了5.12 g·kg-1。與其相比,本研究的管理方式在每年增加的SOM 的數量方面具有優勢。盡管本試驗周期較短,但與其他培肥措施相比,SM 的應用在改善SOM 方面已顯示出優勢。在試驗過程中,各處理的SOM 均呈先升高后降低的趨勢,這可能是由于一些基質產品留在土層中,沒有被完全分解,這與JI 等[24]的研究結果一致,他們將這種有機質下降的現象解釋為有機和無機肥料的聯合添加引起的激發效應,這一措施刺激了土壤微生物的生長,加速了SOM的分解。
3.2 增施基質對土壤營養的影響
基質中的土壤速效養分含量較低,而有機質和微生物成分含量較高,因此增施基質處理對土壤養分供應,特別是對土壤AN 的影響不顯著。但是基質中養分的緩慢釋放仍然存在,并可以被植物快速吸收。增施基質使土壤有機質迅速增加,這與相應處理的產量、AP 和AK 的增加一致。此外,在小麥成熟期,SM3與SM4處理的土壤AP和AK顯著高于CK。盡管豆科作物增加了土壤氮素含量,但其對土壤有機質提升的影響并不顯著[4,7],因此豆科作物的種植并不適合應用于需要短期快速提升土壤有機質的場景。商用有機肥料或肥料也能有效改善貧瘠土壤的有機質含量[25-26],但由于我國糧食主產區的畜牧業集約化生產水平較低,用于大量生產有機肥料的畜禽糞便等原料的獲取在地理上受到限制。因此,基質的生產清潔無污染、原材料易得、應用成本低、施肥效果全面,具有重要優勢。
3.3 增施基質對土壤微生物的影響
土壤微生物通過參與有機質轉化、養分循環和生物修復,在維持土壤功能方面發揮著重要作用[27]。不同的農業管理措施可能會改變土壤化學性質,這些性質通常與土壤微生物群落和豐度密切相關[28]。本研究結果表明,基質處理的土壤MBC 和微生物豐度顯著增加,SM2 和SM3 處理的土壤微生物多樣性高于CK、SM1 和SM4。微生物區系多樣性的增加可能主要與纖維素降解和養分循環有關[29],其特征是生長過程中纖維素酶、脲酶和轉化酶活性的增加。
在本研究中,基質的使用顯著增加了脲酶活性,特別是在拔節期。而CK 處理脲酶活性也有增加,這與LIANG 等[30]的研究結果一致,但與BANDICK 等[31]的結果相反。蔗糖酶活性反映了土壤成熟程度和肥力水平。CK中較低的蔗糖酶活性表明化肥短期不會導致土壤熟化,蔗糖酶的活性不足也會加速籽粒敗育從而導致小麥減產[32]。小麥生長期間纖維素酶活性逐漸增加,這與GAIND 等[33-34]的研究結果一致。纖維素酶活性增加可能促進微生物對有機質的降解并減輕未降解秸稈對作物生長的抑制作用。
基質與化肥配施能提高土壤MBC、MBN 和脲酶活性,這與ZHENG 等[35]的研究結果一致,他們發現,氮磷化學肥料與有機肥料的長期聯合施用,顯著提高了MBC 含量,而土壤微生物生物量通常與土壤生物功能密切相關[36-37]。
許多研究表明,微生物群落的結構和豐度與作物的生長和產量密切相關[38-39]。土壤細菌和真菌數量的顯著增加可能是由于向土壤中引入了大量的土壤改良培肥基質。基質的松散顆粒結構和土壤性質的改善可能為微生物的生長提供了一個合適的環境[40]。與豆科作物覆蓋影響細菌群落不同[41],本研究中DGGE結果顯示真菌群落結構對有機輸入的反應比細菌更敏感,SM3 和SM4 兩處理與其他樣品在CCA 分析中區分明顯,這與LI 等[5]的研究結果一致。在本研究中,真菌比細菌具有優勢可能是由于有機投入物和秸稈導致了土壤有機碳的增加[42]。DGGE 較低的分辨率可能會忽視一些低豐度微生物的變化,因此對于基質施用過程中低豐度微生物的功能和豐度的變化還需要通過進一步的研究來闡明。
土壤性質對解釋土壤微生物群落組成的變化具有重要作用。本研究結果表明,MBC、SOM、TN、AN、AP、BD 對土壤真菌群落組成的影響大于其他土壤性質。先前的研究也表明,有機碳形態的變化與土壤真菌群落組成的變化密切相關[43]。MBC 是解釋土壤真菌群落組成顯著性水平的唯一因子,占土壤真菌群落組成方差的12.6%。土壤有效養分(如AN 和AP)與真菌群落結構之間存在很強的相關性。這表明土壤碳和營養是影響土壤微生物群落的主要影響因子,養分影響真菌群落結構已有研究報道[44]。土壤水穩性團聚體更適合真菌菌絲生長。秸稈的降解降低了土壤BD,這可能是BD影響真菌群落組成的原因。
4 結論
(1)本研究報道了一種管理模式:秸稈發酵+基質生產+田間施用。
(2)與傳統的糞肥和有機肥相比,本研究以廢棄秸稈為原料,通過菌劑發酵和降解生產的有機改良基質減少了病原菌的引入風險并降低了生產成本,可以在全國各地推廣。
(3)田間試驗結果表明該有機改良基質與化肥的聯合施用顯著改善了土壤養分和結構,提高了微生物群落的豐度和多樣性,提高了貧瘠土壤的生產力。
(4)本研究使用的基質本身作為營養源,相對于僅施用化肥的處理,勢必會帶來額外的養分,因此基質添加帶來的額外養分及其對土壤結構的改變等是否對產量產生影響還需進一步的研究。此外,本文對細菌和真菌群落結構的研究僅停留在豐度和多樣性層面,對于具體的群落結構的變化,尤其是一些低豐度微生物的變化了解得還不夠清楚,未來運用高通量測序結合純培養技術研究關鍵微生物在有機添加過程中的變化和作用將有助于開發新的微生物組產品,因此需進一步探究土壤改良過程中微生物的作用和相關機制。
- 農業環境科學學報的其它文章
- 生物菌劑對土壤微生物群落結構和功能的影響
- 土壤環境生物安全與健康專刊特邀主編

