星點設計-效應面法優化負載和厚樸酚的當歸多糖-小檗堿聚合物膠束的處方工藝研究
王彬彬,呂 白,張 琦,王玲鈺,張 旭,于 超,周建文,韓翠艷
星點設計-效應面法優化負載和厚樸酚的當歸多糖-小檗堿聚合物膠束的處方工藝研究
王彬彬,呂 白,張 琦,王玲鈺,張 旭,于 超,周建文,韓翠艷*
齊齊哈爾醫學院藥學院,黑龍江 齊齊哈爾 161006
通過星點設計-效應面法優化負載和厚樸酚(honokiol,HNK)的當歸多糖(polysaccharide,ASP)-小檗堿(berberine,Ber)聚合物膠束(ASP-SS-Ber/HNK)的處方工藝并考察其制劑學性質。HPLC法測定HNK的含量;采用薄膜水化法制備ASP-SS-Ber/HNK,在單因素實驗的基礎上,以粒徑、載藥量以及包封率為評價指標,對載藥比、水化溫度和水化時間進行處方工藝篩選,采用星點設計-效應面法進行3因素3水平的實驗,分析結果得出最優處方工藝并對其進行驗證;使用透射電子顯微鏡(TEM)和粒徑儀觀察測定ASP-SS-Ber/HNK形態、平均粒徑和ζ電位,通過體外釋藥對該載藥系統進行評價并考察其穩定性。優化得到的ASP-SS-Ber/HNK最佳處方工藝:當歸多糖-小檗堿載體(ASP-SS-Ber)與HNK的投藥量分別為5.00 mg和0.71 mg、水化溫度為30 ℃、水化時間為100 min。采用最優處方制得的負載HNK的膠束制劑對HNK的載藥量為(9.22±0.42)%,包封率為(71.77±1.20)%;膠束平均粒徑為(44.38±2.95)nm;ζ電位接近于(?10.32±1.26)mV。在含有谷胱甘肽(GSH為10 mmol/L)的體外釋放介質中72 h累積釋放率達到80.2%;12 h的吸光度維持在0.29±0.01,連續7 d內的粒徑穩定在(45.14±0.67)nm,ζ電位穩定在(?10.46±0.60)mV。星點設計-效應面法所建立的模型精度高,可用于ASP-SS-Ber/HNK膠束制劑的處方優化。
和厚樸酚;當歸多糖;小檗堿;膠束;薄膜水化法;星點設計-效應面法
靶向納米顆粒的制備一般是在納米顆粒表面修飾靶向配體,因而可以與細胞表面受體特異性地相互作用[1]。與引入肝靶向基團的復雜性相比,具有內在肝靶向能力的多糖則使制備更為簡單[2]。當歸多糖(polysaccharide,ASP)是中藥當歸的主要活性成分之一,具有天然的肝臟靶向功能[3]。所以構建以當歸多糖為親水鏈段的膠束而不進行任何靶向修飾是一種很好的策略[4-5]。小檗堿(berberine,Ber)是一種親脂性陽離子,本身具有抗肝癌作用及靶向線粒體的特性[6],但是較差的膜通透性使其不易進入細胞,較低的生物利用度也限制了其應用[7]。利用二硫鍵將當歸多糖與小檗堿相連,將其作為膠束的疏水鏈段,提高了小檗堿的跨膜性[8],小檗堿定位于線粒體處,在線粒體高濃度的谷胱甘肽(glutathione,GSH)下[9],使具有氧化還原敏感的二硫鍵裂解,釋放出所負載的藥物[10]。和厚樸酚(honokiol,HNK)是厚樸的主要活性成分[11],具有線粒體依賴性的抗腫瘤作用[12-13],在抗肝癌方面展現出較好的藥理活性,但是較差的溶解性導致其具有較低的藥效[14-15]。因此,將其包載在當歸多糖與小檗堿連接構建的載體(ASP-SS-Ber)中,可改善其溶解性,在靶向線粒體的同時提高藥效。制備ASP-SS-Ber/HNK理論上可以利用當歸多糖[16]和小檗堿[17]的特性,起到靶向抗腫瘤的作用。
本研究以膠束平均粒徑以及和厚樸酚包封率和載藥量為評價指標,考察負載和厚樸酚的當歸多糖-小檗堿聚合物膠束(ASP-SS-Ber/HNK)處方中主要因素對制劑的影響,確定了最優處方[18-19],為制劑的進一步研究奠定了基礎。
1 儀器與材料
1.1 儀器
高效液相色譜儀,山東魯南瑞虹有限公司;Zetasizer Nano-ZS90納米粒度儀,英國Malvern儀器有限公司;DF-101S集熱式恒溫加熱磁力攪拌器,鞏義市予華儀器有限公司;UV-2550紫外可見分光光度計,北京浦西通用儀器有限公司;5417R高速冷凍離心機,德國Eppendof公司;AL 204電子天平,梅特勒-托利多上海有限公司;一次性無菌注射器,遼寧眾源醫療器械有限公司;Genex Beta移液器,北京普析通用儀器有限公司;HT7700透射電子顯微鏡,日立高新技術公司;S-250D超聲細胞破碎儀,美國Branson公司;EYELA旋轉蒸發儀,鄭州科泰實驗設備有限公司;QT-2渦旋混合器,上海琪特分析儀器有限公司;ZHWY-200D恒溫培養振蕩器,上海智城分析儀器有限公司。
1.2 試藥
和厚樸酚,批號MB5989,質量分數98%,大連美侖生物技術有限公司;當歸多糖,批號B25568,質量分數90%,相對分子質量40 000左右,上海源葉生物科技有限公司;鹽酸小檗堿(批號B802465,質量分數98%)、芘(批號P817273,質量分數99%)、還原型谷胱甘肽(批號G6268,質量分數99%,生物技術級)、聚乙二醇(PEG)2000(批號D875844,質量分數98%),上海麥克林生化科技有限公司;ASP-SS-Ber,課題組自制;甲醇、乙腈,色譜純,天津市科密歐有限公司;泊洛沙姆-188(批號WPWL549B,質量分數98%)、二甲基亞砜(分析純),上海阿拉丁生化科技股份有限公司;Kolliphor ELP(批號Batch Weight,純化級),北京鳳禮精求醫藥股份有限公司;透析袋,截留相對分子質量14 000,上海易佰聚經貿有限公司;丙酮,分析純,哈爾濱化工化學試劑廠;磷酸鹽緩沖液(PBS,pH 7.5),上海盛思生化科技有限公司;2%磷鎢酸負染液,北京酷來搏科技有限公司;聚山梨酯80,質量分數97%,國藥集團化學試劑有限公司;胎牛血清,美國Hyclone公司。
2 方法與結果
2.1 ASP-SS-Ber/HNK的制備
分別稱取一定量的和厚樸酚與ASP-SS-Ber置于50 mL圓底燒瓶中,加入10 mL甲醇,超聲使其充分溶解,加入表面活性劑后采用旋轉蒸發儀去除有機溶劑,緩慢加入5 mL去離子水,使其薄膜水化,10 000r/min離心(離心半徑13.5 cm)10 min后0.22 μm微孔濾膜濾過,即得ASP-SS-Ber/HNK膠束。空白膠束(ASP-SS-Ber)為不加和厚樸酚,其余同ASP-SS-Ber/HNK的制備過程。
2.2 色譜條件
色譜柱為Diamonsil C18柱(250 mm×4.6 mm,5 μm);流動相為乙腈-水(70∶30);檢測波長292 nm;進樣量20 μL;體積流量1.0 mL/min;柱溫40 ℃。在該條件下和厚樸酚對照品溶液峰理論塔板數大于3000,分離度大于1.5。
2.3 和厚樸酚載藥量、包封率的測定
采用濾膜濾過法進行聚合物膠束藥物包封率的測定。取500 μL和厚樸酚聚合物膠束溶液,過0.22 μm濾膜后加入500 μL甲醇超聲破乳,即得ASP-SS-Ber/HNK供試品溶液。按“2.2”項下色譜條件進樣分析,色譜圖見圖1,ASP-SS-Ber/HNK與和厚樸酚峰的分離度()大于1.5,空白膠束在和厚樸酚處無干擾,專屬性良好。將所得峰面積帶入線性方程計算ASP-SS-Ber/HNK中和厚樸酚的含量。
包封率=膠束中包封的藥物的質量/加入藥物的質量
載藥量=膠束中包封的藥物的質量/(加入藥物的質量+加入的載體材料的質量)
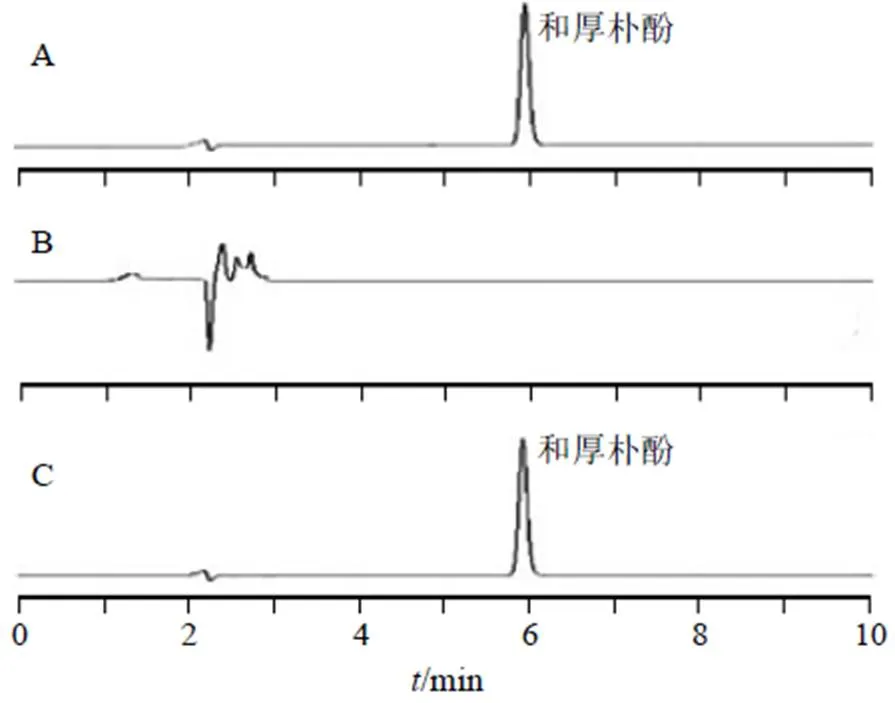
圖1 和厚樸酚對照品溶液(A)、ASP-SS-Ber溶液 (B)、ASP-SS-Ber/HNK溶液(C)的HPLC圖
2.4 單因素考察
2.4.1 溶劑用量的考察 在其他條件固定時,即表面活性劑為聚氧乙烯蓖麻油,用量為200 μL,載藥比為1,水化溫度為20 ℃,水化時間為40 min,加入一定量的ASP-SS-Ber和和厚樸酚分別溶解于3、5、10、15 mL甲醇中,考察不同溶劑用量對粒徑、包封率和載藥量的影響。結果(表1)顯示,當加入甲醇的量為10 mL時和厚樸酚的載藥量與包封率最高,因此選擇10 mL作為溶劑用量。
2.4.2 表面活性劑種類選擇 在其他條件固定時,即溶劑用量為10 mL,表面活性劑用量為200 μL,載藥比為1,水化溫度為20 ℃,水化時間為40 min,分別加入注射劑常用的表面活性劑[20]泊洛沙姆-188、PEG 2000和聚氧乙烯蓖麻油,考察不同表面活性劑種類對粒徑、包封率和載藥量的影響。結果(表2)顯示,當選擇聚氧乙烯蓖麻油時,和厚樸酚的載藥量與包封率最高,因此選擇聚氧乙烯蓖麻油作為表面活性劑來制備ASP-SS-Ber膠束。
表1 ASP-SS-Ber/HNK溶劑用量的選擇 (, n = 3)
Table 1 Selection of ASP-SS-Ber/HNK solvent volume (, n = 3)
甲醇用量/mL粒徑/nmPDI包封率/%載藥量/% 389.39±2.050.216±0.1462.62±0.150.44±0.53 550.05±0.160.175±0.06210.65±0.131.77±0.24 1046.34±1.740.145±0.82326.11±1.248.71±0.15 1545.77±1.230.201±0.45224.15±0.686.32±0.21
表2 ASP-SS-Ber/HNK表面活性劑種類選擇(, n = 3)
Table 2 Selection of ASP-SS-Ber/HNK surfactant types (, n = 3)
表面活性劑種類粒徑/nmPDI包封率/%載藥量/% 泊洛沙姆63.35±1.250.383±0.25312.13±0.082.17±0.03 PEG 200042.67±0.240.585±0.05112.62±0.332.37±0.05 聚氧乙烯蓖麻油67.88±1.030.249±0.55237.63±0.786.47±0.21
2.4.3 表面活性劑聚氧乙烯蓖麻油用量的選擇 在其他條件固定時,即溶劑用量為10 mL,表面活性劑為聚氧乙烯蓖麻油,載藥比為1,水化溫度為20 ℃,水化時間為40 min,分別加入200、300、400、500 μL的聚氧乙烯蓖麻油,考察表面活性劑用量對粒徑、包封率和載藥量的影響。結果(表3)顯示,當聚氧乙烯蓖麻油用量為400 μL時和厚樸酚的載藥量與包封率最高,因此聚氧乙烯蓖麻油用量選擇為400 μL。
表3 ASP-SS-Ber/HNK聚氧乙烯蓖麻油量的選擇(, n = 3)
Table 3 Selection of amount of ASP-SS-Ber/HNK polyoxyethylene castor oil (, n = 3)
聚氧乙烯蓖麻油用量/μL粒徑/nmPDI包封率/%載藥量/% 20060.24±1.650.412±0.12640.05±0.476.56±0.33 30056.14±0.230.256±0.28963.30±1.3510.35±2.53 40044.14±1.200.120±0.22368.52±0.2811.54±0.56 50045.50±1.730.301±0.11264.40±0.6810.27±0.20
2.4.4 載藥比(載體與藥物質量比)的選擇 在其他條件固定時,即溶劑用量為10 mL,表面活性劑為聚氧乙烯蓖麻油,用量為400 μL,水化溫度為20 ℃,水化時間為40 min,精密稱取載體5.00 mg,加入不同質量的藥物,即載藥比分別為1、3、5、7、9時,考察不同載藥比對粒徑、包封率和載藥量的影響。結果(表4)顯示,隨著載體量的增加,和厚樸酚的載藥量與包封率先升高后降低,因此將范圍5、7、9的載藥比設為待優化項進行星點設計-效應面法實驗。
表4 ASP-SS-Ber/HNK載藥比選擇(, n = 3)
Table 4 ASP-SS-Ber/HNK drug loading ratio selection (, n = 3)
載藥比粒徑/nmPDI包封率/%載藥量/% 170.93±1.450.262±0.0714.91±0.102.49±0.06 364.52±1.270.242±0.09563.13±1.3615.60±0.22 544.46±1.560.574±0.12264.57±1.6211.45±0.20 744.49±1.230.512±0.10470.23±1.068.69±0.18 938.25±1.650.562±0.08269.09±0.506.35±0.08
2.4.5 水化溫度的考察 在其他條件固定時,即載體與藥物的比例為7,制劑質量濃度為0.7 mg/mL,溶劑用量為10 mL,表面活性劑為聚氧乙烯蓖麻油,用量為400 μL,水化時間為40 min,考察水化溫度在20、30、40、50、60 ℃時,不同水化溫度對粒徑、包封率和載藥量的影響。結果(表5)顯示,隨著水化溫度的增加,和厚樸酚的載藥量與包封率均先增加后降低。因此將20~40 ℃的水化溫度作為待優化項進行星點設計-效應面法實驗。
2.4.6 水化時間的考察 在其他條件固定時,載體與藥物的比例為7,制劑質量濃度為0.7 mg/mL時,溶劑用量為10 mL,表面活性劑為聚氧乙烯蓖麻油,用量為400 μL,水化溫度為30 ℃,考察水化時間在40、60、80、100、120 min時,不同水化時間對粒徑、包封率和載藥量的影響。結果(表6)顯示,隨著水化時間的增加,和厚樸酚的載藥量與包封率均先增加后降低。因此將80~120 min的水化時間作為待優化項進行星點設計-效應面法實驗。
表5 ASP-SS-Ber/HNK水化溫度選擇(, n = 3)
Table 5 ASP-SS-Ber/HNK hydration temperature selection (, n = 3)
水化溫度/℃粒徑/nmPDI包封率/%載藥量/% 2070.93±1.690.262±0.09110.80±0.291.46±0.15 3044.52±1.520.242±0.06571.59±1.089.68±0.17 4044.46±1.260.574±0.05763.12±0.427.68±0.05 5044.49±1.340.512±0.07658.76±1.949.68±0.17 6038.25±1.260.562±0.04553.04±1.306.96±0.17
表6 ASP-SS-Ber/HNK水化時間選擇(, n = 3)
Table 6 ASP-SS-Ber/HNK hydration time selection (, n = 3)
水化時間/min粒徑/nmPDI包封率/%載藥量/% 6038.91±0.130.583±0.07852.59±0.706.84±0.09 8022.87±1.220.476±0.03464.68±2.188.04±0.36 10040.84±1.570.416±0.02369.54±0.448.27±0.17 12029.94±1.630.736±0.04358.95±1.317.62±0.18 14027.12±1.590.934±0.02256.60±0.287.10±0.04
2.5 星點設計-效應面法優化處方
以單因素實驗結果為依據,進一步采用星點設計-效應面法優化制劑工藝。選取載藥比(1)、水化溫度(2)和水化時間(3)3個因素,每因素設3個水平(代碼值分別為?1、0、+1)。以和厚樸酚包封率(1)、和厚樸酚載藥量(2)和膠束粒徑(3)為考察指標進行3因素3水平的星點設計-效應面法實驗,結果見表7。利用Design-Expert 10.0.3統計軟件對表7數據進行統計處理,并獲得1、2、3值對自變量1、2、3的多元線性回歸方程,各考察指標的2項式擬合方程如下1=70.07+7.551+3.242+4.043-1.2712-1.0613+0.5623-12.0312-11.1322-11.5532,<0.01,2=0.913 4;2=8.63-0.651+0.712+0.383-0.3612-0.1213+0.6223-1.0512-1.4322-1.6832,=0.007 1,2=0.906 7;3=45.73+1.831-0.132+0.683-0.6612+0.2613-1.2123-6.4312-2.9022-5.7332,=0.000 1,2=0.972 2。各方程的方差分析結果見表8,3個模型均具有顯著性差異(<0.05),能較好反映因素對響應值的影響。進一步分析各方程中的各項,1、12、22、32對1有顯著性影響;1、2、12、22、32對2有顯著性影響;1、12、22、32對3有顯著性影響。
利用Design-Expert 10.0.3軟件的Analysis模塊繪制自變量對因變量的三維效應面和二維等高線圖:即1、2對1;1、2對2;1、2對3的三維效應面圖和等高線圖,結果見圖2。結果表明,在考察范圍內,愈接近較佳區,面的彎曲度就越大,限制考察指標1、2、3為盡量大,繼續應用Design-Expert 10.0.3軟件Optimization模塊疊加各模型所得的最佳條件范圍得到最終的最優處方:ASP-SS-Ber與和厚樸酚的投藥量分別為5.00 mg和0.71 mg、水化溫度為30 ℃、水化時間100 min。預測在此條件下制備ASP-SS-Ber/HNK的和厚樸酚載藥量與包封率分別為8.63%、70.07%。
表7 ASP-SS-Ber/HNK制備工藝星點設計安排及結果
Table 7 Central composite design and results of preparation technology of ASP-SS-Ber/HNK
試驗號X1X2/℃X3/minY1/%Y2/%Y3/nm 17 (0)30 (0)100 (0)75.119.1145.85 27 (0)30 (0)100 (0)72.769.0045.83 39 (+1)30 (0)80 (?1)55.055.3734.95 49 (+1)30 (0)120 (+1)59.256.1135.43 57 (0)30 (0)100 (0)61.577.4346.04 65 (?1)30 (0)80 (?1)31.615.4432.23 75 (?1)30 (0)120 (+1)40.036.6731.68 87 (0)30 (0)100 (0)74.368.9745.94 95 (?1)40 (+1)100 (0)48.738.3435.85 109 (+1)40 (+1)100 (0)55.055.3338.60 119 (+1)20 (?1)100 (0)47.614.6738.28 127 (0)20 (?1)120 (+1)50.254.4240.76 137 (0)30 (0)100 (0)66.548.6545.00 147 (0)40 (+1)120 (+1)54.387.1436.19 157 (0)20 (?1)80 (?1)41.525.1335.59 165 (?1)20 (?1)100 (0)36.226.2532.89 177 (0)40 (+1)80 (?1)43.395.3735.89
2.6 最優處方的驗證試驗
以上述最優處方條件制備5批ASP-SS-Ber/ HNK,測定和厚樸酚載藥量、包封率,以及膠束粒徑,結果見表9。和厚樸酚平均載藥量為(9.22±0.42)%、平均包封率為(71.77±1.20)%、膠束平均粒徑為(44.38±2.95)nm,實測值與預測值的誤差均小于3%,實驗預測性較好,且3個考察指標的RSD值均較小,工藝重現性較好。
2.7 粒徑、電位測量
取制備好的ASP-SS-Ber/HNK溶液,用Zetasizer Nano-ZS90納米粒度儀測定其粒徑、粒度分布及電位。結果如圖3所示,ASP-SS-Ber/HNK的粒徑為(44.38±2.95)nm,多分散指數(polydispersed index,PDI)0.473±0.33,粒徑分布較為均勻,ζ電位為(?10.32±1.26)mV。
表8 響應面擬合模型對包封率、載藥量、粒徑的方差分析
Table 8 Response surface fitting model on variance analysis of encapsulation rate, load capacity and particle size
方差來源自由度包封率載藥量粒徑 離均差平方和均方F值P值離均差平方和均方F值P值離均差平方和均方F值P值 模型92 574.74286.088.200.005 638.804.317.560.007 1422.0146.8927.190.000 1 X11455.57455.5713.060.008 63.413.415.970.044 526.6826.6815.470.005 7 X2184.1884.182.410.164 34.084.087.150.031 90.130.130.070.793 5 X31130.73130.733.750.094 11.151.152.010.199 03.673.672.130.187 9 X1X216.436.430.180.680 70.510.510.900.375 31.741.741.010.348 3 X1X314.454.450.130.731 40.060.060.110.755 10.270.270.150.706 6 X2X311.281.280.0370.853 71.541.542.700.144 65.885.883.410.107 3 X121609.63609.6317.480.004 14.654.658.150.024 5174.00174.00100.88<0.000 1 X221521.84521.8414.960.006 18.658.6515.170.005 935.3735.3720.510.002 7 X321561.72561.7216.100.005 111.93 11.9320.920.002 6138.29138.2980.18<0.000 1 殘差7244.1934.88 3.990.57 12.071.72 失擬項3108.4436.151.070.457 32.070.691.430.357 311.383.7921.750.006 1 純誤差4135.7533.94 1.920.48 0.700.17 總離差162 818.93 42.79 434.08
2.8 膠束形態學
取制備好的ASP-SS-Ber/HNK溶液,純化水稀釋10倍后,滴加至TEM專用銅網上,晾至半干后,滴加2%的磷鎢酸負染液,靜置晾干后,轉移至透射電鏡下觀察,如圖4所示,ASP-SS-Ber/HNK在透射電鏡下觀察,呈類圓形,表面較光滑,且分散均勻,無黏連現象。

圖2 X1、X2對Y1、Y2、Y3的效應面圖和等高線圖
表9 最優處方的驗證試驗
Table 9 Three batches samples for verification of optimized formulation
試驗號Y1/%Y2/%Y3/nm 173.959.0646.90 273.348.9842.47 370.728.6643.06 471.879.0941.11 568.9910.3048.36 平均值71.779.2244.38 預測值70.078.6345.73 相對誤差/%1.200.422.95
2.9 體外藥物釋放研究
將1 mLASP-SS-Ber/HNK放入透析袋(截留相對分子質量14 000)中。透析袋兩端夾緊,分別浸沒在不同濃度的GSH(0、0.1、1.0、10.0 mmol/L)的PBS(含0.5%聚山梨酯80、pH 7.4)中,同時設置對照組(游離的和厚樸酚)。于37 ℃恒溫搖床中以100 r/min速率水平震蕩72 h。在預定的時間點(0.5、1、2、4、8、12、24、48、72 h)采集1 mL樣品,然后補充相同體積的新鮮釋放介質。樣品過0.45 μm濾膜后注入HPLC,根據下式計算體外累積釋放率。

圖3 ASP-SS-Ber/HNK的粒徑分布(A)和電位分布(B)
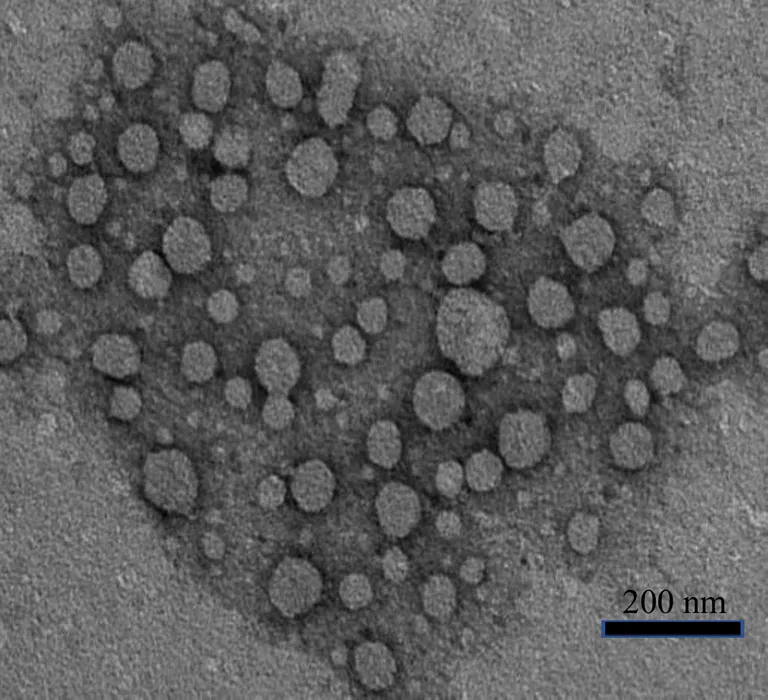
圖4 ASP-SS-Ber/HNK的透射電鏡照片
Q=CV0+∑CV/0
Q為第個時間點的累積釋放百分率,C為第個時間點的藥物濃度,0為釋放介質的體積,C為第個時間點的藥物濃度,V為所取樣品體積,0為載藥膠束中藥物的質量
不同GSH濃度下的ASP-SS-Ber/HNK和和厚樸酚釋放曲線如圖5所示。在最初的12 h內,和厚樸酚快速釋放,累積釋放率為(79.75±2.13)%;24 h累積釋放率為(89.10±3.32)%;72 h累積釋放率為(92.57±2.20)%;隨著釋放介質中GSH濃度的增加,ASP-SS-Ber/HNK中和厚樸酚的累計釋放率也逐漸增加。釋放介質中GSH的濃度為0、0.10、1.00、10.00 mmol/L時,ASP-SS-Ber/HNK中和厚樸酚48 h累積釋放率分別為(4.15±1.27)%、(40.2±2.25)%、(54.10±2.27)%、(78.50±1.25)%;72 h的累積釋放率分別為(5.32±2.36)%、(46.20±2.65)%、(60.70±2.26)%、(80.20±2.21)%。結果表明,ASP-SS-Ber/HNK具有良好的GSH敏感藥物釋放能力,且ASP-SS-Ber/HNK作為載體具有良好的藥物緩釋功能。

圖5 ASP-SS-Ber/HNK在不同溶液中的累積釋放率(, n = 3)
2.10 體外、血清及包封率穩定性考察
2.10.1 儲存穩定性 取ASP-SS-Ber/HNK溶液,通過Zetasizer ZS 90納米粒度儀連續測定其粒徑和電位的數值變化,測定時間為1周,結果見表10。
2.10.2 包封率穩定性 按照“2.3”項下包封率的測定方法,通過HPLC連續測定并計算其包封率的變化,測定時間為1周,考察樣品的包封率穩定性,結果見表10。
2.10.3 血清穩定性 取適量載藥膠束ASP-SS-Ber/ HNK溶液,將其置于加有血清的96孔板中,培養12 h,其中以每小時測定的頻率置于酶標儀下(490 nm)記錄吸光度()值,通過值的改變,考察樣品的血清穩定性,結果見表11。
ASP-SS-Ber/HNK膠束溶液在12 h的吸光度維持在0.29±0.01,7 d內的粒徑穩定在(45.14±0.67)nm,電位穩定在(?10.46±0.60)mV,包封率穩定在(70.42±0.63)%。結果表明,該膠束儲存、血清及包封率穩定性良好。
表10 ASP-SS-Ber/HNK的粒徑、ζ電位、包封率穩定性考察(, n = 3)
Table 10 Investigation of particle size, ζ potential and encapsulation efficiency stability(, n = 3)
t/d粒徑/nmζ電位/mV包封率/% 143.70±0.38?12.03±0.6370.07±0.48 245.75±0.83?9.81±0.5668.59±0.63 345.46±0.93?9.11±0.7370.25±0.83 443.92±0.70?10.90±0.4971.63±0.80 545.57±0.52?11.90±0.5169.45±0.62 646.49±0.41?8.67±0.4470.52±0.71 745.07±0.94?10.77±0.8472.43±0.34
表11 血清穩定性
Table 11 Serum stability
t/hA值t/hA值t/hA值 10.29±0.0250.27±0.0290.30±0.01 20.30±0.0160.29±0.01100.30±0.01 30.29±0.0170.26±0.02110.29±0.01 40.32±0.0180.28±0.02120.31±0.01
3 討論
采用薄膜水化法[21]制備膠束時,初始階段和厚樸酚的載藥量和包封率均偏低,因此嘗試加入表面活性劑來增加載體在溶劑中的溶解量,和厚樸酚的包封率和載藥量均得到了較好的改善。隨后對注射劑中3種常用的表面活性劑進行篩選,其中聚氧乙烯蓖麻油的增溶效果最好并且可溶于水、乙醇、丙二醇等溶劑[22],特別適合含有疏水性物質的水溶液產品的制備,并且在動物體中的毒性試驗表明,聚氧乙烯蓖麻油基本無毒、無刺激性[23]。因此經比較最終確定為不易誘導紅細胞溶血且增溶效果好的聚氧乙烯蓖麻油。
研究表明,腫瘤細胞內的GSH(2~10 mmol/L)濃度是細胞外GSH濃度(2~10 μmol/L)1000倍以上,比正常細胞內濃度高4倍,尤其在一些耐藥腫瘤細胞中,GSH甚至要高出10倍[24]。值得注意的是,腫瘤細胞內線粒體處的GSH濃度則更高[25]。聚合物載體ASP-SS-Ber的親水端當歸多糖和疏水端小檗堿是通過二硫鍵相連,而二硫鍵具有谷胱甘肽敏感性,添加谷胱甘肽,使得二硫鍵裂解,釋放出和厚樸酚[1]。
在釋放實驗中,釋放介質未加入GSH時,HPLC下檢測到極低的和厚樸酚峰面積,72 h和厚樸酚的釋放僅為(5.32±2.36)%。和厚樸酚在0.1 mmol/L GSH釋放介質中72 h的累計釋放率為(46.2±2.65)%,而在1.0、10.0 mmol/L GSH釋放介質中和厚樸酚的累計釋放率達到(60.7±2.26)%和(80.2±2.21)%,分別是0.1 mmol/L GSH的1.3倍和1.7倍,當GSH濃度增加ASP-SS-Ber/HNK二硫鍵裂解,釋放出更多的和厚樸酚,和厚樸酚的釋放具有GSH濃度相關性。而在4種釋放介質中GSH濃度下48 h與72 h的累計釋放率變化很小,可能的原因是,在GSH的作用下,48 h時,ASP-SS-Ber/HNK中二硫鍵裂解的化學反應達到了化學平衡點,和厚樸酚的釋放基本達到平衡,ASP-SS-Ber/ HNK 48 h可基本發揮藥效[2]。
綜上,本研究采用薄膜水化法制備了ASP-SS- Ber/HNK膠束,并通過加入聚氧乙烯蓖麻油作為表面活性劑提高了ASP-SS-Ber/HNK的包封率和載藥量,進一步通過單因素實驗與星點設計-效應面法實驗優化得到ASP-SS-Ber/HNK的最優處方工藝。該膠束制劑在電鏡下形貌呈圓形,粒徑(44.38±2.95) nm,ASP-SS-Ber/HNK的血清穩定性是根據粒子均勻分散在血清中的紫外吸光度值進行考察的,如粒子不穩定,就會在血清中發生聚集,吸光度就會增大。結果顯示的ASP-SS-Ber/HNK血清溶液在12 h內吸光度未見明顯增大,表明粒子未發生聚集,比較穩定。ASP-SS-Ber/HNK具有GSH濃度依賴性的釋放,為該制劑的有效開發奠定了基礎。
利益沖突 所有作者均聲明不存在利益沖突
[1] Fang L, Lin H, Wu Z F,./vivo evaluation of novel mitochondrial targeting charge-reversal polysaccharide- based antitumor nanoparticle [J]., 2020, 234: 115930.
[2] Fang L, Fan H Y, Guo C J,. Novel mitochondrial targeting multifunctional surface charge-reversal polymeric nanoparticles for cancer treatment [J]., 2019, 15(11): 2151-2163.
[3] Guo C J, Hou X Y, Liu Y H,. Novel Chinesepolysaccharide biomimetic nanomedicine to curcumin delivery for hepatocellular carcinoma treatment and immunomodulatory effect [J]., 2021, 80: 153356.
[4] Wang K P, Xu J Y, Liu Y,. Self-assembledpolysaccharide nanoparticles with an instinctive liver-targeting ability as a drug carrier for acute alcoholic liver damage protection [J]., 2020, 577:118996.
[5] Zhang Y, Cui Z, Mei H,.polysaccharide nanoparticles as a targeted drug delivery system for enhanced therapy of liver cancer [J]., 2019, 219: 143-154.
[6] Tuo J, Xie Y Q, Song J,. Development of a novel berberine-mediated mitochondria-targeting nano-platform for drug-resistant cancer therapy [J]., 2016, 4(42): 6856-6864.
[7] Yin J T, Hou Y T, Yin Y Y,. Selenium-coated nanostructured lipid carriers used for oral delivery of berberine to accomplish a synergic hypoglycemic effect [J]., 2017, 12: 8671-8680.
[8] Song J, Lin C C, Yang X,. Mitochondrial targeting nanodrugs self-assembled from 9--octadecyl substituted berberine derivative for cancer treatment by inducing mitochondrial apoptosis pathways [J]., 2019, 294: 27-42.
[9] Cheng Y, Ji Y H. Mitochondria-targeting nanomedicine self-assembled from GSH-responsive paclitaxel-ss-berberine conjugate for synergetic cancer treatment with enhanced cytotoxicity [J]., 2020, 318: 38-49.
[10] Yang G L, Chen C, Zhu Y C,. GSH-activatable NIR nanoplatform with mitochondria targeting for enhancing tumor-specific therapy [J]., 2019, 11(48): 44961-44969.
[11] Tan L H, Wang Y F, Ai G X,. Dihydroberberine, a hydrogenated derivative of berberine firstly identified in, exerts anti-inflammatory effect via dual modulation of NF-κB and MAPK signaling pathways [J]., 2019, 75: 105802.
[12] 史曉佳. 和厚樸酚線粒體靶向衍生物的合成與抗腫瘤活性研究 [D]. 濟南: 山東大學, 2020.
[13] 黃家喜, 李晶, 鮑翠玉. 和厚樸酚對高脂所致心肌細胞氧化應激損傷的保護作用及其與內質網應激-線粒體凋亡通路的相關性 [J]. 中國藥理學通報, 2020, 36(6): 809-814.
[14] Ong C P, Lee W L, Tang Y Q,. Honokiol: A review of its anticancer potential and mechanisms [J]., 2019, 12(1): 48.
[15] 陳一楨, 張文娟, 唐蘭如, 等. 和厚樸酚長循環脂質體的制備及藥動學研究 [J]. 中草藥, 2017, 48(18): 3720-3727.
[16] 孫強, 何曼, 張夢, 等. 小檗堿抗腫瘤作用機制的研究進展 [J]. 中草藥, 2021, 52(2): 603-612.
[17] Zhu D W, Tao W, Zhang H L,. Docetaxel (DTX)-loaded polydopamine-modified TPGS-PLA nanoparticles as a targeted drug delivery system for the treatment of liver cancer [J]., 2016, 30: 144-154.
[18] 梁宇飛, 張欣欣, 許潔, 等. 星點設計-效應面法優化姜黃素-胡椒堿聚合物復方膠束的處方工藝研究 [J]. 中草藥, 2020, 51(1): 43-50.
[19] 張喜武, 李秋晗, 劉美欣, 等. 星點設計-效應面法優化丁香苦苷聚乳酸-羥基乙酸納米粒的制備工藝 [J]. 中草藥, 2019, 50(17): 4108-4113.
[20] Kumar S, Jiang D W, Sun B Y,. Labeling of erythrocytes by porphyrin-phospholipid [J]., 2021, 1(1): 2000013.
[21] 寧雙成, 周莉莉, 王敏, 等. 星點設計-效應面法優化斑蝥素納米結構脂質載體處方工藝 [J]. 中草藥, 2019, 50(17): 4114-4122.
[22] 易紅, 高進, 楊華, 等. 幾種注射用表面活性劑的質量標準及安全性概述 [J]. 中國實驗方劑學雜志, 2010, 16(1): 115-119.
[23] 刁兆玉, 成朋, 王仲妮. 表面活性劑溶血作用的研究進展 [J]. 食品與藥品, 2010, 12(3): 125-129.
[24] 萬冬, 習鈺晶, 李孫帆, 等. 基于腫瘤微環境的響應性納米藥物載體的研究進展 [J]. 化學工業與工程, 2021, 38(5): 80-87.
[25] Fang L, Zhang W, Wang Z,. Novel mitochondrial targeting charge-reversal polysaccharide hybrid shell/core nanoparticles for prolonged systemic circulation and antitumor drug delivery [J]., 2019, 26(1): 1125-1139.
Optimization of prescription process ofpolysaccharide-berberine micelle loaded with honokiol by central composite design-response surface method
WANG Bin-bin, LYU Bai, ZHANG Qi, WANG Ling-yu, ZHANG Xu, YU Chao, ZHOU Jian-wen, HAN Cui-yan
School of Pharmacy, Qiqihar Medical College, Qiqihar 161006, China
To optimize the prescription process ofpolysaccharide (ASP)-berberine (Ber) micelle loaded with honokiol (HNK) (ASP-SS-Ber/HNK) by central composite design-response surface method and investigate its formulation properties.The content of HNK was determined by HPLC; ASP-SS-Ber/HNK was prepared by thin film hydration method. On the basis of single factor experiment, particle size, drug loading and encapsulation rate were used as the evaluation index to screen the prescription process for drug loading ratio, hydration temperature and hydration time. Central composite design-response surface method was used to carry out three factors and three levels experiment, and the results were analyzed to get the optimal prescription process and verify it. The morphology, average particle size and ζ potential of ASP-SS-Ber/HNK were observed and determined by transmission electron microscope and particle size analyzer, and the drug delivery system was evaluated bydrug release and its stability was examined.The optimal preparation process was as follow: the dosage ofpolysaccharide- berberine carrier (ASP-SS-Ber) and HNK was 5.00 mg and 0.71 mg, the hydration temperature was 30 ℃, and the hydration time was 100 min. The compound loaded with HNK micelles prepared by the optimum formulation had the loading capacity of (9.22 ± 0.42)% and entrapment rate of honokiol was (71.77 ± 1.20)%; the average particle size of the micellar preparation was (44.38 ± 2.95) nm and the ζ potential was close to (?10.32 ± 1.26) mV. The cumulative release amount inrelease medium containing glutathione (GSH was 10 mmol/L) reached 80.2% in 72 h; the absorbance for 12 h was maintained at (0.29 ± 0.01)%, the particle size was stabilized at (45.14 ± 0.67)% for seven consecutive days, and the potential was stabilized at (?10.46 ± 0.60) mV.The model established by central composite design-response surface method had high accuracy and could be used to optimize the formulation of ASP-SS-Ber/HNK micelle preparations.
honokiol;polysaccharide; berberine; micelle; film hydration method; central composite design-response surface method
R283.6
A
0253 - 2670(2022)04 - 1021 - 09
10.7501/j.issn.0253-2670.2022.04.008
2021-09-14
齊齊哈爾市科技攻關項目(LHYD-2021001);國家自然科學基金項目(82174097)
王彬彬,碩士研究生。Tel: 18249277702 E-mail: 2076963831@qq.com
韓翠艷,教授,碩士生導師。Tel: (0452)2663822 E-mail: hcymuphar@qmu.edu.cn
[責任編輯 鄭禮勝]

