CRISPR/Cas9技術在家禽育種方面的應用
莊重, 趙龍, 白皓, 畢瑜林, 黃應權, 陳國宏, 常國斌*
(1.揚州大學動物科學與技術學院,江蘇 揚州 225009;2.揚州大學農業科技發展研究院,教育部農業與農產品安全國際合作聯合實驗室,江蘇 揚州 225009;3.江蘇綠佳生態科技有限公司,江蘇 泰州 221000)
基因編輯,又稱基因組編輯或基因工程,能夠精確地對基因組中特定的目標基因進行修飾。近年來,隨著編輯潛能強大的新型基因編輯技術——規律成簇間隔短回文重復序列(clustered regulatory interspersed short palindromic repeat,CRISPR)被發現,基因編輯效率在本質上有了極大的提升。CRISPR技術2013、2015年連續兩次被Science評為年度十大科學突破[1-2];Nature也于2019年將其列為10年內最具影響力的5個重大科學事件之一[3];2020年,埃馬紐埃爾·卡彭蒂耶(Emmanuelle CHARPENTIER)和詹妮弗·杜德納(Jennifer DOUDNA)因對CRISPR基因編輯技術的杰出貢獻被授予諾貝爾化學獎。CRISPR/Cas9技術的出現極大地開拓了人們對生物體研究的領域,為生命本質的研究提供了更多的可能。與傳統基因編輯技術相比,CRISPR/Cas9技術設計簡單、成本低廉、操作方便、效率可觀,已成為目前常用的基因編輯技術。本文綜述了基因編輯的發展歷程,并剖析了CRISPR/Cas9系統的結構與類型以及其在家禽遺傳育種中的應用,總結了CRISPR/Cas9技術在家禽研究中存在的一些問題,并提出意見和建議,為CRISPR/Cas9技術在家禽育種中的深入研究提供參考和借鑒。
1 基因編輯技術的發展
目前運用較多的三種基因編輯技術為鋅指核酸酶(zinc finger endonuclease,ZFN)[4]、轉錄激活因子效應物核酸酶(transcription activitor-like effector nuclease,TALEN)[5]以及CRISPR[6],這些基因編輯技術為基因功能、基因改良以及基因治療的研究拓寬了道路。由于ZFN技術設計復雜、成本高昂,TALEN載體較大、具有高度的重復序列,難以實現多基因敲除,限制了它們的應用和發展,CRISPR逐漸受到人們重視。CRISPR是一種有規律的間隔短回文重復序列,于1987年[7]被發現,隨后科學家們對這種重復序列進行了深入研究,發現細菌和古細菌中普遍存在這種序列,在2002年正式將它命名為“clustered regularly interspaced short palindromic repeats(CRISPR)”[8]。然而,最初人們并不知道這種序列的具體作用,2005年,Bolotin 等[9]、Mojica等[10]、Pourcel等[11]在研究中發現,CRISPR的間隔序列與外來遺傳物質具有非常高的相似性,他們推測CRISPR在細菌抵抗外來遺傳物質入侵的過程中起著一定的作用。2006年,Makarova等[12]使用生物信息學手段對CRISPR進行分析,推測其在細菌與古細菌中作為一種獲得性免疫系統而存在。此后,Barrangou 等[13]與Marraffini等[14]分別驗證了CRISPR能夠在細菌中抵御噬菌體的入侵。
近年來,CRISPR/Cas技術在基因編輯中的應用取得了長足發展,2010年,Garneau等[15]利用間隔序列引導Cas9蛋白對目的基因進行切割,發生了雙鏈斷裂,首次證實CRISPR/Cas9具有基因編輯的潛力。此后不久,對哺乳動物基因的成功編輯[16]更是打開了利用CRISPR/Cas9機制進行基因編輯的大門。2014年,Hai等[17]通過將靶向vWF(血管血友病因子)基因的sgRNA顯微注射入豬受精卵中,成功制備了首例vWF基因敲除豬,并建立起血管性血友病基因豬模型,該模型的建立對提高豬屠宰和采血的出血效率都具有較大幫助。同年,Han等[18]利用相同方法,成功獲得了兩只肌肉生長素(MSTN)基因編輯羔羊,由此證明將Cas9:sgRNA直接注射到受精卵中可以廣泛應用于構建大型家畜基因敲除模型。在此基礎上,Wang等[19]利用CRISPR/Cas9系統成功制備了MSTN和FGF5基因編輯山羊,并證明基因編輯后的山羊次級毛囊數量以及羊絨長度顯著增加,這為改良山羊肉品質以及羊毛纖維品質提供了新的思路。2015年,Heo等[20]首次將CRISPR/Cas9技術使用在牛的基因編輯中,成功獲得了經過基因編輯的牛多能干細胞(ips)和胚胎,為之后基因編輯牛打下基礎。除此之外,Niu等[21]證實,在食蟹猴的單細胞胚胎中同時注射Cas9mRNA和sgRNA,可以使PPAR-γ基因與Rag1基因產生突變,更是讓這項技術在人類疾病基因治療上應用成為了可能。截至目前,CRISPR技術已廣泛應用在模式生物,如斑馬魚[22]、小鼠[23]、細菌[24]和農作物玉米[25],以及山羊[26]、牛[27]、豬[28]等家畜的基因編輯中。隨著CRISPR/Cas9技術的逐漸成熟,這項技術將對基因修飾、疾病治療以及動植物品種改良等研究有劃時代的意義。
2 CRISPR/Cas9系統的組成和作用機制
CRISPR/Cas9系統是一種自適應性免疫系統,在許多細菌與古細菌中基本分為3個步驟發揮作用(圖1)[16,29]:第1步為適應,從外源核酸獲得新的間隔區,插入CRISPR 5’端的兩重復序列之間;第2步是CRISPRRNA(crRNA)的生物發生,CRISPR基因座被轉錄成小的干擾型crRNA;第3步是靶向識別,crRNA引導Cas核酸酶進行同源序列的特異性切割[16]。根據CRISPR/Cas9系統中蛋白的種類不同以及識別機制的差異大致可以分為3類[29],其中Ⅰ型與Ⅲ型系統都需要多種Cas蛋白復合體才能發揮作用,比較復雜,而Ⅱ型系統非常簡便,其主要由Cas9蛋白、crRNA、tracrRNA組成,自身的下游沒有PAM(protospacer adjacent motifs)序列,外源DNA的間隔序列的3’端存在1個PAM序列,Cas9蛋白借此對外源DNA進行識別,從而避免自我免疫[30]。目前,CRISPR/Cas9已成為應用最廣泛的基因編輯技術。
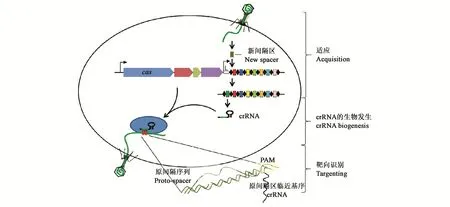
圖1 CRISPR/Cas9系統的功能機制(根據參考文獻[29]修改)Fig.1 Functional characteristics of CRISPR/Cas9 system(modified on reference[29])
CRISPR/Cas9的基因座5’端為能夠與crRNA形成crRNA-tracrRNA復合體的tracrRNA基因,其可以指導Cas9與crRNA-tracrRNA進行結合;Cas蛋白編碼基因3’端為CRISPR基因座,由啟動子、spacers和重復序列組成,其中,spacers主要負責引導Cas9蛋白精確識別非自身DNA與自身DNA,從而實行定點切割并避免自我免疫。Cas9蛋白對于靶DNA的識別不僅需要crRNA-tracrRNA復合物的引導,靶位點上的PAM序列也是其區分外源和內源DNA的重要標識。首先,crRNA-tracrRNA復合物對外源DNA進行掃描,只有當crRNA與外源DNA互補配對且3’端具有PAM序列時,Cas9蛋白才會對外源DNA進行切割,Cas9蛋白中包含有RuvC結構域、HNH結構域、識別區REC以及位于C端的PAM區,RuvC與HNH分別切割目的外源基因DNA的互補鏈與非互補鏈,使DNA的雙鍵斷裂。當RuvC中的D10A失活或突變時會導致RuvC失活,HNH中的H840A突變同樣可使HNH失活。D10A與H840A都突變會形成dCas9(dead Cas9),而單點突變可使Cas9成為切口酶,切割外源DNA后會造成DNA單鏈斷裂[31-32]。
3 CRISPR/Cas9技術在家禽育種中的應用
家禽作為一種農業經濟動物,具有生長周期短、飼料報酬率高、繁殖力強等特點,是生物學領域重要的蛋白質來源[33],也是脊椎動物發育生物學非常有價值的模型[34]。與傳統育種相比,CRISPR/Cas9技術可以給育種者提供更多的遺傳選擇,并通過基因組編輯快速提高后代的生產性能、繁殖性能和抗病性能,以滿足消費者對家禽日益增長的需求。此外,利用CRISPR/Cas9技術在家禽上還可以進行性別決定,不僅降低生產成本,而且可以改善動物福利。因此,通過CRISPR/Cas9技術進行基因改造,進而推動家禽業發展具有廣闊發展前景。以下將對近些年CRISPR/Cas9技術在家禽功能基因研究中的應用進行總結,并重點介紹一些具有經濟價值的基因編輯模型。
3.1 在家禽功能基因研究中的應用
3.1.1 在細胞中的應用 CRISPR/Cas9系統已廣泛應用于家禽細胞基因編輯中(表1),其中在雞成纖維細胞(DF-1)、雞胚胎干細胞(ESCs)、雞原始生殖細胞(PGCs)上應用較多。隨著CRISPR/Cas9的快速發展,細胞培養系統能夠更容易地靶向不同基因,研究者在探究不同功能基因效應的同時,也不斷證明利用CRISPR/Cas9對家禽進行基因編輯從而進行性狀改良與育種研究具有可行性。
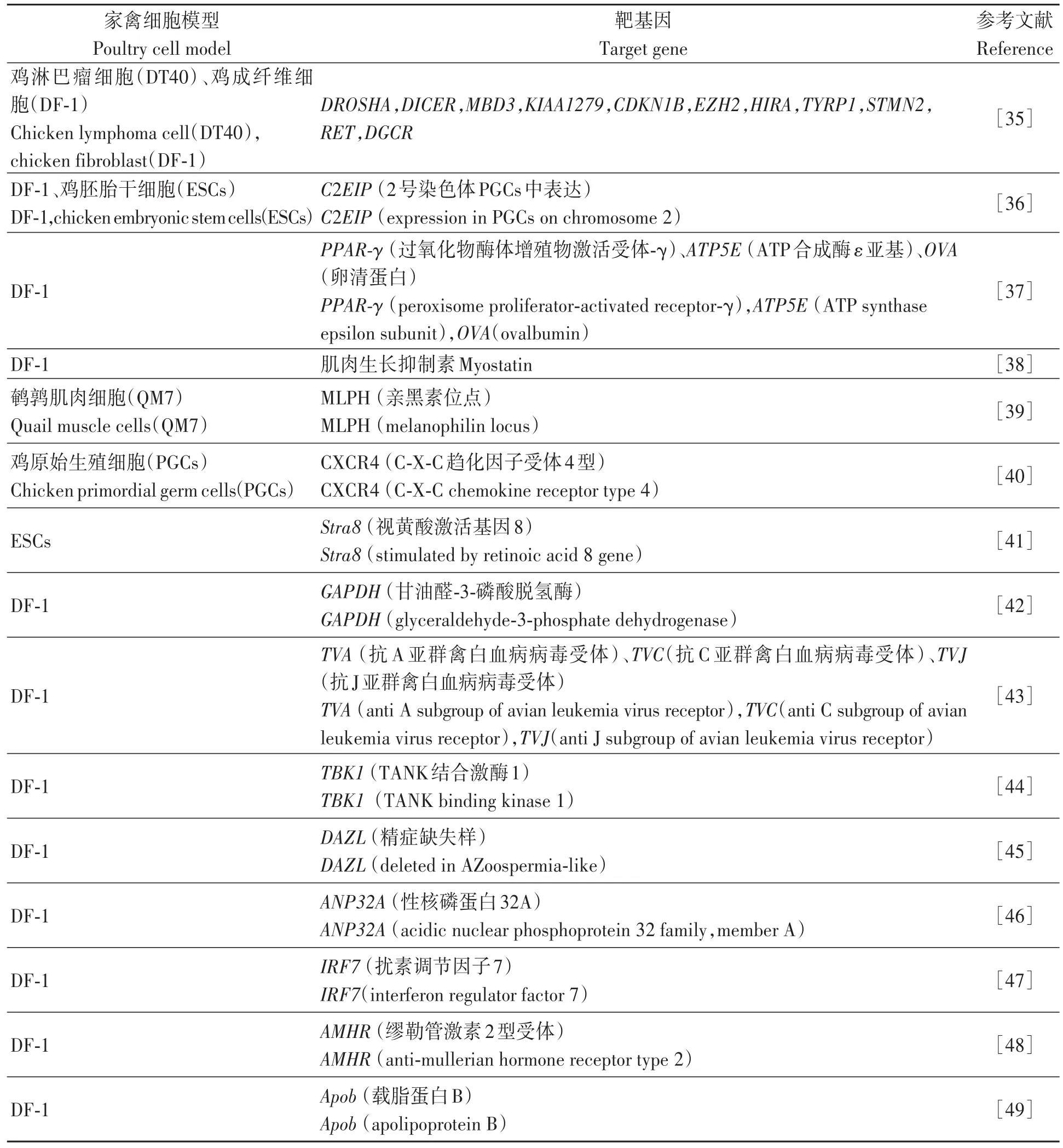
表1 CRISPR/Cas9系統在家禽細胞系模型上的應用Table 1 Application of CRISPR/Cas9 system in poultry basal cell model
3.1.2 在胚胎發育模型中的應用 與其他動物胚胎相比,雞胚發育過程清晰、來源方便、易于操作、利于大量實驗樣本同時觀測[50],是經典的胚胎發育模型,其對于研究脊椎動物胚胎學的生理、病理以及毒理學等也具有重要的指導意義[51-52]。近年來,使用CRISPR/Cas9技術在探究胚胎相關功能基因功能方面取得了豐碩的成果。
2015 年,Véron 等[53]通過電穿孔胚胎以及CRISPR/Cas9技術得到了敲除PAX7基因的雞胚,首次證明了利用CRISPR/Cas9系統對雞胚體細胞進行基因編輯具有可行性。隨后,Abu-Bonsrah等[35]在Véron等[53]的基礎上再次結合兩種技術,敲除了兩個細胞系中DROSHA、DICER、MBD3、KIAA1279、CDKN1B、EZH2、HIRA、TYRP1、STMN2、RET和DGCR共計11個與胚胎發育或胚胎患病相關的基因,并將其轉染入胚胎中,結果表明,CRISPR技術能對雞胚進行有針對性地基因改造,且所有靶基因的切割效率均在20%~68%之間,為胚胎發育過程中的疾病模型研究提供思路。此外,Zuo等[36]還將含有被PEI包裹的gRNA-3載體注射到雞胚胎中,建立了敲低效率為15%的穩定細胞、胚胎CRISPR/Cas9基因敲低系統,為利用CRISPR/Cas9系統在雞胚胎中進行基因改造建立基礎。Williams等[54]構建并優化了雞U6啟動子體內介導sgRNA表達的微型載體系統,創建了能夠對內源性增強子和啟動子進行表觀基因組操作并帶有Citrine報告基因的野生型Cas9表達載體。通過觀察發現,CRISPR/Cas9技術可以對內源性增強子起到調節作用,為接下來探究雞胚中基因間的相互調控作用提供了參考。
3.2 在家禽基因編輯模型制備中的應用
由于難以獲得和操縱合子,傳統基因編輯技術難以應用到家禽上,因此對家禽的基因改造遠遠落后于其他動物。近年來研究發現,通過結合基因編輯技術與PGC體外培育技術,極大地提高了制備家禽基因編輯模型的效率。2013年,Schusser等[55]首次從雞胚胎中獲得PGC細胞,將其體外培養后導入已編輯的基因,再把處理后的PGC細胞顯微注射入受體胚胎血管中,最終完成受體孵化,生產出了第1只敲除JH基因的無B細胞基因編輯雞。2016年,Oishi等[56]通過嘌呤霉素和博來霉素實現了對雞PGC中的卵清蛋白(ovum albumin,OVA)和卵類黏蛋白(ovomucoid,OVM)基因的敲除,并將成功敲除了OVA、OVM基因的PGC細胞注入雞胚血管中,得到3個可以產生突變精子轉基因嵌合體的公雞種系,突變效率高達90%。此后,不同基因編輯模型的研究進程大大加快,為開發家禽優質育種資源提供了更多選擇。
3.2.1 在家禽疾病中的應用 疾病對于家禽的生產有較大的限制,隨著CRISPR/Cas技術在基因編輯方面日漸成熟,使用該技術對家禽抗病性能進行品種改良便成為熱點課題。
禽白血病病毒(avian leukosis virus,ALV)是生產中對家禽危害較大的病原之一,給家禽業造成了嚴重的經濟損失。2017年,Lee等[57]通過將CRISPR/Cas9載體與單鏈寡脫氧核苷酸(singlestranded oligonucleotide nucleotide,SSODN)組合的同源定向修復(homology directed repair,HDR)對NHE1進行精確地基因組編輯,致使DF-1細胞對ALV-J感染產生抗性,為抗病雞品種培育奠定了基礎。之后不久,Lee等[58]又使用相同的方法對TVA基因外顯子2進行敲除,得到了可以增強ALV-A的抗性的DF-1細胞。他們還準備采用相同的方法對PGC以及ECS細胞進行基因組編輯,以獲得新型的多抗病基因組編輯雞。2020年,Koslová等[59]使用CRISPR/Cas9完成了對NHE1基因的精確敲除,制備出的基因編輯模型對禽白血病病毒J亞群產生抗性。這些研究表明,使用CRISPR/Cas9對家禽基因組進行編輯可以培育出高抗病性的基因編輯品系,為緩解疾病對家禽生產的影響提供了新的思路。
火雞皰疹病毒(herpesvirus of turkeys,HVT)是一種α皰疹病毒,因其與馬立克式病毒(Marek’s disease virus,MDV)抗原相關而被廣泛用作預防馬 立 克 病(MD)的 活 疫 苗 。 Tang等[60]使 用CRISPR/Cas9技術代替傳統的重組和BAC重組技術,將IBDV的VP2插入HVT的基因座,快速高效地制備了表達VP2基因的重組HVT疫苗,證明通過在病毒的不同基因座位置插入其他病毒抗原基因來開發多價重組HVT載體疫苗是可行的,為使用CRISPR/Cas9系統平臺開發新型多價載體疫苗奠定基礎。2020年,Tang等[61]又在此基礎上使用CRISPR/Cas9技術在HVT的基因座中插入IBDV的VP2基因、ILTV的gDgI基因和H9N2流感病毒的HA基因,構建出HVT-VP2-gDgI-HA三重插入重組HVT疫苗,為生產可預防多種禽類疾病的疫苗提供參考。
在鴨疾病中主要是利用CRISPR/Cas技術進行鴨乙肝病毒[62]、禽孢疹病毒疫苗[60]及禽類流感病毒的相關研究[56]。CRISPR/Cas9技術在家禽病毒方面的應用和貢獻也說明了這項技術在家禽的致病性基因的編輯和治療方面擁有廣泛的應用前景。
3.2.2 在家禽生長發育和性別決定中的應用
CRISPR/Cas9技術也廣泛地用于研究家禽生長發育和性腺分化,Myostatin(肌肉生長抑制素)于1997年被發現,其參與肌肉生長發育及分化的各個階段,與肌肉質量有較高的相關性[63]。2017年,Lee等[38]對肌生成過程中抑制肌肉細胞生長和分化的雞Myostatin進行靶向缺失和突變,通過檢測發現突變效率為100%,這為進一步探討Myostatin對雞肌肉質量的影響奠定基礎。邱桂如等[64]利用CRISPR/Cas9技術敲除雞DF-1細胞中IHH基因,并證明了該基因與雞的匍匐性狀關系密切,為解決生產中雞的匍匐性狀問題提供了思路。載脂蛋白B(apolipoprotein B,Apob)主要在小腸和肝臟中合成,在甘油三脂的合成和分泌中發揮重要作用,對雞的生長和脂肪沉積有較大影響[65],吉琳等[49]通過構建Apob基因敲除載體轉染DF-1細胞,得到了成功敲除Apob基因的DF-1細胞,并證明亞克隆細胞的mRNA表達量顯著降低,這為繼續研究Apob基因對雞脂肪沉積的影響建立了平臺。
2017年,Zhang等[41]設計了3個sgRNA來完成對雞DF-1、ESCs細胞中Stra8基因的敲除,發現ESCs向 SSCs(spermatogonia stem cells,精原干細胞)的分化受到抑制,由此證實Stra8基因對控制ESCs向SSCs分化起著決定性的作用,這為家禽性別控制提供可能。同年,Zuo等[66]通過RNA測序發現C1EIS基因在SSCs優先表達,隨后構建了C1EIS基因敲除載體以探究其在ESCs向SSCs分化過程中所起的作用。結果表明,經T7EI酶切和TA克隆測序檢測敲除效率為40%,當C1EIS缺乏時,ESCs向SSCs分化受到抑制,這證明了C1EIS基因在雞性腺發育過程中起著重要的作用,為家禽性腺發育與誘導發育的研究拓寬了思路和視野。作為雞性腺分化和生長發育的候選基因,DMRT1一直被廣泛關注,楊秀榮等[67]利用sgRNA平臺進行DMRT1基因敲除,成功構建了一個DMRT1基因敲除模型,為接下來進一步研究DMRT1基因功能奠定基礎。研究表明,抗繆勒氏管激素(anti-mullerian hormone,AMH)對卵泡選擇有重要影響,黃思嘉等[48]通過靶向構建AMRH2敲除載體,成功敲除了DF-1細胞中的AMRH2基因,為繼續研究AMHR2基因在細胞中的作用構建了敲除模型。
4 CRISPR/Cas9技術在家禽應用中存在的問題
CRISPR/Cas9基因編輯技術設計簡單、便于操作、成本低廉,且能夠高效地對目的基因進行編輯修飾,不斷地推動著人類對生命的探究,但其也逐漸暴露出一些關鍵問題。下面分析CRISPR/Cas9系統在家禽應用中存在的部分問題,并總結一些具有可行性的優化方法,以期為問題的解決提供參考。
4.1 脫靶效應
無論是傳統的還是新型的基因編輯技術都存在一定的脫靶問題,雖然CRISPR的脫靶率相較傳統基因編輯技術有所降低,但是其脫靶效應仍然給研究工作帶來了諸多的困擾。已經有多項研究表明,在使用CRISPR/Cas9技術對目的基因進行敲除的過程中存在著較為明顯的脫靶現象,但是目前還未能找到有效控制脫靶效應的方法,這是限制CRISPR技術發展的主要因素,也是目前該技術的瓶頸。CRISPR/Cas9技術在家禽方面應用的脫靶效應尤為明顯,編輯效率僅有26%[36],遠低于在哺乳動物以及植物中的基因編輯效率,并且脫靶效應還會對家禽隨機位點產生不利突變,這會對生產中轉基因家禽的安全性和有效性產生重大影響,因此解決脫靶效應是當前亟待解決的問題。為了降低脫靶效應,研究者們已經從各個方面對CRISPR/Cas9系統進行優化,下面將從Cas9核酸酶優化、載體傳遞優化、實驗設計優化等方面進行總結,為此后家禽基因編輯研究中最大程度降低脫靶效應提供思路和參考。
4.1.1 Cas9核酸酶優化 對Cas9核酸酶變異體優化來說,目前應用在家禽中最為廣泛的Cas9核酸酶是來源于化膿性鏈球菌(SpCas9),但是其對于全基因組會產生非靶標突變。近年來人們一直努力開發Cas9變異體以及其他同源基因來代替SpCas9,使系統表現出更小的突變性以及更高的特異性,從基礎上改善脫靶效應。2018年,Kumar等[68]利用金黃色葡萄球菌Cas9核酸酶(SaCas9)開發出一種AAV(腺相關病毒)載體工具包,并將其對體外細胞基因編輯后發現,SaCas9可以識別較長的PAM序列,相對只能識別較短PAM序列的SpCas9來說,使用SaCas9基因編輯可能會產生非常小的非目標突變。除此之外,研究者還發現XCas9[69]、Cas9-NG[70]和 evoCas9[71]等 SpCas9 變異體都表現出比SpCas9更低的脫靶效應,并且已經逐漸將其應用于目前的CRISPR/Cas9技術中。
4.1.2 載體傳遞優化 改變病毒載體傳遞方法也是降低脫靶效應的手段,由于現行的CRISPR/Cas9系統進行基因編輯時會一直存在于目的細胞中,很容易導致細胞基因組改變,從而影響目標效應。因此,腺病毒由于其難以整合到靶細胞基因組的特點[72]而被逐漸用于傳遞病毒載體構建中,通過腺病毒傳遞病毒載體可以很大程度地避免目的效應偏離,降低脫靶效應。使用非病毒進行載體遞送研究近年來也逐漸興起,研究者們通過直接向靶細胞遞送核糖核蛋白復合物(ribonucleoprotein,RNP)發現,RNP隨著時間延長逐漸降解[73],這對于利用優化載體傳遞方法最大限度地減少基因組改變,從而減少靶外突變、降低脫靶效應具有重要意義。
4.1.3 實驗設計優化 除了以上優化方法,未來研究還可以通過對靶點的慎重篩選、適當縮小sgRNA長度以及設計成對sgRNA結合單切口酶或者dcas9-fokI融合酶等來降低CRISPR技術的脫靶效應。盡量確保CRISPR/Cas9系統的穩定性和重復性,并在提高CRISPR/Cas9技術精準性的同時深入探索cas9基因的特異性,在破除技術壁壘的同時逐漸完善CRISPR/Cas9在家禽基因功能以及基因組的應用。
4.2 其他問題
除了脫靶效應,轉染效率[74]、生殖系傳遞效率較低[75]也是限制家禽CRISPR/Cas9技術發展的重要因素。隨著PGC介導的轉基因和基因組編輯的廣泛應用,這方面問題已經逐漸得到解決。通過先對PGC進行轉染,再將體外培養的PGC細胞注射到宿主體內的方法,可以大大提升細胞轉染效率以及生殖系傳遞效率(高達90%)。伴隨該技術的逐漸優化與成熟,轉染效率以及生殖系傳遞效率在此基礎上還會再進一步提升。此外,不同的物種所需要的cas9基因以及sgRNA啟動子也不盡相同,RNA聚合酶Ⅲ依賴的U6和U3便可較好地在時間和空間上表達原核生物的gRNA[76],而非U6和U3啟動子就可能出現在動物中不正常表達的gRNA。所以通過尋找家禽最適啟動子這一方法來提高CRISPR技術的穩定性和高效性也值得研究者們重視。
5 結語
CRISPR/Cas9技術的出現打破了傳統基因工程技術效率低、成本高、穩定性差的局面,推動家禽基因編輯技術快速發展,對家禽基因組編輯模型的發展以及生產性能的提高作出杰出貢獻。但脫靶效應很大程度上制約了CRISPR/Cas9技術在家禽中的應用,應盡快找到控制其脫靶效應的突破口,大力推廣CRISPR/Cas9技術在家禽遺傳育種中的應用,提升家禽生產效率,相信其在家禽的各項研究領域必然擁有很廣闊的發展空間。近幾年,能夠切割出黏性末端便于插入連接的CRISPR/cpf1系統的發現與應用[77],以及基于失活的Cas9系統利用FokⅠ酶進行切割從而提高切割效率等方法的發現[78],都展現出CRISPR/Cas9系統的強大潛力與開發和利用的空間。科學家們也在不斷努力地尋找可以控制CRISPR/Cas9系統的開關蛋白[79],并且已有一些成功降低脫靶效應的效應蛋白得到了驗證[80]。這些都展現出CRISPR技術還擁有巨大的改進空間和廣闊的發展前景。通過人們不斷地努力探索和完善,CRISPR技術變得更加精確之后必然會得到廣泛的應用,成為探索生命本質的利器從而帶來更大的效益。

