浸潤性乳腺癌中miR-608和MIF的表達及臨床意義
張 偉,劉 霞,何 雷,張偉璇,焦南林
2020年全球癌癥報告顯示,乳腺癌的發病率和病死率位居女性癌癥的首位[1]。乳腺癌術后復發和轉移是導致患者死亡的主要原因,因此,探索乳腺癌發生、發展機制和尋找新的分子靶點具有重要意義。非編碼小RNA(microRNAs, miRNAs)具有調節信使RNA翻譯和降解的功能,其在乳腺癌的發生、進展和治療中發揮重要作用[2-3]。文獻報道miR-608可以調控AKT/FOXO3a信號通路抑制膀胱癌的增殖[4],還可以結合TFAP4蛋白抑制非小細胞肺癌的遷移[5]。關于乳腺癌中miR-608的報道較少[6],miR-608在乳腺癌中的表達及其生物學功能尚不清楚。巨噬細胞移動抑制因子(macrophagemigration inhibitory factor, MIF)是一種多功能細胞因子,在免疫調節、炎癥反應及腫瘤發生中均具有重要作用[7]。文獻報道肺腺癌[8]和腦膠質瘤[9]中miR-608靶向結合MIF調控腫瘤的侵襲和轉移。本文通過檢測乳腺癌中miR-608與MIF的表達,分析兩者表達的相關性,初步探討miR-608調控MIF促進乳腺癌進展的可能機制。
1 材料與方法
1.1 臨床資料收集2016年1月~2018年4月我院存檔的行乳腺癌改良根治術患者的新鮮組織25例和石蠟組織82例(乳腺癌和癌旁正常乳腺組織)。患者均為女性,新鮮組織來源患者年齡29~77歲(中位年齡53歲),腫瘤直徑1.2~4.5 cm(中位直徑2.5 cm),組織學分級:Ⅰ+Ⅱ級14例、Ⅲ級11例,淋巴結轉移13例,TNM分期:Ⅰ期6例、Ⅱ期12例、Ⅲ期7例;石蠟組織來源患者年齡36~80歲(中位年齡51歲),腫瘤直徑0.6~8.0 cm(中位直徑2.7 cm),組織學分級:Ⅰ+Ⅱ級62例、Ⅲ級20例,淋巴結轉移35例,TNM分期:Ⅰ期15例、Ⅱ期46例、Ⅲ期21例。入組標準:所有患者均未接受術前新輔助治療,樣本均為初治手術切除標本,經組織病理學確診為非特殊型浸潤性乳腺癌(invasive breast carcinoma of no special type, IBC-NST)。
1.2 數據庫分析使用TargetScan Human(http://www.targetscan.org/vert_72/)數據庫預測miR-608和MIF的結合位點。
1.3 方法
1.3.1qRT-PCR 采用SYBR Green qPCR Mix qRT-PCR試劑盒(德國DBI公司)和All-in-One miRNA qRT-PCR Detection System試劑盒(美國基因復能公司)分別檢測MIF和miR-608的表達;qRT-PCR引物序列:MIF上游引物:5′-CGGACAGGGTC TACATCAACTATTA-3′,下游引物:5′-ACCGTTTAT TTCTCCCCACCA-3′;GAPDH上游引物:5′-GGAGC GAGATCCCTCCAAAAT-3′,下游引物:5′-GGCTGTT GTCATACTTCTCATGG-3′; miR-608上游引物:5′-A GGGGTGGTGTTGGGACAGCTCCGT-3′,下游引物:5′-ACGGAGCTGTCCCAACACCACCCCT-3′;U6上游引物:5′-GATTCCTATGTGGGCGACGAG-3′,下游引物:5′-CCATCTCTTGCTCGAAGTCC-3′。以Folds=2-△△Ct表示組間相對倍比關系,GAPDH和U6作為內參。
1.3.2免疫組化及FISH檢測 免疫組化染色采用EliVision兩步法,ER(克隆號SP1)、PR(克隆號SP2)、Ki-67(克隆號MIB1)及EliVision試劑盒均購自福州邁新生物公司;HER-2(克隆號4B5)檢測使用Ventana全自動免疫組化檢測平臺;MIF(克隆號E7T1W,稀釋比1 ∶200)購自Cell Signaling公司,以人甲狀腺組織濾泡上皮細胞染色作為陽性對照,PBS代替一抗作為空白對照。HER-2 FISH探針由廣州安必平醫藥科技公司提供。
1.3.3結果判讀 免疫組化及FISH判讀由兩位高年資乳腺專科病理醫師獨立閱片。MIF陽性定位于胞質。(1)按癌細胞陽性比例進行評分:陽性細胞數<5%為0分,5%~25%為1分,26%~50%為2分,>50%為3分;(2)按著色強度進行評分:無陽性著色為0分,淡黃色為1分,棕黃色為2分,棕褐色為3分;將兩項得分結果相乘,>4分為陽性[10]。
HER-2免疫組化0~1+為陰性,3+為陽性,2+行FISH檢測,HER-2基因擴增為陽性,無擴增為陰性。Ki-67計數熱點區胞核陽性數。乳腺癌分子分型依據2019年st Gallen乳腺癌會議共識:管腔A型(ER≥1%,PR>20%,Ki-67增殖指數<30%且HER-2陰性)、管腔B型(一種為ER≥1%,Ki-67增殖指數≥30%或PR<20%,HER-2陰性;另一種為ER≥1%、PR>20%及HER-2陽性,任何水平Ki-67)、HER-2過表達型(ER及PR陰性,HER-2陽性)和三陰型(ER、PR及HER-2均陰性)[11]。
1.3.4Western blot法 將miR-608 mimics及miR-608 inhibitor(蘇州吉瑪基因公司)轉染人乳腺癌細胞株SK-BR-3(HER-2過表達型),提取蛋白及測定蛋白濃度后進行Western blot檢測,一抗包括MIF(稀釋比1 ∶1 000,美國Cell Signaling公司,#87501)和GAPDH(稀釋比1 ∶1 000,武漢三鷹生物公司,#10494-1-AP)。
1.4 隨訪對82例IBC-NST患者術后通過電話隨訪19~64個月,中位隨訪時間46個月,其中2例失訪。無進展生存期(progression free survival, PFS)定義為從患者手術后至出現乳腺癌進展(包括復發或轉移)或任何原因的死亡之間的時間;總生存期(overall survival, OS)定義為從患者手術后至因任何原因死亡或隨訪終止之間的時間。
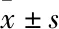
2 結果
2.1 IBC-NST組織中miR-608和MIF mRNA的表達及兩者表達的相關性采用qRT-PCR檢測25例IBC-NST和癌旁正常乳腺組織中miR-608和MIF mRNA的表達,結果顯示:miR-608在IBC-NST組織中的表達水平顯著低于癌旁正常乳腺組織(t=2.934,P<0.01,圖1A、B);MIF mRNA在IBC-NST組織中的表達顯著高于癌旁正常乳腺組織(t=4.850,P<0.000 1,圖1C、D)。以上結果提示miR-608低表達和MIF mRNA高表達可能與IBC-NST的發生相關。利用IBC-NST和癌旁正常乳腺組織中miR-608和MIF mRNA相對表達量制作ROC曲線評價兩者的診斷價值,結果顯示:miR-608的AUC為0.725,敏感性為58.2%,特異性為86.8%(圖2A);MIF mRNA的AUC為0.824,敏感性為70.5%,特異性為94.3%(圖2B)。結果提示,檢測miR-608和MIF mRNA的表達對于鑒別正常乳腺組織和IBC-NST組織具有一定的診斷價值。Pearson相關性分析結果顯示,25例IBC-NST組織中miR-608和MIF mRNA的表達呈負相關(r=-0.669 5,P=0.000 3,圖3A、B)。
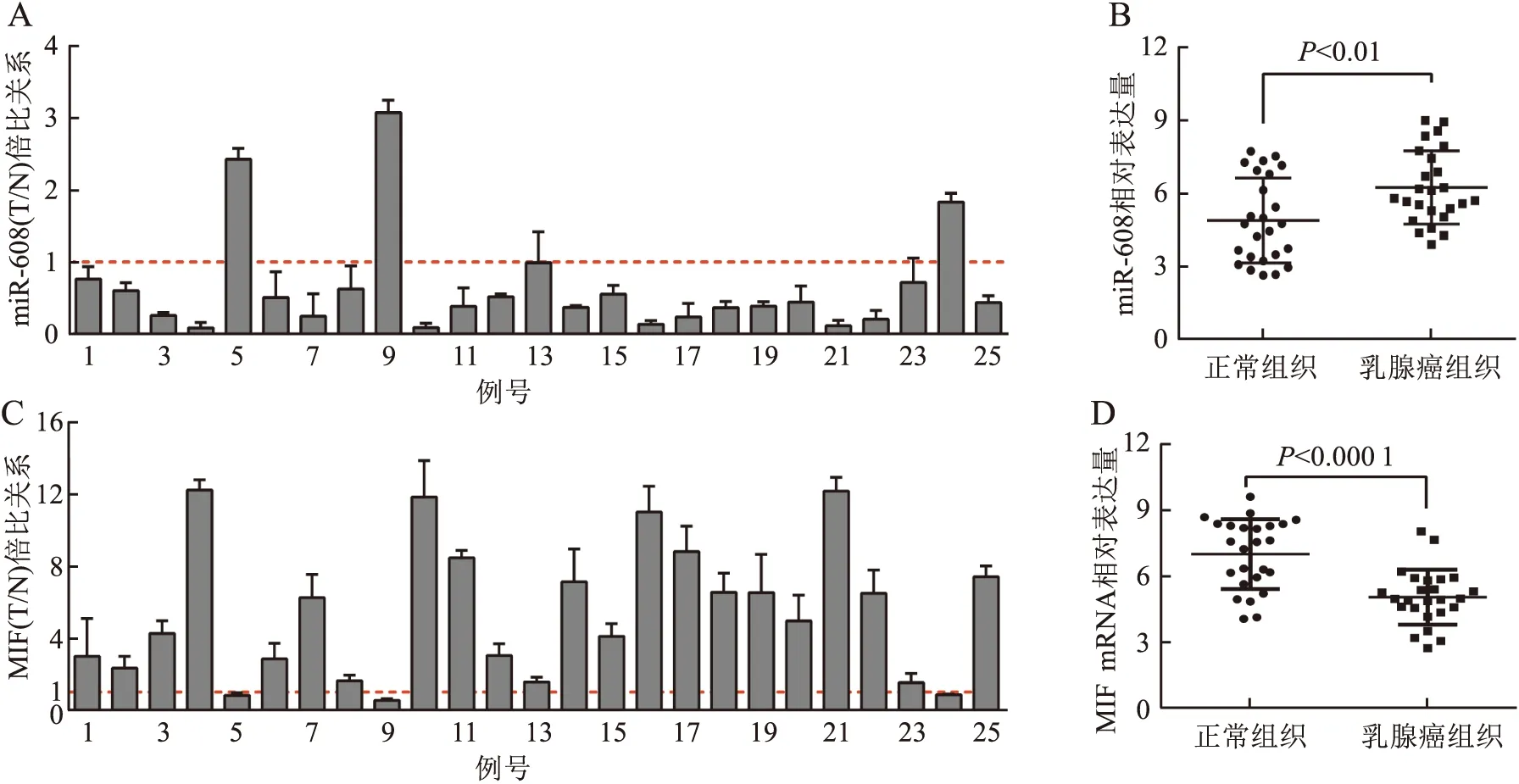
圖1 A.qRT-PCR檢測25例IBC-NST組織和癌旁正常乳腺組織中miR-608表達量的倍比關系:T. IBC-NST組織;N.癌旁正常乳腺組織;B.qRT-PCR檢測25例IBC-NST組織和癌旁正常乳腺組織中miR-608的相對表達量;C.qRT-PCR檢測25例IBC-NST組織和癌旁正常乳腺組織中MIF mRNA表達量的倍比關系:T. IBC-NST組織;N.癌旁正常乳腺組織;D.qRT-PCR檢測25例IBC-NST組織和癌旁正常乳腺組織中MIF mRNA的相對表達量
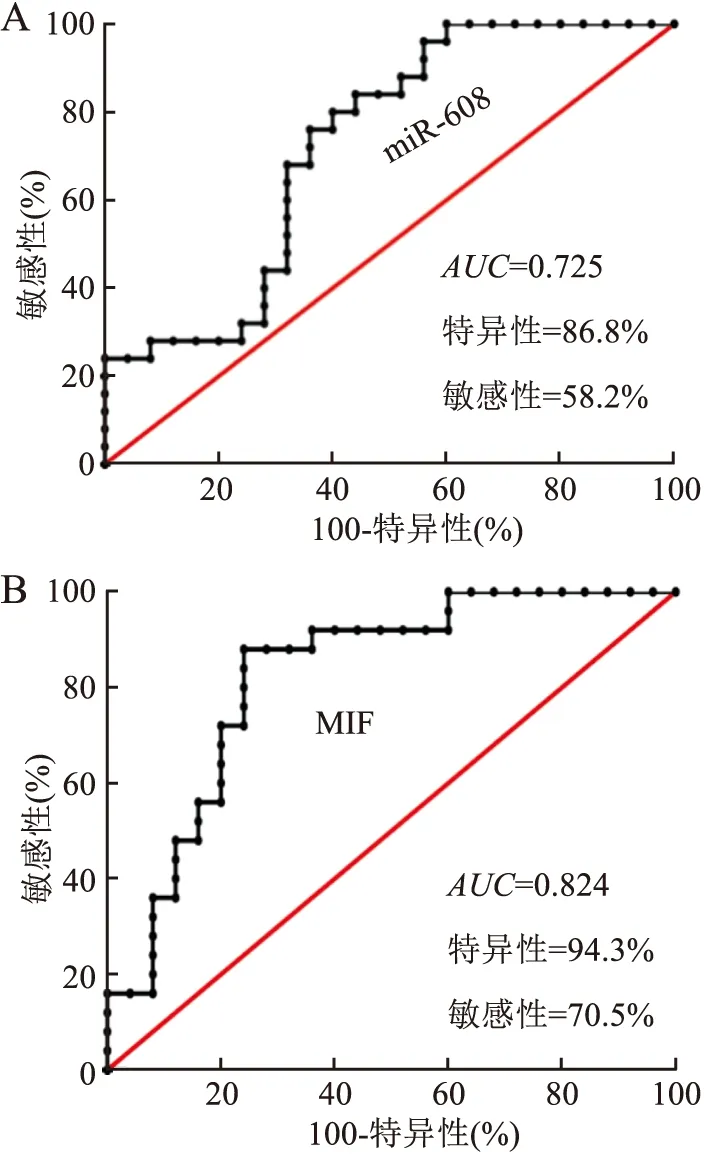
圖2 A.ROC曲線評估miR-608的診斷價值;B.ROC曲線評估MIF的診斷價值
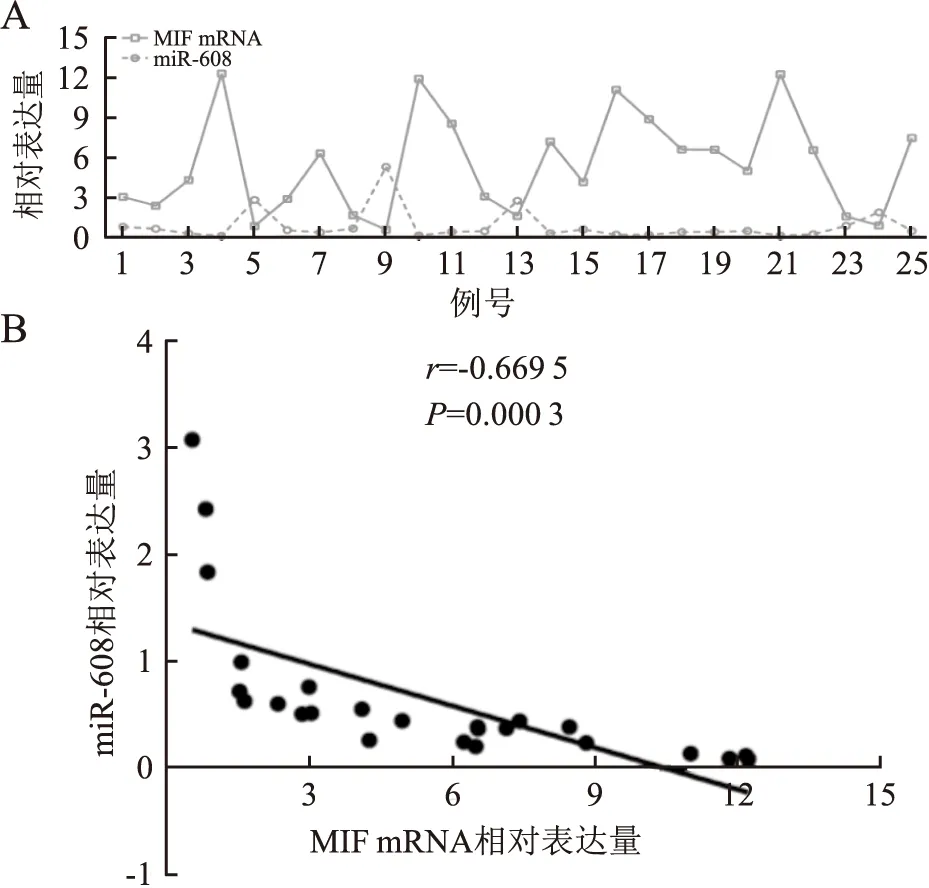
圖3 A.25例IBC-NST組織中miR-608與MIF mRNA相對表達量折線圖;B.Pearman相關性分析25例IBC-NST組織中miR-608與MIF mRNA表達的相關性
2.2 IBC-NST組織中miR-608和MIF mRNA表達與臨床病理特征的關系利用miR-608或MIF mRNA表達量的中位值將25例IBC-NST分為高表達組和低表達組。有淋巴結轉移組miR-608的低表達率(69.2%,9/13)顯著高于無淋巴結轉移組(25.0%,3/12)(P<0.05);TNM分期Ⅲ期組miR-608的低表達率(85.7%,6/7)顯著高于TNM分期Ⅰ+Ⅱ期組(33.3%,6/18)(P<0.05);有淋巴結轉移組MIF mRNA的高表達率(76.9%,10/13)顯著高于無淋巴結轉移組(25.0%,3/12)(P<0.05);TNM分期Ⅲ期組MIF mRNA的高表達率(100%,7/7)顯著高于TNM分期Ⅰ+Ⅱ期組(33.3%,6/18)(P<0.05)。而在患者年齡、腫瘤直徑及組織學分級方面,miR-608和MIF mRNA的表達差異均無統計學意義。miR-608表達與淋巴結轉移及TNM分期(P<0.05)呈負相關,MIF mRNA表達與淋巴結轉移及TNM分期(P<0.05)呈正相關,兩者表達均與患者年齡、腫瘤直徑及組織學分級無關(P>0.05,表1)。
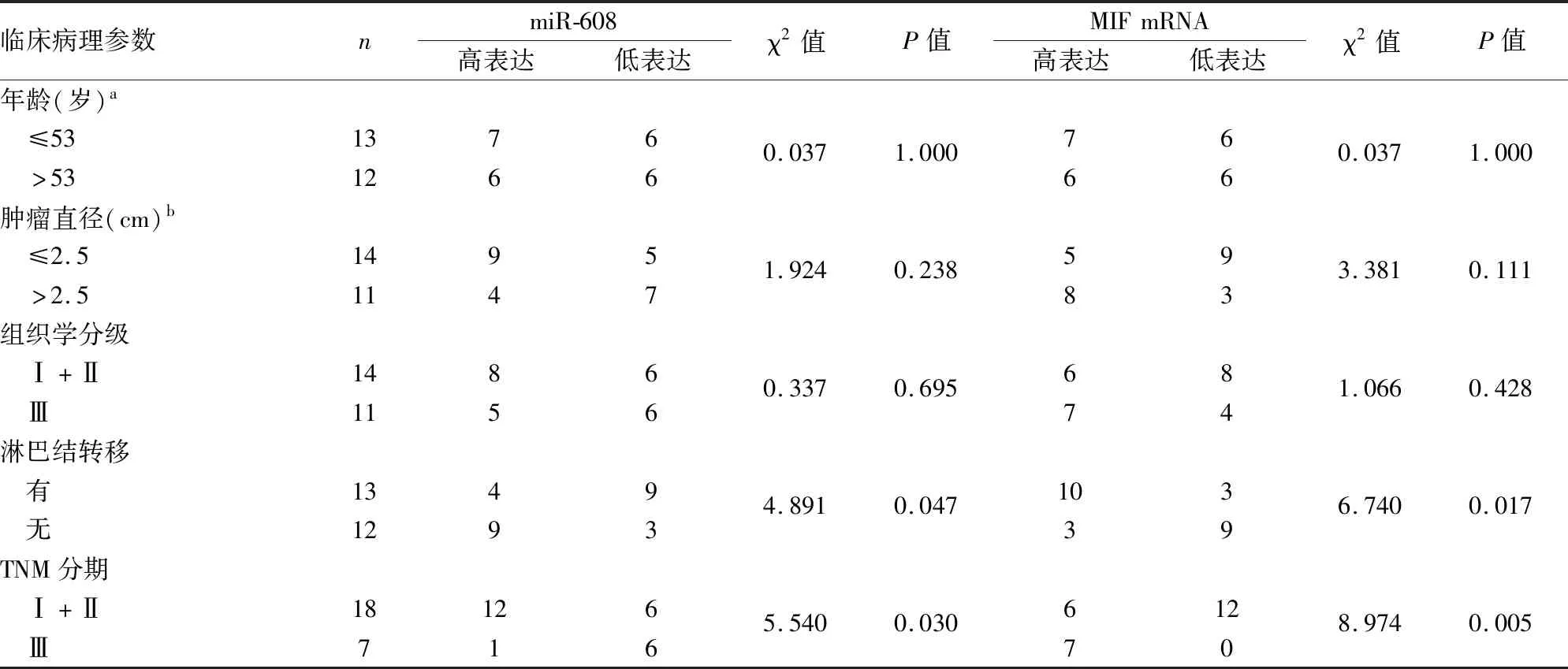
表1 miR-608和MIF mRNA表達與IBC-NST臨床病理特征的關系[n(%)]
2.3 IBC-NST細胞中miR-608調控MIF表達的初步機制初探通過TargetScan數據庫預測miR-608與MIF的結合位點,結果顯示兩者結合位點類型是“8mer”,即miR-608第2~8位種子序列與MIF-3′UTR區堿基存在完全互補配對;“context ++ score percentile”為99,該評分反應結合位點的保守性,數值越接近100,表示該位點是真正結合靶點的概率越大(圖4)。將人乳腺癌細胞株SK-BR-3轉染miR-608 mimics和inhibitor后,qRT-PCR檢測結果顯示,與NC組(對照組)相比,轉染miR-608 mimics后miR-608表達量顯著升高(t=24.84,P<0.000 1,圖5A),MIF mRNA表達量顯著降低(t=20.05,P<0.000 1,圖5B);Western blot檢測結果顯示,與NC組相比,轉染miR-608 mimics后MIF蛋白表達顯著下降(圖5C)。與inh-NC組(對照組)相比,轉染miR-608 inhibitor后miR-608表達顯著降低(t=49.07,P<0.000 1,圖5D),MIF的mRNA(t=13.34,P<0.001,圖5E)和蛋白表達顯著增加(圖5F)。以上結果提示:miR-608負向調控MIF表達,兩者間可能存在位點特異性結合關系。
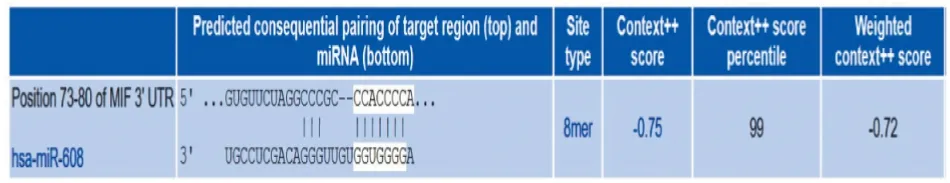
圖4 TargetScan數據庫預測miR-608和MIF存在結合位點
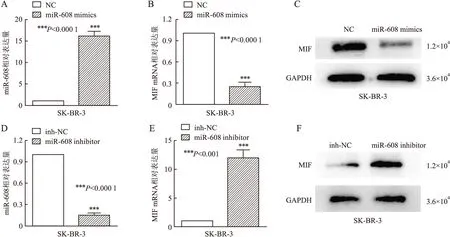
圖5 A.qRT-PCR檢測人乳腺癌細胞株SK-BR-3轉染miR-608 mimics后miR-608的表達;B.qRT-PCR檢測人乳腺癌細胞株SK-BR-3轉染miR-608 mimics后MIF mRNA的表達;C.Western blot法檢測人乳腺癌細胞株SK-BR-3轉染miR-608 mimics后MIF蛋白表達;D.qRT-PCR檢測人乳腺癌細胞株SK-BR-3轉染miR-608 inhibitor后miR-608的表達;E.qRT-PCR檢測人乳腺癌細胞株SK-BR-3轉染miR-608 inhibitor后MIF mRNA的表達;F.Western blot法檢測人乳腺癌細胞株SK-BR-3轉染miR-608 inhibitor后MIF蛋白的表達
2.4 免疫組化法檢測IBC-NST組織中MIF蛋白的表達及其與臨床病理特征的關系免疫組化結果顯示,82例IBC-NST和癌旁正常乳腺組織中MIF陽性率分別為68.3%(56/82)和31.7%(26/82),兩組間差異有統計學意義(χ2=21.951,P<0.001,圖6)。在有淋巴結轉移乳腺癌組中MIF的陽性率(82.9%,29/35)顯著高于無淋巴結轉移組(57.4%,27/47)(P<0.05)。在TNM分期Ⅰ期乳腺癌組中MIF的陽性率(40%,6/15)顯著低于TNM分期Ⅱ期(78.3%,36/46)和Ⅲ期(66.7%,14/21)乳腺癌組(P<0.05)。82例IBC-NST中管腔A型占22.0%(18/82),管腔B型占52.4%(43/82),HER-2過表達型占13.4%(11/82),三陰型占12.2%(10/82),MIF在HER-2過表達型(90.9%,10/11)和三陰型(90.0%,9/10)乳腺癌組中的陽性率顯著高于管腔A型(44.4%,8/18)和管腔B型組(67.4%,29/43),差異有統計學意義(P<0.05)。p53突變型(79.2%,38/48)IBC-NST組中MIF的陽性率顯著高于p53野生型組(52.9%,18/34)。然而患者年齡、腫瘤發生側別、腫瘤直徑及組織學分級方面,MIF的陽性率差異均無顯著性(P>0.05)。綜上,82例IBC-NST中MIF表達與淋巴結轉移、TNM分期、分子分型及p53突變相關(P<0.05),與患者年齡、腫瘤部位、腫瘤直徑、組織學分級均無關(表2)。
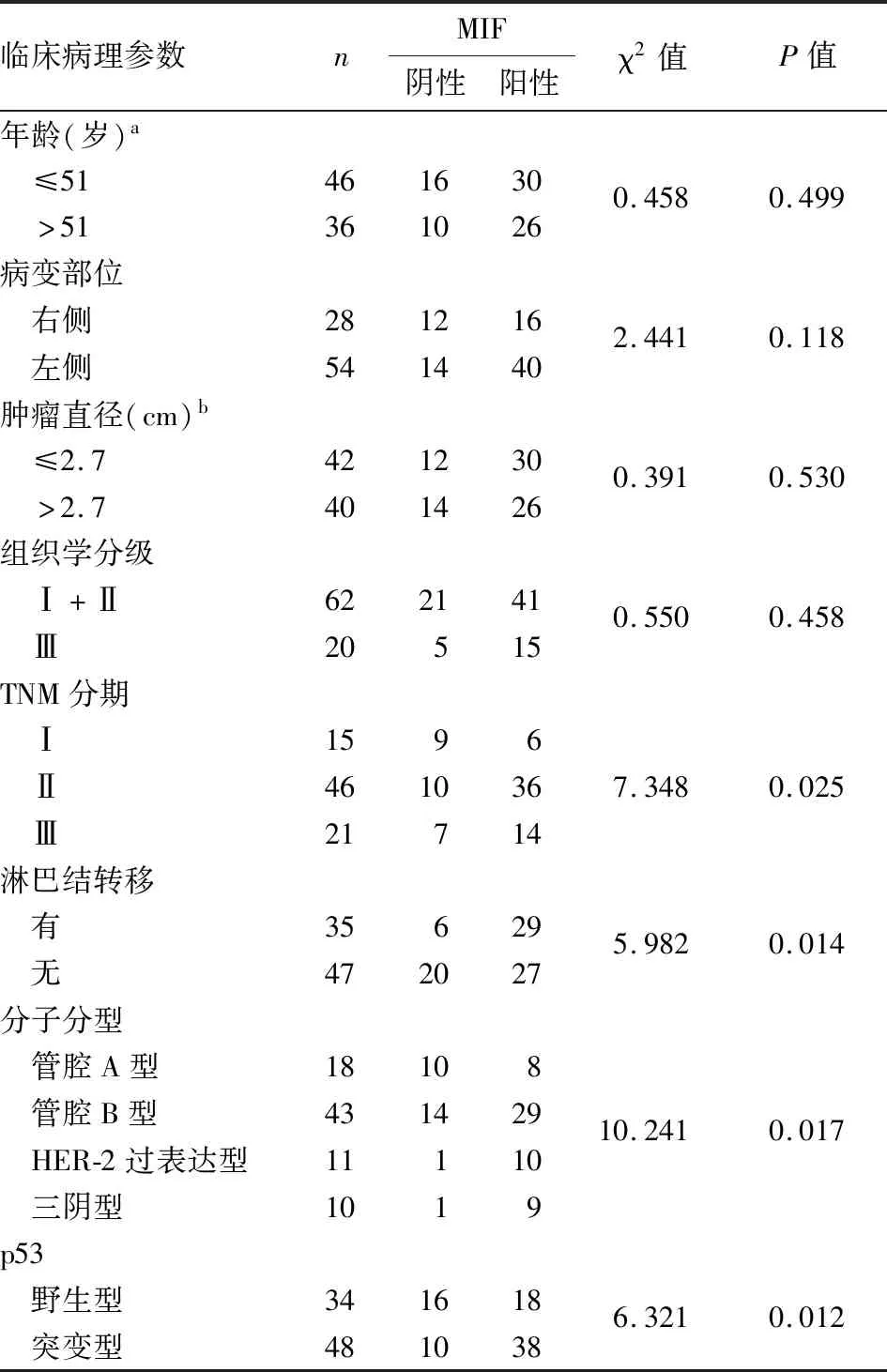
表2 MIF蛋白表達與IBC-NST臨床病理特征的相關性[n(%)]
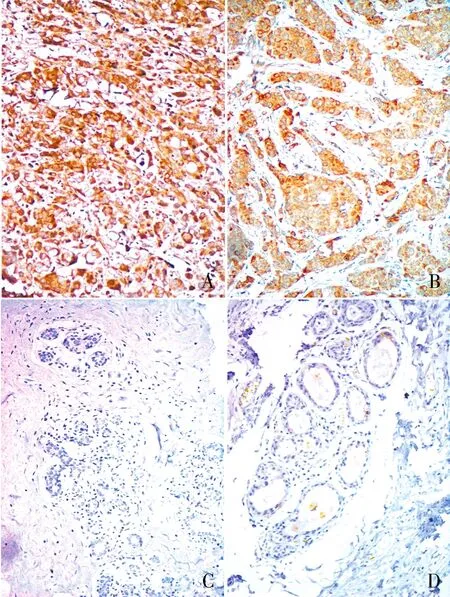
圖6 IBC-NST組織中MIF的表達,EliVision兩步法:A.MIF在三陰型乳腺癌組織中陽性;B.MIF在HER-2過表達型乳腺癌組織中陽性;C.MIF在三陰型乳腺癌癌旁正常乳腺組織中陰性;D.MIF在HER-2過表達型乳腺癌癌旁正常乳腺組織中陰性
2.5 IBC-NST組織中MIF表達與患者預后的關系獲得隨訪的80例IBC-NST患者中有13例疾病進展(其中5例患者因乳腺癌死亡,余8例患者出現乳腺癌復發或轉移)。80例IBC-NST患者的3年和5年PFS分別為90%(72/80)和83.8%(67/80);3年和5年OS分別為95%(76/80)和93.8%(75/80)。利用GraphPad-Prism 6.0軟件繪制生存曲線結合Gehan-Breslow-Wilcoxon檢驗分析,結果顯示MIF陰性患者(平均47.2±9.87個月)的OS優于MIF陽性患者(平均31.2±11.99個月),但差異無統計學意義(χ2=1.448,P=0.229,圖7A);MIF陰性患者(平均55.1±6.52個月)的PFS優于MIF陽性患者(平均42.5±9.99個月),差異有統計學意義(χ2=4.196,P=0.041,圖7B)。
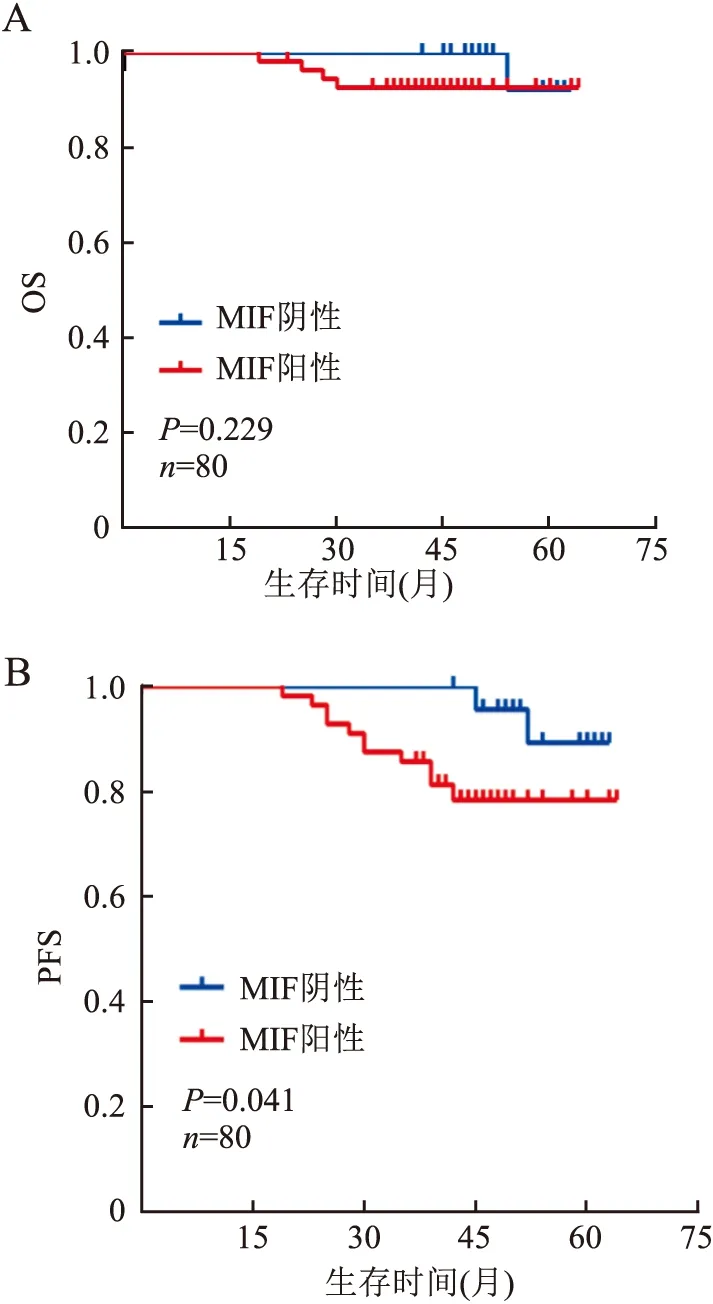
圖7 A.MIF表達與IBC-NST患者OS的關系;B.MIF表達與IBC-NST患者PFS的關系
3 討論
目前乳腺癌已然成為威脅女性健康的第一殺手,從表觀遺傳學角度深入挖掘其發生、發展機制,將為乳腺癌診治提供新思路。miRNAs是具有20~22個核苷酸的非編碼小RNA,是重要的細胞功能和發育調控因子。目前生物界存在的miRNA主要包括細胞內和細胞外miRNA,在哺乳動物細胞中,細胞內miRNA的功能由細胞器驅動,細胞外miRNA通過循環在細胞外空間發揮通信作用[12]。miRNA主要通過誘導其靶基因的mRNA降解或抑制其蛋白翻譯發揮作用,可以將其分為促癌miRNA、抑癌miRNA及促癌和抑癌雙重作用miRNA[13]。Fong等[14]研究發現miR-122可促進乳腺癌的轉移,動物實驗亦證實抑制miR-122能恢復遠處器官(包括腦和肺)的葡萄糖攝取,降低乳腺癌的轉移率。miR-199a-5p通過調節EGF和SP1下調ERK5表達抑制乳腺癌細胞的侵襲[15]。miR-608是新近報道的miRNA分子,目前研究顯示其在不同腫瘤中發揮的作用并不一致。miR-608通過靶向BRD4抑制細胞增殖,在肝癌中發揮抑癌作用[16]。在肺癌中miR-608通過與靶基因AKT2結合促進細胞凋亡,發揮抑癌作用[17]。Xiang等[18]報道顯示,在膀胱癌中miR-608發揮促進腫瘤增殖和抑制腫瘤凋亡的作用。目前,miR-608在乳腺癌中的表達情況及其生物學功能尚未見報道。本實驗結果顯示,miR-608在IBC-NST組織中的表達顯著低于癌旁正常乳腺組織,并且miR-608低表達與淋巴結轉移及TNM高分期相關,以上結果提示miR-608可能在IBC-NST中發揮抑癌作用。
MIF定位于人染色體22q11.2,是由115個氨基酸組成的進化保守蛋白[19],在炎癥反應和免疫調節中發揮重要功能。近年來,MIF與腫瘤的關系報道較多,其在非小細胞肺癌[20]、黑色素瘤[21]、膀胱癌[22]和乳腺癌[23]中均發現MIF表達上調。本實驗結果與上述一致,本實驗從mRNA和蛋白水平均檢測出IBC-NST組織中MIF高表達;且MIF表達與淋巴結轉移、TNM高分期、分子分型及p53突變相關,MIF在HER-2過表達型和三陰型乳腺癌中的陽性率顯著高于管腔A和管腔B型。Wang等[24]對732例乳腺癌的研究顯示,MIF在三陰型乳腺癌中的表達顯著高于管腔型(P<0.05)。目前研究顯示,人類半數以上的惡性腫瘤均存在p53基因突變,p53的突變形式包括錯義突變和無義突變[25],乳腺癌中p53蛋白表達大多數為錯義突變模式[26]。Hainaut等[27]報道p53突變在基底細胞樣型和HER-2過表達型乳腺癌中常見(分別為65%和53.4%),在管腔A和管腔B型中少見(分別為9.3%和24.8%),且p53突變在HER-2過表達型中與患者不良預后相關。Jung等[28]在乳腺癌細胞株MCF7和結直腸癌細胞株HCT116中均發現,MIF通過穩定胞質中MDM2和p53的結合來抑制后者的活性。以上研究結果提示:在乳腺癌不同分子亞型中MIF蛋白表達與p53基因突變關系密切,且兩者間可能存在潛在的作用機制。此外,對本組IBC-NST患者進行生存分析,結果顯示MIF表達與患者PFS呈負相關。Wang等[24]分析3 951例乳腺癌微陣列數據亦發現,MIF高表達與患者總生存率降低相關(P<0.01)。綜上,MIF可能是IBC-NST患者不良預后預測因子。目前,針對MIF靶點相關治療的研究取得較大進展;體外實驗證實MIF抑制劑ISO-1可顯著抑制結腸癌和黑色素瘤細胞的增殖[29]。MIF小分子抑制劑CPSI-1306能抑制小鼠原位乳腺癌模型的腫瘤生長和轉移[30]。隨著研究的深入,MIF抑制劑可能進入臨床實驗階段。
馬穎光等[31]報道miR-451可直接結合MIF的3′-UTR區來調控人結直腸癌細胞的增殖、侵襲和遷移。李曉娜等[32]報道miR-451靶向MIF,經由PI3K/AKT通路抑制甲狀腺癌細胞增殖和促進其凋亡。由此可見,在不同腫瘤中MIF接受同種miRNA調控是常見的分子事件。Yu等[8]研究發現miR-608通過靶向MIF抑制肺腺癌侵襲和遷移。Wang等[9]報道miR-608負向調控MIF表達介導PI3K/AKT和JNK通路失活,抑制膠質瘤細胞增殖、侵襲和遷移。miR-608通過下調EGFR和p53介導MAPK信號通路調控造釉細胞瘤細胞增殖、分化、凋亡和細胞周期。本實驗結果顯示,在IBC-NST組織中miR-608與MIF表達呈負相關;在人乳腺癌細胞株SK-BR-3中,miR-608模擬物和抑制劑能負調控MIF的mRNA和蛋白表達;TargetScan數據庫提示miR-608和MIF存在高評分結合位點。因此,筆者推測miR-608可能通過結合MIF的3′-UTR區在IBC-NST中發揮抑癌作用。本課題組后續將通過設計雙熒光素酶報告基因實驗等進一步驗證兩者的結合關系,并深入探索miR-608和MIF結合后其下游的信號通路是否與p53基因突變相關。
綜上所述,在IBC-NST中miR-608呈低表達,MIF呈高表達,兩者均與不良臨床病理特征相關;在人乳腺癌細胞株中miR-608負向調控MIF表達。miR-608和MIF可能是IBC-NST的預后標志物和潛在的治療靶點。

