葡萄籽原花青素柔質體凝膠劑的制備工藝研究
竇晨,潘蕊,趙聲蘭*,程欣,3* (1. 云南中醫藥大學 中藥學院,昆明 650500;2. 云南中醫藥大學 云南省高校外用給藥系統與制劑技術研究重點實驗室,昆明 650500;3. 云南中醫藥大學 云南省傣醫藥與彝醫藥重點實驗室,昆明650500)
葡萄籽原花青素(grape seed proanthocyanidins,GSP)是從葡萄籽中提取出來的一種黃酮類多酚化合物。據研究報道,原花青素具有抗氧化[1]、清除自由基[2]、抗癌[3]、抗菌[4]、抑制酪氨酸酶[5]等藥理學活性,可作為一種生態可持續和低成本的天然抗氧化劑來源,具有重要的經濟效益和社會效益。但其分子結構中的酸性酚羥基和不飽和鍵使其缺乏長期儲存穩定性,容易降解、氧化、聚合等[6]。
將藥物包載于柔質體中可增強藥物在皮膚中的滲透性[7],改善水溶性和增加藥物穩定性,并控制生物活性劑的釋放[8-9]。但作為緩釋載體,其物理性質不穩定,磷脂雙分子層滲透性的增加會導致生物活性分子的泄漏失活、儲存周期縮短以及易于聚集、融合或沉淀,并且由于脂質體的流動性使其不宜長時間停留在皮膚上,均限制了柔質體的廣泛應用。凝膠劑作為廣泛使用的藥物劑型,系指藥物與適宜基質制成具有凝膠特性的半固體或稠厚液體制劑[10]。將脂質體分散在凝膠基質中制備成脂質體凝膠劑,形成多貯庫型系統,能夠有效解決流動性問題[11],有效提高藥物皮膚滯留時間、穩定性及緩釋性的優點[12]。本文將包載原花青素的柔質體嵌入水凝膠中,探究藥物的釋放規律,為GSP的進一步開發利用提供依據。
1 材料
1.1 試藥
原花青素對照品(批號:1024K021SX,純度≥95%,北京索萊寶科技有限公司),GSP(天津市尖峰天然產物研究開發有限公司,批號:002200604028,純度≥95%),大豆卵磷脂(Solarbio公司,批號:1112J021),膽固醇(BIOSHARP生物公司,批號:624J033),脫氧膽酸鈉(BIOSHARP生物公司,批號:909P021,純度>99%),卡波姆940(上海麥克林生化科技有限公司,批號:C12058025),甘油(廣東光華科技股份有限公司,批號:20200113),PEG-400(批號:C1925030)、三乙醇胺(批號:C2127395)(上海阿拉丁生化科技股份有限公司)。
1.2 儀器
超聲波處理器(德國elma公司,型號:P180H);旋轉蒸發儀(倍捷科技,型號:OSB-2100);納米激光粒度儀(美國布魯克海文公司,型號:90Plus型);安捷倫高效液相色譜儀(安捷倫,型號:1260infin);氮吹儀(天津市恒奧科技發展公司,型號:HSC-12A)。
1.3 實驗動物
SPF級KM小鼠,雄性,體質量(20±2)g[湖南斯萊克景達實驗動物有限公司,許可證號:SCXK(湘)k2017-0005]。
2 方法與結果
2.1 GSP含量測定的方法學建立
2.1.1 色譜條件 色譜條件1:色譜柱:ZORBAX SB-C18(4.6 mm×250 mm,5.0 μm);溶劑為20%乙醇-生理鹽水時,流動相為乙腈∶水=18∶82,流速 1.0 mL·min-1,檢測波長 280 nm,進樣量10 μL,柱溫 30℃。
色譜條件2:溶劑為甲醇時,流動相為甲醇∶水=32∶68,進樣量10 μL,柱溫25℃,流速1 mL·min-1,檢測波長280 nm。
2.1.2 專屬性考察 取空白柔質體(BFL)、葡萄籽原花青素柔質體(GSP-FL)、空白脂質體(BL)、葡萄籽原花青素脂質體(GSP-L)的透皮接收液以及GSP對照品溶液按色譜條件1進樣分析。取甲醇溶液、原花青素甲醇溶液、原花青素對照品甲醇溶液,按色譜條件2進樣分析。由于GSP的出峰時間較早,伴有溶劑峰的干擾,因此在計算時需扣除溶劑峰峰面積。
2.1.3 線性關系考察 精密稱取適量的原花青素對照品,加20%乙醇-生理鹽水和甲醇溶解,分別配成系列對照品溶液,按照色譜條件1和2進樣分析,計算得到的線性回歸方程分別為y1=2391.5x-4.943,R2=0.9991,結果表明原花青素在0.0181~0.2896 mg·mL-1與峰面積線性關系良好;y2=1486.8x-159.67,R2=0.9997,結果表明原花青素在0.1252~0.4382 mg·mL-1與峰面積線性關系良好。
2.1.4 精密度實驗 配制GSP對照品溶液,按色譜條件1連續進樣8次,結果對照品溶液中原花青素峰面積的RSD值為1.1%,表明儀器精密度良好。
2.1.5 重復性實驗 取GSP-FL體外經皮滲透樣品6份進行重復性考察,按色譜條件1進樣分析,結果樣品中原花青素峰面積的RSD值為1.8%,表明方法重復性良好。
2.1.6 穩定性實驗 精密量取GSP-FL體外經皮滲透液 1.0 mL,0.22 μm微孔濾膜過濾,放置0、2、4、6、8、12 h后,按色譜條件1進樣分析,結果顯示原花青素峰面積的RSD值為2.4%,表明樣品在12 h內穩定性較好。
2.1.7 加樣回收實驗 取GSP-FL體外經皮滲透接收液樣品0.5 mL(含原花青素0.1318 mg)9份,分別加入低、中、高質量濃度的對照品溶液各2份,按色譜條件1進樣分析,結果低、中、高質量濃度的平均加樣回收率分別為100.82%、102.78%、104.62%,RSD值 分 別1.3%、0.37%、1.7%。精密稱定GSP樣品粉末9份加入甲醇溶解,分別加入低、中、高質量濃度的對照品溶液各3份,按色譜條件2進樣分析,結果低、中、高質量濃度的平均加樣回收率分別為97.8%、100.3%、102.7%,RSD值 分別為1.2%、0.33%、0.23%。符合方法學要求。
2.2 GSP-FL與GSP-L的制備
根據前期實驗研究得到的最佳制備工藝,采用薄膜分散-超聲法制備GSP-FL。精密稱定一定量的卵磷脂、膽固醇溶于15 mL氯仿中,將脫氧膽酸鈉溶于5 mL甲醇中超聲溶解后置于圓底燒瓶中混合均勻,在40℃水浴條件下,減壓旋轉蒸發除去有機溶劑,直至在燒瓶內壁上形成干燥透明的均勻薄膜。精密稱取處方量的GSP溶于6 mL水中,將水相加到圓底燒瓶中,在40℃水浴條件下繼續旋轉水合30 min后,所得混合液于超聲波處理器冰浴超聲混勻(150~180 W,5 min),0.22 μm微孔濾膜過濾后得到GSP-FL。同法制備得到不加膜軟化劑脫氧膽酸鈉的GSP-L,于冰箱4℃密封保存待用。采用超速離心法測定GSP-FL包封率為(70.79± 0.02)%,載藥量為(1.16±0.01)%,粒徑為(156.47±7.03)nm,PDI為0.26±0.01,Zeta電位為(-42.35±4.00)mV(n=5)。
2.3 GSP-FL凝膠劑(GSP-FLG)的制備
精密稱取一定量的凝膠基質,加入適量的純水過夜,使其充分溶脹,加入適量保濕劑、促滲劑,滴加三乙醇胺調整pH值后,再加入適量GSP-FL混懸液后,加入純水至50 g,攪拌均勻即得。同法制備不加藥物的空白凝膠。
2.3.1 凝膠基質的篩選 分別精密稱定確定質量的凝膠基質卡波姆940、卡波姆934、羧甲基纖維素鈉、明膠、西黃著膠各0.5 g,加入適量純水溶脹過夜,用研缽研磨直至細膩,加入甘油2 g,用三乙醇胺調節pH至6.5,用純水補充至50 g。結果表明,卡波姆940能夠形成凝膠,黏度適宜、易于涂布,因此使用卡波姆940作為凝膠劑的基質。
2.3.2 凝膠劑的評價指標 根據《中國藥典》2020年版對凝膠劑的規定,一般應檢查pH值,膠粒應分散均勻,不應下沉結塊,凝膠劑應均勻、細膩、在常溫時保持膠狀、不干涸或液化等。因此,本文主要考察凝膠劑的失水率、成型性、pH值、均勻度、光澤度、穩定性等因素。
① pH值。將制備好的凝膠劑置于100 mL燒杯中,按照1∶50(W/W)加入超純水,超聲30 min,充分攪拌使其溶解,室溫條件下用pH計測定其pH值。
② 穩定性實驗。離心實驗:精密稱取1 g凝膠劑于離心管中,3500 r·min-1離心30 min,觀察樣品是否分層;低溫實驗:精密稱取1 g凝膠劑于離心管中,密封保存于-20℃冰箱中,觀察樣品是否分層;熱恒溫實驗:精密稱取1 g凝膠劑于離心管中,60℃放置6 h,觀察是否分層。
③ 涂展性實驗。在一塊干凈的玻璃板上畫一個直徑為1 cm的圓,取1 g凝膠劑涂在圓內,并覆蓋一塊干凈的玻璃板,取1 kg重物壓在玻璃板上,5 min后量取凝膠劑延展后的直徑。
④ 失水率實驗。精密稱定5 g凝膠劑放入干燥至恒重的玻璃器皿內,將其質量記為Wa,置于55℃的烘箱中干燥,每隔1 h后取出,放冷之后,稱定總質量記為Wb,繼續干燥至質量不再損失時為終點,計算每個時刻的失水率(S)。
S=(Wa-Wb)/5×100%
2.3.3 卡波姆940用量的考察 精密稱定0.05、0.25、0.50、0.75、1.00 g [即分別為0.1%、0.5%、1%、1.5%、2%(W/W)]的卡波姆940均勻灑于純水表面,充分溶脹,用研缽研磨直至細膩,加入甘油2 g,丙二醇2 g,用三乙醇胺調節pH至6.5,用純水補充至50 g。主要以外觀,成型性,黏稠性,涂展性來考察卡波姆940的用量。結果顯示,當卡波姆940用量超過1%時,凝膠劑隨著卡波姆940用量的增加,黏度逐漸增大。因此卡波姆940的用量應控制在1%以內。
2.3.4 保濕劑的選擇 精密稱定卡波姆940約0.5 g,均勻灑于純水表面,充分溶脹,不加保濕劑或以甘油2 g、PEG-400 2 g、甘油∶PEG-400(1∶1)為保濕劑,再加入丙二醇2 g,用三乙醇胺調節pH至6.5,用純水補充至50 g。以失水率為指標,考察最適保濕劑的種類。結果顯示,在1~6 h內甘油具有較小的平均失水率,因此選擇甘油為保濕劑。
2.3.5 保濕劑用量的選擇 精密稱定卡波姆940 0.5 g,均勻灑于純水表面,使其充分溶脹,分別加入1、2、3、4、5 g甘油,再加入丙二醇2 g,充分攪勻,用三乙醇胺調節pH至6.5,用純水補充至50 g。以失水率為指標,考察保濕劑的最適用量,結果顯示,當甘油用量為3 g時,凝膠劑具有較小的失水率。
2.3.6 三乙醇胺用量的考察 精密稱定卡波姆940 0.5 g,均勻灑于純水表面,充分溶脹,加入3 g甘油,2 g丙二醇,分別加入0.1、0.5、1、2、3 g三乙醇胺,充分攪勻,用純水補充至50 g。以外觀、涂展性、黏度、pH值為指標,考察三乙醇胺的用量。結果顯示,當凝膠劑的pH>8時,狀態較稀,不易涂布。因此,三乙醇胺的用量采用0.1、0.5、1 g這三個水平作為影響因素。
2.3.7 正交實驗設計與優化選擇 根據單因素實驗結果,選擇卡波姆、甘油和三乙醇胺用量作為影響凝膠劑的主要因素進行考察,綜合評分標準見表1,采用L9(34)正交設計表進行基質篩選,優化處方(見表2)。

表1 綜合評分標準(20分)Tab 1 Comprehensive scoring criteria (20 points)

表2 正交實驗因素與水平Tab 2 Orthogonal experimental factor and level
2.3.8 正交實驗結果 以綜合評分為評價指標,各因素對綜合評分的影響分別為A>C>B,因素A和C對綜合評分具有顯著影響(P<0.05),因此考慮GSP-FLG凝膠基質的最佳制備工藝條件為A1B3C2,即每50 g凝膠中含有卡波姆940 0.5%,甘油10%及三乙醇胺1%(見表3、表4)。
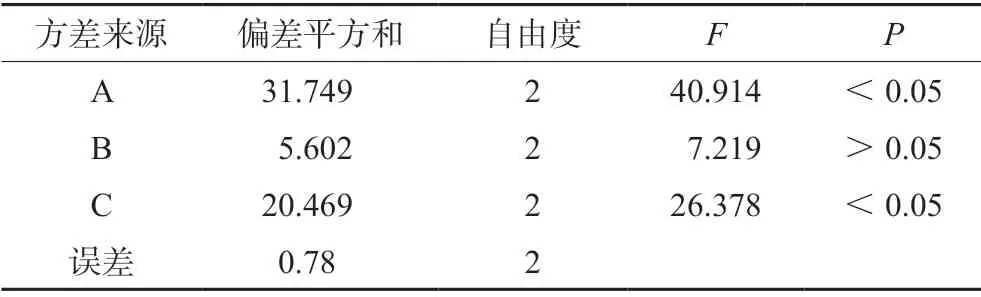
表4 方差分析結果Tab 4 Variance analysis
2.3.9 驗證實驗 按優選的處方工藝制備4批GSP-FLG,對其進行考察,其6 h的平均失水率分別為23.26%、24.33%、22.22%、30.36%,凝膠質地光滑有光澤、涂展性、穩定性良好,綜合評分分別為16.5、16.9、17.0、16.2,平均值為16.65,RSD為2.2%,結果表明制備工藝合理,穩定可行且結果可靠。
2.4 GSP-FL、GSP-FLG的體外經皮滲透實驗
2.4.1 離體小鼠皮膚的制備 將昆明種小鼠脫頸椎處死后,固定于木板上,小心剔除腹部毛發,立即剪下其腹部皮膚,剝離皮下組織及脂肪,將其浸泡于生理鹽水,選用表皮完整無破損皮膚于-80℃冷凍保存,備用。
2.4.2 經皮滲透實驗 采用Franz透皮擴散池法,分別以游離GSP為對照進行GSP-FL及GSP-L的體外經皮滲透實驗,以葡萄籽原花青素凝膠(GSP-G)為對照進行GSP-FLG的體外經皮滲透實驗。將預處理好的鼠皮固定于透皮杯上,使角質層面向樣品供給池,真皮層面向接收池,用夾子夾緊。向樣品池中加入等量的GSP、GSP-FL及GSP-L樣品溶液(含GSP 9.30 mg)或1 g凝膠劑(含GSP 13.12 mg)并均勻鋪展開,再向接收池加入20%乙醇-生理鹽水作為接收介質,于水浴溫度(32±0.5)℃,轉速300 r·min-1的條件下進行實驗。分別于第0.5、1、2、4、6、8、12、24、48、72 h取樣,同時補加等量同溫度的接收介質。接收液用0.22 μm的微孔濾膜濾過后,按色譜條件1進樣分析,計算GSP在不同時間點的單位面積累積透過量Qt(mg·cm-2),以時間t(h)為橫坐標,以Qt為縱坐標作圖,結果如圖1所示。對曲線中的直線部分進行線性回歸,直線的斜率即為穩態透皮速率[Js,mg/(cm2·h)]。

圖1 GSP-FL、GSP-L、GSP、GSP-G、GSP-FLG單位面積累積透過量曲線( ±s,n=4)Fig 1 Cumulative transmittance curve of GSP-FL,GSP-L,GSP,GSP-G,and GSP-FLG drugs per unit area( ±s,n=4)
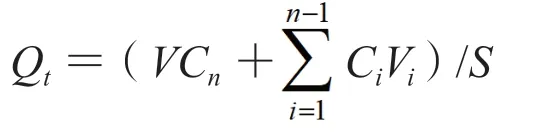
S為有效擴散面積,V為接收液總體積,Cn為第n次取樣時接收液中藥物的質量濃度,Ci為第i次取樣時接收液中藥物的質量濃度,Vi為取樣體積。
結果如表5所示,GSP組表現出明顯的突釋現象,GSP-FL組(含GSP 9.30 mg)24 h的單位面積累積透過量顯著高于GSP-L組(P<0.05),穩態透皮速率也高于GSP-L組,猜測柔質體的可形變性使其比脂質體更易透過皮膚。GSP-FLG組(含GSP 13.12 mg)72 h的單位面積累積透過量顯著低于GSP-G組(P<0.01),穩態透皮速率也低于GSP-G組,因此GSP-FLG表現為明顯的緩釋效果。通過藥物釋放動力學方程對體外經皮滲透結果進行擬合,結果顯示 GSP-FL、GSP-L、GSP-G及GSP-FLG組均以Weibull 方程進行擬合時具有較好的擬合度;而GSP 組以一級動力學方程擬合度較高。擬合結果如表6所示。
表5 GSP-FL、GSP-L、GSP、GSP-G和GSP-FLG累積釋放動力學參數( ±s,n=4)Tab 5 Cumulative release kinetics parameters of GSP-FL,GSP-L,GSP,GSP-G and GSP-FLG ( ±s,n=4)
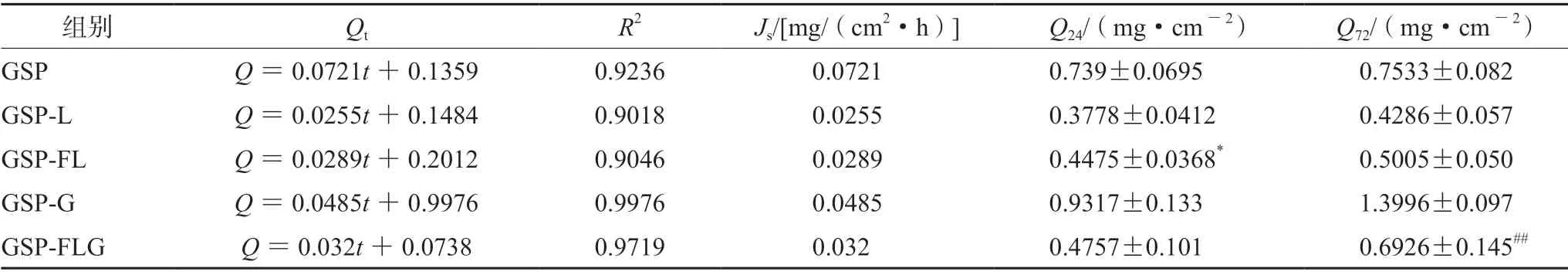
表5 GSP-FL、GSP-L、GSP、GSP-G和GSP-FLG累積釋放動力學參數( ±s,n=4)Tab 5 Cumulative release kinetics parameters of GSP-FL,GSP-L,GSP,GSP-G and GSP-FLG ( ±s,n=4)
注(Note):與GSP-L組相比,*P<0.01;與 GSP-G組相比,##P<0.01(Compared with the GSP-L group,*P<0.01; compared with the GSP-G group,##P<0.01)。
組別 Qt R2 Js/[mg/(cm2·h)] Q24/(mg·cm-2) Q72/(mg·cm-2)GSP Q=0.0721t+0.1359 0.9236 0.0721 0.739±0.0695 0.7533±0.082 GSP-L Q=0.0255t+0.1484 0.9018 0.0255 0.3778±0.0412 0.4286±0.057 GSP-FL Q=0.0289t+0.2012 0.9046 0.0289 0.4475±0.0368* 0.5005±0.050 GSP-G Q=0.0485t+0.9976 0.9976 0.0485 0.9317±0.133 1.3996±0.097 GSP-FLG Q=0.032t+0.0738 0.9719 0.032 0.4757±0.101 0.6926±0.145##
表6 GSP-FL、GSP-L、GSP、GSP-G和GSP-FLG藥物單位面積累積透過量曲線方程擬合( ±s,n=4)Tab 6 Equation fitting of cumulative transmittance curve per unit area of GSP-FL,GSP-L,GSP,GSP-G and GSP-FLG ( ± s,n=4)

表6 GSP-FL、GSP-L、GSP、GSP-G和GSP-FLG藥物單位面積累積透過量曲線方程擬合( ±s,n=4)Tab 6 Equation fitting of cumulative transmittance curve per unit area of GSP-FL,GSP-L,GSP,GSP-G and GSP-FLG ( ± s,n=4)
擬合方式 組別 方程 R2零級釋放動力學方程GSP Q=0.0061t+0.4404 0.2862 GSP-L Q=0.0031t+0.2512 0.5010 GSP-FL Q=0.0032t+0.3176 0.4572 GSP-G Q=0.0185t+0.2593 0.8977 GSP-FLGQ=0.008t+0.2103 0.8386一級釋放動力學方程GSP Q=0.7371(1-e-0.2844t) 0.9973 GSP-L Q=0.3686(1-e-0.4641t) 0.8451 GSP-FL Q=0.4342(1-e-0.6198t) 0.8282 GSP-G Q=1.4657(1-e-0.0434t) 0.991 GSP-FLGQ=0.6625(1-e-0.0762t) 0.9513 Higuchi方程GSP Q=0.0727t1/2+0.2983 0.5366 GSP-L Q=0.0339t1/2+0.1891 0.7374 GSP-FL Q=0.0355t1/2+0.2517 0.6965 GSP-G Q=0.1857t1/2-0.0752 0.9802 GSP-FLGQ=0.0817t1/2+0.0597 0.9646 Weibull方程GSP Q=0.7410(1-e-[0.283(t-0.019)]0.9487)0.9972 GSP-L Q=0.4285(1-e-[0.2863(t-0.1806)]0.4422)0.9941 GSP-FL Q=0.4947(1-e-[0.4044(t-0.1358)]0.4345)0.9921 GSP-G Q=1.4522(1-e-[0.0386(t-2.5093)]1.169)0.9956 GSP-FLGQ=0.9078(1-e-[0.0284(t-0.3397)]0.5705)0.9933 Ritgerpeppas方程GSP Q=0.3385(t0.2235) 0.7195 GSP-L Q=0.2031(t0.1899) 0.9019 GSP-FL Q=0.2629(t0.1655) 0.8855 GSP-G Q=0.1462(t0.5443) 0.9763 GSP-FLGQ=0.1302(t0.4043) 0.9797
2.4.3 藥物的皮膚滯留量測定 體外透皮實驗結束后,取出小鼠皮膚,用生理鹽水反復沖洗小鼠皮膚表面,直到將皮膚表面的藥物清洗干凈為止,再剪下給藥部位置于10 mL離心管中,用眼科剪將其剪碎,加入甲醇4 mL,置于勻漿機中使其破碎,水浴超聲30 min,140 00 r·min-1離心30 min后,棄去鼠皮,將上清液用氮氣吹干,以甲醇復溶,過0.22 μm微孔濾膜后,按色譜條件2進樣分析測定GSP的藥物含量,測定藥物的皮膚滯留量(Q)=藥物量/有效擴散面積(2.92 cm2)。結果顯示,GSP-FL 組72 h皮膚內藥物滯留量顯著高于GSP 組(P<0.01)。GSP-FLG組在72 h皮膚內藥物滯留量顯著高于GSP-G組(P<0.05),見表7。
表7 GSP-FL、GSP-L、GSP、GSP-G和GSP-FLG的藥物皮膚滯留量( ±s,n=3)Tab 7 Drug skin retention of GSP-FL,GSP-L,GSP,GSP-G and GSP-FLG ( ±s,n=3)
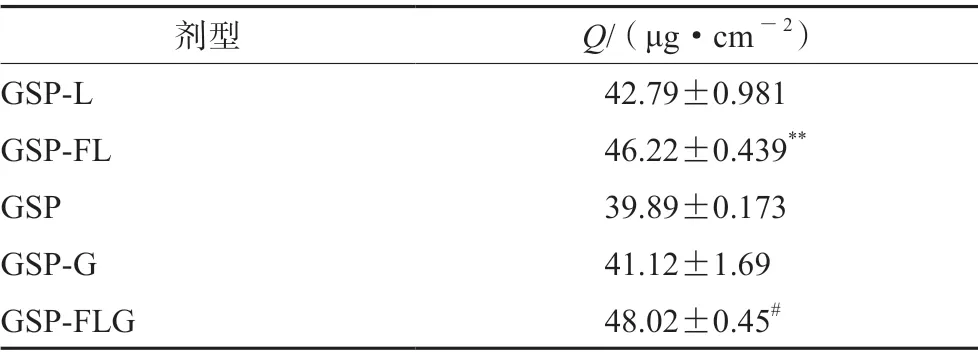
表7 GSP-FL、GSP-L、GSP、GSP-G和GSP-FLG的藥物皮膚滯留量( ±s,n=3)Tab 7 Drug skin retention of GSP-FL,GSP-L,GSP,GSP-G and GSP-FLG ( ±s,n=3)
注(Note):與GSP組相比,**P<0.01;與GSP-G組相比,##P<0.01(Compared with the GSP group,**P<0.01;compared with the GSP-G group,##P<0.01)。
劑型 Q/(μg·cm-2)GSP-L 42.79±0.981 GSP-FL 46.22±0.439**GSP 39.89±0.173 GSP-G 41.12±1.69 GSP-FLG 48.02±0.45#
2.5 體外釋放度考察
精密量取2 mL游離GSP溶液、GSP-FL、GSP-L混懸液以及1 g GSP-G和GSP-FLG 至透析袋(100 kDa)中,以8 mL 20%乙醇-生理鹽水為釋放介質,于Franz體外透皮擴散池上以300 r·min-1的轉速恒溫(32±0.5)℃釋放,分別于0.5、2、4、6、8、12、24、48、72 h后取樣,同時補加等量同等溫度的釋放介質,接收液用0.22 μm的微孔濾膜濾過后,按照“2.1.1”項下色譜條件1進樣分析,計算藥物的累積釋放量,累積釋放率=累積釋放量/投藥量。結果如表8所示,GSP組在12 h后累積釋放率逐漸增加,48 h時后顯著高于GSP-FL組(P<0.01),至72 h仍呈釋放趨勢,表現出明顯的突釋現象。與GSP-L組相比,12 h后GSP-FL組的累計釋放率逐漸增加,48 h后顯著高于GSP-L組(P<0.01),GSP-L與GSP-FL表現出長時間的緩釋效果。GSP-G組的累計釋放率在12 h后顯著高于GSP-FLG組(P<0.01),至72 h仍呈釋放趨勢,表現出明顯的突釋現象,而GSP-FLG組則在12 h后緩慢釋放。將藥物制備成GSP-FLG后,在12 h內的藥物累積釋放率顯著小于GSP-FL組(P<0.05),表明凝膠劑型使藥物緩釋效果更加明顯。通過藥物釋放動力學方程對體外藥物累積釋放結果進行擬合,結果顯示 GSP-FL、GSP-L組以 Weibull 方程,GSP-G以Higuchi方程進行擬合時具有較好的擬合度,而 GSP 、GSP-FLG組以Ritger-peppas擬合度較高。擬合結果如表9 所示。。
表8 GSP-FL、GSP-L、GSP、GSP-G和GSP-FLG藥物體外累積釋放實驗結果 ( ±s,n=4,%)Tab 8 In vitro cumulative release data of GSP-FL, GSP-L, GSP, GSP-G and GSP-FLG ( ±s,n=4,%)

表8 GSP-FL、GSP-L、GSP、GSP-G和GSP-FLG藥物體外累積釋放實驗結果 ( ±s,n=4,%)Tab 8 In vitro cumulative release data of GSP-FL, GSP-L, GSP, GSP-G and GSP-FLG ( ±s,n=4,%)
注(Note):與GSP-FL相比,*P<0.05,**P<0.01;與GSP-L相比,#P<0.05,##P<0.01;與GSP-FLG組相比,ΔP<0.01(Compared with the GSP-FL group,*P<0.05,**P<0.01;compared with the GSP-L group,#P<0.05,##P<0.01;compared with the GSP-FLG group,ΔP<0.01)。
時間(h) GSP GSP-L GSP-FL GSP-G GSP-FLG 0.5 7.77±0.011 10.71±0.013 8.60±0.0072 4.76±0.005 5.39±0.007*1 10.59±0.014 13.70±0.013 11.47±0.008 7.00±0.010 8.15±0.0156*2 14.58±0.015 16.98±0.018 15.72±0.013 10.38±0.015 11.00±0.021*4 20.66±0.022 21.36±0.026 20.91±0.004 16.67±0.020 15.83±0.027*6 25.02±0.033 23.76±0.031 24.43±0.013 20.98±0.0189 18.79±0.032*8 28.47±0.031 25.35±0.032 27.35±0.011 24.49±0.025 20.49±0.038*10 30.96±0.033 26.87±0.03 30.04±0.014 26.59±0.021 22.12±0.038*12 32.41±0.032 27.70±0.037 31.17±0.017 29.07±0.019Δ 23.55±0.040*24 38.77±0.024 30.57±0.036 35.99±0.017# 40.04±0.012Δ 31.01±0.050 48 60.38±0.021* 40.08±0.010 46.75±0.0235## 62.44±0.014Δ 46.77±0.078 72 63.58±0.042* 40.20±0.008 47.55±0.0232## 73.97±0.018Δ 50.35±0.107
表9 GSP-FL、GSP-L、GSP、GSP-G和GSP-FLG藥物累積釋放率曲線方程擬合( ±s,n=4)Tab 9 Equation fitting of cumulative release rate curve of GSP-FL,GSP-L,GSP,GSP-G and GSP-FLG ( ±s,n=4)

表9 GSP-FL、GSP-L、GSP、GSP-G和GSP-FLG藥物累積釋放率曲線方程擬合( ±s,n=4)Tab 9 Equation fitting of cumulative release rate curve of GSP-FL,GSP-L,GSP,GSP-G and GSP-FLG ( ±s,n=4)
擬合方式 組別 方程 R2零級釋放動力學方程GSP Q=0.0075t+0.0.1749 0.8658 GSP-L Q=0.0037t+0.1899 0.7396 GSP-FL Q=0.005t+0.1884 0.741 GSP-G Q=0.0094t+0.1272 0.9347 GSP-FLGQ=0.0061t+0.1271 0.8919一級釋放動力學方程GSP Q=0.5886(1-e-0.0.0742t) 0.8992 GSP-L Q=0.3437(1-e-0.2283t) 0.7013 GSP-FL Q=0.4351(1-e-0.1349t) 0.8751 GSP-G Q=0.7354(1-e-0.0434t) 0.9619 GSP-FLGQ=0.4801(1-e-0.0648t) 0.9135 Higuchi方程GSP Q=0.0735t1/2+0.0533 0.9765 GSP-L Q=0.0372t1/2+0.1257 0.9160 GSP-FL Q=0.0506t1/2+0.1011 0.9225 GSP-G Q=0.08991/2-0.0175 0.9975 GSP-FLGQ=0.0589t1/2+0.0306 0.9874 Weibull 方程GSP Q=2.0585(1-e-[0.0016(t-0.0233)]0.4415)0.9827 GSP-L Q=0.7311(1-e-[0.0074(t-0.2019)]0.3030)0.9836 GSP-FL Q=0.5714(1-e-[0.0505(t-0.0492)]0.4848)0.9920 GSP-G Q=9.9378(1-e-[0.0001(t-0.1501)]0.5313)0.9969 GSP-FLGQ=3.5(1-e-[0.0002(t-0.0978)]0.442) 0.9893 Ritger-peppas方程GSP Q=0.1174(t0.4037) 0.9851 GSP-L Q=0.1470(t0.2461) 0.9789 GSP-FL Q=0.1377(t0.3048) 0.9747 GSP-G Q=0.0783(t0.5282) 0.9973 GSP-FLGQ=0.0835(t0.4278) 0.9913
3 討論
體外透皮實驗時接收液應該滿足漏槽條件,常用的透皮接收液有生理鹽水、等滲磷酸鹽緩沖液等,對一些脂溶性強的物質,常在接收液中加入醇類和非離子表面活性劑等。GSP作為聚合物,低聚部分分子量小,水溶性好,隨著聚合度增加,溶解度逐漸降低[13-14]。前期嘗試過在生理鹽水、PBS中加入吐溫20、無水乙醇來進行溶解度考察,發現GSP在無水乙醇-生理鹽水中具有較好的溶解度且滿足漏槽條件,但超過20%的乙醇對皮膚有較強脂質提取和屏障破壞作用,并且容易揮發[15],所以在實驗中選擇20%乙醇-生理鹽水作為接收介質。透皮吸收首選的皮膚屏障是人體皮膚,但由于獲得人體皮膚組織較為困難,常用動物皮膚來代替。在使用大鼠皮膚出現了藥物的累積透過量低的問題,為減少皮膚差異性的問題,統一采用同一批昆明種小鼠的腹部皮膚作為滲透膜進行透皮實驗。
透析袋實驗中,通過釋藥曲線與擬合方程分析GSP-FL及GSP-FLG的釋藥機制,由釋藥曲線推測,GSP-FL組釋藥分為快釋和緩釋,在10 h后藥物開始緩慢釋放,推測藥物快釋過程是由于柔質體中未被包載藥物的快速釋放。而GSP-FLG組也表現出同樣的釋藥規律,12 h后包裹于脂質體中的藥物通過凝膠緩慢釋放藥物,推測藥物快釋是由于凝膠劑中附在脂質體表面的或包埋較淺的原花青素或未被包載的游離藥物的釋放,12 h后包裹在脂質體中的藥物通過凝膠緩慢釋放。脂質體被致密的凝膠基質固定,使得其聚集、相容更加困難,增加脂質體的穩定性,也進一步增強了藥物的緩釋效果,徐蕾[16]在進行高烏甲素脂質體凝膠透皮釋藥考察的實驗中也得出了同樣的釋藥規律。通過透析袋釋藥初步考察脂質體凝膠的釋放過程,發現GSP-FLG的釋放過程符合Ritgerpeppas釋放特性。陳積[17]進行體外透皮實驗發現,復方莪術油脂質體凝膠中吉馬酮和維A酸24 h的累積透皮量均顯著低于復方莪術油凝膠,可長時間穩態釋藥,具有緩釋作用,相較于藥物凝膠,脂質體凝膠的緩釋作用更加顯著。
本實驗比較了GSP、GSP-L、GSP-FL的體外透皮性能,游離的GSP表現出突釋效果,將其制備為柔質體后,可顯著降低其釋放速率,達到緩釋效果。相比GSP-L,由于GSP-FL的柔韌性和形變性,表現出更高的累計釋放率和透皮速率。GSP-FL的皮膚滯留量顯著高于GSP,說明將其制備為柔質體能使藥物更多地滯留在皮膚內。而將柔質體進一步制備成凝膠后可減少其流動性,使藥物長時間與皮膚接觸,皮膚滯留量更高,有利于藥物在皮膚局部發揮作用;并且水凝膠無油膩感,易涂展,局部給藥后易吸收,具有制備工藝簡單、穩定性好等優點[18]。張小靈[19]制備的雙丹脂質體凝膠劑具有較強緩釋作用,可延長給藥時間,皮膚內藥物貯量較大,藥物大多蓄積在真皮層中,有利于瘢痕的治療。時軍等[20]制備的丹皮酚陽離子脂質體凝膠的累積透過量、藥物透皮速率與皮膚蓄積量亦顯著大于普通凝膠。有研究報道,GSP具有抑制酪氨酸酶的活性[21],而酪氨酸酶是黑色素生成的關鍵限速酶[22-23],因此有望將GSP-FLG開發為具有美白功效的化妝品制劑,但其效果還需要進一步實驗驗證。
本研究以柔質體為載體,并將其進一步制備成凝膠劑,實現了皮膚局部給藥并具有緩釋的效果,充分發揮了柔質體和凝膠劑的優勢,具有廣闊的應用前景。

