甘遂中的新三萜及其抗氧化活性
馬 麗,王嘉霖,柴 甜,王鋮博,孟憲華,楊軍麗*
?化學成分 ?
甘遂中的新三萜及其抗氧化活性
馬 麗1, 2,王嘉霖3,柴 甜1,王鋮博1,孟憲華1,楊軍麗1*
1. 中國科學院蘭州化學物理研究所,中國科學院西北特色植物資源化學重點實驗室,甘肅省天然藥物重點實驗室,甘肅 蘭州 730000 2. 中國科學院大學,北京 100049 3. 西北民族大學,甘肅 蘭州 730030
對甘遂塊根中的三萜化學成分和抗氧化活性進行研究。采用多種柱色譜法進行分離純化,并運用譜學分析鑒定化合物的結構。通過CCK-8法,對分離的化合物在SH-SY5Y細胞中的抗氧化活性進行了篩選。從甘遂塊根甲醇提取物中分離鑒定出5個三萜,其中包括3個大戟烷型,分別為大戟-8,24-二烯-3β-醇-7,11-二酮(1)、(24)-大戟-8,25-二烯-3β,24-二醇(2)、大戟二烯醇(3);2個羊毛脂烷型三萜,3β,11β-二羥基羊毛脂-8,24-二烯-7-酮(4)、3β,7β-二羥基羊毛脂-8,24-二烯-11-酮(5)。化合物5為新化合物,為羊毛脂烷型三萜,命名為甘遂羊毛脂酮A;化合物1和4為首次從該植物中分離得到;化合物2和5在SH-SY5Y細胞中具有一定的抗氧化能力和潛在的神經保護活性。
甘遂;三萜;大戟烷型三萜;羊毛脂烷型三萜;甘遂羊毛脂酮A;大戟二烯醇;抗氧化活性;神經保護活性
甘遂是大戟科大戟屬植物甘遂S.L.Liou ex S.B.Ho的干燥塊根,是我國特有的植物,主要分布在甘肅、河南、山西、陜西和青海等地。甘遂干燥的塊根為其主要入藥部分,廣泛地被用于治療各種疾病,如癌癥、水腫、腹水和哮喘[1-3]。目前,從甘遂中分離得到的化學成分為三萜、二萜和甾醇類化合物,其他成分包括香豆素、脂肪酸、蔗糖、鞣質和樹脂等[4-7]。其中,二萜和三萜類是甘遂的主要化學成分,具有廣泛的藥理活性,如抗病毒、抗炎、抗腫瘤等活性[8-13]。通過對甘遂甲醇提取物進一步分離純化,共分離出5個三萜類化合物(圖1),甘遂-8,24-二烯-3β-醇-7,11-二酮(eupha-8,24-diene-3β-ol-7,11-dione,1)、(24)-甘遂- 8,25-二烯-3β,24-二醇 [(24)-eupha-8,25-diene-3β, 24-diol,2]、大戟二烯醇(euphol,3)、3β,11β-二羥基羊毛脂-8,24-二烯-7-酮(3β,11β-dihydroxy- lanosta-8,24-dien-7-one,4)、3β,7β-二羥基羊毛脂- 8,24-二烯-11-酮(3β,7β-dihydroxylanosta-8,24-dien- 11-one,5)。化合物1~3為大戟烷型三萜,化合物4和5為羊毛脂烷型三萜,其中化合物5為新化合物,命名為甘遂羊毛脂酮A(euphokansuione A)。化合物1和4為首次從該植物中分離得到。對化合物的抗氧化活性進行了篩選,發現化合物2和5在SH-SY5Y細胞中具有一定的抗氧化能力和潛在神經保護活性。

圖1 化合物1~5的化學結構
1 儀器與材料
Bruker Avance III 400核磁共振波譜儀(美國Bruker公司);Bruker microTOF-Q II質譜儀(美國Bruker公司);IFS120HR 670 FT-IR(德國布魯克公司);UV-vis spectrophotometer(美國珀金埃爾默公司)。反相色譜Lichroprep RP18(40~63 μm,美國Merck公司)。薄層硅膠板和柱色譜用正相硅膠(200~300目)均為青島海洋化工廠生產。制備型HPLC C18色譜柱(250 mm×10 mm,10 μm)、ODS-2色譜柱(250 mm×20 mm,10 μm)(中國漢邦公司)。
藥材2017年從蘭州黃河藥材市場購買,經中國科學院蘭州化學物理研究所戚陽歡副研究員鑒定為甘遂S.L.Liou ex S.B.Ho的塊根,植物樣本(GS-HHTS-201701)存放在中國科學院西北植物資源化學重點實驗室。
2 提取與分離
將甘遂的干燥塊根粉碎并用甲醇在室溫下浸泡3次,每次7 d,共提取3次。合并提取液,減壓濃縮干燥,得到總浸膏(1031 g)。然后,將其分散在水中,依次用石油醚、醋酸乙酯和正丁醇進行萃取,每相萃取3次。合并萃取液蒸干溶劑后,得到石油醚萃取物(354.4 g),用等量硅膠拌樣,干法裝柱,以石油醚-丙酮(10∶1~0∶1)梯度洗脫,薄層色譜進行檢測,合并相同組分,共得到11個組分(Fr. 1~11)。
Fr. 4(9.1 g)用反相C18柱色譜,甲醇-水(50%~100%)洗脫,得到6個亞組分(Fr. 4a~4f)。通過反相制備HPLC(90%甲醇-水)進一步分離和純化Fr. 4a(158.1 mg),得到化合物1(11.7 mg,R=22.8 min)和2(5.9 mg,R=25.4 min)。通過反相制備HPLC(88%甲醇-水)純化Fr. 4e(148.6 mg),得到化合物3(5.1 mg,R=35.1 min)。
Fr. 6(13.5 g)用反相C18柱色譜,用甲醇-水(50%~100%)洗脫;然后用正相硅膠柱色譜,以石油醚-丙酮(10∶1~0∶1)梯度洗脫進行純化,得到化合物4(10.3 mg)和5(5.5 mg)。
3 結構鑒定
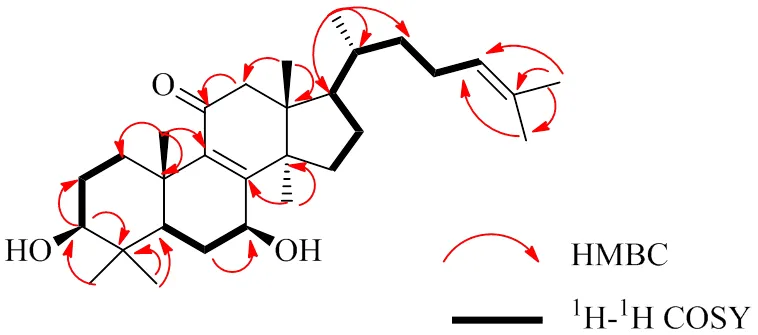
化合物5:無色膠狀物,HR-ESI-MS準分子離子/495.340 4 [M+K]+(計算值C30H48O3K,495.340 6),表明分子式為C30H48O3,存在7個不飽和度。(nm): 254 (3.38);(cm?1): 3439, 2968, 2931, 1670, 1458, 1378, 1185。3439和1670 cm?1處的強紅外吸收表明存在羥基和羰基。254 nm處的紫外吸收是共軛羰基的特征峰。1H-和13C-NMR數據見表1,化合物5的13C-NMR數據顯示共有30個碳信號,1H-NMR譜中顯示化合物5中含有2個羥基,4.27 (1H, brs, H-7), 3.32 (1H, dd,= 11.2, 5.6 Hz, H-3), 4.27 (1H, brs, H-7) 和1個不飽和雙鍵5.07 (1H, d,= 6.4 Hz, H-24)。通過譜學數據對比,發現化合物5與已知化合物3β,7α-二羥基羊毛脂-8,24-二烯-11-酮的分子結構相似[5],僅在C-7處的羥基構型不同,化合物5中C-7處的羥基的相對構型被指定為β取向,在NOE譜圖中H-3和H3-28與H-7和H3-30的相關性(圖2)可進一步證明。故化合物1的結構鑒定為3β,7β-二羥基羊毛脂-8,24-二烯-11-酮,經Sci-Finder檢索,為1個新化合物,命名為甘遂羊毛脂酮A。
表1 化合物5的核磁共振數據(400/100 MHz, CDCl3)
Table 1 1H- and 13C-NMR spectral data of compound 5 (400/100 MHz,CDCl3)
碳位δHδC 1α1.01 (m)33.9 1β2.55 (m) 21.69 (m)28.1 33.32 (dd, J = 11.2, 5.6 Hz)78.8 4 38.6 51.41 (m)45.6 61.80 (m)28.6 74.27 (brs)65.6 8 157.3 9 141.6 10 38.5 11 200.4 12α2.56 (d, J = 17.2 Hz)51.8 12β2.37 (d, J = 17.2 Hz) 13 51.1 14 44.3 15α1.36 (m)29.7 15β1.24 (m) 16α2.02 (m)27.9 16β1.40 (m) 171.72 (m)50.9 180.92 (s)18.3 191.17 (s)18.1 201.43 (m)36.0 210.88 (d, J = 6.4 Hz)18.6 220.95, 1.44 (m)35.3 231.86, 2.04 (m)25.3 245.07 (d, J = 6.4 Hz)124.8 25 131.4 261.67 (s)25.9 271.60 (s)17.8 281.05 (s)28.3 290.85 (s)16.2 301.01 (s)26.0
化合物1:黃色膠狀物。1H-NMR (400 MHz, CDCl3): 0.91 (3H, s, H-18), 1.02 (3H, s, H-29), 1.07 (3H, s, H-30), 0.87 (3H, d,= 6.6 Hz, H-21), 0.90 (3H, s, H-28), 1.30 (3H, s, H-19), 1.68 (3H, s, H-26), 1.60 (3H, s, H-27), 3.29 (1H, dd,= 10.5, 5.8 Hz, H-3), 5.07 (1H, m, H-24);13C-NMR (100 MHz, CDCl3): 34.0 (C-1), 27.6 (C-2), 78.1 (C-3), 38.7 (C-4), 48.6 (C-5), 35.8 (C-6), 200.1 (C-7), 149.9 (C-8), l54.9 (C 9), 38.2(C-10), 202.2 (C-11), 51.7 (C-12), 45.2(C-13), 48.0 (C-14), 31.9 (C-15), 28.3 (C-16), 49.5 (C-17), 18.5 (C-18), l7.9 (C-19), 35.9 (C-20), 18.6 (C-21), 35.3 (C-22), 25.2 (C-23), 124.7 (C-24), l31.5 (C-25), 25.9 (C-26), 17.8 (C-27), 15.2 (C-28), 27.7 (C-29), 24.2 (C-30)。以上波譜數據與文獻報道一致[14-15],故鑒定化合物1為甘遂-8,24-二烯-3β-醇-7,11-二酮。
化合物2:白色無定形粉末。1H-NMR (400 MHz, CDCl3): 4.92, 4.83 (2H, brs, H-26), 4.01 (1H, t,= 6.1 Hz, H-24), 3.23 (1H, dd,= 4.5, 11.7 Hz, H-3), 1.72 (3H, brs, H-27), 0.99 (3H, s, H-19), 0.94 (3H, s, H-28), 0.86 (3H, s, H-30), 0.85 (3H, d,= 6.2 Hz, H-21), 0.79 (3H, s, H-29), 0.75 (3H, s, H-18);13C-NMR (100 MHz, CDCl3): 35.3 (C-1), 27.9 (C-2), 79.0 (C-3), 38.9 (C-4), 51.0 (C-5), 18.9 (C-6), 27.7 (C-7), 134.0 (C-8), 133.5 (C-9), 37.3 (C-10), 21.5 (C-11), 30.9 (C-12), 44.1 (C-13), 50.0 (C-14), 31.1 (C-15), 28.0 (C-16), 49.7 (C-17), 15.7 (C-18), 20.1 (C-19), 36.0 (C-20), 19.0 (C-21), 37.3 (C-22), 31.6 (C-23), 76.6 (C-24), 147.6 (C-25), 111.1 (C-26), 17.4 (C-27), 28.0 (C-28), 15.5 (C-29), 24.5 (C-30)。以上波譜數據與文獻報道一致[6],故鑒定化合物2為(24)-甘遂-8,25-二烯-3β,24-二醇。
化合物3:白色無定形粉末;1H-NMR (400 MHz, CDCl3):0.75 (3H, s, H-18), 0.79 (3H, s, H-29), 0.84 (3H, s, H-30), 0.86 (3H, d,= 6.4 Hz, H-21), 0.95 (3H, s, H-28), 1.00 (3H, s, H-19), 1.60 (3H, s, H-26), 1.66 (3H, s, H-27), 3.21 (1H, dd,= 11.5, 4.5 Hz, H-3), 5.08 (1H, t,= 7.0 Hz, H-24);13C-NMR (100 MHz, CDCl3): 35.7 (C-1), 24.3 (C-2), 79.1 (C-3), 39.0 (C-4), 50.6 (C-5), 18.4 (C-6), 27.9 (C-7), 134.6 (C-8), l33.5 (C-9), 36.3 (C-10), 21.1 (C-11), 28.2 (C-12), 44.7(C-13), 49.9 (C-14), 30.9 (C-15), 31.2 (C-16), 50.6 (C-17), 15.8 (C-18), l9.2 (C-19), 36.4 (C-20), 18.7 (C-21), 35.6 (C-22), 25.0 (C-23), 125.3 (C-24), l31.0 (C-25), 17.6 (C-26), 25.6 (C-27), 26.6 (C-28), 28.0 (C-29), 15.4 (C-30)。以上波譜數據與文獻報道一致[6],故鑒定化合物3為大戟二烯醇。
化合物4:無色膠狀物;1H-NMR (400 MHz, CDCl3): 0.71 (3H, s, H-18), 0.91 (3H, s, H-29), 1.14 (3H, s, H-30), 0.87 (3H, d,= 6.4 Hz, H-21), 0.99 (3H, s, H-28), 1.26 (3H, s, H-19), 1.68 (3H, s, H-26), 1.61 (3H, s, H-27), 3.32 (1H, dd,= 11.2, 5.6 Hz, H-3), 4.70 (1H, t,= 7.2 Hz, H-11), 5.09 (1H, t,= 7.2 Hz, H-24);13C-NMR (100 MHz, CDCl3): 33.8 (C-1), 28.0 (C-2), 78.4 (C-3), 39.2 (C-4), 49.4 (C-5), 36.0 (C-6), 200.2 (C-7), 140.6 (C-8), l61.3 (C-9), 39.7 (C-10), 68.3 (C-11), 43.0 (C-12), 48.2 (C-13), 46.3 (C-14), 32.0 (C-15), 27.5 (C-16), 48.8 (C-17), 16.4 (C-18), l9.8 (C-19), 35.9 (C-20), 18.9 (C-21), 35.9 (C-22), 25.0 (C-23), 125.0 (C-24), l31.3 (C-25), 25.9 (C-26), 17.9 (C-27), 27.7 (C-28), 15.3(C-29), 25.9 (C-30)。以上波譜數據與文獻報道一致[5],故鑒定化合物4為3β,11β-二羥基羊毛脂- 8,24-二烯-7-酮。
4 生物活性研究
對分離出的化合物進行抗氧化活性篩選。首先,利用SH-SY5Y細胞建立氧化損傷模型[16],篩選化合物的抗氧化活性。通過初步篩選,發現化合物2和5在一定程度上具有保護SH-SY5Y細胞免受氧化損傷的活性,化合物2與模型組(H2O2)相比有顯著差異(圖3)。然后,通過對化合物2和5(圖4)的進一步抗氧化研究,發現化合物2和5在1、5、10 μmol/L濃度下與模型組的抗氧化活性存在顯著差異。它可以顯著增強SH-SY5Y細胞對氧化損傷的耐受性,表明化合物2和5具有一定的抗氧化能力和潛在的神經保護活性。

與模型組比較,*P<0.05

與模型組比較,**P<0.01 ***P<0.001
5 討論
本實驗從甘遂的甲醇提取物中分離出5個三萜化合物,包括2個羊毛脂烷三萜和3個大戟烷型三萜,其中化合物5為新的羊毛脂烷型三萜,化合物1和4為首次從該植物中分離得到。此外,用CCK-8法對分離得到的5個化合物進行了抗氧化活性篩選,結果表明化合物2和5具有一定的抗氧化活性。
利益沖突 所有作者均聲明不存在利益沖突
[1] Zhang J S, Weng H Z, Huang J L,. Anti-inflammatory ingenane diterpenoids from the roots of[J]., 2018, 84(18): 1334-1339.
[2] Lee J W, Jin Q H, Jang H,. Jatrophane and ingenane-type diterpenoids frominhibit the LPS-induced NO production in RAW 264.7 cells [J]., 2016, 26(14): 3351-3354.
[3] Meng X H, Wang K, Chai T,. Ingenane and jatrophane diterpenoids fromand their antiproliferative effects [J]., 2020, 172: 112257.
[4] Wang L Y, Wang N L, Yao X S,. Euphane and tirucallane triterpenes from the roots ofand theireffects on the cell division of[J]., 2003, 66(5): 630-633.
[5] Lu Z Q, Chen G T, Zhang J Q,. Four new lanostane triterpenoids from[J]., 2007, 90(11): 2245-2250.
[6] Guo J, Zhou L Y, He H P,. Inhibition of 11β-HSD1 by tetracyclic triterpenoids from[J]., 2012, 17(10): 11826-11838.
[7] Cheng F F, Yang Y J, Zhang L,. A natural triterpene derivative frominhibits cell proliferation and induces apoptosis against rat intestinal epithelioid cell line[J]., 2015, 16(8): 18956-18975.
[8] Yan X J, Zhang L, Guo J M,. Processing of Kansui roots stir-baked with vinegar reduces Kansui-induced hepatocyte cytotoxicity by decreasing the contents of toxic terpenoids and regulating the cell apoptosis pathway [J]., 2014, 19(6): 7237-7254.
[9] Zheng W F, Cui Z, Zhu Q. Cytotoxicity and antiviral activity of the compounds from[J]., 1998, 64(8): 754-756.
[10] Shi Q W, Su X H, Kiyota H. Chemical and pharmacological research of the plants in genus[J]., 2008, 108(10): 4295-4327.
[11] Zhang Q, Zhou Q R, Lou J W,. Chemical constituents from[J]., 2017, 22(12): 2176.
[12] Peng Q, Li G Y, Ma Y P,. Chemical constituents of[J]., 2012, 43: 64-66.
[13] Shen J, Kai J, Tang Y P,. The chemical and biological properties of[J]., 2016, 44(2): 253-273.
[14] Lu C J, Guo Y Y, Yan J,. Design, synthesis, and evaluation of multitarget-directed resveratrol derivatives for the treatment of Alzheimer's disease [J]., 2013, 56(14): 5843-5859.
[15] Yuan F Y, Xu F, Fan R Z,. Structural elucidation of three 9, 11-tetracyclic triterpenoids enables the structural revision of euphorol J [J]., 2021, 86(11): 7588-7593.
[16] 王書云, 李國玉, 張珂, 等. 維吾爾族藥大戟脂中三萜類化學成分研究 [J]. 中國中藥雜志, 2018, 43(18): 3688-3693.
New triterpenes from roots ofand their antioxidant activities
MA Li1, 2, WANG Jia-lin3, CHAI Tian1, WANG Cheng-bo1, MENG Xian-hua1, YANG Jun-li1
1. CAS Key Laboratory of Chemistry of Northwestern Plant Resources, Gansu Key Laboratory for Natural Medicine, Lanzhou Institute of Chemical Physics, Chinese Academy of Sciences, Lanzhou 730000, China 2. University of Chinese Academy of Sciences, Beijing 100049, China 3. Northwest Minzu University, Lanzhou 730030, China
To isolate compounds from the roots ofand investigate their antioxidant activities.Various column chromatography techniques were used to isolate and purify the compounds and their structures were identified by spectral data. Meanwhile, the isolated compounds were evaluated for antioxidant activity in SH-SY5Y cells.Five triterpenes were isolated and identified from the methanol extract of the roots of, including three euphane triterpenes, namely eupha-8,24-diene-3β-ol-7,11-dione(1), (24)-eupha-8,25-diene-3β,24-diol (2), euphol (3), and two lanostane triterpenes namely 3β,11β-dihydroxylanosta-8,24-dien-7-one (4), 3β,7β-dihydroxylanosta-8,24-dien-11-one(5).Compound 5 is a new compound named euphokansuione A and compounds 1 and 4 are isolated from this plant for the first time. Compounds 2 and 5 have certain antioxidant capacity in SH-SY5Y cells and potential neuroprotective activity.
S.L.Liou ex S.B.Ho; triterpenes; euphane triterpene; lanostane triterpene; euphokansuione A;euphol; antioxidant activity; potential neuroprotective activity
R284.1
A
0253 - 2670(2022)08 - 2269 - 05
10.7501/j.issn.0253-2670.2022.08.001
2022-01-05
甘肅省自然科學基金項目(21JR7RA075);甘肅省自然科學基金項目(20JR5RA570)
馬 麗,碩士研究生,研究方向為甘遂的活性成分研究。E-mail: mali@licp.cas.cn
楊軍麗,博士生導師,研究員,從事中草藥活性成分和新藥研究。E-mail: yangjl@licp.cas.cn
[責任編輯 王文倩]

