CESM量化特征聯合形態學對BI-RADS 3~5類乳腺單發腫塊的診斷價值
徐維敏,鄭博文,潘德潤,文嬋娟,汪思娜,曾 輝,何子龍,秦耿耿,陳衛國
南方醫科大學南方醫院放射科,廣東 廣州 510515
乳腺癌是中國女性的第一好發惡性腫瘤[1]。對比增強能譜乳腺攝影(contrast enhancement spectral mammography,CESM)是乳腺X線攝影的新技術,診斷效能與乳腺磁共振成像(magnetic resonance imaging,MRI)相似[2-3]。不同于全視野數字乳腺X線攝影(fullfield digital mammography,FFDM)、數字乳腺體層合成(digital breast tomosynthesis,DBT),CESM基于碘離子的K緣,運用低能量(26~32 kVp)和高能量(45~49 kVp)于同一壓迫下攝影,獲得低能圖和高能圖,并通過后處理得到減影圖;CESM能通過病灶對碘離子的攝取,更明顯地突出病灶[4],其低能圖及減影圖形態學是診斷乳腺良惡性病變的基礎。國內外學者[5-7]通過CESM形態學對乳腺病變的研究顯示,部分良惡性病變的表現相似,導致鑒別診斷存在一定困難。且對于致密類乳腺,有研究[5]發現,CESM較常規乳腺X線攝影,診斷特異度僅為67.9%(CESM vs FFDM為67.9% vs 51.8%)。為了降低CESM形態學主觀分析的影響,Deng等[8]通過對CESM乳腺強化病灶的量化分析,結果顯示根據病灶強化程度的量化值診斷乳腺良惡性病變的靈敏度為75.5%,特異度為88.6%,準確度為82.1%。筆者前期通過對乳腺腫塊的強化量化值及動態強化特征研究[9],發現腫塊強化量化值聯合動態強化特征診斷乳腺良惡性腫塊的靈敏度為63.4%~90.2%,特異度為54.1%~75.8%,準確度為66.0%~82.0%。
為了更客觀地評價乳腺疾病及更好地提高診斷效能,我們設想乳腺腫塊的CESM量化特征聯合其形態學特征,可能提高乳腺良惡性病變的診斷效能。
1 資料和方法
1.1 研究對象
本研究通過了南方醫科大學南方醫院倫理委員會的批準(批準文號NFEC-2017-136),所有受檢者檢查前均簽署知情同意書。
研究時間為2018年1月—2020年12月。受檢者納入標準:① 經常規FFDM或超聲檢查懷疑為乳腺影像報告和數據系統(Breast Imaging Reporting and Data System,BI-RADS)3~5類乳腺單發腫塊型病變;② CESM前無放化療病史和/或6個月內無乳腺手術史;③ CSEM檢查順序為患側頭尾(craniocaudal,CC)位、患側內外斜(mediolateral oblique,MLO)位、健側CC位及健側MLO位。排除標準:① 妊娠期、準備妊娠或哺乳期婦女;② 不能配合檢查的嚴重疾病患者;③ 碘對比劑過敏或腎功能不全;④ 減影圖多個強化病灶;⑤ 減影圖乳腺腫塊與背景強化不能區分、影響病灶感興趣區(region of interest,ROI)勾畫者;⑥ 患側CC位或MLO位病灶未能包全者;⑦ 最終診斷無病理學檢查證實者。
1.2 影像學檢查方法
采用美國GE公司的Senographe Essential全數字乳腺機進行CESM檢查。對比劑采用非離子型碘對比劑碘海醇(含碘300 mg/mL),劑量為1.5 mL/kg。經高壓注射器以3 mL/s的流率注入上臂靜脈,注射完成2 min后開始攝影,每例受檢者在7 min內完成全部體位攝片。
具體攝影順序如下:① 患側CC位;② 患側MLO位;③ 健側乳腺CC位;④ 健側MLO位。患側乳腺具體攝影時間如下:在注射對比劑后第2、4 min分別開始CC位、MLO位攝影,并在3、5 min內完成。早期時相定義為T1(注射對比劑結束后第2~3 min拍攝的患側CC位);晚期時相定義為T2(注射對比劑結束后第4~5 min拍攝的患側MLO位)。
每個投照位置攝片時,在1次壓迫的1.5 s內連續獲得1次低能和1次高能曝光。每個攝片體位在工作站上均可獲得2張圖像,即低能圖像和經過特定算法處理的高能減去低能的減影圖像。
1.3 圖像分析
1.3.1 CESM形態學分析
所有圖像采集完成后均自動傳送至影像存儲與傳輸系統(picture archiving and communication system,PACS)進行讀片和評價。CESM低能圖和減影圖分別由2名具有8年和9年乳腺影像學診斷經驗的醫師參考第5版美國放射學會(American College of Radiology,ACR)BI-RADS[10]雙盲分析。
CESM低能圖形態學著重分析:① 病變類型(單純腫塊、腫塊伴鈣化);② 腫塊密度(含脂肪密度、低密度、等密度及高密度);③ 腫塊形態(圓形/橢圓形、不規則形);④ 腫塊邊緣(清晰、遮蔽、模糊、淺分葉、毛刺)。
CESM減影圖腫塊型強化病灶著重描述:① 腫塊形態(圓形/橢圓形、不規則形);② 強化特點(均勻、不均勻及環形強化);③ 強化程度(輕度、中度、明顯);④ 病灶邊緣(清楚、模糊、毛刺)。
1.3.2 CESM減影圖量化分析
CESM減影圖由1名有9年乳腺影像診斷經驗的醫師運用ITK-SNAP軟件(3.8.0版)在CESM的2個攝影時相(患側CC及MLO位)減影圖像上分別沿著腫塊(腫塊直徑≥5 mm)的邊緣手動勾畫腫塊的ROI(圖1)。隨后,使用基于Python 3.7的Simple ITK(Version 1.2.0)和Open CV(Version 4.1.2)讀取Dicom格式的勾畫好的CESM減影圖像,將減影圖轉換成16-bit圖像(灰度值范圍0~65 536),并計算ROI內病灶強化灰度值(lesion grey value,LGV)。由于無法分離出與強化病灶重疊的正常腺體組織強化值,因此病灶強化值的結果僅代表ROI內整個病灶范圍的強化值。背景的ROI由病灶ROI反轉后,減去乳腺輪廓內的極度致密的點(乳頭、皮膚褶皺等)得到。MLO位的背景ROI還需要進一步減去胸大肌范圍。本研究分別測量了患側乳腺CC、MLO位圖像的病灶LGV。另外,我們利用公式⑴來計算病灶的不同時相病灶強化灰度值變化率(lesion grey value difference,LGVD)。
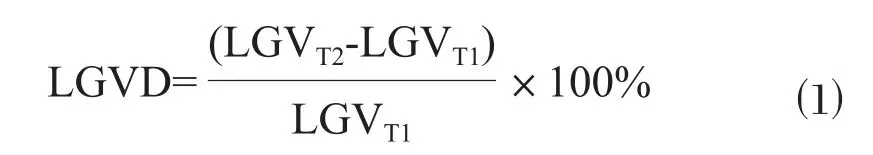
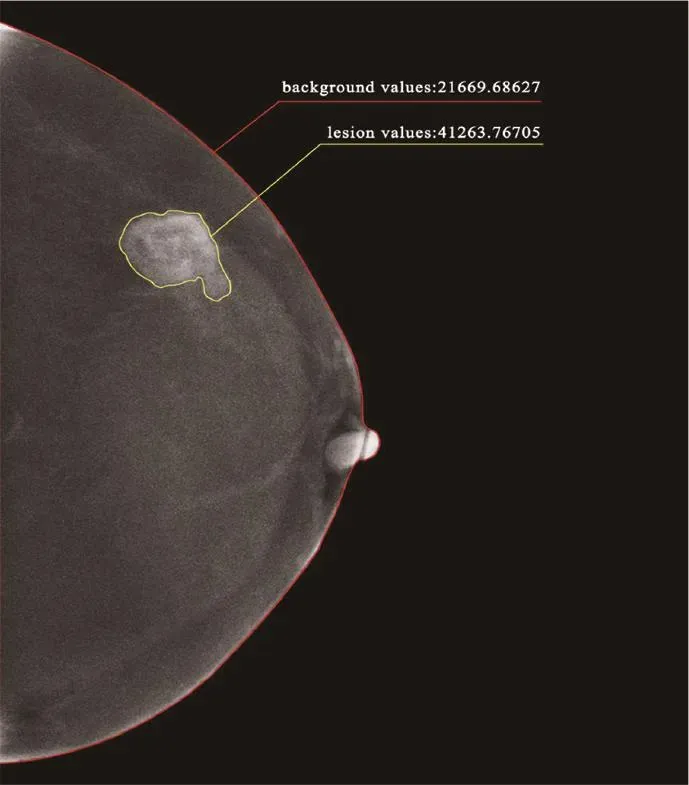
圖1 減影圖強化病灶的ROI勾畫
根據兩個相鄰攝影時相病灶的LGVD,本研究參考ACR BI-RADS MRI強化方式[10]將CESM動態強化特征分為3種:① 上升型,變化率>10%;② 平臺型,-10%≤變化率≤10%;③ 流出型,變化率<-10%(圖2)。
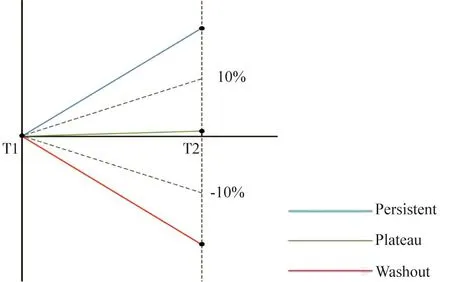
圖2 腫塊的動態強化特征分型
閱片者首先閱讀C E S M圖像,判斷BI-RADS分類,并記錄結果。為避免CESM形態學對量化特征診斷結果產生影響,醫師對同一受檢者的CESM量化值及動態強化特征診斷時間間隔2周;再間隔2周后,綜合CESM形態學及量化特征(量化值+動態強化特征)進行診斷。本研究中,2名閱片者意見不一致時,由上一級醫師共同商定;將BI-RADS 1~4A類判定為良性,4B~5類判定為惡性。
1.4 統計學處理
采用SPSS 22.0軟件進行統計學分析。采用χ2檢驗和受試者工作特征(receiver operating characteristic,ROC)曲線分析CESM形態學、量化分析、形態學+量化分析的診斷效能,根據約登指數[Y=(靈敏度+特異度)-1]確定特征的最佳閾值,并計算其診斷的靈敏度、特異度和準確度。使用兩獨立樣本t檢驗分析不同時相良惡性腫塊LGV的差異。基于LGVD的動態強化特征采用χ2檢驗的方法進行統計學分析。P<0.05為差異有統計學意義。
2 結 果
2.1 基本資料
171例患者符合上述標準納入研究,其中11例中途要求退出,最終160例納入研究(表1)。患者均為女性,年齡24~74歲,平均年齡(47.86±9.78)歲。118例為乳腺癌,包括導管原位癌4例、浸潤性導管癌95例及其他類型乳腺癌19例;42例為良性病變,包括纖維腺瘤11例、導管內乳頭狀瘤5例、囊腫合并感染3例、炎癥8例、分葉狀腫瘤4例、腺病6例及纖維囊性乳腺病5例。乳腺癌患者平均發病年齡[(49.24±9.67)歲]較良性病變[(43.98±9.13)歲]大。乳腺良惡性病變均以致密型(包括c類及d類)乳腺多見,良性病變vs乳腺癌為88.1%vs88.2%(圖3、4)。
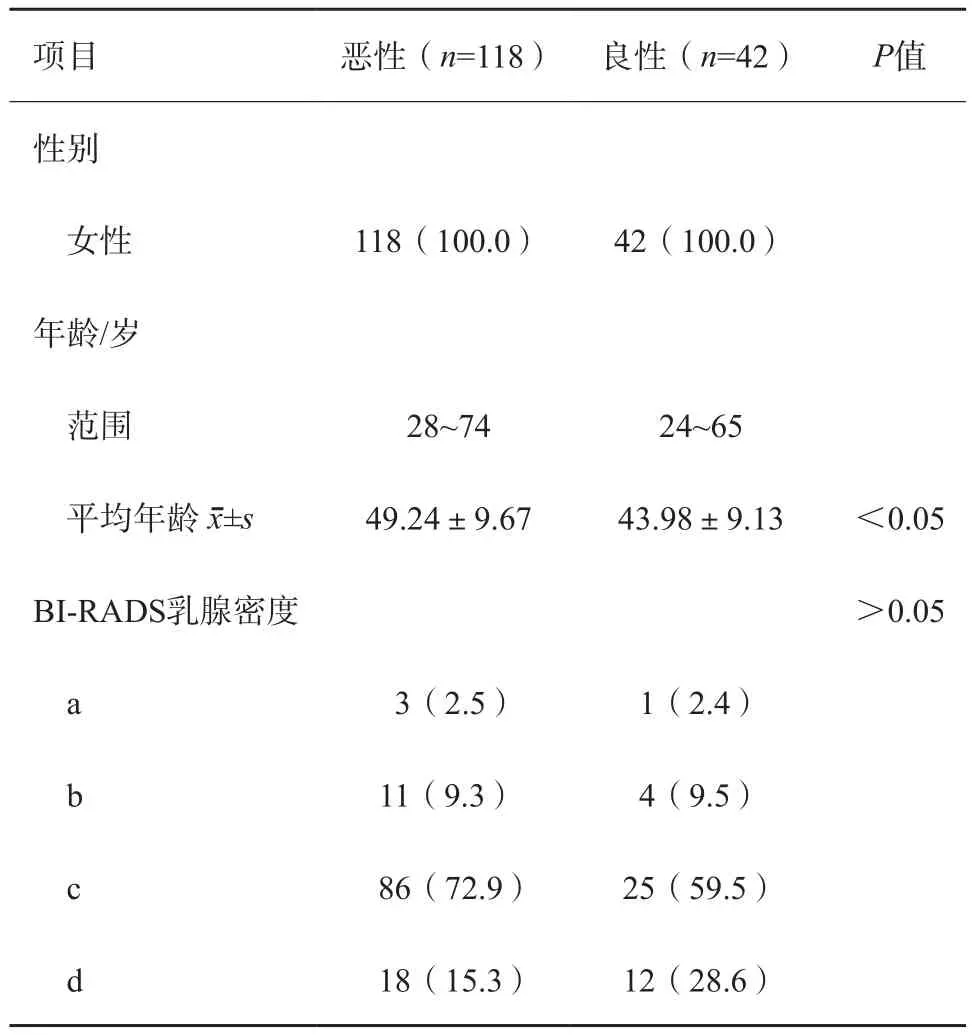
表1 160例患者基本資料 n(%)
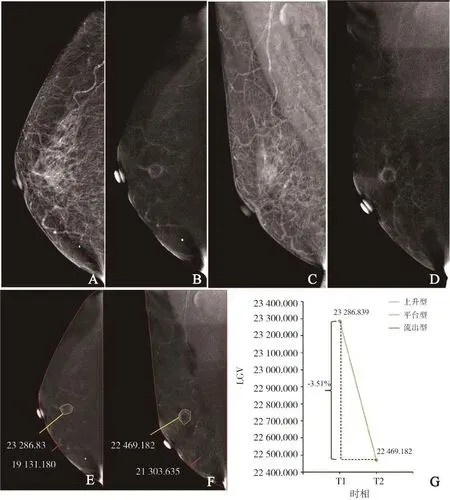
圖3 典型病例1(患者,女性,62歲,乳腺淋巴細胞性乳腺炎)的CESM形態學及量化值圖像
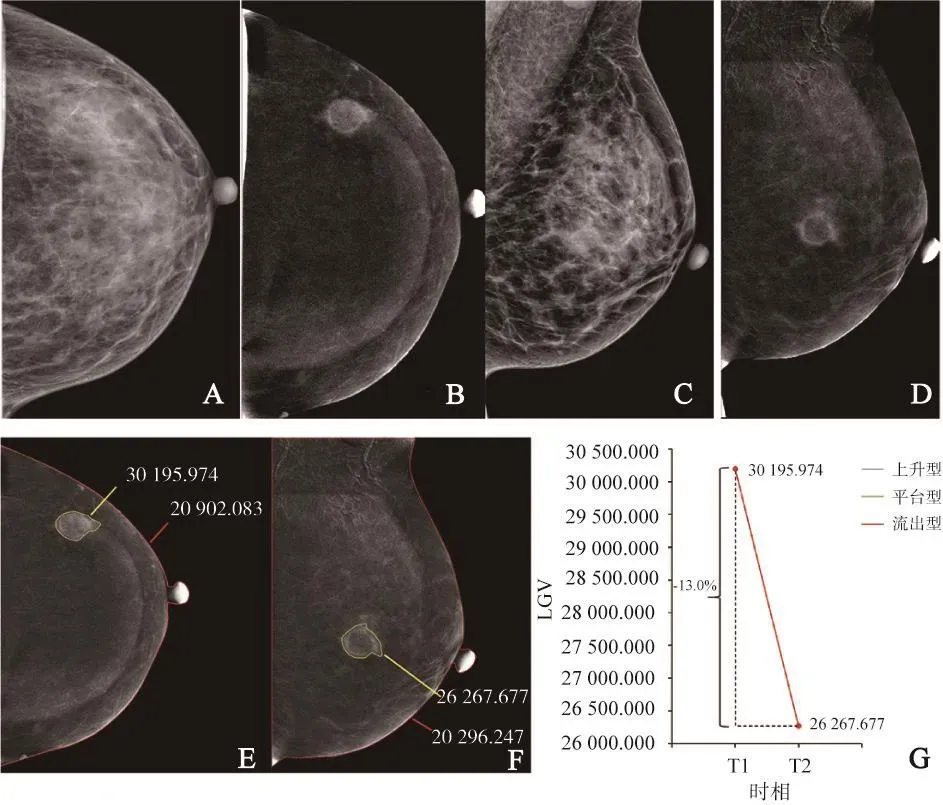
圖4 典型病例2(患者,女性,48歲,乳腺浸潤性導管癌2級,非特殊類型)的CESM形態學及量化值圖像
2.2 乳腺單發腫塊CESM低能圖及減影圖形態特點
由表2可見,乳腺單發腫塊CESM低能圖及減影圖的特點在良惡性病變中的差異均有統計學意義(P<0.05)。乳腺良性腫塊低能圖多表現為單純腫塊(90.5%),等密度(61.9%),圓形/橢圓形(57.1%),邊緣模糊(50.0%);減影圖多表現為圓形/橢圓形(66.7%),邊緣模糊(61.9%),均勻強化(59.5%)。而乳腺惡性腫塊低能圖多表現為單純腫塊(59.35%),高密度(55.9%),不規則形(77.1%),邊緣毛刺(45.8%);減影圖多表現為不規則形(76.3%),邊緣模糊(78.0%),明顯強化(82.2%),不均勻強化(47.5%)。
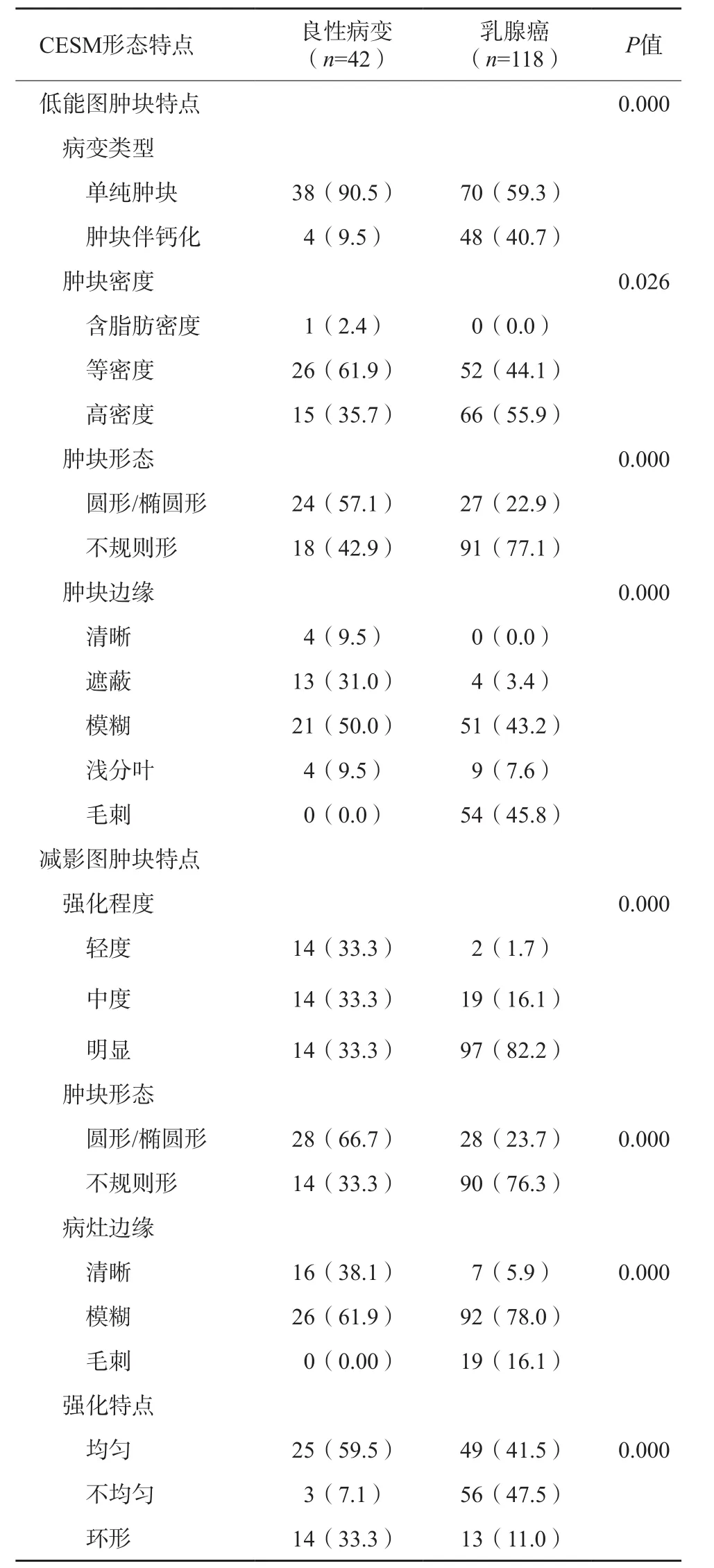
表2 乳腺良惡性腫塊的CESM低能圖及減影圖特點 n(%)
2.3 乳腺單發腫塊CESM減影圖的量化值及動態強化特征
乳腺良惡性腫塊的平均LGV在T1和T2時間點的差異均有統計學意義(P<0.05),其中T1時間點,乳腺良惡性腫塊的平均LGV分別為26 739.0、32 435.7(圖5);T2時間點,乳腺良惡性腫塊的平均LGV分別為27 555.4、30 833.4(圖6)。
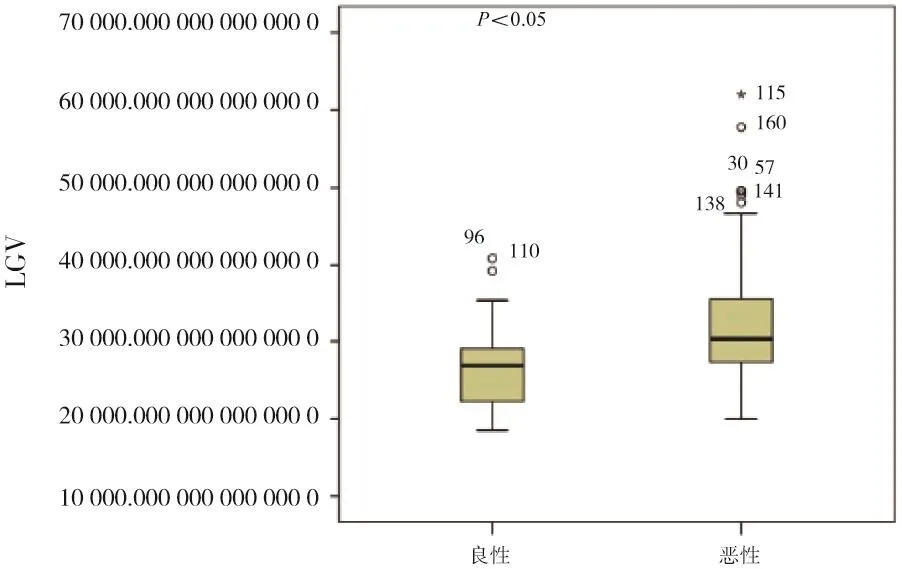
圖5 乳腺良惡性腫塊于T1時間點的LGV
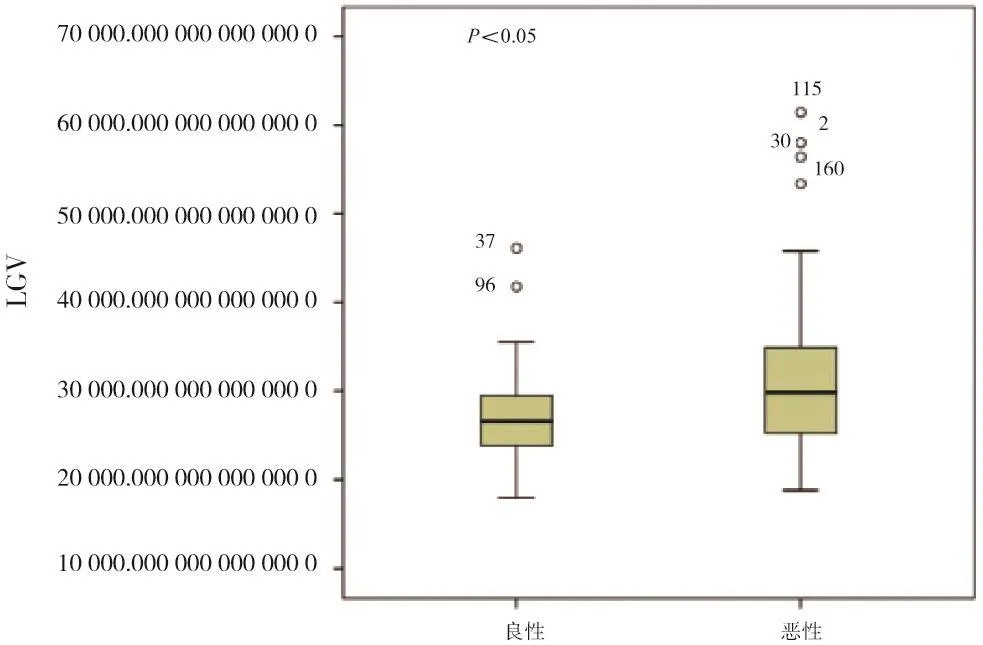
圖6 乳腺良惡性腫塊于T2時間點的LGV
乳腺良惡性腫塊于T1和T2時間點之間的動態強化特征差異有統計學意義(P<0.05)。雖然乳腺良惡性腫塊的強化特征均以平臺型多見(約占50%),但是乳腺良性腫塊上升型強化特征比例高于惡性腫塊(31.0%vs13.6%),乳腺惡性腫塊流出型強化特征比例較良性腫塊高17.4%(36.4%vs19.0%)(圖7)。
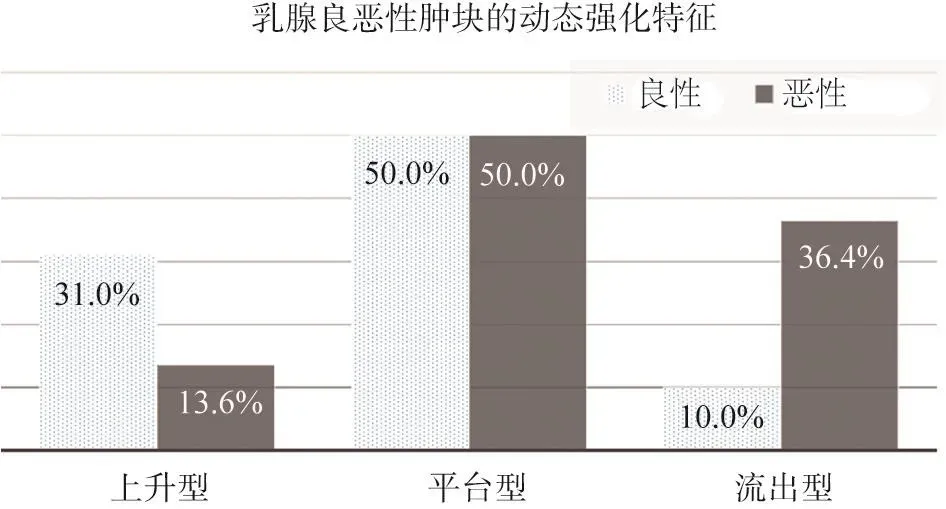
圖7 乳腺良惡性單發腫塊的動態強化特征
2.4 不同方法對乳腺單發腫塊的診斷效能
由表3可見,CESM+LGVT1+LGVT2+動態強化診斷乳腺腫塊的曲線下面積(area under curve,AUC)、靈敏度、陽性預測值、陰性預測值及準確度最高,分別為0.927、96.6%、93.4%、89.4%及92.5%。LGVT1+LGVT2+動態強化診斷乳腺腫塊的效能最低,以陰性預測值為著,僅為48.2%。CESM+LGVT1+LGVT2、CESM、CESM+動態強化這3種方法的靈敏度、陰性預測值及準確度逐漸增高,而AUC、特異度及陽性預測值相近(圖8)。
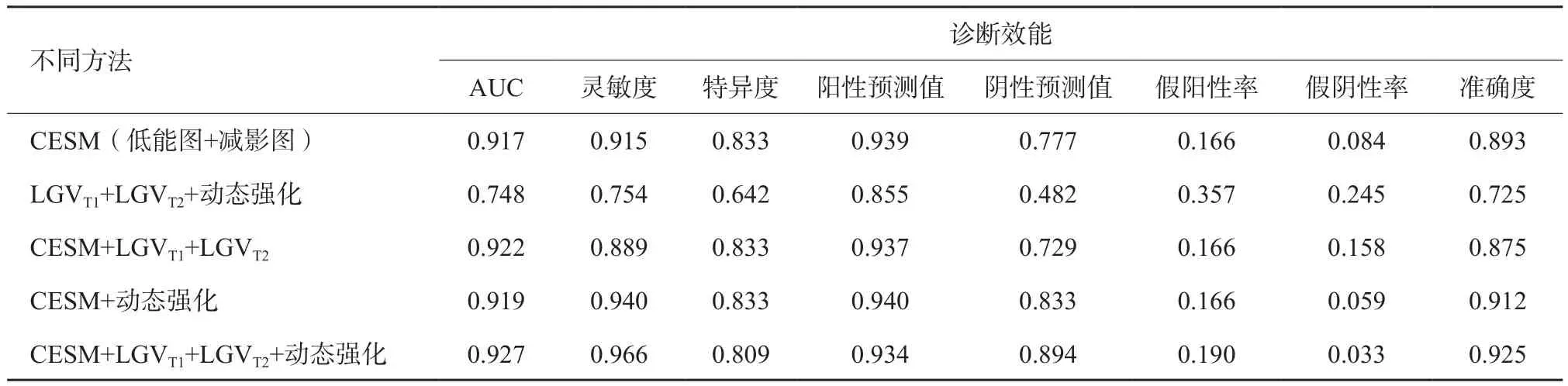
表3 不同方法對乳腺單發腫塊的診斷效能
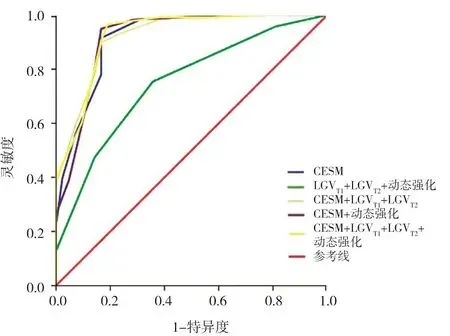
圖8 不同方法對乳腺腫塊的診斷效能比較
由表4可見,對于CESM低能圖表現為邊緣模糊的乳腺腫塊,LGVT1+LGVT2+動態強化、CESM+LGVT1+LGVT2、CESM+動態強化、CESM+LGVT1+LGVT2+動態強化診斷效能逐漸增高。相比于LGVT1+LGVT2+動態強化,CESM+LGVT1+LGVT2+動態強化的靈敏度、特異度、陰性預測值及準確度增高為著,分別增高了19.6%、9.5%、32.4%及16.6%。
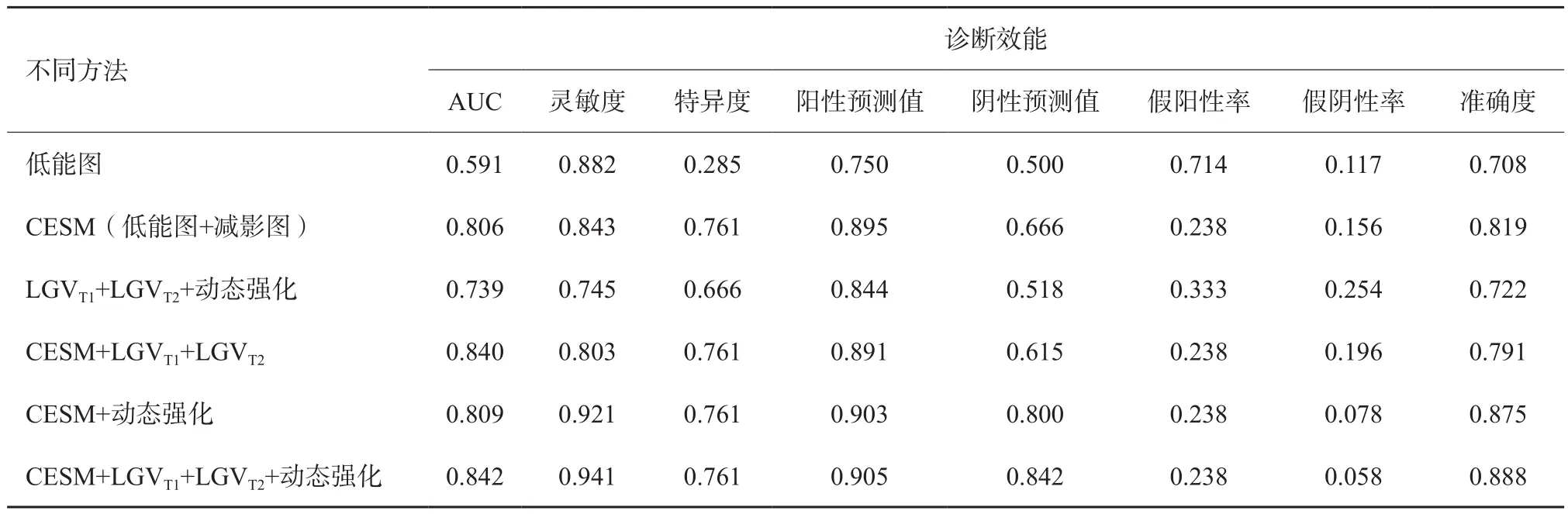
表4 不同方法對CESM低能圖邊緣模糊乳腺單發腫塊的診斷效能
3 討 論
對于BI-RADS 3~5類的乳腺單發腫塊,本研究中低能圖乳腺癌腫塊具有高密度(55.9%)、不規則形(77.1%)、邊緣毛刺(45.8%)的典型表現,而良性腫塊具有等密度(61.9%)及形態規則(57.1%)的特征;惡性腫塊減影圖特征同既往研究[11],主要表現為明顯強化、不均勻強化、邊緣模糊或毛刺的腫塊樣強化。本研究發現聯合CESM的低能圖及減影圖的形態特征能較好地鑒別乳腺腫塊的良惡性,其靈敏度、特異度、準確度分別為91.5%、83.3%及89.3%;聯合CESM低能圖及減影圖的總診斷效能高于劉迎春等[12]基于常規乳腺X線攝影BI-RADS分類鑒別乳腺良惡性腫塊的研究,其鑒別乳腺良惡性腫塊的AUC、靈敏度和特異度分別為0.82、71.11%和83.05%。雖然本組中低能圖仍有部分的良惡性腫塊(72/160,45.0%)均表現為等密度、邊緣模糊腫塊,但聯合減影圖可使診斷特異度提高47.6%。而本研究CESM總的效能低于姜婷婷等[13]的研究,其CESM診斷乳腺良惡性病灶的靈敏度、特異度和準確度分別達95.80%、91.18%和94.77%;分析原因可能是因為本研究僅納入了BI-RADS 3~5類的乳腺單發腫塊。
本研究乳腺良性腫塊強化程度多樣,邊緣模糊,與既往研究[14-15]不同,特別是邊緣模糊/形態不規則的炎癥腫塊(圖3)與乳腺癌腫塊(圖4)鑒別困難。為了降低主觀因素影響,更好地鑒別表現相似乳腺良惡性腫塊,我們進一步提出了強化腫塊的量化研究。本組中良惡性腫塊的平均LGV及動態強化特征差異有統計學意義,惡性腫塊早期和晚期的平均LGV均高于良性腫塊,這與筆者前期的研究[9]相似。本研究發現良惡性腫塊的動態強化特征均主要表現為平臺型(均約50%),但良性腫塊具有上升型強化特征(31.0%)的趨勢,惡性腫塊具有流出型強化特征(36.4%)的趨勢,這與筆者前期的研究[9]相似。本研究良惡性腫塊的動態強化特征結果類似Huang等[16]研究,而不同于Deng[8]等的研究。Huang[16]等研究發現,在2~4 min內,71%乳腺癌和80%良性病變最常見的對比增強乳腺X線攝影的動力強化模式是平臺型;在2~10 min內,51%乳腺癌表現為流出型,而67%良性病變表現為平臺型。Deng等[8]的研究根據乳腺惡性病變流出型動態強化特征(66/98,67.3%)及良性病變上升型動態強化特征(7/12,58.3%)能在一定程度上鑒別病變良惡性。兩者的差異可能性是因為本研究僅納入了單發腫塊型病變及攝影時間不同。然而單純依靠強化腫塊的LGVT1+LGVT2+動態強化特征診斷,診斷效能欠佳,其靈敏度僅為75.4%,而特異度更低,僅為64.2%,這是因為單純的量化分析沒有考慮腫塊內部的強化特征及腫塊強化邊緣的細節改變,且良惡性腫塊的典型動態強化特征不顯著。
綜合強化腫塊的形態學聯合量化特征鑒別乳腺腫塊良惡性,本研究發現CESE+LGVT1+LGVT2、CESM+動態強化、CESM+LGVT1+LGVT2+動態強化診斷效能逐漸增高,以CESM+LGVT1+LGVT2+動態強化診斷效能最佳,尤其是其陰性預測值較單獨CESM增高了11.7%,比單純量化分析(LGVT1+LGVT2+動態強化)增高了41.2%,這很大程度降低了乳腺良性腫塊的活檢率。CESM+LGVT1+LGVT2+動態強化能避免良性腫塊不必要的活檢,可能的原因是乳腺腫塊低能圖形態、邊緣特征和強化腫塊的形態及強化程度鑒別良惡性更有代表性。我們的研究結果與Kamal等[17]研究相似,強化腫塊形態不規則、邊緣模糊/毛刺及內部不均勻強化高度提示惡性病變,其中腫塊形態不規則預測惡性病變的陽性預測值為92.4%。此外,我們分析每個時間點腫塊強化程度的LGV在一定程度上減少了主觀強化程度的影響,同時綜合兩個時間點的強化程度變化趨勢,能由內及外更全面地剖析良惡性腫塊的差異。
本研究的不足之處:① 患者數相對偏少,且僅納入了BI-RADS 3~5類的乳腺單發腫塊。② 強化腫塊的LGV測量時沒有考慮腫塊內部強化特征。③ 缺乏乳腺動態增強MRI的對比。④ 沒有對腫塊的具體病理學類型進行分組。
綜上所述,對于BI-RADS 3~5類的乳腺單發腫塊,綜合考慮腫塊的CESM低能圖、減影圖、每個時間點的LGV及動態強化特征,能降低乳腺良性腫塊活檢率,提高惡性腫塊的檢出率,CESM量化特征聯合形態學鑒別良惡性腫塊具有較大的臨床應用前景。

