適用于微創(chuàng)消融治療研究的小鼠胰腺癌原位模型建立方法及比較
毛璐婧, 張娜娜, 劉 昊, 史愛華, 朱子語, 呂 毅,5
(1.西安交通大學(xué)第一附屬醫(yī)院Med-X研究院再生與重建醫(yī)學(xué)研究所,西安 712000; 2.西安交通大學(xué)第一附屬醫(yī)院精準(zhǔn)外科與再生醫(yī)學(xué)國家地方聯(lián)合工程研究中心,西安 710061; 3.西安交通大學(xué)第一附屬醫(yī)院陜西省再生醫(yī)學(xué)與外科工程研究中心,西安 710061; 4.西安交通大學(xué)醫(yī)學(xué)部,西安 710061; 5.西安交通大學(xué)第一附屬醫(yī)院肝膽外科,西安 710061)
胰腺癌因惡性程度高,患者生存期短,被稱為“癌癥之王”。全球最新癌癥數(shù)據(jù)統(tǒng)計(jì)分析顯示,胰腺癌發(fā)病率占惡性腫瘤的2.6%,而死亡率高達(dá)4.7%[1],且絕大部分患者在診斷為胰腺癌后半年內(nèi)死亡,5年生存率約為10%[2]。胰腺癌因具有高度纖維化的腫瘤間質(zhì),放化療、分子靶向藥物和免疫療法均對其治療效果欠佳[3]。近年來,隨著CT、超聲等影像技術(shù)的進(jìn)步,局部選擇性破壞腫瘤組織的物理消融療法為胰腺癌患者帶來了良好的治療前景[4]。研究表明,微創(chuàng)消融療法可顯著延長進(jìn)展期胰腺癌患者的總生存期[5]。而各種物理消融方法在用于胰腺癌治療的過程中仍存有一些問題,如熱消融引起的熱沉效應(yīng),消融效果不徹底,以及如何聯(lián)合其他治療方案等,均需要進(jìn)一步的實(shí)驗(yàn)探究。
建立小鼠胰腺癌移植瘤模型是胰腺癌研究的重要基礎(chǔ)。目前主要的造模方法有皮下移植瘤模型及原位移植瘤模型等。皮下移植瘤生長時(shí)易被纖維包繞,腫瘤血管生成易受干擾,不能很好地模擬人胰腺癌真實(shí)情況,有一定的局限性[6]。而原位胰腺癌模型是胰腺癌研究中較為理想的一種,為探究胰腺癌原位消融治療方案等提供了合理的動(dòng)物模型。因物理消融是腫瘤局部消融,對原位胰腺癌模型的要求較高,如腫瘤模型同質(zhì)性差(腫瘤體積差異大)、腹腔臟器粘連嚴(yán)重、腹腔轉(zhuǎn)移等均會(huì)影響腫瘤消融效果。目前,關(guān)于小鼠原位胰腺癌模型建立的研究報(bào)告較少。因此,如何高效準(zhǔn)確地建立具有較高同質(zhì)性的小鼠原位胰腺癌模型對于探究胰腺癌治療方案具有重要意義。本研究對比分析了應(yīng)用腫瘤細(xì)胞原位注射法以及腫瘤組織塊移植法建立小鼠原位胰腺癌模型的優(yōu)缺點(diǎn),并總結(jié)建模過程中遇到的相關(guān)問題和解決方案,以期為小鼠胰腺癌原位模型的建立提供技術(shù)參考。
1 材料與方法
1.1 細(xì)胞及其培養(yǎng)
小鼠胰腺癌細(xì)胞系Panc02 購自河北北納生物科技有限公司,用含10%胎牛血清、100 μg/mL青鏈霉素的DMEM培養(yǎng)液,置于37 ℃含5%CO2的細(xì)胞培養(yǎng)箱中培養(yǎng),每2 d換液1次。細(xì)胞單層貼壁生長,約80%融合時(shí)使用胰蛋白酶消化傳代。
1.2 實(shí)驗(yàn)試劑及其配制
DMEM 高糖培養(yǎng)液、胎牛血清購自以色列Biological Industries 公司;體積分?jǐn)?shù)為0.25%的胰蛋白酶、青鏈霉素購自上海碧云天生物技術(shù)有限公司;Matrigel 基質(zhì)膠購自美國BD 公司;兔抗Ki67 一抗購自武漢愛博泰克生物科技有限公司;鼠抗α 平滑肌肌動(dòng)蛋白(α-smooth muscle actin,α-SMA)一抗購自武漢博士德生物工程有限公司;辣根過氧化物酶標(biāo)記的羊抗鼠和羊抗兔二抗購自北京蘭杰柯科技有限公司(Biosharp 品牌)。DAB 顯色試劑盒(20×) 和改良Harris蘇木精染色液購自北京索萊寶科技有限公司。
水凝膠為本實(shí)驗(yàn)室制備的雙網(wǎng)絡(luò)強(qiáng)韌水凝膠,由丙烯酰胺單體(3.6 g)、海藻酸鈉(0.6 g)和去離子水(30 g)按照原料配比6∶1∶50制備所得。殼聚糖溶液的制備:首先將0.976 g 嗎啉乙磺酸加入50 g 去離子水中,并通過逐滴加入質(zhì)量比為1∶10的NaOH溶液調(diào)節(jié)pH值約為4.5,然后加入1 g殼聚糖并攪拌至完全溶解。粘接腫瘤組織前,將12 g/L 1-乙基-3-(3-二甲基氨丙基)-碳化二亞胺(EDC)和12 g/L的N-羥基硫代琥珀酰亞胺(Sulfo-NHS)加入之前配制好的殼聚糖溶液中,作為膠水用來粘接腫瘤組織與水凝膠。待粘接組織和強(qiáng)韌水凝膠中的羧基與殼聚糖鏈中帶正電的氨基反應(yīng)生成酰胺鍵,同時(shí)分子鏈之間還存在著氫鍵和靜電相互作用,從而形成牢固粘接。該水凝膠已被證實(shí)具有良好的生物安全性,在起到物理粘接作用的同時(shí)還可以減輕炎性反應(yīng)[7]。殼聚糖則能有效防止腫瘤組織與周圍組織粘連的發(fā)生,促進(jìn)創(chuàng)面的修復(fù)與愈合[8]。
1.3 實(shí)驗(yàn)動(dòng)物
SPF 級C57BL/6 小鼠20 只,雄性,6~8 周齡,體質(zhì)量為(20±3)g,由西安交通大學(xué)醫(yī)學(xué)部實(shí)驗(yàn)動(dòng)物中心[SCXK(陜)2018-001]提供,質(zhì)量合格證號為1439。實(shí)驗(yàn)小鼠在西安交通大學(xué)醫(yī)學(xué)部實(shí)驗(yàn)動(dòng)物中心[SYXK(陜)2020-005]屏障環(huán)境中飼養(yǎng)管理,環(huán)境溫度維持在(25±2)℃,相對濕度控制在50%~80%,光照時(shí)間12 h,動(dòng)物可自由進(jìn)食、飲水。動(dòng)物飼養(yǎng)、管理和實(shí)驗(yàn)操作嚴(yán)格按照國家和學(xué)校有關(guān)實(shí)驗(yàn)動(dòng)物管理方面的規(guī)定進(jìn)行,實(shí)驗(yàn)方案經(jīng)西安交通大學(xué)動(dòng)物倫理委員會(huì)批準(zhǔn)[2018倫審科字第G-196號]。
1.4 小鼠原位胰腺癌模型建立
1.4.1 細(xì)胞懸液直接注射法
該方法定義為實(shí)驗(yàn)A組,隨機(jī)取5只小鼠。將培養(yǎng)好的小鼠胰腺癌Panc02細(xì)胞系消化并吹打,制備成單細(xì)胞懸液,PBS 洗滌1 次,生理鹽水(即0.9%NaCl 溶液)洗滌2 次,細(xì)胞計(jì)數(shù)板計(jì)數(shù),生理鹽水稀釋細(xì)胞至1×107/100 μL。用異氟烷麻醉小鼠后,在小鼠左側(cè)肋下部位用脫毛膏脫毛,消毒腹部備皮,逐層打開小鼠腹腔,首先尋找脾臟位置,在胃與脾臟之間連接緊密的類似脂肪組織的部分即為小鼠胰腺。用無菌胰島素注射器將制備好的細(xì)胞懸液20 μL/只(2×106個(gè)/只)接種于小鼠胰腺原位,棉簽輕按注射部位約30 s 后,將小鼠腹部器官歸位,逐層縫合腹部。每隔2 d觀察小鼠腫瘤生長情況,記錄小鼠體質(zhì)量。
1.4.2 含基質(zhì)膠的細(xì)胞懸液注射法
該方法定義為實(shí)驗(yàn)B組,隨機(jī)取5只小鼠。采用含50%Matrigel基質(zhì)膠的生理鹽水混懸小鼠胰腺癌Panc02細(xì)胞,采用與1.4.1節(jié)中同樣的方法進(jìn)行接種及觀察。
1.4.3 腫瘤組織塊移植法
該方法定義為實(shí)驗(yàn)C組,隨機(jī)取5只小鼠。根據(jù)預(yù)實(shí)驗(yàn)的結(jié)果可知,按1.4.1節(jié)腫瘤細(xì)胞懸液直接注射到小鼠胰腺原位后第10天時(shí),即可在小鼠左上腹部(即胰腺在體表的投影部位)觸及質(zhì)硬的包塊;于第14天時(shí)開腹剝離腫瘤的長徑約5~7 mm,第21 天時(shí)腫瘤長徑約7~10 mm,此時(shí)腫瘤組織活力好,內(nèi)部無壞死,因此取接種后第21天的腫瘤組織作為腫瘤組織塊移植建立胰腺癌模型的“瘤組織源”。將采用細(xì)胞懸液直接注射法形成的任意一只荷瘤小鼠脫頸處死,浸泡在75%乙醇溶液中約20 min,逐層打開小鼠腹腔將小鼠胰腺及腫瘤組織均取出,將腫瘤組織剝離,用組織剪剪成1 mm3的腫瘤組織塊,無菌PBS沖洗2次,放在DMEM 培養(yǎng)液中待用。異氟烷麻醉新的待接種小鼠后取右臥位,用組織剪在小鼠左側(cè)肋下做一切口,找到脾臟后順著脾門找到胰腺,將胰腺充分暴露并攤平,使用7-0 可吸收縫線將1 mm3腫瘤小塊縫入胰腺組織上,將小鼠腹部器官歸位,逐層縫合腹部。每隔2 d觀察小鼠腫瘤生長情況,記錄小鼠體質(zhì)量。
1.4.4 腫瘤組織塊水凝膠粘接法
該方法定義為實(shí)驗(yàn)D 組,隨機(jī)取5 只小鼠。同1.4.3 節(jié)方法,用手術(shù)剪將由細(xì)胞懸液直接注射法獲得的小鼠腫瘤組織剪成1 mm3的腫瘤組織塊待用。接種時(shí),剪開胰腺包膜約1 mm,將水凝膠浸入殼聚糖溶液中,將腫瘤組織塊置于水凝膠上,將負(fù)載腫瘤組織塊的水凝膠粘附于胰腺組織上,按壓約60 s。將小鼠腹部器官歸位,逐層縫合腹部。每隔2 d觀察小鼠腫瘤生長情況,記錄小鼠體質(zhì)量。
1.5 觀察指標(biāo)及方法
1.5.1 手術(shù)時(shí)長及術(shù)后小鼠一般情況
計(jì)算從開腹手術(shù)開始計(jì)時(shí)至完全完成關(guān)腹的時(shí)間,即手術(shù)時(shí)長。然后在建模后前2 d,每天觀察小鼠的飲水、進(jìn)食及活動(dòng)情況;之后每2 d觀察一次,并稱量小鼠體質(zhì)量。
1.5.2 腫瘤生長和大小測定
于接種后腫瘤生長16 d 時(shí),脫頸處死小鼠,觀察成瘤情況。從各組小鼠胰腺組織中均可找到肉眼可辨認(rèn)的腫瘤組織,其質(zhì)韌,呈灰白色,凸出于胰腺組織生長。統(tǒng)計(jì)各組小鼠的成瘤率。然后剝離移植瘤,用游標(biāo)卡尺測量并記錄腫瘤最長徑(a)和最短徑(b)。腫瘤大小以腫瘤體積(V/mm3)表示,按公式V=a×b2/2計(jì)算。
1.5.3 腹腔臟器粘連程度的分級判定
在文獻(xiàn)[9]的基礎(chǔ)上改進(jìn),設(shè)立等級分級法。0級:完全無粘連。Ⅰ級:胰腺腫瘤組織與內(nèi)臟組織有點(diǎn)狀或膜狀粘連,或腫瘤組織與腹壁或內(nèi)臟之間有一條粘連帶,分離鉗容易分離且無出血。Ⅱ級:胰腺腫瘤組織與內(nèi)臟或腹壁間有兩條粘連帶,可分離且出血少,內(nèi)臟器官無損傷。Ⅲ級:胰腺腫瘤組織與內(nèi)臟或腹壁間有多于兩條的粘連帶,分離困難且出血多,內(nèi)臟器官外膜及包膜層可出現(xiàn)損傷。Ⅳ級:胰腺腫瘤組織與其他內(nèi)臟器官糾集成團(tuán),與腹壁粘連緊密,分離很困難,強(qiáng)行分離可致內(nèi)臟器官撕裂。0~Ⅱ級為輕度粘連;Ⅱ~Ⅳ級為重度粘連。
1.5.4 腫瘤轉(zhuǎn)移情況判斷
將各組小鼠中除胰腺外的其他臟器(肝、腸、胃、腎與脾)均分離取出,仔細(xì)觀察有無轉(zhuǎn)移灶的形成。
1.5.5 HE染色法觀察腫瘤組織形態(tài)學(xué)變化
將取出的腫瘤組織經(jīng)脫水、包埋、切片后進(jìn)行HE染色,然后光學(xué)顯微鏡下觀察腫瘤組織病理學(xué)形態(tài)特點(diǎn)。具體染色方法參見改良Harris 蘇木精染色液說明書,顯微鏡觀察的放大倍數(shù)為400倍。
1.5.6 免疫組織化學(xué)法檢測Ki67和α-SMA表達(dá)
將取出的腫瘤組織經(jīng)常規(guī)脫水、包埋、切片后,采用免疫組織化學(xué)法檢測Ki67表達(dá)水平,以此評估腫瘤細(xì)胞的增殖情況;檢測α-SMA表達(dá)水平,以此了解腫瘤間質(zhì)中腫瘤相關(guān)成纖維細(xì)胞所占比例。具體按照免疫組化SP 三步法[10]進(jìn)行檢測;一抗的工作液體積稀釋比例為1∶150,4 ℃孵育過夜;二抗的工作液體積稀釋比例為1∶150,37 ℃孵育30 min;DAB顯色15 min。選擇10 個(gè)高倍視野進(jìn)行半定量結(jié)果判定。細(xì)胞不著色記0分,染淡黃色記1分,棕黃色記2分,棕褐色記3 分。采用Image J 軟件評估著色細(xì)胞百分率,并據(jù)此判定蛋白表達(dá)結(jié)果:≤5%為陰性,記0分;5%~25%為弱陽性,記1 分;26%~50%為中等陽性,記2 分;51%~75%為陽性,記3 分;≥75%為強(qiáng)陽性,記4分。
1.6 統(tǒng)計(jì)學(xué)分析
采用SPSS 22.0 軟件對所有實(shí)驗(yàn)數(shù)據(jù)進(jìn)行統(tǒng)計(jì)分析。計(jì)量結(jié)果用-x±s顯示,計(jì)數(shù)結(jié)果用n(%)表示。率的比較采用卡方檢驗(yàn)。多組間均數(shù)比較采用方差分析,組內(nèi)兩兩比較采用LSD-t檢驗(yàn)。以P<0.05(雙側(cè)檢驗(yàn))認(rèn)為差異具有統(tǒng)計(jì)學(xué)意義。
2 結(jié)果
2.1 原位胰腺癌模型小鼠的手術(shù)時(shí)長和一般情況
4種手術(shù)方法的手術(shù)時(shí)長記錄為表1,其中腫瘤組織塊水凝膠粘接法的手術(shù)時(shí)間最短(P=0.009)。在建模手術(shù)后第2 天直至第16 天,4 組20 只小鼠均可正常飲水、進(jìn)食,活動(dòng)力良好,而且各組小鼠的體質(zhì)量呈現(xiàn)逐漸增加的趨勢(圖1A)。
2.2 小鼠成瘤率、腫瘤大小
用細(xì)胞懸液直接注射(A 組)或含基質(zhì)膠的細(xì)胞懸液注射(B 組)后小鼠原位胰腺癌成瘤率分別為60%與80%,而用腫瘤組織塊移植(C組)及腫瘤組織塊水凝膠粘接移植(D 組)后小鼠原位胰腺癌成瘤率均為100%(表1)。各組小鼠的剝離腫瘤見圖1B,可見A 組小鼠腫瘤體積大小不一,均質(zhì)性差;B、C 與D組小鼠腫瘤體積大小接近,均質(zhì)性較好。另外,A、B組小鼠腫瘤組織因與周圍組織粘連嚴(yán)重,腫瘤組織表面粗糙;C、D組腫瘤組織表面較光滑。而且D組的腫瘤組織體積較大(P=0.001),剖開腫瘤切面,可見水凝膠未完全降解(圖1C)。4 組小鼠的腫瘤平均體積見表1。

表1 4組小鼠胰腺原位癌成瘤率比較Table 1 Comparison of tumor formation rate of pancreatic carcinoma in situ among the four groups of mice

圖1 各組胰腺癌原位模型小鼠的生長情況及剝離腫瘤情況Figure 1 Growth and tumor dissection of pancreatic cancer orthotopic model mice in each group
2.3 小鼠腹腔臟器粘連程度和腫瘤轉(zhuǎn)移情況
各組小鼠腹腔粘連程度統(tǒng)計(jì)見表2。A組小鼠腹腔重度粘連率為100%,B組小鼠腹腔重度粘連率為80%,C 組與D 組均未出現(xiàn)重度腹腔粘連。各組小鼠腫瘤腹腔轉(zhuǎn)移情況見表3。A 組小鼠轉(zhuǎn)移率最高為100%,其中2例為腸系膜轉(zhuǎn)移(圖1D),2例為肝轉(zhuǎn)移(圖1E),1例為胃轉(zhuǎn)移;B組小鼠轉(zhuǎn)移率為60%,2例為肝轉(zhuǎn)移,1例為腸系膜轉(zhuǎn)移;C、D組小鼠未發(fā)現(xiàn)轉(zhuǎn)移瘤。

表2 各組小鼠腫瘤腹腔粘連等級比較Table 2 Comparison of abdominal adhesion grade among the four groups[n(%)]
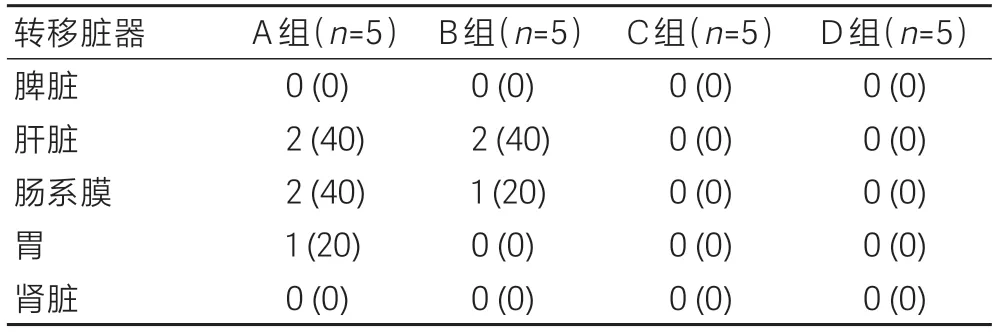
表3 各組小鼠腹腔轉(zhuǎn)移情況比較Table 3 Comparison of intraperitoneal metastasis among the four groups[n(%)]
2.4 腫瘤組織形態(tài)學(xué)特點(diǎn)
HE 染色(圖2A)顯示4 組小鼠原位胰腺癌的病理組織形態(tài)學(xué)特點(diǎn),發(fā)現(xiàn)移植瘤在組織學(xué)上無顯著差異。腫瘤細(xì)胞均呈現(xiàn)低分化,細(xì)胞核不規(guī)則且缺乏極性,核仁多呈分葉狀,腫瘤細(xì)胞對周圍正常胰腺組織有顯著的侵襲性,腫瘤間質(zhì)具有大量腫瘤相關(guān)成纖維細(xì)胞。
免疫組織化學(xué)染色(圖2A)顯示,Ki67與α-SMA在4 組小鼠腫瘤組織中均呈現(xiàn)陽性表達(dá),提示胰腺癌細(xì)胞增殖活躍、腫瘤間質(zhì)高度纖維化、侵襲性強(qiáng)等生物學(xué)特點(diǎn)。圖2B統(tǒng)計(jì)顯示Ki67和α-SMA在4組小鼠腫瘤組織中的相對表達(dá)水平無明顯差異(PKi67=0.619,Pα-SMA=0.946),表明上述4種原位胰腺癌建模法所形成的腫瘤組織均具有胰腺癌生物學(xué)特性。
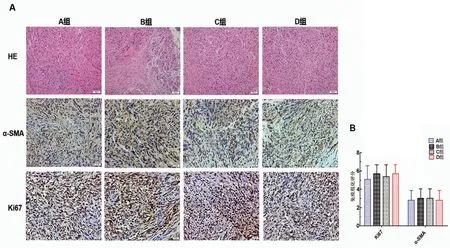
圖2 HE染色法和免疫組織化學(xué)法(DAB染色)分別檢測各組小鼠原位胰腺癌形態(tài)組織特點(diǎn)及Ki67和α-SMA表達(dá)情況Figure 2 Tumor histomorphology and the expressions of Ki67 and α-SMA proteins were detected by HE staining and immunohistochemistry,resp(DAB staining)
此外,C與D組腫瘤組織中可吸收縫合線及水凝膠均未被完全降解,在水凝膠局部有輕度的炎性反應(yīng)。
3 討論
局部物理消融對胰腺癌的治療具有很好的應(yīng)用前景,但由于消融后腫瘤復(fù)發(fā)率偏高,限制了其在臨床腫瘤治療領(lǐng)域的廣泛應(yīng)用[11-12]。腫瘤原位消融對胰腺癌模型的要求較高,因其為局部消融,腫瘤應(yīng)具有良好的均質(zhì)性;此外,模型建立過程中所致的種植性轉(zhuǎn)移可顯著影響預(yù)后。小鼠原位胰腺癌模型能夠?yàn)樘骄恳认侔┫谥委熜Ч约捌渌委煼桨柑峁┖芎玫难芯炕A(chǔ)。Tan 等[13]首先將人胰腺癌細(xì)胞株AsPC-1 注射于裸鼠胰腺十二指腸葉,以此建立胰腺癌細(xì)胞懸液的裸鼠原位種植模型。Liu等[14]將人胰腺癌手術(shù)標(biāo)本剪為成小瘤塊,直接種植于BALB/c-nu/nu 裸小鼠的胰腺被膜下。Huynh等[15]利用超聲將胰腺癌細(xì)胞注入主胰管建立模型,避免了種植性轉(zhuǎn)移。Tsuji 等[16]利用熒光蛋白標(biāo)記胰腺癌細(xì)胞并注入小鼠膽總管,成功建立腫瘤模型。前兩種方法是目前建立小鼠胰腺癌原位模型的主要方法,但存在諸多缺陷,如前者易造成人為的種植性轉(zhuǎn)移,后者則操作復(fù)雜、對胰腺損傷較大。
據(jù)此,本研究分別探究了腫瘤細(xì)胞原位注射法和腫瘤組織塊移植法建立小鼠原位胰腺癌模型的優(yōu)缺點(diǎn),并分析了各種方法在建立過程中遇到的相關(guān)問題,提出了解決方案。腫瘤細(xì)胞原位注射法建立模型快速,操作簡單,但由于胰腺包膜極薄,單純的細(xì)胞懸液在注射及回納臟器的過程中,細(xì)胞懸液容易滲出而影響建模效果,導(dǎo)致小鼠胰腺癌成瘤率低且易發(fā)生轉(zhuǎn)移。值得注意的是,此處的腹腔轉(zhuǎn)移并非傳統(tǒng)意義上的腫瘤轉(zhuǎn)移,而是由于腫瘤細(xì)胞懸液直接注射法易致細(xì)胞外滲引起的種植性轉(zhuǎn)移。因此,在A 組小鼠模型中,腹腔轉(zhuǎn)移率可高達(dá)100%,而成瘤率僅為60%;此外,腫瘤大小不均,腫瘤組織與周圍組織粘連嚴(yán)重。高發(fā)的腹腔轉(zhuǎn)移嚴(yán)重影響荷瘤小鼠的生存預(yù)后。腫瘤大小不均導(dǎo)致胰腺癌消融治療效果存在顯著差異。腫瘤組織與周圍組織粘連嚴(yán)重,導(dǎo)致消融損傷正常組織,引起荷瘤小鼠的預(yù)后差異,影響胰腺癌消融治療效果的可靠性。總之,低成瘤率和高發(fā)的腹腔轉(zhuǎn)移主要是因?yàn)橐认俳M織包膜極薄,且周圍有許多實(shí)質(zhì)性器官和血管,關(guān)腹時(shí)發(fā)生的擠壓導(dǎo)致Panc02細(xì)胞混懸液流入腹腔,容易形成種植性的播散轉(zhuǎn)移。
本研究對單純細(xì)胞懸液注射方法進(jìn)行了改進(jìn),即把基質(zhì)膠加入Panc02 細(xì)胞混懸液后注射入小鼠胰腺,建立原位胰腺癌模型。采用此方法后,胰腺癌成瘤率提升至80%,轉(zhuǎn)移率減少至60%,形成的腫瘤均質(zhì)性較好,但仍與周圍組織粘連嚴(yán)重,重度粘連率高達(dá)80%。由于胰腺位置深、周圍有許多重要器官和大血管等解剖特點(diǎn),手術(shù)后易發(fā)生腹腔內(nèi)組織器官粘連。而常見的熱消融、非熱消融(納米刀)在局部腫瘤消融過程中釋放熱輻射以及高壓脈沖電場,均會(huì)對正常組織器官造成嚴(yán)重?fù)p傷,因此在實(shí)驗(yàn)過程中,常需將負(fù)荷腫瘤組織的胰腺分離遷出腹腔進(jìn)行消融治療。所以,以探究腫瘤原位消融療效為目的建立原位胰腺癌模型時(shí),避免腹腔內(nèi)組織器官粘連就顯得極為重要。
腫瘤組織塊移植法是先建立小鼠胰腺癌原位移植瘤,小鼠成瘤后剝離出腫瘤組織,剪成1 mm3大小的組織塊,然后縫合于胰尾被膜上。本研究中,采用此方法的成瘤率高,且短時(shí)間內(nèi)無轉(zhuǎn)移,腫瘤均質(zhì)性良好,粘連較輕,但仍存在一定程度的粘連,II 級粘連可達(dá)60%。整體而言,腫瘤組織塊移植法是建立小鼠胰腺癌原位模型較好的方案。
生物水凝膠材料是近年來極具潛力的醫(yī)用生物材料,被廣泛應(yīng)用于生物醫(yī)學(xué)領(lǐng)域[17-18]。本研究采用強(qiáng)韌的聚丙烯酰胺-海藻酸鈣雙網(wǎng)絡(luò)水凝膠將腫瘤組織粘接于胰腺上,此方法不需縫合,手術(shù)時(shí)間短,腹腔暴露時(shí)間短,且殼聚糖具有一定的防粘連作用,腹腔粘連顯著減輕。因此,這種建模方法具有成瘤率高、粘連少、無轉(zhuǎn)移及腫瘤大小均一的優(yōu)點(diǎn),是建立原位胰腺癌模型較理想的方案。但是本研究中水凝膠在16 d內(nèi)不能完全降解,導(dǎo)致腫瘤組織局部發(fā)生慢性炎性反應(yīng)。因此,在開展腫瘤微環(huán)境的相關(guān)研究時(shí)應(yīng)慎用該方法,或需嚴(yán)格做好對照。未來研發(fā)具有降解速度快、防粘連、可減輕炎性反應(yīng)的新型生物水凝膠材料有望為高效建立原位胰腺癌模型提供有效輔助。
綜上所述,腫瘤細(xì)胞懸液直接注射法、含基質(zhì)膠的腫瘤細(xì)胞懸液注射法、腫瘤組織塊移植法和腫瘤組織塊水凝膠粘接法建立的小鼠原位胰腺癌在病理組織學(xué)上均無顯著差異,腫瘤細(xì)胞具有相似的生物學(xué)行為,且符合人類胰腺癌的生物學(xué)特性。其中腫瘤組織塊移植法及水凝膠粘接法所形成的移植瘤并未改變腫瘤細(xì)胞的生物學(xué)特性,且其成瘤率高,轉(zhuǎn)移少,粘連程度輕,易于操作和普及,為探究胰腺癌物理消融效果提供了較理想的建模方案,也可廣泛應(yīng)用于胰腺癌其他治療方案的相關(guān)研究。

