皂素與十二烷基硫酸鈉對陽性血培養瓶直接質譜鑒定處理效果的影響
韋國文,黃麗月
廣西河池市人民醫院 (廣西 河池 547000)
血流感染是敗血癥和菌血癥的統稱,是由各種病原微生物(細菌或真菌)及病毒等侵入血液所引起的一類臨床綜合征。據統計,全球每年約發生20萬例血流感染,病死率為20%~50%[1]。有研究報道,血流感染患者抗菌藥物治療每延遲1 h,平均生存率將下降7.6%[2]。近年來,隨著臨床抗菌藥物、免疫抑制劑、抗腫瘤類藥物及各類創傷性診療手段的應用,血流感染的發病率不斷增高,因其致死率高,危害嚴重,準確快速地檢測血流感染越來越受到人們的關注[3-5]。
血培養是通過采集患者血液標本并將其接種到培養瓶中,用以發現、識別引起菌血癥或真菌血癥的病原微生物,是診斷菌血癥或真菌血癥的基本且重要的方法[6-7]。近年來,質譜檢測技術已被成功用于臨床微生物的鑒定中,且其在細菌、酵母菌等鑒定方面均具有良好的應用價值[8-9]。由于其在微生物鑒定領域的優勢極大,眾多研究人員開始著手進行其在血培養病原菌方面的鑒定研究。陽性血培養液的組分復雜,含有多種干擾微生物鑒定的化合物及病原菌生長代謝物[10],直接質譜鑒定整體準確率普遍不高[11],研究人員多采用常規差速離心法以及加入針對血培養液的表面活性劑[如皂素[12]、十二烷基硫酸鈉(sodium dodecyl sulfate,SDS)[13]等]法進行研究。本研究通過分析對比皂素、SDS 這兩種實驗室常用表面活性劑對陽性血培養瓶直接質譜鑒定準確率的影響,并以傳統鑒定方法為參考,期望找到一種快速而準確的直接質譜鑒定血培養目標菌的表面活性劑應用方案,以期為感染性疾病的診斷、治療和預后提供依據。
1 材料與方法
1.1 材料與試劑
材料:模擬臨床血培養陽性菌出現頻次搜集血培養陽性分離菌株共9種56株,菌株詳細信息見表1。
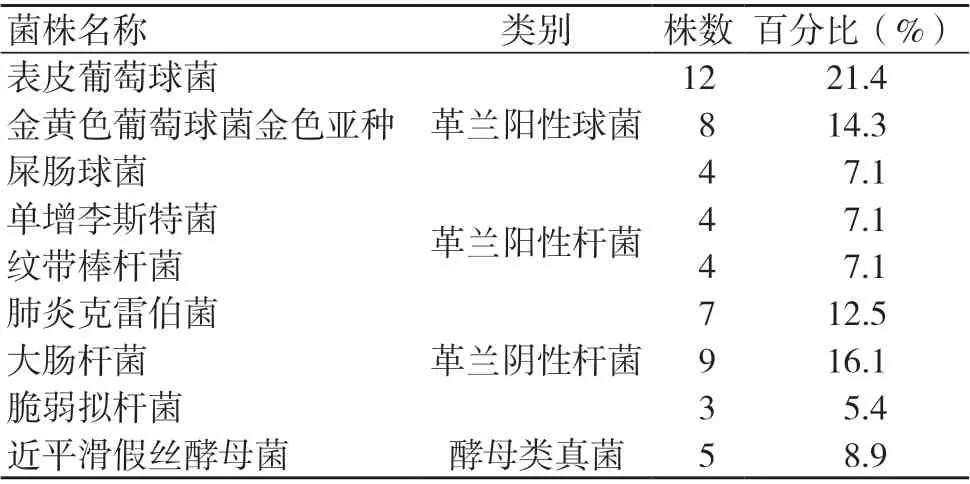
表1 菌株信息
試劑:皂素(上海阿拉丁生化科技股份有限公司),SDS[西格瑪奧德里奇(上海)貿易有限公司],上機血培養瓶(安圖生物工程股份有限公司),質譜樣品處理基質溶液(安圖生物工程股份有限公司),甲酸(上海阿拉丁生化科技股份有限公司),乙腈[西格瑪奧德里奇(上海)貿易有限公司]。
1.2 儀器與設備
BC120自動化血培養系統[安圖實驗儀器(鄭州)有限公司],Autof ms1000全自動微生物質譜檢測系統[安圖實驗儀器(鄭州)有限公司],Sartorius 1-14離心機(Sigma 公司),微量移液器(Eppendorf 公司)。
1.3 方法
1.3.1 模擬血培養瓶方法
培養活化轉接臨床菌株24~72 h,刮取單菌落并使用0.9%氯化鈉注射液制備100 cfu/ml 濃度菌懸液,吸取100 μl 注入血培養瓶,并注入4~5 ml 新鮮羊血,放入全自動血培養儀內,培養至報陽。
1.3.2 傳統鑒定方法
血培養報陽后,根據革蘭染色結果將血培養液轉接至血瓊脂平板或沙保羅培養平板上,37 ℃培養12~48 h,待菌落生長完成挑取1~2個單菌落均勻涂抹靶板,并覆蓋1 μl 基質溶液,采集指紋圖譜并與標準數據庫進行匹配,記錄鑒定結果與得分[14]。
1.3.3 皂素法直接鑒定陽性血培養瓶
使用超純水配制1%、2%、3%、4%、5%濃度梯度皂素溶液,按皂素溶液濃度梯度設置5組驗證,每組分別于1.5 ml 離心管中先加入1 ml 陽性血培養液,然后加入200 μl 不同濃度皂素溶液;充分混勻靜置3~5 min,以500×g 離心10 min,去除上清液,使用1 ml 0.9%氯化鈉注射液重懸沉淀2次,以11 000×g 離心1 min,充分去除上清液并收集沉淀,先加入50 μl 70%甲酸溶液混勻,然后加入50 μl 乙腈混勻,以11 000×g 離心1 min,吸取1 μl 上清液點靶,晾干后覆蓋1 μl 基質溶液行質譜鑒定。
1.3.4 SDS 法直接鑒定陽性血培養瓶
使用超純水配制1%、2%、3%、4%、5%濃度梯度SDS溶液,按SDS溶液濃度梯度設置5組驗證,每組分別于1.5 ml 離心管中先加入1 ml 陽性血培養液,然后加入200 μl 不同濃度SDS 溶液;充分混勻后靜置(10±5)s,以11 000×g 離心2 min,去除上清液,使用1 ml 0.9%氯化鈉注射液重懸沉淀,再次以11 000×g 離心2 min,充分去除上清液,先加入50 μl 70%甲酸溶液混勻,然后加入50 μl 乙腈混勻,以11 000×g 離心1 min,吸取1 μl 上清液點靶,晾干后覆蓋1 μl 基質溶液行質譜鑒定。
2 結果與分析
2.1 皂素法與傳統鑒定方法的鑒定準確率比較
本研究共設置5組實驗組,每組共56份報陽血培養標本,包含57%革蘭陽性菌、34%革蘭陰性菌及9%酵母類真菌,分別行鑒定準確率測定并將其與傳統鑒定方法進行比較,結果見圖1。
由圖1可知,傳統鑒定方法在血培養的質譜鑒定方面有較大的優勢,經過處理的56株模擬陽性血培養瓶成功鑒定52株,準確率達92.9%,鑒定時長13~49 h(從血培養瓶報陽計);皂素溶液的濃度對鑒定準確率有顯著的影響,隨著皂素溶液濃度增加,鑒定準確率增高,到達4%濃度時達到最優的鑒定準確率[82.1%(46/56)],鑒定耗時<1 h(從血培養瓶報陽計),較傳統鑒定方法節省了90%以上的時間,繼續提高皂素溶液濃度,鑒定準確率未出現顯著提升,可能是由于皂素中含有的多種植物成分干擾了質譜峰的鑒定,以金黃色葡萄球菌為例,通過對使用不同濃度皂素溶液進行處理后獲取的質譜峰圖進行對比(圖2),發現對比結果與鑒定成功率結果吻合,經4%皂素溶液處理后的質譜峰圖在基線平穩度、峰強度、峰數量方面均優于其他處理方案,因此,4%皂素溶液為較優的配比方案。
2.2 SDS 法與皂素法及傳統鑒定方法的鑒定準確率比較
采用不同濃度的SDS 溶液對模擬血培養陽性的培養液進行鑒定處理,并將鑒定結果與皂素法及傳統鑒定方法進行比較,結果見圖3。
由圖3可知,低濃度或高濃度的SDS 溶液均不能達到較好的鑒定效果,在3%濃度時的鑒定準確率最高,達76.8%(43/56),但仍顯著低于皂素溶液最高82.1%的鑒定準確率,此外,皂素溶液(4%)及SDS 溶液(3%)的鑒定效果與傳統鑒定方法仍存在一定的差距。3種方法的具體鑒定結果見表2,所選標本可分為革蘭陽性球菌、革蘭陽性桿菌、革蘭陰性桿菌及酵母類真菌,根據平均鑒定準確率可分析3種方法在菌株類型方面鑒定的差異(均值越小,差異越大),由表2可知,3種方法在鑒定酵母類真菌時的差異最大,其次是革蘭陽性桿菌及球菌,革蘭陰性桿菌的差異最小,表明SDS 法、皂素法及傳統鑒定方法均能夠很好地鑒定此類菌。
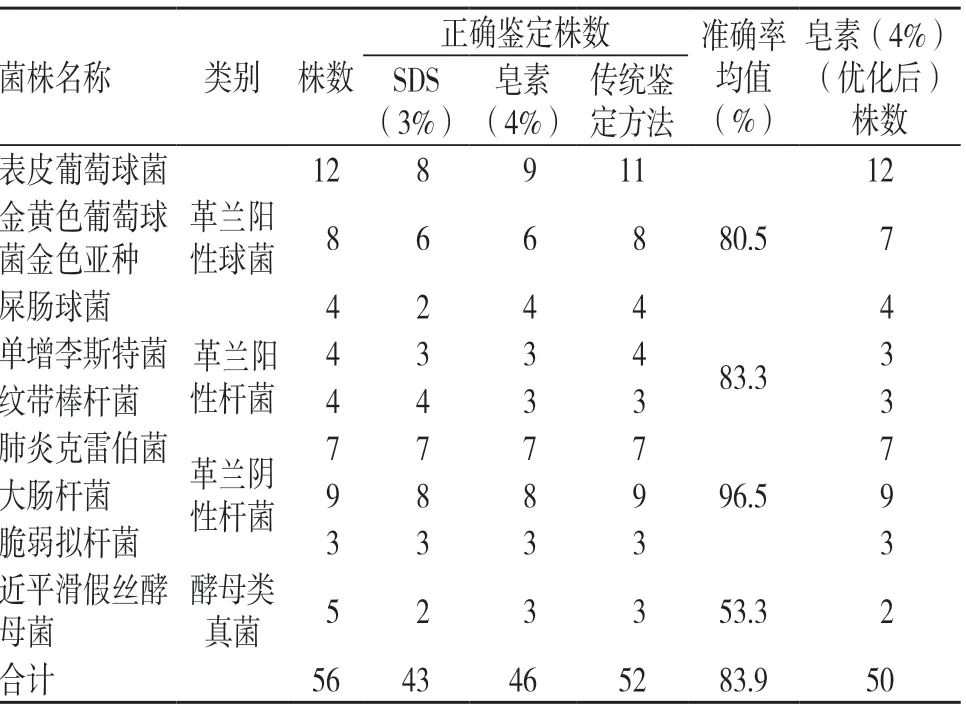
表2 SDS 法與皂素法及傳統鑒定方法的鑒定結果
大量驗證表明,在行陽性血培養瓶直接質譜鑒定時,可將多數鑒定分值為屬水平的鑒定直接確定為種水平,鑒定得分低的原因可能是血培養液中成分比較復雜,鑒定結果受代謝物、雜質等的影響。為進一步提高鑒定準確率,我們對皂素表面活性劑直接用于質譜鑒定的評分規則進行了調整,按照經典評分規則,得分>9.0分為種水平可信,介于6.0~9.0分為屬水平可信,<6.0分為不可信;評分規則優化后,對每個樣品設置4個樣品點,有不少于2個樣品點鑒定結果一致且得分≥6.0分即為可信鑒定,優化后的鑒定準確率達到89.3%(50/56,表2),與傳統鑒定方法的鑒定準確率比較無顯著差異,表明經過評分優化后的4%皂素溶液可用于陽性血培養瓶的直接質譜鑒定,并且可節省90%以上的鑒定耗時。
3 討論
血流感染病原菌確診困難及預后較差等情況一直是困擾臨床醫患的一大難題,傳統鑒定方法在血培養瓶報陽后一般需經過12~48 h 的轉接培養獲得純菌落后方能進一步對病原菌進行分析鑒定[15],而快速而準確地鑒定血流感染病原菌可以極大地降低患者病死率,微生物質譜技術——基質輔助激光解吸飛行時間質譜(matrix-assisted laser desorption / ionization time of flight mass spectrometry,MALDI-TOF MS)在臨床上的應用為這一難題提供了新的思路[16]。
皂素、SDS 是臨床常見可直接用于陽性血培養瓶質譜鑒定前處理的表面活性劑,其作用主要在于裂解血細胞,釋放微生物菌體,便于后續進行質譜鑒定[17]。由于不同科室及實驗室的環境存在差異,使用效果參差不齊,因此,本研究驗證了不同濃度的SDS 溶液及皂素溶液的應用效果并將其與傳統鑒定方法進行了對比評估,發現濃度為3%的SDS溶液對陽性血培養瓶直接進行質譜鑒定可獲得較好的鑒定效果,鑒定準確率達76.8%,但低于4%皂素溶液的鑒定效果82.1%,表明4%皂素溶液相對于SDS 溶液擁有更好的病原菌提純效果。為進一步提高鑒定準確率,對質譜評分規則進行了調整,定義有不少于2個樣品點鑒定結果一致且得分≥6.0分即為可信鑒定,優化后4%皂素溶液的鑒定準確率達到89.3%,與傳統鑒定方法的鑒定準確率92.9%比較無顯著差異,并且整個前處理過程耗時<1 h,節省了90%以上的鑒定耗時,表明經過評分優化后的4%皂素溶液在陽性血培養瓶的直接質譜鑒定處理方面擁有較好的應用前景。

