單操作孔全胸腔鏡下二尖瓣置換的臨床療效觀察
肖宗位,李 源,劉 先,李 陽,程 涵,王曉瑋
(成都市第二人民醫院胸心外科,四川 成都 610017)
需要外科治療的二尖瓣病變既往常采用正中切口,鋸開胸骨,進行二尖瓣置換手術治療,但其切口長,破壞胸廓穩定性,術后切口疼痛重,影響患者身體機能快速康復。近年來隨著胸腔鏡等微創手術設備的科技進步,腔鏡器械在外科已取得廣泛應用,并在多個學科獲得良好的臨床結果[1,2]。但在心臟大血管外科領域,由于心血管外科醫生擔心胸腔鏡手術視野小、暴露受限,影響人工假體植入,延長術中主動脈阻斷時間及體外循環時間,造成患者獲得潛在風險,因此,全胸腔鏡下人工瓣膜假體置換術式開展異常緩慢,但是胸腔鏡設備在心臟外科的微創治療中的應用也是心臟外科醫生和患者追求的目標。成都市第二人民醫院對風濕性二尖瓣病變患者分別采用單操作孔全腔鏡與常規胸骨正中切口開胸術行二尖瓣置換術,比較兩種術式圍術期臨床資料,探討單操作孔全腔鏡行二尖瓣置換的可行性。現報道如下。
1 資料與方法
1.1 一般資料2019年9月至2020年9月成都市第二人民醫院胸心外科收治入院的51例心臟瓣膜病患者。納入標準:心臟彩色多普勒超聲檢查診斷為風濕性二尖瓣病變;患者及家屬知情同意。排除標準:心包炎和胸膜炎病史;體重<30 kg;升主動脈直徑>40 mm;嚴重胸廓畸形;肺功能異常;過度肥胖;腔鏡組中轉開胸。根據手術方式不同分為單操作孔全腔鏡組(腔鏡組)21例和胸骨正中切開常規開胸組(常規組)30例。腔鏡組男8例,女13例;年齡37~74歲[(58.62±10.23)歲];體表面積(BSA)1.34~1.81m2[(1.60±0.12)m2];術前EF值43%~60%[(48.19±5.18)%];左室舒張末期內徑(LVEd)44~62 mm[(50.71±4.67)mm];左室收縮末期內徑(LVEs)29~44 mm[(35.71±3.64)mm]。常規組男10例,女20例;年齡36~75歲[(61.40±9.06)歲];體表面積(BSA)1.38~1.78 m2[(1.58±0.09)m2];術前EF值43%~60%[(50.10±4.05)%];左室舒張末期內徑(LVEd)44~65 mm[(52.20±5.73)mm];左室收縮末期內徑(LVEs)28~41 mm[(36.53±3.79)mm]。兩組患者一般資料比較,差異無統計學意義(P>0.05)。本研究經醫院醫學倫理委員會批準(2020086)。
1.2 方法①腔鏡組:全身靜脈復合麻醉,雙腔氣管插管,體表粘貼除顫電極貼膜,仰臥位,右胸部墊高30°,經股動靜脈建立體外循環,開始體外循環后做右胸沿第4肋間腋前線和腋中線兩個斜切口,斜線長分別為3 cm和1 cm,腋前線切口為操作孔,腋中線切口為腔鏡孔,該孔有腔鏡鏡頭、主動脈阻斷鉗和左心吸引管通過。對于女性患者做沿患者右側乳腺下緣弧形皮膚切口,乳腺往前上方移動后再做右胸第四肋間兩個切口。右膈神經前方2~3 cm縱行切開心包并懸吊,充分暴露右心系統及升主動脈,用長36 cm圣騎士加長主動脈阻斷鉗經腔鏡孔阻斷體循環血流,心臟停跳后經房間溝入路切開左心房,實施人工瓣膜置換術。合并中度以上三尖瓣關閉不全患者經右房行三尖瓣成形術。②常規組:全麻后經胸骨正中切口建立體外循環,阻斷循環心臟停跳后沿右心耳至下腔靜脈方向縱向切開右心房、房間隔,行人工二尖瓣假體置換術。合并中度以上三尖瓣關閉不全患者行三尖瓣成形術。兩組患者在體外循環減循環流量時常規行血液超濾,在體外循環停機即刻和停機后24小時內每6小時測血氣一次,于每次測血氣出現低鈣血癥時靜脈注射葡萄糖酸鈣1g,術后送重癥監護單元(ICU),患者用呼吸機輔助支持呼吸、腎上腺素等藥物維持血壓在合理范圍。
1.3 觀察指標①術中指標:主動脈阻斷時間、體外循環時間、手術時間;②術后指標:機械呼吸時間、ICU停留時間、胸腔液體引流量;③心功能指標:射血分數(EF)、甲狀旁腺素(PTH)、肌鈣蛋白(cTnT)。入院時和術后第24小時用心臟超聲測量左心室EF值,而于入院時(T1)、體外循環停機即刻(T2)、術后第24 h(T3)、術后第48 h(T4)4個時點從患者橈動脈抽取4 ml血液,用化學發光免疫法測PTH水平,同時于入院時(T1)、手術后第6小時(T2)、術后第24 h(T3)、術后第48 h(T4)4個時點抽取靜脈血4 ml用電化學發光免疫法測cTnT的值;④視覺模擬評分(VAS)疼痛評分[3]:術后第1、3、5天指導患者在疼痛評分直尺上標出代表自己疼痛程度的相應分值,每日重復記錄3次VAS評分,取當日最高值;⑤切口長度。
1.4 統計學方法應用SPSS 21.0統計軟件分析數據。計數資料以率(%)表示,組間比較采用卡方檢驗。計量資料組間比較采用獨立樣本t檢驗,組內不同時間點比較采用重復測量方差分析。P<0.05為差異有統計學意義。
2 結果
2.1 兩組術中指標比較腔鏡組體外循環時間和主動脈阻斷時間比常規組長,差異有統計學意義(P<0.05)。兩組手術時間和手術方式比較,差異無統計學意義(P>0.05)。 見表1。
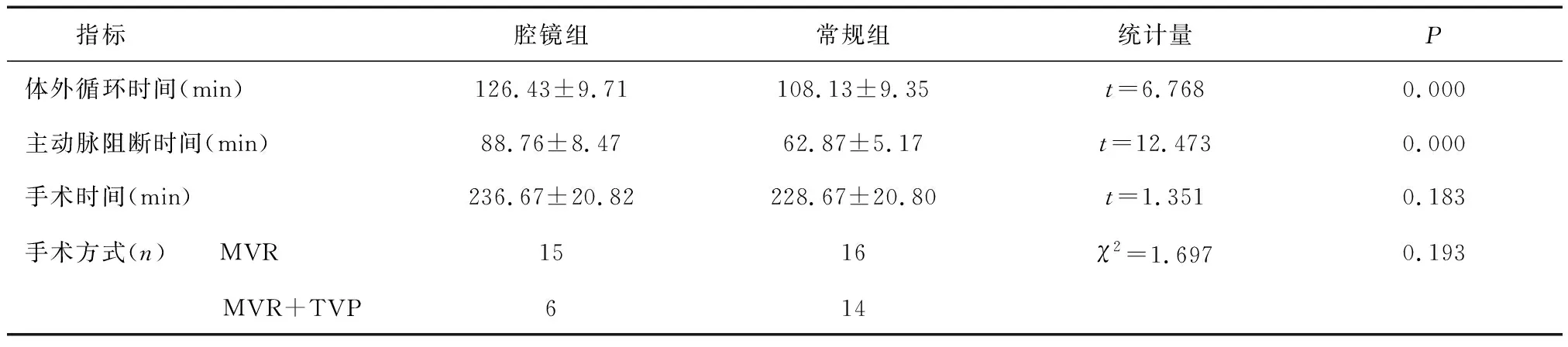
表1 兩組術中指標比較
2.2 兩組術后指標比較與常規組比較,腔鏡組術后胸腔液體總引流量更少,切口長度更短,術后EF值也更低,但呼吸機輔助時間和ICU停留時間更長,差異有統計學意義(P<0.05)。腔鏡組有2例患者出現右肺復張性肺水腫,但無術中轉胸骨正中切口開胸病例。兩組其余患者均無低心排血綜合征、腎功能不全、中樞神經系統障礙、呼吸系統功能不全等嚴重并發癥,也無術后死亡病例。見表2。

表2 兩組術后指標比較
2.3 兩組不同時間點血液PTH比較在T2、T3兩個時點腔鏡組PTH值均高于常規組,差異有統計學意義(P﹤0.05);其余兩個時點比較差異無統計學意義(P>0.05)。見表3。
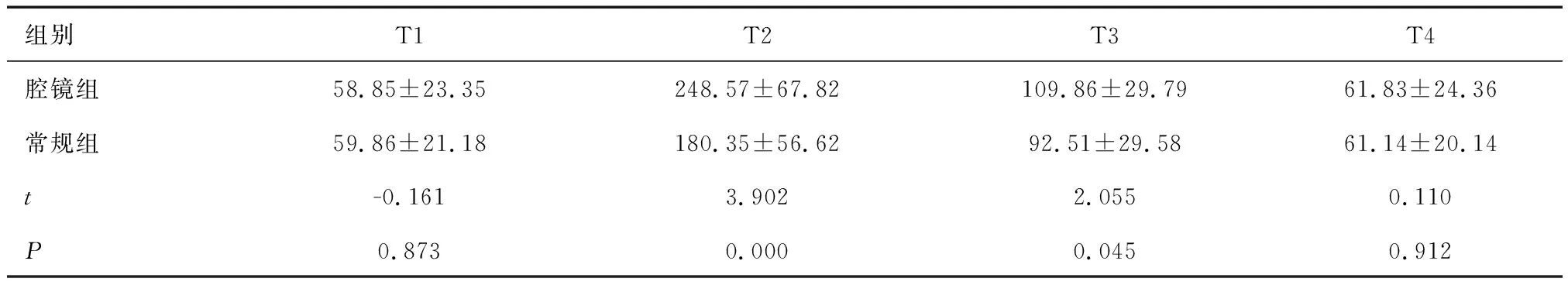
表3 兩組不同時間點血液PTH比較 (pg/ml)
2.4 兩組不同時間點cTnT比較入院時兩組cTnT值比較差異無統計學意義(P>0.05);術后6、24、48 h腔鏡組cTnT均高于常規組,差異有統計學差異(P<0.05)。見表4。
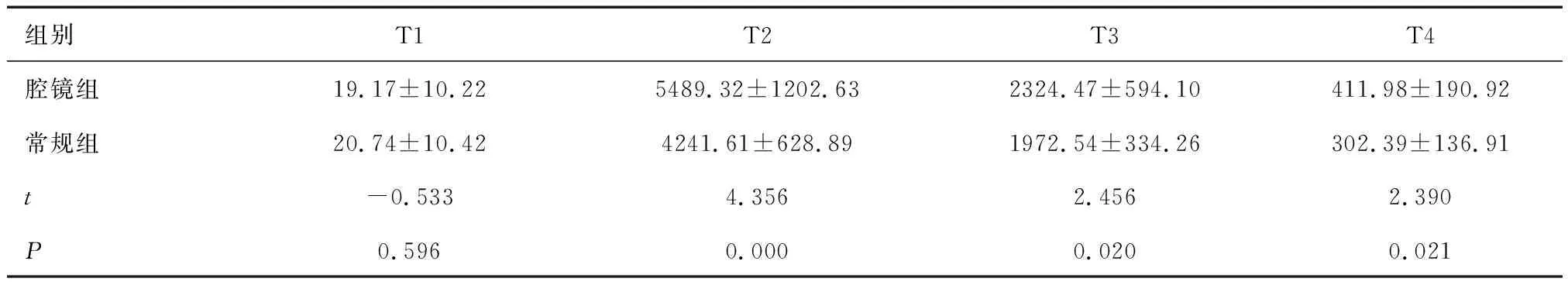
表4 兩組不同時間點cTnT比較 (ng/L)
2.5 兩組不同時間點VAS評分比較腔鏡組各時點VAS評分均低于常規組,差異有統計學意義(P<0.05)。見表5。
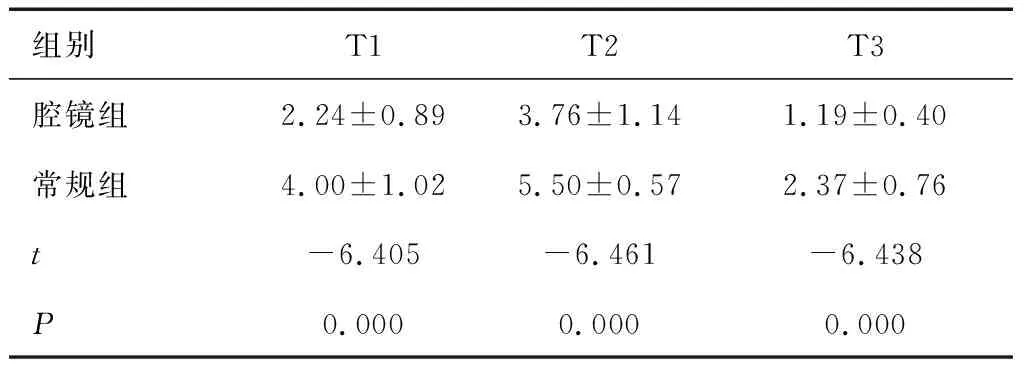
表5 兩組不同時間點VAS評分比較 (分)
3 討論
近年來隨著微創技術和腔鏡器械不斷進步,腔鏡微創手術在各個學科得到逐步開展。胸腔鏡微創外科不僅改善患者美觀性,而且還可促進患者機體快速恢復[3]。但是,心臟外科手術不僅需切除病變的組織,而且需用人工假體替代病變組織,手術技巧相對復雜,因此,心臟外科醫生需更長學習曲線才能達到熟練胸腔鏡技術操作。1996年Carpentier等[4]在胸腔鏡輔助下完成首例微創二尖瓣外科手術,隨后全球范圍內多個心臟中心相繼開展了二尖瓣微創手術,但全腔鏡下二尖瓣手術在國內開展較晚,發展較慢。
既往心臟手術常用胸骨正中切口,該切口可以完成心臟外科絕大部分手術[5],但術后切口瘢痕長,機體創傷大,影響患者功能康復。一旦患者出現胸骨愈合不良,甚至縱膈感染,住院30天死亡率高達24%[6,7]。因此,國內外學者嘗試采用胸腔鏡下進行心臟手術。既往胸腔鏡下心臟手術常采用經肋間經典三孔法[8],其中操作孔位于胸壁正前方,長3~4 cm,愈合后仍影響患者外觀。應用單操作孔全腔鏡法的心臟手術患者切口位于較隱蔽的右后方胸壁,比常規組短19.79 cm,具用較好美觀性。對于女性患者本研究是做沿右側乳腺下緣弧形切口,乳腺向前上方移位后才進入右側胸腔,該切口具有很好的隱蔽性。
術后疼痛、拔除胸腔引流管和下床運動的早晚,是影響患者術后機體快速康復的重要因素[9]。常規手術需鋸開胸骨,破壞胸廓穩定性,造成術后切口疼痛明顯。胸腔鏡下手術雖不破壞胸廓穩定性,但肋間神經損傷有一定損傷[10],也會出現切口較重疼痛。Eren 等[11]用胸骨正中切口和經右胸三個肋間切口(三孔法)行胸腺腫瘤切除,研究發現正中切口組術后第一天VAS評分高,疼痛重,術后胸腔液體總引流量多,胸腔引流管拔除較晚。Ye等[12]用經典三孔法和單操作孔法行非小細胞肺癌根治術,發現單操作孔法術后VAS評分值低,切口疼痛較輕,原因可能是經典三孔法有三根肋間神經受損傷,而單操作孔法僅有兩根肋間神經受損傷。本研究使用同一肋間的單操作孔法行瓣膜置換,術中僅有一根肋間神經受影響,術后1、3、5天的VAS值均比常規組低,疼痛輕。本研究結果還顯示單操作孔全腔鏡手術比胸骨正中切口常規手術胸腔液體引流量少,患者可更早期拔除引流管,減輕疼痛。術后切口疼痛減輕有助于患者早期下床運動,促進身體快速康復。
盡管體外循環不斷進步,但是體外循環后心功能障礙仍是最常見的并發癥之一。PTH是甲狀旁腺分泌的一種激素,毛龍[13]研究認為體外循環術后24小時PTH值越高,心功能受損程度越重。本研究結果顯示在T2、T3兩個時點PTH值腔鏡組比常規組高,術后心功能(EF值)測定腔鏡組下降的更明顯,均反應腔鏡組心功能損傷更重。cTnT是心肌特異性肌鈣蛋白,是心肌損傷的特異性極高的指標[14]。Koppen 等[15]認為cTnT值高低與主動脈阻斷時間呈正相關,是反映體外循環后心肌損傷程度的定量指標。本研究結果顯示腔鏡組的體外循環時間和主動脈阻斷時間較常規組長,cTnT值在術后6小時和24小時腔鏡組升高更多,更多的心肌細胞出現損傷。盡管腔鏡組有更多心肌細胞損傷和更差的術后心功能,但是術后無出現嚴重并發癥。
綜上,心臟外科醫生經過嚴格腔鏡手術訓練,單操作孔完全胸腔鏡下二尖瓣置換與常規手術有相似的臨床結果,在選擇合適患者前提下,單操作孔全腔鏡二尖瓣置換也是心外科醫生和患者可追求的手術方式。

