HPLC-DAD法同時測定金花清感顆粒中7種成分
曹洪杰, 夏方亮, 邵曉瑋, 王玉林, 王建強, 王洪明
[1.濱州市食品藥品檢驗檢測中心,山東 濱州 256600;2.濱州市化學藥物研發與質量控制重點實驗室(籌),山東 濱州 256600]
金花清感顆粒是在2009年首個抗擊甲型H1N1流感的中成藥[1],而在2020年該制劑在治療輕型、普通型新型冠狀病毒肺炎方面療效確切,退熱時間縮短,輕癥轉重癥比例降低[2-3],被納入《新型冠狀病毒肺炎診療方案》試行第六版的推薦中成藥[4]。該制劑用于治療流行性感冒風熱犯肺證,功效清熱解毒、疏風宣肺,方中牛蒡子所含牛蒡苷具有明顯的抗病毒作用,黃芩所含黃芩苷、漢黃芩苷具有抗菌、抗病毒、抗血栓作用[5],苦杏仁所含苦杏仁苷具有降氣、止咳、平喘作用[6],知母所含芒果苷具有抗炎、降血糖、抗氧化、調節免疫等作用[7],連翹所含連翹苷、連翹酯苷A等成分具有抗炎、抗病毒、抗菌等多種作用[8]。前期課題組查閱國內外文獻發現,對金花清感顆粒的研究集中在流行性感冒[9-12]、新型冠狀病毒肺炎的臨床治療[2]及藥效物質基礎[13-14],尚無質量控制方面的報道,并且相關質量標準[15]僅涉及鹽酸麻黃堿、鹽酸偽麻黃堿、牛蒡子苷、薄荷腦的含量控制,操作復雜。因此,本實驗采用HPLC-DAD法同時測定金花清感顆粒中苦杏仁苷、芒果苷、連翹酯苷A、黃芩苷、連翹苷、牛蒡苷、漢黃芩苷的含量,旨在實現該制劑全面的質量控制。
1 材料
1.1 儀器 Agilent 1260型高效液相色譜儀(美國Agilent公司);電子分析天平(瑞士Mettler-Toledo公司,精度0.01 mg);KQ-300VDV 型超聲波清洗儀(昆山市超聲儀器有限公司)。
1.2 試劑與藥物 黃芩苷(批號110715-201318,純度93.3%)、漢黃芩苷(批號112002-201702,純度98.5%)、芒果苷(批號11607-201704,純度98.1%)、牛蒡苷(批號110819-201108,純度94.6%)、連翹苷(批號110821-201816,純度95.1%)、連翹苷A(批號111810-201103,純度92.9%)、苦杏仁苷(批號110820-201808,純度88.2%)對照品及金銀花(批號121060-201608)、黃芩(批號120955-201810)、(草)麻黃(批號121051-201606)、甘草(批號120904-202021)、薄荷(批號120916-201812)、苦杏仁(批號121554-201204)、青蒿(批號121016-201506)、知母(批號121070-201806)、連翹(批號120908-201817)、浙貝母(批號120972-201906)、牛蒡子(批號120903-201811)對照藥材均購自中國食品藥品檢定研究院。金花清感顆粒[聚協昌(北京)藥業有限公司,批號20200218、20200228、20201005]購于康宇堂大藥房。甲醇、乙腈為色譜純(德國默克公司);磷酸為分析純;水為自制超純水。
2 方法與結果
2.1 對照品溶液制備 精密稱取苦杏仁苷、芒果苷、連翹酯苷A、黃芩苷、連翹苷、漢黃芩苷、牛蒡苷對照品適量,甲醇溶解并稀釋成質量濃度分別為0.885 5、0.536 6、1.904 4、0.946 1、1.013 8、1.007 5、1.009 6 mg/mL的貯備液,分別精密量取適量,置于同一10 mL 量瓶中,甲醇稀釋并定容至刻度,搖勻,過0.45 μm微孔濾膜,取續濾液,即得(各成分質量濃度分別為35.421、10.732、19.044、75.685、10.138、102.168、20.193 μg/mL)。
2.2 供試品溶液制備 取3包本品內容物,混勻,研細,精密稱取1 g,置于50 mL具塞錐形瓶中,加50%甲醇20 mL,稱定質量,超聲提取40 min,冷卻,50%甲醇補足減失的質量,濾過,精密量取續濾液5 mL,置于25 mL量瓶中,50%甲醇稀釋至刻度,搖勻,0.45 μm微孔濾膜過濾,取續濾液,即得。
2.3 陰性樣品溶液制備 根據處方分別制備缺炒苦杏仁、缺黃芩、缺連翹、缺牛蒡子、缺知母的陰性樣品,按“2.2”項下方法制備,即得。
2.4 色譜條件 Agilent XDB-C18色譜柱(250 mm×4.6 mm,5 μm);流動相乙腈(A)-0.1%磷酸(B),梯度洗脫(0~8 min,10%A;8~18 min,10%~14%A;18~35 min,14%~20%A;35~50 min,20%~32%A;50~60 min,32%~100%A;60~65 min,100%A;65~68 min,100%~10%A;68~78 min,10%A);體積流量1.0 mL/min;柱溫30 ℃;檢測波長207 nm(苦杏仁苷)、228 nm(芒果苷、連翹酯苷A、黃芩苷、連翹苷、牛蒡苷、漢黃芩苷);進樣量10 μL。
2.5 方法學考察
2.5.1 專屬性考察 取供試品、對照品、陰性樣品溶液適量,在“2.4”項色譜條件下進樣測定,結果見圖1。由此可知,各成分色譜峰與相鄰峰之間的分離度均符合要求,理論塔板數均大于3 000,陰性無干擾,表明該方法專屬性良好。
2.5.2 線性關系考察 取“2.1”項下貯備液適量,50%甲醇制成每1 mL分別含苦杏仁苷、芒果苷、連翹酯苷A、黃芩苷、連翹苷、漢黃芩苷、牛蒡苷177.11、53.66、95.22、378.42、50.69、100.96、510.84 μg的對照品溶液,逐級稀釋成系列質量濃度,分別精密吸取20 μL,在“2.4”項色譜條件下進樣測定。以對照品質量濃度為橫坐標(X),峰面積為縱坐標(Y)進行回歸,并分別以信噪比10∶1、3∶1為定量限、檢測限,結果見表1,可知各成分在各自范圍內線性關系良好。

1.苦杏仁苷 2.芒果苷 3.連翹酯苷A 4.黃芩苷 5.連翹苷 6.牛蒡苷 7.漢黃芩苷1. amygdalin 2. mangferin 3. forsythoside A 4. baicalin 5. forsythin 6. arctiin 7. wogonoside圖1 各成分HPLC-DAD色譜圖Fig.1 HPLC-DAD chromatograms of various constituents
2.5.3 精密度試驗 取“2.1”項下對照品溶液,同一天在“2.4”項色譜條件下進樣測定6次,計算日內精密度;每天測定2次,連續3 d,計算日間精密度,測得苦杏仁苷、芒果苷、連翹酯苷A、黃芩苷、連翹苷、漢黃芩苷、牛蒡苷兩者分別為1.9%、2.0%;1.3%、2.1%;1.7%、1.8%;0.21%、0.5%;0.7%、0.8%;0.4%、0.4%;0.14%、0.26%,表明儀器精密度良好。
2.5.4 穩定性試驗 取“2.2”項下同一份供試品溶液,室溫下于0、2、4、8、12、24 h在“2.4”項色譜條件下進樣測定,測得苦杏仁苷、芒果苷、連翹酯苷A、黃芩苷、連翹苷、漢黃芩苷、牛蒡苷峰面積RSD分別為1.60%、1.55%、1.94%、0.32%、0.54%、0.61%、0.38%,表明溶液在24 h內穩定性良好。
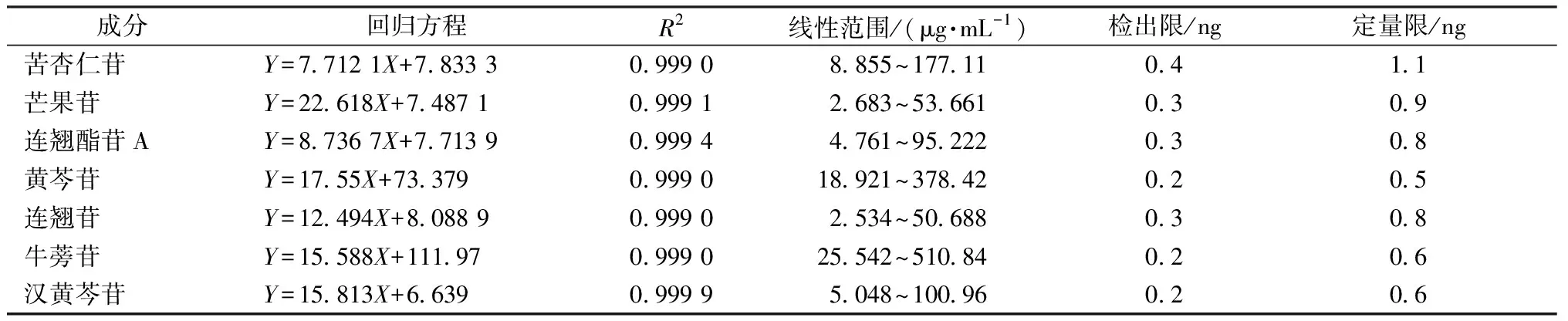
表1 各成分線性關系
2.5.5 重復性試驗 精密稱取同一批本品(批號20200218)6份,每份0.5 g,按“2.2”項下方法制備供試品溶液,在“2.4”項色譜條件下進樣測定,測得苦杏仁苷、芒果苷、連翹酯苷A、黃芩苷、連翹苷、漢黃芩苷、牛蒡苷峰面積RSD分別為0.70%、0.18%、1.82%、2.14%、2.01%、1.66%、2.07%,表明該方法重復性良好。
2.5.6 加樣回收率試驗 精密稱取6份各成分含量已知的本品(批號20200218)0.5 g,加入適量對照品,按“2.2”項下方法制備供試品溶液,在“2.4”項色譜條件下進樣測定,計算回收率。結果,苦杏仁苷、芒果苷、連翹酯苷A、黃芩苷、連翹苷、漢黃芩苷、牛蒡苷平均加樣回收率分別為98.36%、99.57%、99.24%、100.28%、99.33%、99.40%、99.85%,RSD分別為1.76%、0.58%、1.37%、0.83%、0.77%、1.17%、0.23%。
2.6 樣品含量測定 取3批本品,每批約0.5 g,精密稱定,按“2.2”項下方法制備供試品溶液,在“2.4”項色譜條件下進樣測定,計算含量,結果見表2。

表2 各成分含量測定結果(mg/g,n=3)
3 討論
3.1 提取條件選擇 本實驗比較了不同提取溶劑(甲醇、70%甲醇、50%甲醇)、超聲時間(20、40、60 min)、溶劑用量(10、20、40 mL)的提取效果,最終確定20 mL 50%甲醇超聲提取40 min作為提取條件。
3.2 流動相選擇 本實驗考察了乙腈-水、甲醇-水、乙腈-0.1%磷酸,發現乙腈-0.1%磷酸能顯著提高各成分色譜峰與雜質峰之間的分離度,并且峰形明顯更優。
3.3 檢測波長選擇 本實驗采用二極管陣列檢測器對供試品、對照品溶液進行全波長掃描(200~400 nm),發現苦杏仁苷在207 nm波長處有最大吸收,而其他成分在228 nm波長處均有較好的紫外吸收,并且互不干擾,雜質峰少,故選擇207、228 nm波長切換模式。
4 結論
本實驗建立HPLC-DAD法同時測定金花清感顆粒中黃芩苷、漢黃芩苷、牛蒡苷、芒果苷、連翹苷、連翹酯苷A、苦杏仁苷的含量,該方法簡便可靠,重復性好,可實現該制劑更有效全面的質量控制。

