高效、寬帶發射有機-無機金屬鹵化物熒光材料
赫世輝 趙 靜 劉泉林
(北京科技大學材料科學與工程學院,北京 100083)
0 引 言
有機-無機金屬鹵化物(OIMHs)半導體材料是目前研究的熱點,其作為發光材料、太陽能電池材料、非線性光學材料、輻射探測器材料等在光電領域有著廣泛的應用前景[1]。目前,照明及顯示背光源主要是藍光二極管(LED)結合熒光粉產生所需要的光色。現在應用的熒光粉中都需要引入稀土元素作為發光中心,為了減少對稀土元素的依賴,OIMHs憑借其優異的發光性能,成為當前發光領域研究的關注點。OIMHs的優越性主要體現在高的發光量子效率(PLQY)[2]和寬譜發射[3]兩方面。OIMHs是實現單一組分白光發射LED的有力候選材料,通過組分調控可實現單一組分發射光譜覆蓋整個可見光區[4]。其成功應用將解決多組分熒光粉在照明中由于自吸收引起的效率降低,以及隨使用時間推移,降解速率不同所導致的光色偏差問題。
OIMHs與雜化鈣鈦礦材料聯系緊密,三維(3D)鈣鈦礦結構中八面體高度有序,結構剛性強。3D鈣鈦礦結構的通式為ABX3,其中A是甲基銨(MA)、甲脒(FA)或銫(Cs),B是Pb2+、Sb3+、Sn2+、Bi3+等金屬離子,X是一種或多種鹵化物(Cl、Br或I),它由無限[BX6]4-八面體通過角共享和A位陽離子占據的空隙空間構成的3D框架。形成的3D鈣鈦礦結構是直接帶隙半導體,在其中價帶最大值(VBM)的特定反鍵特性和導帶最小值(CBM)中的自旋軌道效應僅形成封閉在導帶或價帶中的淺陷阱[3]。由于晶格常數的改變,FA大于MA,MA又大于Cs,A位陽離子的選擇改變了帶隙,導致從FA到MA再到Cs的帶隙增加[1,5]。隨著有機物陽離子的增加,帶隙也會相應地增加。因此,3D鈣鈦礦結構中帶隙很窄且不存在自陷態激子(STE),使其無法形成寬帶發射。目前報道的化合物CsPbX3(X=Cl、Br或I)鈣鈦礦納米晶,PLQY最高可達90%,但是均為窄帶發射,其半峰寬最高為35 nm[6]。MAPbX3(X=Cl、Br或 I)也為窄帶發射[7]。
OIMHs與傳統鈣鈦礦結構ABX3的最大區別在于A位陽離子不再是簡單的無機或小體積有機陽離子[8],而是換成了大的有機陽離子(CNH+、CNH+92079等)[9];B位的金屬陽離子包括最外層具有不同電子組態的+1、+2、+3、+4價離子;X位為鹵素離子。值得注意的是,低維度的OIMHs中B位和X位結合形成的多面體,不再局限于八面體結構,還有三面體、四面體、蹺蹺板、金字塔以及多核聚集體等結構。
本文首先按照金屬陽離子的最外層電子層分布將OIMHs發光材料分為3類(ns2、d10、d5)。然后,討論OIMHs發光機理,包括STE發光、ns2孤立中心發光、Mn2+孤立中心發光以及混合機理。最后,重點討論了提高OIMHs的PLQY的方法并對該系列化合物的發展前景進行了展望。
1 高效發光OIMHs材料的分類
1.1 ns2系列
含有ns2電子的陽離子包括 Pb2+、Bi3+、Sn2+、Sb3+等。ns2離子在光激發過程中表現出ns2孤對電子躍遷特性。
1.1.1 6s2系列
6s2系列金屬陽離子中包括Pb2+和Bi3+等,該系列雜化金屬鹵化物的發光主要來自無機基團,其中孤對電子會引起激發態結構畸變,降低激子的輸運能力。使運輸過程中造成的復合減弱,相應的非輻射躍遷就會降低,其PLQY則會增加[10]。但是受限于畸變程度較低,導致其PLQY整體不高。通常通過摻雜或者形成多聚體發光中心的形式來調整結構,進而提高其PLQY。
Ma課題組[11]較早合成了高PLQY的C4N2H14PbBr4,其晶體結構如圖1a所示。該化合物為一維(1D)結構,2個八面體通過共邊連接形成雙八面體鏈,其單晶在紫外燈照射下呈現藍白光,PLQY約20%。另外,Zhang課題組報道了(2cepiH)PbBr3[12],如圖1b所示,其由共面PbBr64-八面體組成1D無限[PbBr3]n-鏈狀結構,其PLQY為16.8%。其它Pb2+基的高效熒光材料如表1所示。Bi3+基的OIMHs研究很少[13-16],其存在形式主要是八面體[BiX6]3-,目前報道的化合物的PLQY都很低,即使形成二聚體[17-18][Bi2X9]3-、[Bi2X10]4-、[Bi2X11]5-,PLQY仍然很低。因此,對于追求高效發光材料而言,以Bi3+作為中心陽離子的化合物有待進一步研究。
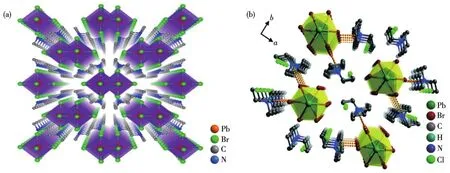
圖1 (a)C4N2H14PbBr4[11]和(b)(2cepiH)PbBr3[12]的晶體結構Fig.1 Crystal structures of(a)CNHPbBr[11]and(b)(2cepiH)PbBr[12]421443
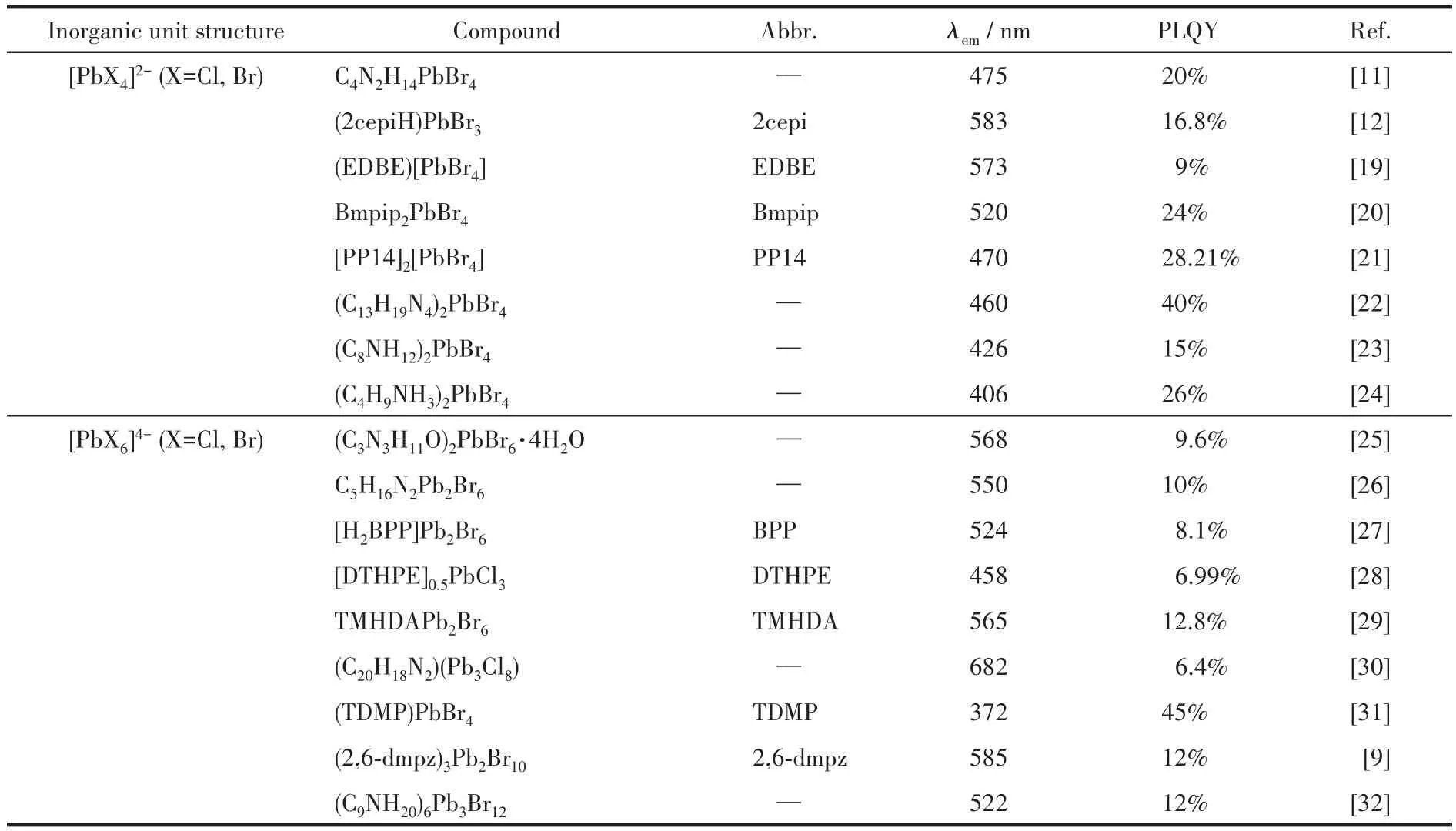
表1 6s2系列OIMHs的無機結構單元和主要發光性質參數Table 1 Inorganic unit structure and main luminescent property parameters of 6s2series OIMHs*
1.1.2 5s2系列
含有5s2孤對電子的金屬陽離子有Sn2+、Sb3+和Te4+,雖然5s2和6s2雜化金屬鹵化物的基態電子結構相似,但是其孤對電子的立體活性和結構可調性都比6s2更好,其中化學活性較高的Sn2+孤對電子導致該系列化合物激發態結構畸變更強,斯托克斯(Stokes)位移更大。大的Stokes位移可以減少激發和發射之間的光譜重疊,從而限制了激發能的共振傳遞。如果不滿足諧振條件,激子轉移需要聲子輔助,從而顯著降低能量傳輸效率。激子遷移的抑制降低了激子遇到缺陷的概率,從而降低了非輻射復合率,提高了光致PLQY。溫度的升高使激發和發射帶變寬[10,33-34]。
Fan 課題組[35]合成的(C10H28N4Cl2)SnCl4·2H2O 的PLQY高達92.3%,其中Sn2+形成四面體結構[SnCl4]2-(圖2a)。Ma課題組[36]合成出化合物(C4N2H14Br)4SnBr6,其中Sn2+形成八面體配位結構[SnBr6]4-,其PLQY接近100%(圖2b)。這些研究結果說明Sn2+替代Pb2+在降低材料毒性的同時有效提高了PLQY,但是Sn2+穩定性較低,易被氧化為Sn4+,制約了其進一步發展。相較而言,Sb3+的穩定性更高,其主要結構為金字塔型[SbX5]2-和八面體型[SbX6]3-。統計發現,含有[SbX5]2-的OIMHs的PLQY更高一些(表2)。Ma課題組[36]合成出(C9NH20)2SbCl5,其在紫外燈下呈現黃色,PLQY接近于100%(圖2c)。關于Te4+的研究較少,其主要是以八面體[TeX6]4-形式存在。Kundu課題組[37]報道了(BzTEA)2TeCl6,其在紫外燈下呈現橙色,PLQY為15%(圖2d)。總體而言,5s2體系PLQY較高,是研究高效發光材料的重點。
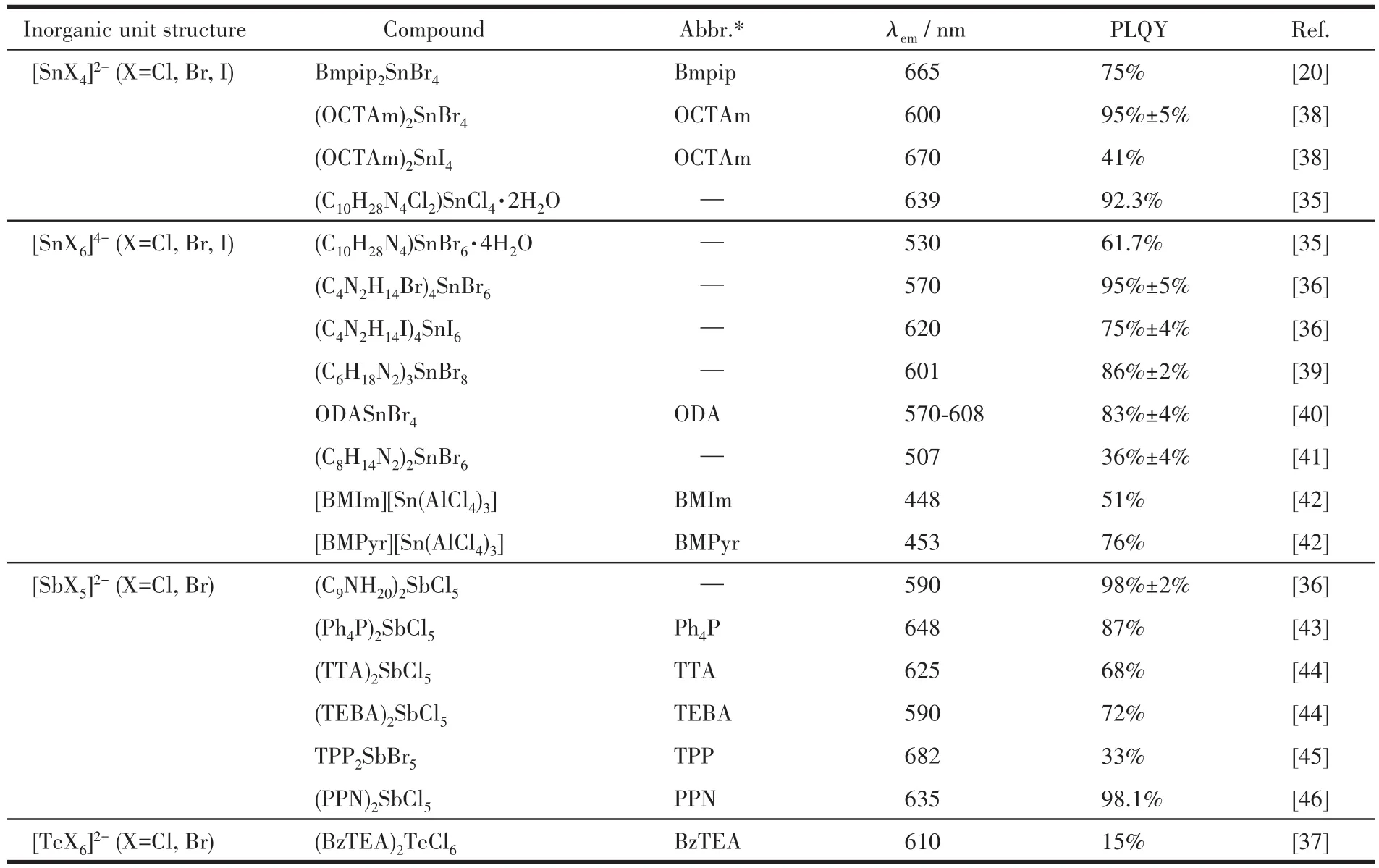
表2 5s2系列OIMHs的無機結構單元和主要發光性質參數Table 2 Inorganic unit structure and main luminescent property parameters of 5s2series OIMHs
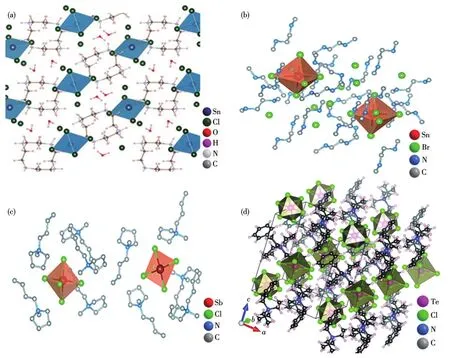
圖2 (a)(C10H28N4Cl2)SnCl4·2H2O[35]、(b)(C4N2H14Br)4SnBr6[36]、(c)(C9NH20)2SbCl5[36]和(d)(BzTEA)2TeCl6[37]的晶體結構Fig.2 Crystal structures of(a)(CHNCl)SnCl·2HO[35],(b)(CNHBr)SnBr[36],(c)(CNH)SbCl[36],and(d)(BzTEA)TeCl[37]102842424214469202526
1.2 d10系列
d10系列金屬陽離子也是OIMHs發光材料研究的重點,包括Ag+、Cu+、Cd2+、Zn2+、In3+、Sn4+等。
其中,研究較多的是 In3+、Zn2+和 Cu+。In3+存在八面體[InX6]3-和四面體[InX4]-兩種配位形式。(PMA)3InBr6具有0D結構,含有[InBr6]3-八面體,PLQY為35%,其發射光顏色為橙色(圖3a)[47]。RInBr4含有孤立的[InBr4]-四面體,PLQY為16.36%,其發射光顏色為藍色(圖3b)[48]。Zn2+多以四面體結構[ZnX4]2-形式存在[49],Ma課題組[50]合成的TPP2ZnCl4具有優良的長余輝性能,PLQY為28.8%。Tang團隊[51]合成的(C16H36N)CuI2中含有[Cu2X4]2-二聚體,PLQY達到54.3%(圖3c)。Zhang課題組[52]合成的 Hmta[(Hmta)Ag4I4]結構由四面體Ag4I4單元和Hmta交替排列組成,PLQY達到18.5%。
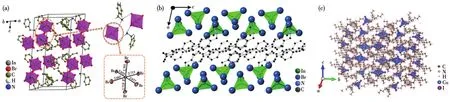
圖3 (a)(PMA)3InBr6[47]、(b)RInBr4[48]和(c)(C16H36N)CuI2[51]的晶體結構Fig.3 Crystal structures of(a)(PMA)InBr[47],(b)RInBr[48],and(c)(CHN)CuI[51]36416362
對于空氣和熱穩定性,Sn4+基材料是Sn2+基材料的理想替代品。但是,Sn4+由于沒有立體化學活性孤對的電子以及[SnX6]2-中幾乎沒有結構畸變[8],因此其發光性能較弱,目前已知結構中(C6N2H16Cl)2SnCl6的效率最高,為 8.1%[53]。當 Sn2+被氧化成Sn4+時,其會失去最外層的5s2電子,化學活性降低,相應的激發態結構畸變也會隨之減少,Stokes位移減小,相應的激發和發射之間的光譜重疊,增加了激發能的共振傳遞。激子遷移的增加提高了激子遇到缺陷的概率,從而增加了非輻射復合率,使PLQY降低[33]。由于沒有孤對電子的存在,d10整體的PLQY相比于5s2系列低一些(表3),對于d10系列的研究可以通過摻雜等方式來進一步改善其PLQY。
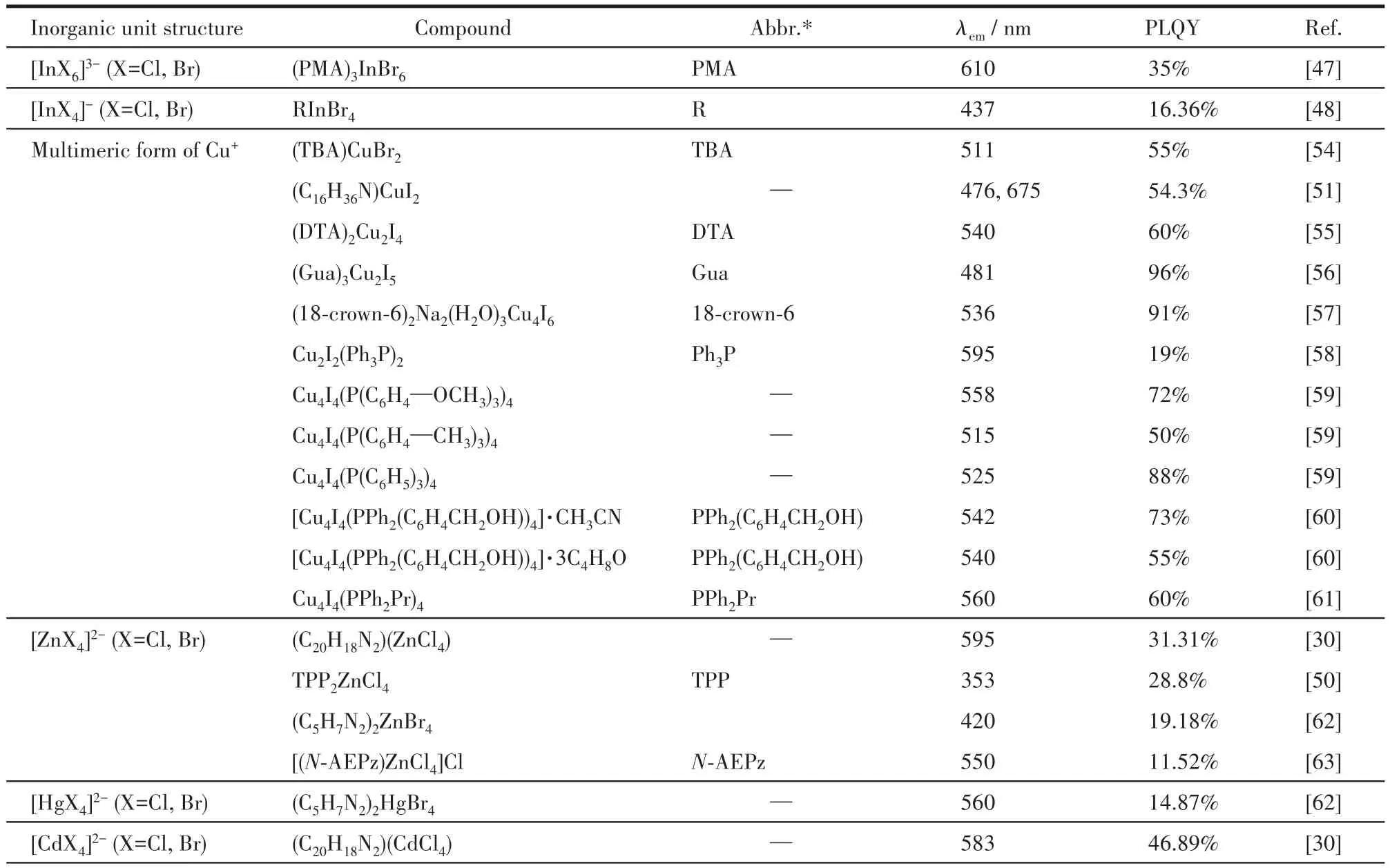
表3 d10系列OIMHs的無機結構單元和主要發光性質參數Table 3 Inorganic unit structure and main luminescent property parameters of d10series OIMHs

續表3
1.3 d5系列
d5系列中,主要的研究對象是Mn2+,其形成的配位多面體主要是四面體[MnX4]2-和八面體[MnX6]4-,還有少部分會形成三聚體結構[Mn3X12]6-。
目前合成的OIMHs中,Mn2+形成四面體結構的居多,其在紫外燈光下呈現出綠光發射。Gong等[65]報道了2種化合物[P14]2[MnBr4]和[PP14]2[MnBr4](圖4a、4b)。其中,前者的PLQY為81%,后者的PLQY為55%。[P14]2[MnBr4]中的[MnBr4]2-是完全有序的,[PP14]2[MnBr4]中的[MnBr4]2-是無序的,四面體結構的有序性對于PLQY有很大的影響。六配位的Mn2+在紫外燈光下呈現出紅光發射。Zou團隊[66]合成的(CH6N3)2MnCl4表現出強烈的紅光發射,其PLQY為55.9%(圖4c)。其它Mn基高效發光的化合物見表4。Mn可以作為中心金屬陽離子存在于OIMHs的晶格中,還可作為摻雜劑的形式存在,使其在高效OIMHs的研究中所占的比重日益增加。
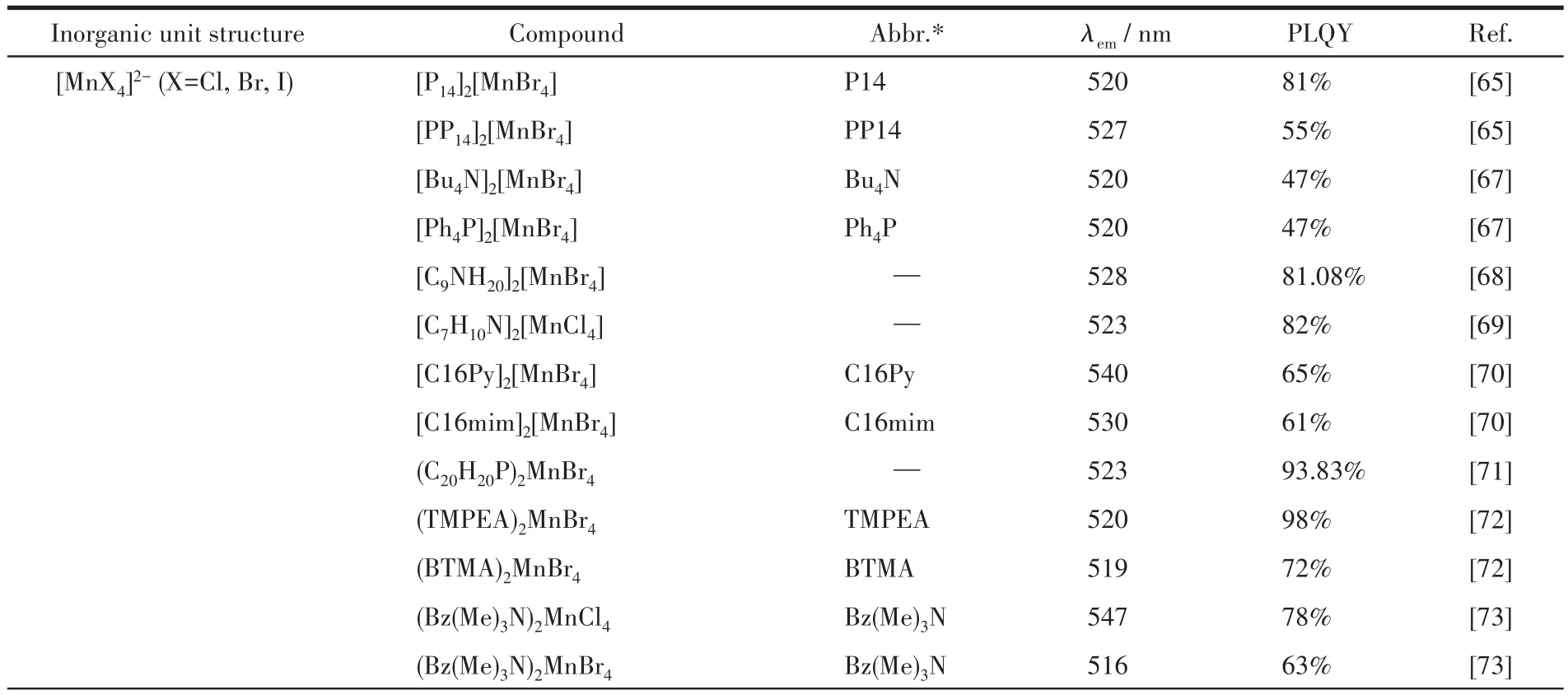
表4 Mn系列OIMHs的無機單元結構和主要發光性質參數Table 4 Inorganic unit structure and main luminescent property parameters of Mn series OIMHs
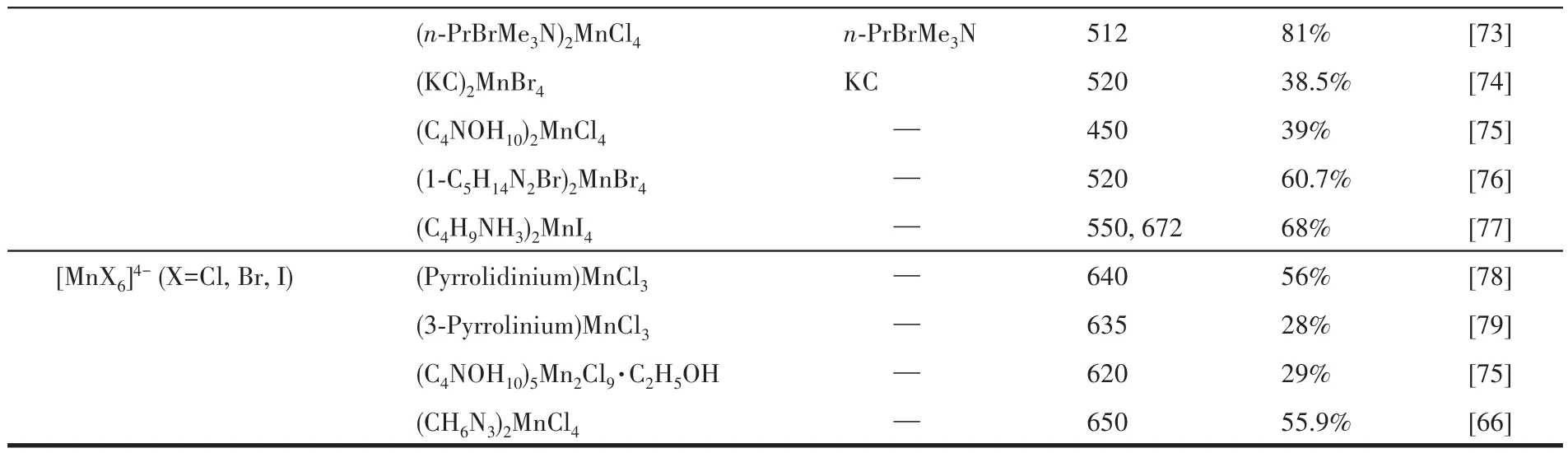
續表4
1.4 含有多個B位陽離子的OIMHs
研究表明在單一金屬陽離子OIMHs的基礎上,通過引入另外的金屬陽離子,形成多中心金屬陽離子OIMHs,可以進一步擴展發射光譜的寬度實現單一組分白光發射。Ma課題組[80]合成的(HMTA)4PbMn0.69Sn0.31Br8包括了PbBr42-、MnBr42-、SnBr42-單體結構,實現了白光發射,其PLQY達到73%(圖5a和5b)。多中心金屬陽離子化合物的另外一種存在方式就是多聚體和單體結構結合,多聚體研究中以[Pb3X11]5-三聚體研究最多,它是由3個[PbX6]4-八面體通過共面連接形成的,結構中引入另外一種金屬離子的單體結構進行光譜調控,形成不同顏色的光,多個陽離子中心同時也會使材料PLQY得到極大的提高(表5)。例如 Xia課題組[81]報道的(C9NH20)9Pb3X11(MBr4)2(X=Br、Cl;M=Mn、Fe、Co、Ni、Cu和Zn)系列化合物,其呈現出不同顏色的發光且PLQY也不盡相同(圖5c~5e)。其它多中心金屬陽離子化合物見表5,多中心金屬陽離子化合物的合成和研究正在逐漸成為調整發光譜圖和提高PLQY的有效措施。
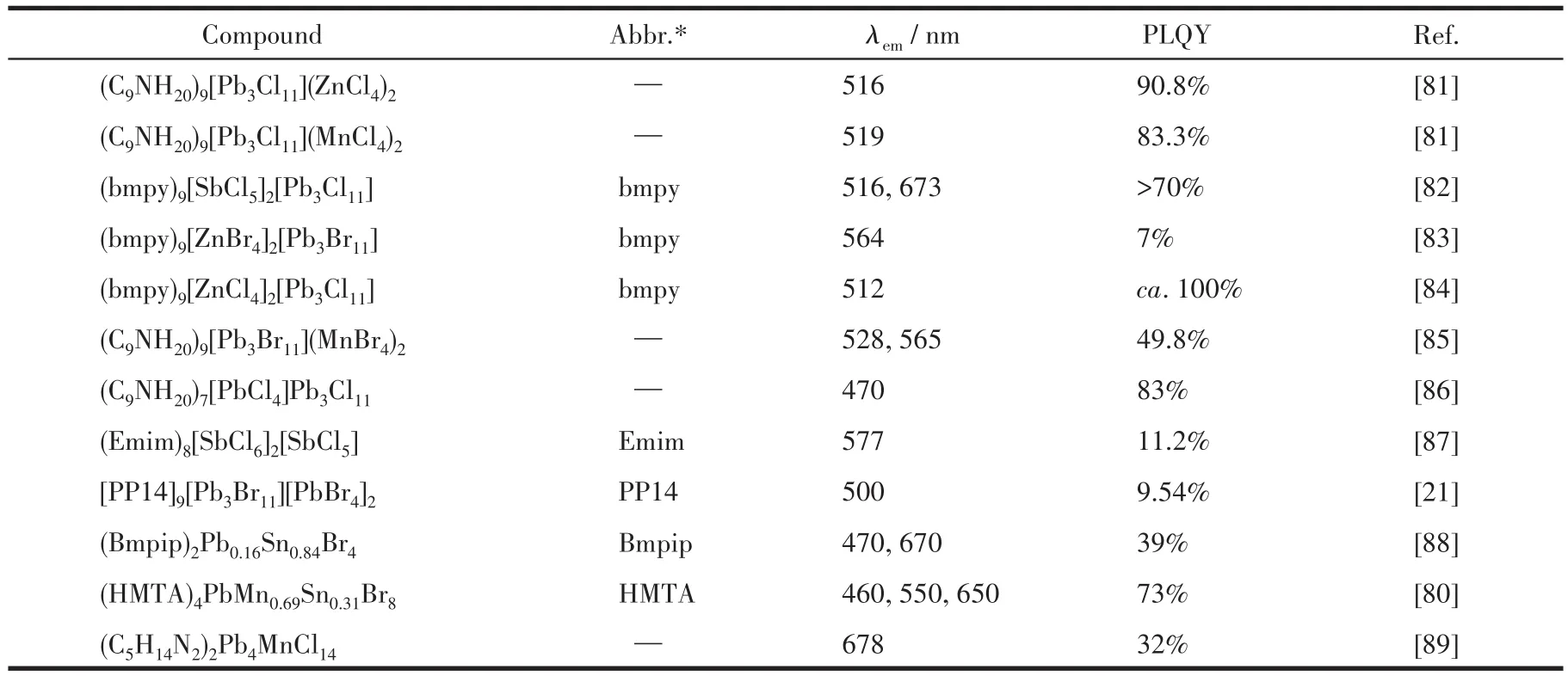
表5 多中心金屬陽離子OIMHs的無機單元結構和主要發光性質參數Table 5 Inorganic unit structure and main luminescent property parameters of multi-component OIMHs
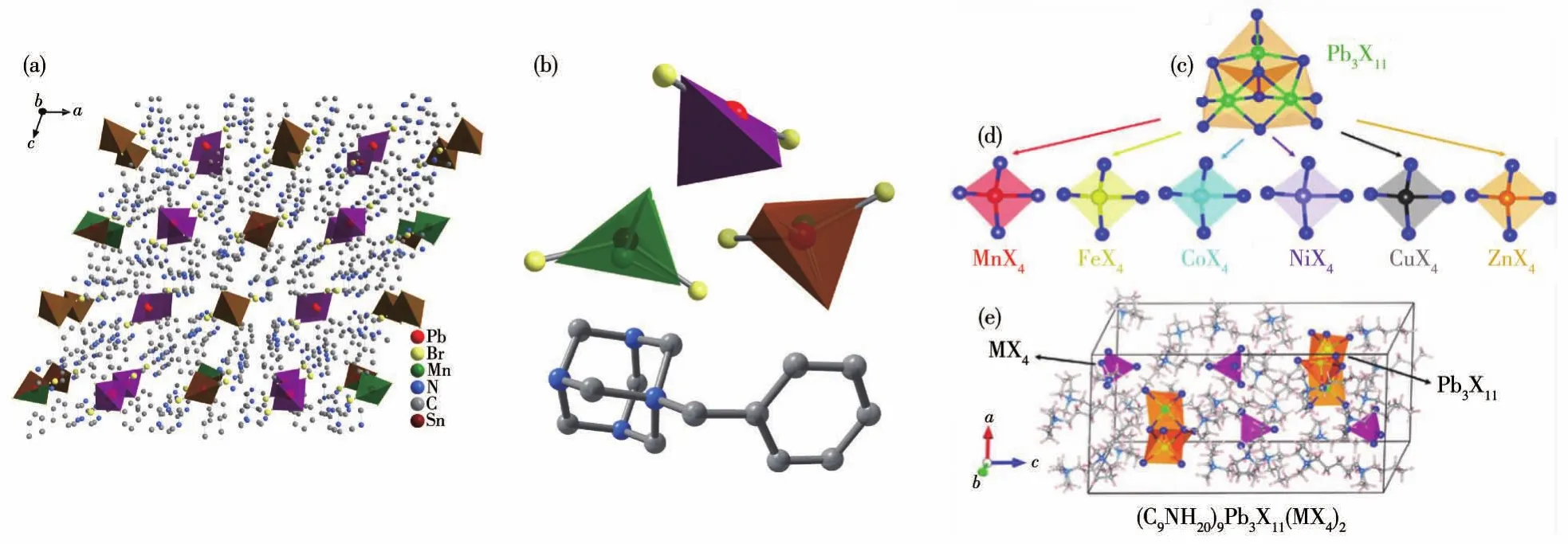
圖5 (a)(HMTA)4PbMn0.69Sn0.31Br8的單晶結構;(b)結構單元:PbBr42-(紫色四面體)、MnBr42-(綠色四面體)、SnBr42-(棕色四面體)和有機陽離子HAMT+[80];(c)提出(C9NH20)9Pb3X11(MX4)2的結構設計原理,突出[Pb3X11]5-三聚體的局部結構;(d)具有不同M位陽離子的[MX4]2-;(e)(C9NH20)9Pb3X11(MX4)2的晶胞[81]Fig.5 (a)Single-crystal structure of(HMTA)4PbMn0.69Sn0.31Br8;(b)Building blocks:PbBr42-(purple tetrahedron),MnBr42-(green tetrahedron),SnBr42-(brown tetrahedron),and the organic cation HAMT+[80];(c)Proposed structural design principle of(C9NH20)9Pb3X11(MX4)2highlighting the local structure of[Pb3X11]5-block;(d)[MX]2-block with different M-position cations;(e)Unit cell of(CNH)PbX(MX)[81]4920931142
2 OIMHs的發光機理
目前,有關OIMHs的研究在不斷增加,其發光本質也逐漸被揭示。已報道的發光機理主要包括STE、ns2孤對電子、Mn2+孤立中心發光以及混合機理發光。
2.1 STE發光
STE發光是目前解釋具有低晶體結構維度的OIMHs發光的主流機理(圖6)。STE的產生是由于激子-聲子的強耦合,使激發態晶格產生了瞬態的彈性畸變,造成了自由激子(FE)的俘獲,也被稱為本征STE[90]。STE可以通過輻射躍遷的方式釋放出能量。當能量增加時,STE也可以向FE進行轉換[91]。STE參與的光發射的表現是寬帶發射且斯克托斯位移較大。材料處于基態時這種產生STE的瞬態畸變消失,它不同于永久缺陷。永久缺陷有時也會與FE相互耦合,促進STE的形成,也被稱為非本征STE。缺陷可能會從穩態吸收光譜中表現出亞帶隙吸收,而STE沒有從穩態吸收中表現出吸收信號[92]。此外,從瞬態吸收來看,缺陷會表現出負的亞帶隙漂白信號,而STE則表現出正的吸收信號[93]。此外,從激勵功率相關的光致發光(PL)測量結果來看,當由永久缺陷主導寬帶發射時,預期會出現飽和PL。相反,如果寬帶發射來自STE,則激勵功率與PL呈線性關系,不會出現飽和的PL現象[19,25,90,94]。
由于晶格變形和載流子-聲子耦合,基于STE的穩態光譜通常表現出較大的Stokes位移和寬譜發射;在低溫光譜中,可以看到化合物隨著溫度升高會出現展寬的現象;在壽命光譜中,其從激發態躍遷回基態的時間更長。在瞬態光譜中,STE的光誘導信號(PIA)比FE的PIA達到峰值所需要的時間更長,衰減弛豫時間也更長[92]。
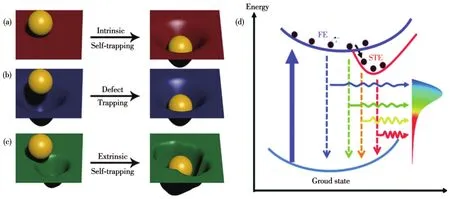
圖6 (a)自捕獲、(b)永久缺陷的捕獲和(c)受永久缺陷影響的自捕獲[90];(d)STE和FE的發射機理圖[91]Fig.6 (a)Self-trapping,(b)trapping at permanent defects,and(c)self-trapping influenced by permanent defects[90];(d)Emission mechanism diagram of STE and FE[91]
2.2 ns2孤對電子發光
目前,對于ns2系列合成的化合物,主要使用的模型有3種:(1)如圖7a所示,自由ns2離子的能級圖中,其基態用1S0表示,當發生庫侖和交換相互作用時,nsnp激發態會分裂為1P和3P,然后經過自旋軌道耦合,3P會分裂為非簡并態的3P0、3P1、3P2;(2)如圖7b所示,分子軌道理論中,由于配位場的作用,中心金屬和配體之間的電子軌道會發生很大程度的雜化,進而形成分子能級;(3)如圖7c所示,在半導體材料中,通常用STE模型來解釋ns2發光,激發態結構扭曲程度會影響到達激發態所需能量,進而影響發射。Kovalenko課題組將3個模型進行結合,形成了如圖7d所示的統一模型[10]。
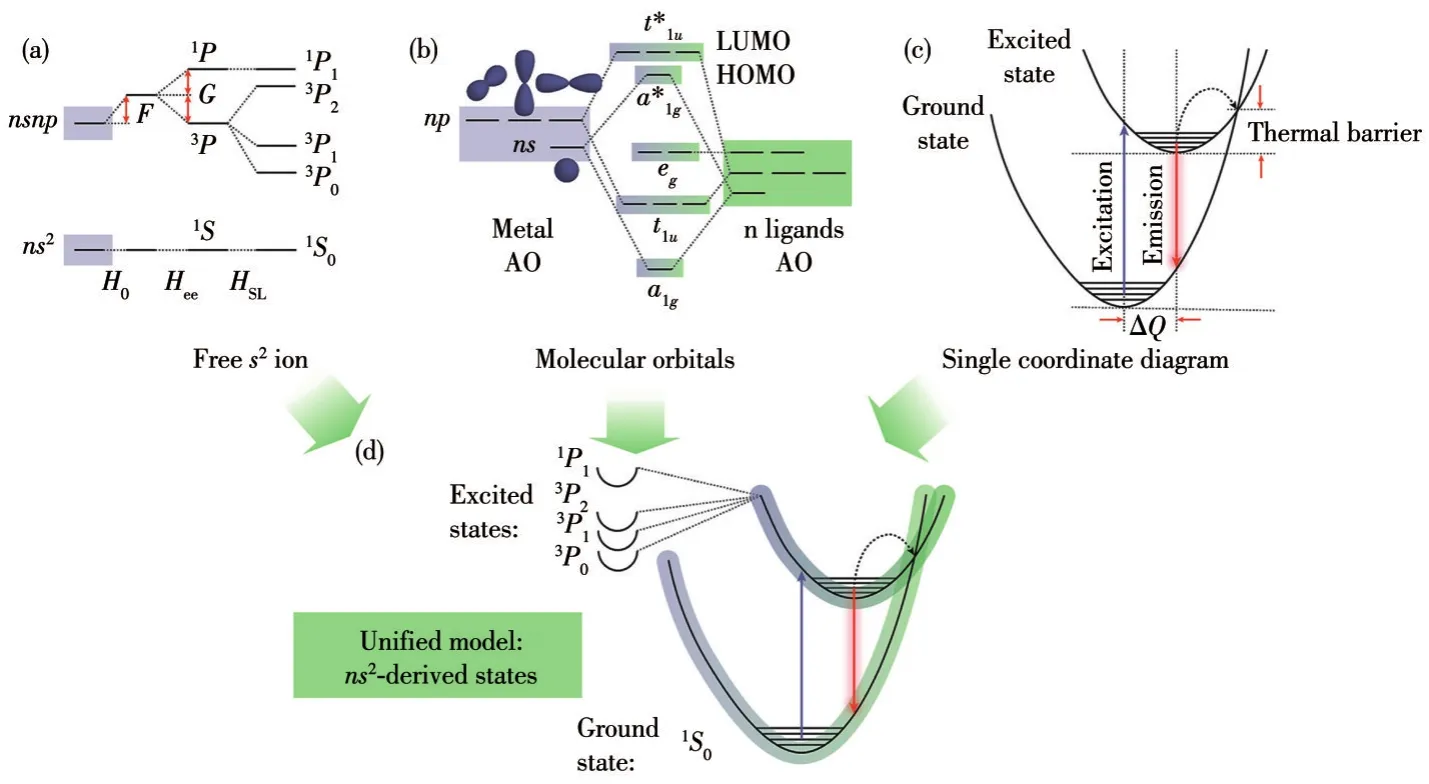
圖7 (a)自由ns2離子的能級圖;(b)金屬-鹵化物分子軌道圖,圖中AO表示原子軌道;(c)簡化STE模型在0D 5s2金屬鹵化物中的位型坐標圖;(d)用位型坐標圖表示的統一模型,其中基態和激發態使用其從活性ns2金屬離子衍生的原子特性進行描述[10]Fig.7 (a)Energy band diagram associated with the free ns2ion;(b)Metal-halide molecular orbital diagram where AO represents atomic orbital;(c)Configurational coordinate diagram of the simplified STE model in 0D 5s2metal halides;(d)Unified model with the configurational coordinate diagram,in which the ground and excited states are described using their atomic character as derived from the active ns2metal ion[10]
2.3 Mn2+的孤立發光中心
四面體配位的[MnX4]2-處于弱晶體場,發射綠光;八面體配位的[MnX6]4-處于強晶體場,發射紅光。其發射機理均為4T1→6A1躍遷(圖8a和8b)[73,95]。對于Mn2+摻雜而言,則是主體化合物吸收激發光,進行能量轉移,Mn2+作為激活劑,實現4T1→6A1的輻射躍遷。在此過程中,Mn作為發光中心的引入,提高了OIMHs的PLQY。
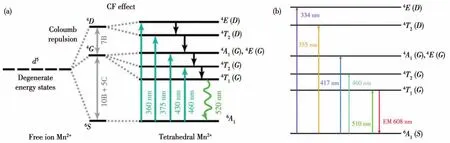
圖8 (a)(Bz(Me)3N)2MnCl4在綠光發射下的d-d躍遷[73];(b)(CH3NH3)2MnCl4在紅光發射下的d-d躍遷,圖中CF表示晶體場,EM表示發射[95]Fig.8 (a)d-d transition of(Bz(Me)3N)2MnCl4under green light emission[73];(b)d-d transition of(CH3NH3)2MnCl4under red light emission,where CF represents crystal field and EM represents emission[95]
2.4 混合機理
對于多中心金屬陽離子化合物,其發光中心也在隨之增加,相應的發射機理也會隨之改變,通常包含以上幾種機理或者引入一些新的機理:(1)有機發光中心和無機發光中心同時存在。Yue課題組[27]合成出的化合物[H2BPP]Pb2X6存在2個發射峰,高能峰來自[H2BPP]2+的發射,低能峰來自[Pb2X6]2-。(2)金屬-配體電荷轉移或鹵化物-配體電荷轉移(MLCT/HLCT)、簇中心(CC)相互作用。Xia課題組[57]合成出的化合物(18-crown-6)2Na2(H2O)3Cu4I6(CNCI)的光譜圖呈現出雙發射,其中高能發射峰位于536 nm,低能發射峰位于700 nm,其高能發射峰歸因于MLCT/HLCT,低能發射峰歸因于CC(圖9a~9d,PLE=光致發光激發)。
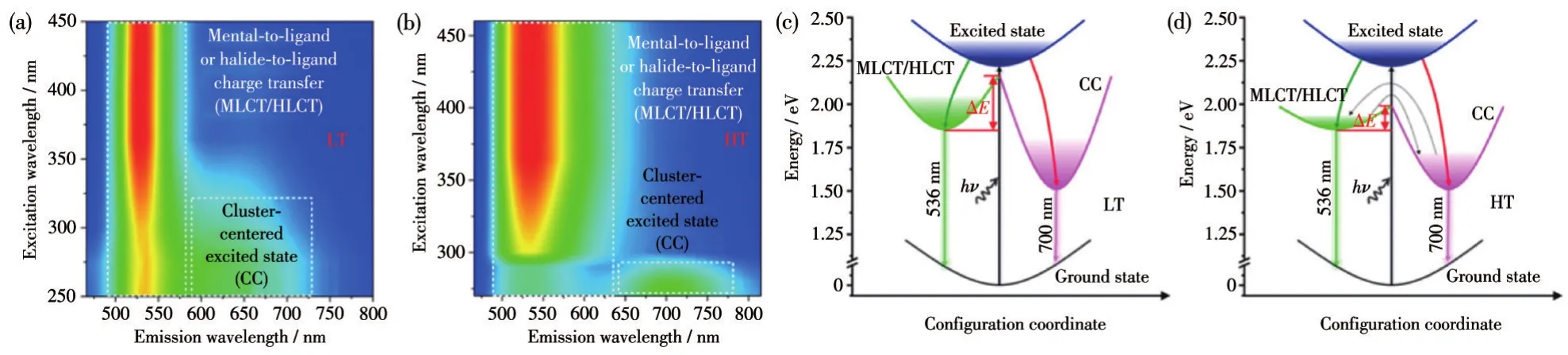
圖9 CNCI在(a)低溫(LT,15 K)和(b)高溫(HT,298 K)下的連續PL/PLE相關圖;(c)LT和(d)HT的發射機理示意圖[57]Fig.9 Consecutive PL/PLE correlation charts of CNCI(a)at a low temperature(LT,15 K)and(b)at a high temperature(HT,298 K);Schematic diagram of the emission mechanism at(c)LT and(d)HT[57]
3 提高OIMHs的光致PLQY的方法
目前提高OIMHs化合物PLQY的策略,主要通過降低晶體結構維度、摻雜發光中心離子、改變配位多面體之間的距離和鹵素替代方式對結構進行調節等。
3.1 降低晶體結構維度
降低鈣鈦礦材料的維度可以調節它們的光學特性[1]。由于角共享的BX6八面體晶體結構,使得3D的ABX3結構具有剛性結構約束,通過增加有機陽離子的長度,可以增加其結構的靈活性,從而實現結構維度的調節。長鏈烷基銨有機-無機雜化鹵化物鈣鈦礦分子式為A′2BX4,通常被稱為2D鈣鈦礦。這里A′是長有機烷基銨陽離子。大多數報道的2D鈣鈦礦衍生物具有單銨和二銨陽離子,通式為(NH3RNH3)BX4或(RNH3)2BX4,R 為有機官能團。對于化合物而言,隨著結構維度的降低,化合物的帶隙會增加。其中低維材料是天然的量子阱結構,由于量子阱內勢壘之間不同的介電環境產生了強烈的電子-空穴相互作用,使得它們具有較大的激子結合能(>100 meV)。這提高了PL強度,并且高量子產率也得益于禁阻電子躍遷的減少[1]。同時隨著維度的降低,STE的束縛能力越來越強,相應會形成一個寬譜發射[10]。因此,結構靈活、低維金屬鹵化物的強約束廣泛適用于發光應用。
目前報道的PLQY較高的OIMHs主要集中在1D和0D結構中。Ma課題組[96]報道表明(PEA)2SnBr4(2D)的 PLQY 極低(<0.1%),主要原因就是該化合物的非局域化電子態導致較弱的激子結合、較高的激子遷移率和較高的非輻射衰變。在其合成方法中加入了二氯甲烷,形成了[(PEA)4SnBr6][(PEA)Br]2[CCl2H2]2(0D),其PLQY高達90%,主要就是因為激子的高度局域化,導致了強烈的激子-聲子耦合作用。Mao等[9]合成的(2,6-dmpz)3Pb2Br10(1D)是其合成的系列化合物中PLQY最高的,可以達到12%,其發射峰同時具有FE發射和STE發射,此文章中報道的其他2D和3D的化合物都只具有較窄的FE發射。因此,設計、合成具有低維度晶體結構的化合物是實現高PLQY的有效途徑之一。本文作者近期研究發現,當OIMHs中有機物為軟鏈結構(不含苯環、雙鍵、三鍵等剛性結構),同時有機物與無機八面體作用的位點(如N)空間位阻大時,形成的化合物PLQY相對較高[11,36,81,84,88]。
3.2 摻雜發光中心離子
使用Sb3+、Mn2+和Sn2+等激活劑進行摻雜,可以引入發光中心(圖10)。Chen課題組[97]在InCl6(C4H10SN)4·Cl中摻入 Sb3+,其 PLQY 從 20% 提高到90%,Sb3+的引入造成激子的局域化,呈現出寬帶發射和大的Stokes位移。對于Sb3+摻雜的化合物還有很多[98-100],比如(C8NH12)6InBr9·H2O,該化合物 PLQY也得到了極大的提升,通過調整濃度實現了白光發射。對于Mn2+摻雜[31,89,101-107]的研究更為普遍,Kundu課題組[105]報道Mn2+摻雜(C4H9NH3)PbBr4,PLQY最高可達37%,強束縛激子從基質材料到Mn2+發生能量轉移,從而產生4T1→6A1發射。Gautier課題組[31]也做了相關的研究,在(TDMP)PbBr4中摻入Mn2+,其PLQY可以達到60%。關于Sn2+摻雜的研究較少,Chen課題組[108]在(PEA)2PbI4中摻入 Sn2+,實現了PLQY從0.7%到6%的增加。對OIMHs材料進行摻雜,實現高效、寬帶發光,已經成為了當前提高該類材料熒光性能的主要途徑之一。
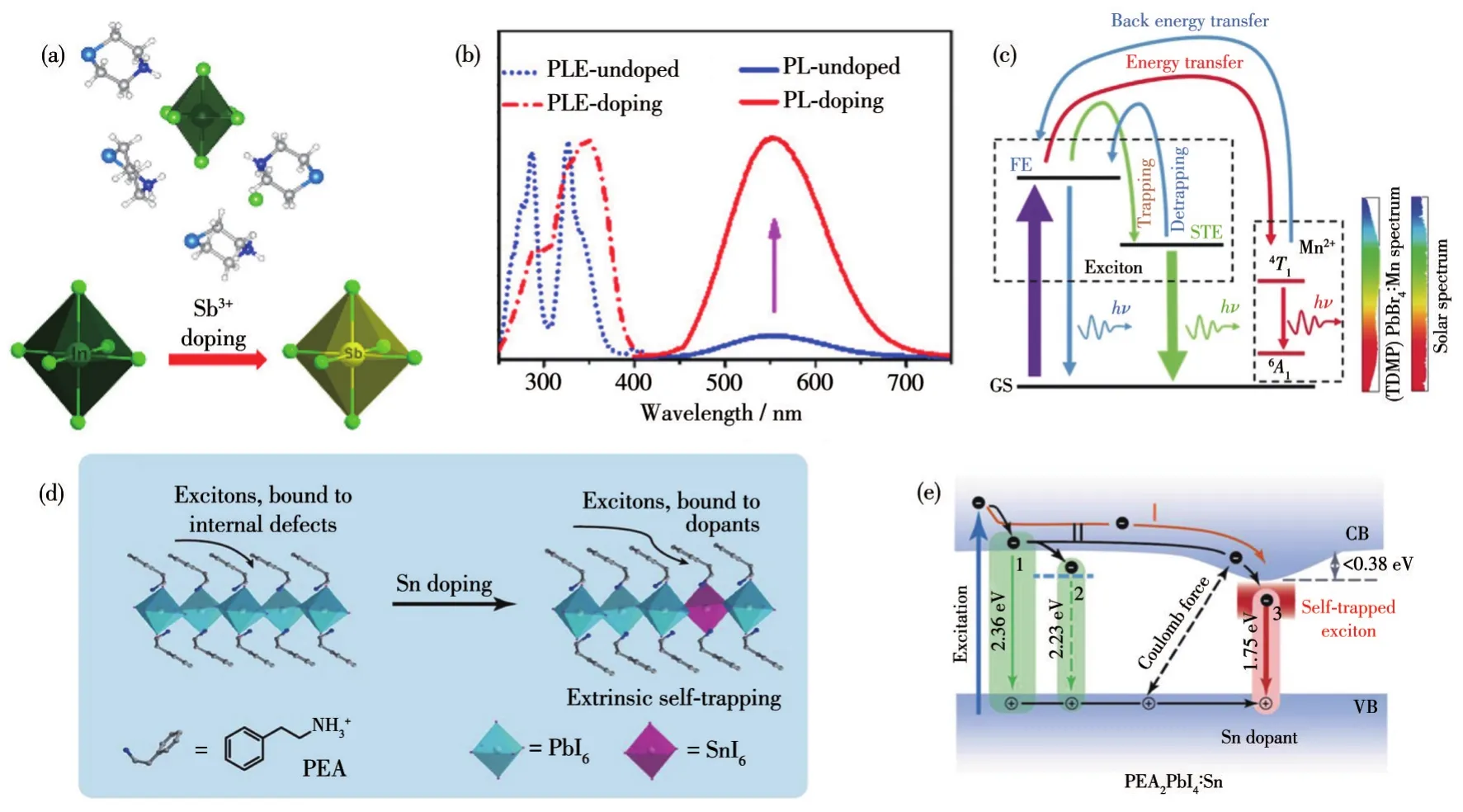
圖10 (a)在InCl6(C4H10SN)4·Cl中進行Sb3+摻雜的替代過程示意圖;(b)Sb3+摻雜和未摻雜InCl6(C4H10SN)4·Cl的穩態光譜圖[97];(c)(TDMP)PbBr4∶Mn的發光機理[31];(d)未摻雜和摻雜Sn的2D鈣鈦礦晶體中的激子捕獲示意圖;(e)Sn摻雜(PEA)2PbI4輻射通道示意圖[108]Fig.10 (a)Schematic diagram of the substitution process for Sb3+doping in InCl6(C4H10SN)4·Cl;(b)Steady-state spectra of Sb3+doped and undoped InCl6(C4H10SN)4·Cl[97];(c)Mechanism of luminescence for(TDMP)PbBr4∶Mn[31];(d)Schematic illustration of exciton trapping in undoped and Sn-doped 2D perovskite crystals;(e)Schematic illustration of radiative channels in Sn-doped 2D perovskites[108]
3.3 改變配位多面體之間的距離
通過選擇有機陽離子增加Mn-Mn之間的距離[72,109-110],減少能量轉移,可實現高效發光(圖11a、11b)。也有研究表明,并不是距離越遠越好,Mn-Mn距離增加到0.925 4 nm,其PLQY達到最大,之后隨距離增加其PLQY反而開始降低[111]。
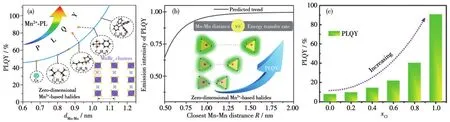
圖11 (a)所選的0D Mn2+基金屬鹵化物的最近Mn-Mn距離和PLQY的圖示;(b)預測0D Mn2+基金屬鹵化物中Mn2+的發射強度與最近Mn-Mn距離的依賴關系[109];(c)Cl元素含量與PLQY變化之間的關系[112]Fig.11 (a)Illustration of the closest Mn-Mn distance and PLQY for the selected 0D Mn2+-based metal halides;(b)Predicted dependences of the emission intensity of Mn2+on the closest Mn-Mn distance in 0D Mn2+-based metal halides[109];(c)Relationship between the content of Cl element and the change of PLQY[112]
3.4 鹵素替代
對于雜化金屬鹵化物發光材料而言,其發光主要來自無機結構[BX6]2-、[BX4]2-等,隨著B位置上金屬離子不同,PLQY會發生改變;同樣其配位鹵素發生改變,也會嚴重地影響發光基團,從而影響PLQY[10]。如圖11c所示,Xia課題組[112]報道隨著(C9NH20)9Pb3Zn2Br19(1-x)Clx(x=0~1)中x的增加其發射峰位不斷藍移,同時PLQY從8%增加到91%。其中隨著Cl含量的增加,熱輔助非輻射復合作用減弱,產生更有效的輻射躍遷通道,最終使PLQY增強。
4 穩定性
對于OIMHs而言,其穩定性是制約發展的關鍵,目前并未形成可以提高其穩定性的統一理論。針對A位而言,引入大的含硫有機陽離子與中心金屬陽離子進行有機構筑,其中陽離子半徑需要大于Cs、MA和FA,其形成的化合物更傾向生成低維度結構,結構維度的降低可以提高化合物的穩定性。對于金屬離子而言,目前穩定性較高的是Sn4+,此前Lin課題組[53]合成出的(C6N2H16Cl)2SnCl6在高達523 K(250℃)的溫度下表現出顯著的空氣和熱穩定性。He課題組[113]合成的(C8H22Cl)2SnCl6在高溫(>200 ℃)和高濕度(相對濕度大于70%)下均表現出顯著的結構穩定性。其他金屬離子也用于合成有高穩定性的化合物,如 (TMA)2SbCl5·DMF[114]、[H2DABCO][Ag2Br4(DABCO)][64]、MEA(MnBr4)2(MEA=((CH3)4N)((C2H5)4N)2·NH4)[115]、(C24H20P)2MnBr4[71]等。
5 總結與展望
本文主要總結了高效的OIMHs,按照B位金屬陽離子的不同電子特征進行分類(ns2、d10、d5),當前研究顯示仍然是ns2系列OIMHs的PLQY最高,Pb2+的毒性制約了其進一步發展,Sn2+基材料中高效發光的較多,但是其室溫穩定性問題阻礙了其應用的步伐。d10系列金屬陽離子最為豐富,每種金屬陽離子都有不同的特性,豐富了OIMHs的光學性能。d5系列的Mn2+可以形成分立發光中心,正在成為單中心金屬陽離子、多中心金屬陽離子以及摻雜OIMHs爭相研究的重點。不同類型的發光材料,其發光機理不盡相同,目前比較認可的機理主要包括:STE發光、ns2孤對電子發光、Mn2+的孤立發光中心以及混合發光機理。其中在低維的金屬鹵化物研究中,仍以STE發光為主。d10系列化合物中的寬帶發射機理尚不清楚,當前主要使用STE模型進行解釋。為了制備出更加高效的發光材料,通常會嘗試使用降低結構維度、摻雜、調整發光中心之間的距離以及鹵素共取代等措施,產生寬帶發射同時提高PLQY。這些材料的持續開發將推動OIMHs發光材料領域新一輪的研究熱潮并最終促進其商業應用。
然而,合成高效的OIMHs發光材料的未來發展仍然面臨許多挑戰,包括但不局限于:
(1)熱穩定性。雖然目前已經合成了高效率的發光材料,但是隨著溫度的升高,其PLQY就會驟降(熱猝滅)。提高其在70℃左右(商業LED表面溫度)的熱猝滅性能是實現其商業化的關鍵一步。
(2)有機物對PLQY的影響尚不清楚。即使是相同的金屬陽離子,當有機陽離子不同時,其PLQY也不盡相同。
(3)實現單一組分白光發射仍然存在困難,目前通過調整多中心金屬陽離子可以實現白光發射,但是其PLQY比較低。
(4)對于d10系列的金屬陽離子研究還較少,其發光機理仍不清楚,此方面還需要更多的理論研究。
- 無機化學學報的其它文章
- La-Doped BaSnO3/Multi-walled Carbon Nanotube Modified Separator:Synthesis and Application in Lithium-Sulfur Battery
- Co(Ⅱ)/Ni(Ⅱ) Coordination Polymer of Isomeric Terphenyl-2,2″,4,4″-tetracarboxylic Acids with a Single Water Bridge:Syntheses,Structures,and Magnetic Properties
- Micromotors Based on Ni-Mn Binary Oxide and Its Application for Effective Dye Adsorption
- Direct Synthesis of Dimethyl Carbonate from CO2 and Methanol by Mg-Doped Ceria Monolithic Catalyst
- Hydrogen Storage Capabilities of the Low-Lying Ca2B4Clusters
- 盤狀鏑簇合物的合成及緩慢磁弛豫

