國家藥品集中采購對3 種抗腫瘤藥物臨床使用的影響*
萬 茜,王 晶,顧申勇
(復(fù)旦大學(xué)附屬中山醫(yī)院青浦分院藥劑科,上海 201700)
世界衛(wèi)生組織國際癌癥研究機(jī)構(gòu)發(fā)布的2020年癌癥負(fù)擔(dān)數(shù)據(jù)顯示,全球新發(fā)癌癥病例1 929 萬例,死亡996 萬例,其中我國分別為 457 萬例、300 萬例。且惡性腫瘤死亡人數(shù)占我國居民全部死因的30%,居致死性疾病之首。抗腫瘤藥物可延長患者的生存期,改善其生活質(zhì)量,但昂貴的藥價大幅增加患者的經(jīng)濟(jì)負(fù)擔(dān)[1]。為了降低醫(yī)療開支,控制藥品費用,經(jīng)國家醫(yī)療保障局批準(zhǔn),《4+7城市藥品集中采購文件》于2018年11月15日正式發(fā)布(上海市于2019 年3 月20 日起正式執(zhí)行),共25 種藥品中標(biāo),通過以“量”換“價”的方式,達(dá)到合理降低藥品費用的目的[2]。在此,基于上海市某三級綜合醫(yī)院數(shù)據(jù),分析第一批國家集中采購(簡稱集采)中標(biāo)品種中的抗腫瘤藥物吉非替尼片、甲磺酸伊馬替尼片、注射手培美曲塞二鈉在集采政策實施前后使用情況的變化,以期了解集采政策對這3種藥品的價格、可負(fù)擔(dān)性、使用量的影響,為下一步的政策制訂提供參考。
1 對象與方法
1.1 研究對象
選擇目標(biāo)藥物為吉非替尼片(口服常釋劑型)、甲磺酸伊馬替尼片(口服常釋劑型)及注射用培美曲塞二鈉(注射劑型)。藥品的品規(guī)及價格信息來源于上海市醫(yī)藥采購服務(wù)與監(jiān)管信息系統(tǒng),納入統(tǒng)計品種數(shù):吉非替尼片,原研1 品規(guī)(中選),仿制3 品規(guī);甲磺酸伊馬替尼片,原研1 品規(guī),仿制2 品規(guī)(中選1 品規(guī));注射用培美曲塞二鈉原研2 品規(guī),仿制12 品規(guī)(中選2 品規(guī))。藥品的使用數(shù)據(jù)來源于某三級綜合醫(yī)院信息系統(tǒng),分別調(diào)取集采政策實施前1 年內(nèi)(2018 年3 月20 日至2019年3月19日)、集采政策實施后第1年(2019年3月20日至 2020 年 3 月 19 日),以及集采政策實施后第 2 年(2020 年 3 月 20 日至 2021 年 3 月 19 日)上述 3 種抗腫瘤藥物的用藥數(shù)據(jù),包括藥品消耗量、銷售金額等。
1.2 方法
利用限定日劑量(DDD)法可消除因藥品銷售價格、包裝變化等產(chǎn)生的影響,相比于藥品價格、銷售金額和消耗量指標(biāo)更合理,可較好地反映藥物的使用情況。本研究中各藥的DDD 值根據(jù)上海市衛(wèi)生健康委員會醫(yī)政處《關(guān)于報送國家集中采購藥品相關(guān)監(jiān)測數(shù)據(jù)的通知》所附藥品費用結(jié)構(gòu)監(jiān)測表及相關(guān)藥品說明書確定[3]。并結(jié)合以下指標(biāo)判定用藥情況。
用藥頻度(DDDs),DDDs = 某藥品的消耗總劑量(mg)/該藥DDD 值(mg),反映某藥的使用人數(shù)和人均使用頻率,該值越大表明該藥使用頻率越高[4]。日均費用(DDC),DDC=某藥品的銷售額/該藥DDDs,反映某藥的價格水平,該值越小表明該藥的藥物經(jīng)濟(jì)學(xué)情況越好[5]。其中原研藥和仿制藥DDC 是所有原研或仿制藥DDC的加權(quán)平均價格。
采用世界衛(wèi)生組織/ 國際健康行動機(jī)構(gòu)(WHO/HAI)標(biāo)準(zhǔn)調(diào)查法[6]評價3種藥物的可負(fù)擔(dān)性,考慮到腫瘤治療的療程及用藥周期較長,本研究中參考文獻(xiàn)[7]改進(jìn)該法,計算得出3 種藥品使用21 d 費用,并換算為相當(dāng)于上海市每月最低工資標(biāo)準(zhǔn)[上海市人力資源和社會保障局《關(guān)于調(diào)整本市最低工資標(biāo)準(zhǔn)的通知》(滬人社規(guī)〔2019〕5 號)顯示,2019 年該值為2 480 元]的倍數(shù),<1記為可負(fù)擔(dān),≥1記為不可負(fù)擔(dān)。
2 結(jié)果
2.1 價格
國家集采政策實施前后目標(biāo)藥品(含原研藥和仿制藥)的DDC見表1。
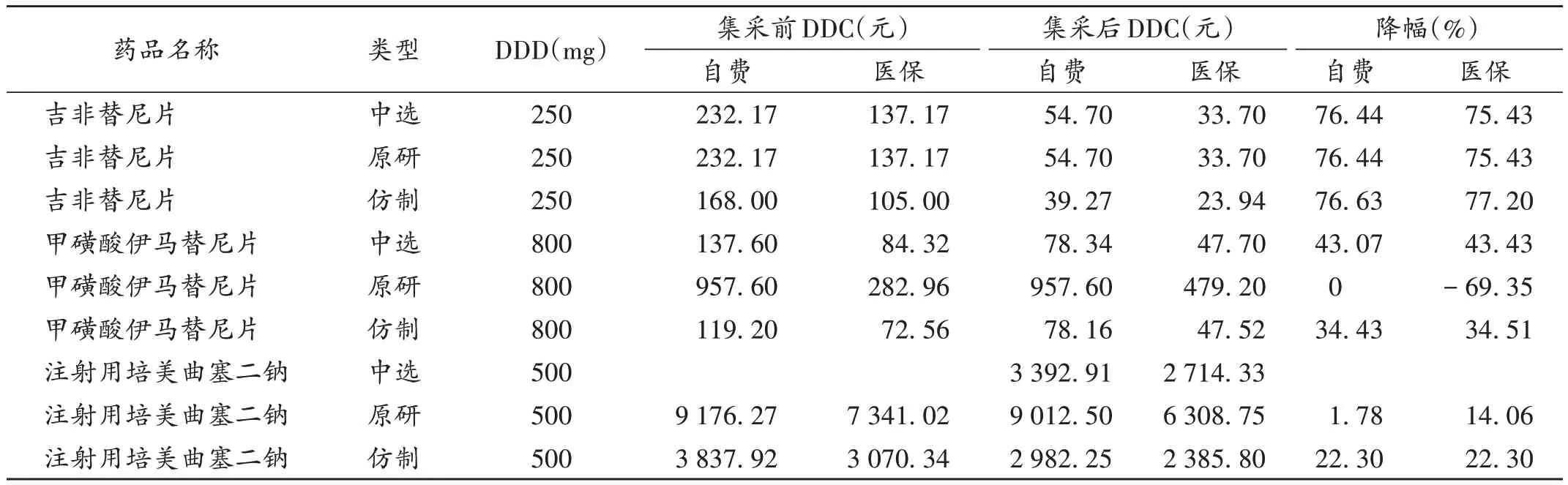
表1 國家藥品集采實施前后抗腫瘤藥物DDCTab.1 DDC of anti-tumor drugs before and after implementation of the NCDP policy
可見,3 種抗腫瘤藥物的DDC 均呈降低趨勢,其中吉非替尼片自費及醫(yī)保支付金額降幅均最大。相比于仿制藥,原研藥的DDC 降幅較小,特別是甲磺酸伊馬替尼片及注射用培美曲塞二鈉的原研藥DDC 均未見明顯降低。集采政策實施后,吉非替尼片和甲磺酸伊馬替尼片中標(biāo)品種與仿制藥中醫(yī)保基金支付金額同比例下降,原研藥的降幅相對較弱,而甲磺酸伊馬替尼片的醫(yī)保基金支付金額不僅未下降,反而大幅上升。
2.2 可負(fù)擔(dān)性
前述價格影響分析中發(fā)現(xiàn),中標(biāo)品種與仿制藥的價格降幅基本一致,故在可負(fù)擔(dān)性評價中,僅統(tǒng)計原研和仿制2 種類型。3 種抗腫瘤藥物的可負(fù)擔(dān)性結(jié)果見表2。可知,對于自費患者,集采政策實施前原研藥或仿制藥均不可負(fù)擔(dān),集采政策實施后3種抗腫瘤藥物的可負(fù)擔(dān)性大幅提高,但甲磺酸伊馬替尼片和注射用培美曲塞二鈉的原研藥仍不可負(fù)擔(dān)。國家醫(yī)療保障局《關(guān)于國家組織藥品集中采購和使用試點醫(yī)保配套措施的意見》(醫(yī)保發(fā)〔2019〕18 號)顯示,非中標(biāo)的“價高藥”自付比例提升。這導(dǎo)致了原研的注射用培美曲塞二鈉在集采政策實施后增加了醫(yī)保患者的負(fù)擔(dān)。
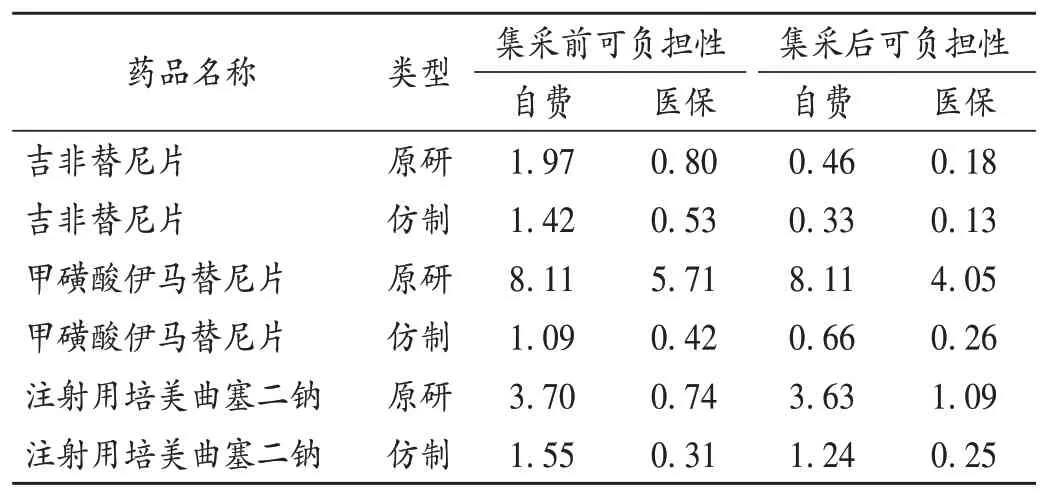
表2 3種抗腫瘤藥物的可負(fù)擔(dān)性Tab.2 Affordability of three anti-tumor drugs
2.3 DDDs
國家集采政策實施前后3 年時間內(nèi),3 種目標(biāo)藥品的DDDs見表3。集采實施后,吉非替尼片和甲磺酸伊馬替尼片的DDDs 顯著增加,中選品種占比均超過85%,其中吉非替尼片集采后1年內(nèi)的DDDs較集采前增加了128.16%。而注射用培美曲塞二鈉的DDDs 漲幅最小,在政策實施首年甚至較政策實施前略有下降,中標(biāo)品種占比不足50%。

表3 國家藥品集采政策實施前后3種抗腫瘤藥物DDDsTab.3 DDDs of anti-tumor drugs before and after implementation of the NCDP policy
3 討論
3.1 仿制藥價格降幅高于原研藥
全球范圍內(nèi),每10 例惡性腫瘤幸存者里就有3 例面臨經(jīng)濟(jì)問題,這導(dǎo)致了其持續(xù)的心理和生理問題。許多腫瘤患者都會因昂貴的治療費用放棄或推遲就醫(yī)、錯過隨訪,而這些均會增加惡性腫瘤復(fù)發(fā)的風(fēng)險[7]。2018 年起我國加快抗癌藥品的準(zhǔn)入,更多抗癌藥品得以進(jìn)入醫(yī)保目錄,更多的患者因此能使用此前望而卻步的創(chuàng)新藥,但藥費依舊讓多數(shù)患者難以負(fù)擔(dān)[8-9]。國家集采政策實施后,中標(biāo)藥品價格降低,帶動了仿制藥價格的降低,進(jìn)一步緩解了患者的經(jīng)濟(jì)負(fù)擔(dān),同時也減少了醫(yī)保基金支出,實現(xiàn)了醫(yī)保“騰籠換鳥”目標(biāo)。從藥品價格分析,非中標(biāo)仿制藥價格低于中標(biāo)品種,而原研品種幾乎無變化,這與國內(nèi)藥企對政策變化的理解力和適應(yīng)力更強(qiáng)有關(guān)。以往不少跨國藥企的原研藥品種在國內(nèi)市場占據(jù)主導(dǎo)地位,非中標(biāo)的仿制藥品種為搶占市場份額,用盡可能低的價格去參與競爭將是主要方向。
3.2 國家集采對抗腫瘤藥使用的影響
吉非替尼片及甲磺酸伊馬替尼片中標(biāo)品種的使用量約為集采政策實施前的2 倍,DDDs 的增長及中標(biāo)品種的使用占比遠(yuǎn)高于其他研究中報道的高血壓和糖尿病治療藥物[10-12]。與高血壓和糖尿病等慢性病的治療相比,腫瘤靶向治療價格昂貴,中標(biāo)與非中標(biāo)品種絕對價格差巨大,患者因為經(jīng)濟(jì)因素更易接受中標(biāo)品種。政策實施后的第2年里,吉非替尼片及甲磺酸伊馬替尼片的用量增速放緩,后者的使用量約與實施后第1 年持平。近10年,全球腫瘤藥物的研發(fā)和生產(chǎn)投入遠(yuǎn)高于其他疾病領(lǐng)域,我國更是如此,特別是肺癌領(lǐng)域與血液系統(tǒng)腫瘤的熱度更高[10]。此外,國家醫(yī)保談判政策的推出,使得更多抗腫瘤創(chuàng)新藥如埃克替尼、安羅替尼、達(dá)沙替尼、奧希替尼等,通過政府談判降低價格納入醫(yī)保,給患者和醫(yī)師更多的選擇,也加劇了藥品間的競爭。
注射用培美曲塞二鈉在集采政策實施前后3 年內(nèi),總用量基本持平,無明顯增長,集采中標(biāo)品種的使用占比還處于下降趨勢。該藥為抗代謝類化學(xué)治療(簡稱化療)藥物,集采前國內(nèi)已有多個廠家仿制上市,其中標(biāo)廠家為當(dāng)時唯一通過一致性評價的廠家。但集采政策實施后,其他廠家為占據(jù)市場份額,主動降價至中標(biāo)價格以下,導(dǎo)致中標(biāo)品種在臨床使用選擇中優(yōu)勢并不明顯,且難以靠價格拉動使用量[11]。另一方面,化療藥為周期性使用,幾乎不存在品牌依賴度,至于使用哪個廠家的藥品,選擇權(quán)在醫(yī)師,患者極少主動指定品牌。因此,政策的落地執(zhí)行還需依靠臨床醫(yī)師的配合。
3.3 藥品集采倒逼醫(yī)藥產(chǎn)銷企業(yè)優(yōu)勝劣汰
藥品集采政策以一致性評價政策為前提,在此背景下,加速一致性評價成為仿制藥企的必要選擇。2012 年,我國《藥品安全“十二五”規(guī)劃》提出,要提高仿制藥質(zhì)量、分期分批開展一致性評價。2016 年3 月,國務(wù)院辦公廳發(fā)布《關(guān)于開展仿制藥質(zhì)量和療效一致性評價的意見》(國辦發(fā)〔2016〕8 號),拉開了藥品提升質(zhì)量價格回歸的序幕。隨著越來越多的仿制藥通過一致性評價,將有更多的仿制藥品參與到集中帶量采購中,藥品價格虛高問題將得到真正的解決。集采政策實施后,上海藥品采購平臺對于通過一致性評價的生產(chǎn)企業(yè)達(dá)到3家及以上的品種暫停采購,減少了同通用名同種劑型仿制藥間的競爭,企業(yè)自主研發(fā)創(chuàng)新的積極性也將進(jìn)一步增強(qiáng)。在藥品集采模式下,市場競爭促使國內(nèi)藥企持續(xù)強(qiáng)化自身核心競爭力,以“量”換“價”亦會有效凈化行業(yè)生態(tài),完善合理價格發(fā)現(xiàn)機(jī)制。

