淺談晶體中八面體空隙和四面體空隙
四川 李小寶 劉 濤
近年高考試題常涉及晶體中八面體空隙和四面體空隙相關內容的考查,如2018年高考全國卷Ⅱ、2019年高考全國卷Ⅰ、2020年高考全國卷Ⅰ、2021年高考遼寧省選擇性考試。實際上教師引導學生在利用硬球接觸的認知模型研究晶體結構的時候,晶體中都會出現八面體空隙和四面體空隙等類型的空隙,教師引導學生研究這些空隙對學生晶體知識關聯的結構化、認識思路的結構化以及促使學生落實化學學科的核心觀念有著重要意義。內容的結構化是促進學生從化學學科知識向化學學科核心素養轉化的關鍵。本文結合筆者對近幾年高考題的研究,梳理分析晶體八面體空隙和四面體空隙的相關內容,以期為晶體相關內容的結構化提供參考。
一、晶體中八面體空隙和四面體空隙的基本知識
晶體空隙的基本知識是關聯知識結構化的基礎。如圖1和圖2所示,面心立方最密堆積(ccp結構)、六方最密堆積(hcp結構)和體心立方結構(bcp結構)的晶胞中均會出現八面體空隙和四面體空隙。面心立方最密堆積(ccp結構)和六方最密堆積(hcp結構)的每個晶胞均攤到4個八面體空隙和8個四面體空隙。ccp結構和hcp結構中的四面體和八面體結構是規則的,但由于ccp結構和hcp結構中的小球相對位置不同,結構中的空隙的大小也不相同。

圖1


圖2
在2018年高考全國卷Ⅱ35題和2021年遼寧省選擇性考試第7題就考查了ccp結構中的八面體空隙大小。

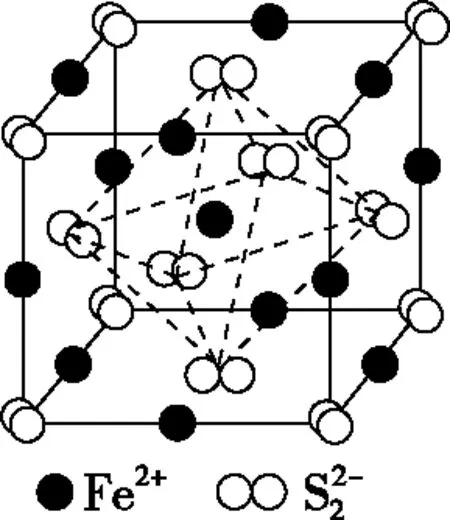
圖3

【例2】(2021·遼寧省選擇性考試·7)單質硫和氫氣在低溫高壓下可形成一種新型超導材料,其晶胞如圖4所示。下列說法錯誤的是
( )

圖4
A.S位于元素周期表p區
B.該物質的化學式為H3S
C.S位于H構成的八面體空隙中
D.該晶體屬于分子晶體
【參考答案】D
【分析】圖4中S原子確實位于H原子構成的八面體空隙內,所以C正確。雖然不論在2020年版人教版高中化學新教材必修2《物質結構與性質》還是在2009年版人教版高中化學教材選修3《物質結構與性質》中均有“所有非金屬氫化物”屬于分子晶體的闡述,但能導電不是分子晶體性質,綜合前面的選項可認為D錯誤,所以本題選D。本題在考查晶體類型的判別,對晶體的空隙的理解上體現了中國高考評價體系“四翼”中“創新性”中強調的創新意識和創新思維以及“綜合性”中強調的融會貫通。
二、晶體中八面體或四面體空隙的穩定性和離子晶體的配位數密切相關

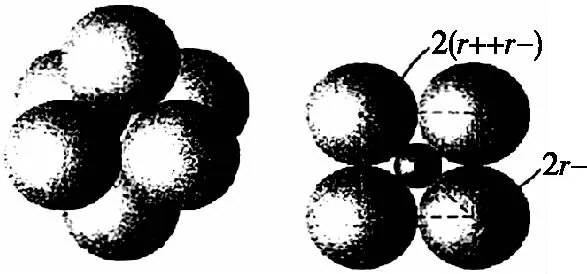
正負離子和負負離子均相互接觸的八面體
代表性晶胞NaCl晶胞就可以看成是Cl-為ccp堆積,Na+填充在Cl-形成的八面體空隙中,填充率為100%。CaF2晶胞可看成是Ca2+為ccp堆積,F-填充全部的8個四面體空隙,填充率為100%,若陰、陽離子的排列方法恰恰與螢石結構相反,則該結構為反螢石結構,如在研究2018年高考全國卷Ⅰ35題中的Li2O晶胞時,就可把O2-看作ccp堆積,Li+填充全部的8個四面體空隙,填充率為100%。需注意空隙的填充率不一定都是100%,如立方ZnS晶胞則可看成是S2-做ccp堆積,Zn2+填充在一半的四面體空隙中,填充率為50%。如圖6所示。教師應引導學生對于晶胞堆積模型理解透徹,靈活變通。

圖6
【例3】(2017·全國卷Ⅲ·35節選)(5)MgO具有NaCl型結構(如圖7所示),其中陰離子采用面心立方最密堆積方式,X射線衍射實驗測得MgO的晶胞參數為a=0.420 nm,則r(O2-)為________nm。MnO也屬于NaCl型結構,晶胞參數為a′=0.448 nm,則r(Mn2+)為________nm。

圖7
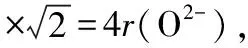

圖8
三、晶體中八面體或四面體空隙填充復雜單元的現象
研究晶體中八面體或四面體空隙填充復雜單元的現象涉及的問題可促進學生認識思路的結構化,對學生建構和形成化學學科的核心觀念有著重要意義。晶體的八面體或四面體空隙不一定填充的是一個原子或離子,這些空隙也可看成填充的是其他結構單元。
【例4】(2019·全國卷Ⅰ·35節選)(4)圖9(a)是MgCu2的拉維斯結構,Mg以金剛石方式堆積,八面體空隙和半數的四面體空隙中,填入以四面體方式排列的Cu。圖9(b)是沿立方格子對角面取得的截圖。可見,Cu原子之間最短距離x=________pm,Mg原子之間最短距離y=________pm。

(a)
【參考答案及解析】解答本題更需要學生掌握離子晶體空隙填充的知識。Mg以金剛石方式堆積,可以認為Mg以ccp結構堆積,形成4個八面體空隙和8個四面體空隙,且Mg原子自身占據4個四面體空隙,一共有8個Mg原子。晶體中剩余的4個八面體空隙和4個四面體空隙填充的是4個Cu原子構成的正四面體結構,注意此時的每個4個Cu原子構成的正四面體結構的頂點Cu原子均為兩個4個Cu原子構成的正四面體結構共有,意味著均攤后Mg形成的每個八面體空隙或四面體空隙中只填充了2個Cu原子,最終晶體中剩余的8個空隙填充了16個Cu原子,所以其化學式為MgCu2。
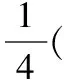

(a)


(a)
四、Li離子電池的電池材料常涉及晶體中的八面體或四面體空隙知識
在“碳達峰”“碳中和”的背景下,Li離子電池備受關注,而Li離子電池的材料常常涉及晶體的八面體或四面體空隙知識,這些晶體的八面體或四面體空隙的填充內容和連接方式一般比較復雜,這些問題情境往往是高考需要的復雜學習探索情境。如2020年全國卷Ⅰ35題就提及了鈷酸鋰、磷酸鐵鋰電池正極材料。如圖12所示橄欖石結構的LiFePO4晶體中的O原子為六方最密堆積方式排列,P原子占據O原子的四面體空隙,形成PO4結構,Fe原子和Li原子占據O原子的八面體空隙,形成FeO6八面體結構和LiO6八面體結構。每個FeO6八面體結構與兩個LiO6八面體結構和一個PO4四面體結構共邊,而每個PO4四面體結構與一個FeO6八面體結構和兩個LiO6八面體結構共邊,同一平面上相鄰的FeO6八面體共用一個O原子從而形成Z字形的FeO6層。在FeO6八面體結構層之間,相鄰的LiO6八面體結構通過兩個O原子連接。

LiFePO4結構示意圖
該題中提及的鈷酸鋰中同樣有八面體空隙,如圖13所示,其結構為氧離子作ABCABC的立方堆積,鋰離子和鈷離子交替占據立方密堆積的八面體。另外,科研人員在研究單斜晶系的Li1+xV3O8、正交結構的Li2MnSO4和尖晶石結構的LiMn2O4等Li離子電池的結構時都涉及晶體的四面體空隙或八面體空隙的填充。
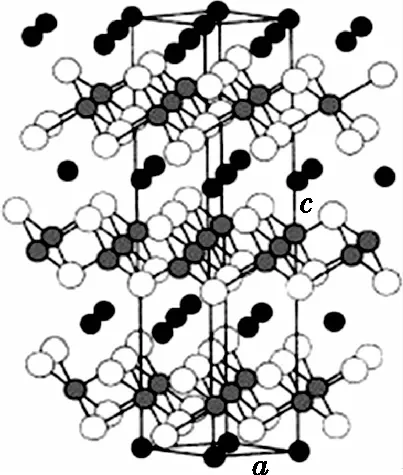
LiCoO2的結構,白色小球代表O離子
五、總結反思與教學建議


