補中益氣湯聯合生物電刺激治療對產后盆底康復療效研究
鄭永明,王一楠,閆冰瑩,吳云霞,劉素蘭
(蚌埠市第一人民醫院,安徽 蚌埠 233099)
盆底功能障礙性疾病(pelvic floordys function,PFD)是指因盆底支持結構缺陷、損傷及功能障礙造成的疾患[1],臨床多表現為盆腔器官脫垂、尿失禁、糞失禁和性功能障礙等,已被臨床公認為影響人類生活質量的五大慢性病之一。研究表明[2],妊娠和分娩是導致其獨立危險因素,產后42天至產后半年是盆底康復治療的最佳時間,若恢復不理想,可引發FPD,嚴重危害女性健康。目前,臨床常采用盆底肌肉鍛煉、生物反饋治療、電刺激等方法,操作簡便,安全有效,不會造成新的損傷,但患者因無法準確識別以及自主收縮盆底肌肉,療程長,依從性差,導致盆底功能恢復不佳,影響預后[3]。因此,如何促進PFD 患者盆底功能的恢復,對于改善患者預后具有重要意義。中醫認為PFD屬“陰挺”范疇,中氣不足、體虛、氣虛、腎虛為其發病氣機,故應以補中益氣、補腎溫陽作為主要治療原則。基于此,本研究擬在生物電刺激治療的基礎上,聯合補中益氣湯,觀察產后盆底康復臨床治療效果,以期為中西醫結合治療產后PFD 提供可靠的臨床依據。
1 資料與方法
1.1 一般資料 選取本院2021 年1~12 月收治的產后PFD 患者90 例,按照隨機數字表法分為觀察組和對照組各45例。觀察組年齡22~35(25.13±1.35)歲,產后天數(43.58±3.67)天,BMI(21.58±1.67)kg/m2,盆底肌力分級:0 級9 例,I級8 例,Ⅱ級12 例,Ⅲ級18 例;疾病類型:尿失禁35 例,子宮脫垂30 例,性功能障礙28例;對照組年齡21~36(25.18±1.42)歲,產后天數(43.21±3.62)天,BMI(21.63±1.57)kg/m2,盆底肌力分級:0級8例,I級16例,Ⅱ級33例,Ⅲ級36 例。疾病類型:尿失禁37 例,子宮脫垂29 例,性功能障礙27 例;本研究已經本院醫學倫理委員會批準。兩組年齡、疾病類型及盆底肌力分級方面差異無統計學意義(P>0.05)。
1.2 納入標準 符合《婦產科學》[4]中關于PFD 診斷標準;初產婦,足月分娩,頭位,陰道試產已過第一產程活躍期;年齡18~40 歲,產后42~180 天;患者知情并簽署知情同意書者。
1.3 排除標準 經產婦、多胎或過期妊娠,胎位異常,分娩時現頭盆不稱,胎盤早剝,先兆子癇等;神經系統疾病者;泌尿系統發生感染與畸形者;有治療依從性較差者。
1.4 方法
1.4.1 生物電刺激 患者排空膀胱,平臥位,放松,采用生物反饋電刺激治療儀(廣州杉山,型號:PHENIXUSB4),將消毒過的探頭放入患者陰道內,以脈寬250μs、頻率50Hz,電流大小以患者耐受為度,喚醒其淺層及深層肌肉收縮本體感覺。給患者脈寬320~740μs、頻率8~32Hz 生物電刺激掌握I類肌纖維收縮,收縮10s,放松15s;給患者脈寬20~320μs、頻率20~80Hz生物電刺激掌握Ⅱ類肌纖維收縮,收縮4s,放松10s。患者根據計算機語音提示和肌電曲線不斷收縮、放松盆底肌群,當收縮肌電值達到電刺激閾值時,就會給予電刺激。先進行I 類肌纖維訓練,然后進行II 類肌纖維訓練,最后交替進行訓練。每次30min,每周2 次,每個療程10 次,共進行2個療程。
1.4.2 補中益氣湯 處方:黃芪18g,黨參16g,白術12g,炙甘草8g,陳皮12g,當歸18g,升麻12g,川芎12g,益母草18g,山萸肉10g,川斷15g,益智仁10g,訶子10g,用水300mL,煎至150mL,去滓,空腹時稍熱服,1劑/d,早晚服用,1周為1個療程,共治療2個療程。
1.5 觀察指標
1.5.1 手測盆底肌力(OxfordScale 評分法)[5]0 分,無收縮反應;1 分,偶爾會出現收縮反應,收縮不正常;2分,輕微收縮,力小;3分,有輕度壓迫及上提,普通收縮;4 分,壓迫及內縮明顯上提,收縮力正常;5分,收縮力強,肌肉群正常。
1.5.2 肌電活動、疲勞度 采用廣州杉山PHENIXUSB4 肌電活動和疲勞度,肌電活動以點位平均值表示,疲勞度以每秒肌力下降百分比表示。
1.5.3 尿失禁問卷表簡表(ICI-Q-SF)評分[6]總分21分,包含漏尿頻率、漏尿量及漏尿影響3大項,分數越高,尿失禁程度越嚴重。
1.5.4 盆腔脫垂分期[7]根據國際尿控協會盆腔器官脫垂定量分期法(POP-Q)評估盆腔臟器脫垂的程度,I 度為脫垂最遠處在處女膜內,距離處女膜>1cm;II度為脫垂最遠處在處女膜邊緣1cm內外;III度為脫垂至處女膜外邊緣1~2cm;IV 度為陰道完全或幾乎完全脫垂,脫垂最遠處≥2cm。
1.5.5 產后性功能[8]應用盆腔器官脫垂一尿失禁性功能問卷(PISQ-12)評估性生活質量,得分越高質量越高。
1.5.6 中醫癥候積分[9]根據《中醫新藥臨床研究指導原則》對受試者進行中醫證候量化評分,氣虛癥狀:神疲、氣短、自汗、乏力及懶言,癥狀較輕者計2分,中計4分,癥狀較重者計6分。
2 結果
2.1 手測盆底肌力 治療前,兩組患者的手測盆底肌力差異無統計學意義(P>0.05)。治療后,兩組患者的手測盆底肌力均較治療前升高(P<0.05),且觀察組治療后的手測盆底肌力顯著高于對照組(P<0.05)。見表1。
表1 兩組患者治療前后手測盆底肌力比較(± s)

表1 兩組患者治療前后手測盆底肌力比較(± s)
注:與治療前比較,①P<0.05;與對照組比較,②P<0.05
手測肌力(級)1.58±0.54 4.25±0.72①②1.78±0.62 3.16±0.72①組別觀察組對照組例數45 45時間治療前治療后治療前治療后
2.2 肌電活動、疲勞度 治療前,兩組患者的肌電活動、疲勞度差異無統計學意義(P>0.05)。治療后,兩組患者的肌電活動較治療前升高(P<0.05),疲勞度較治療前降低(P<0.05),且觀察組治療后的肌電活動、疲勞度顯著優于對照組(P<0.05)。見表2。
表2 兩組患者治療前后肌電活動和疲勞度比較(± s)
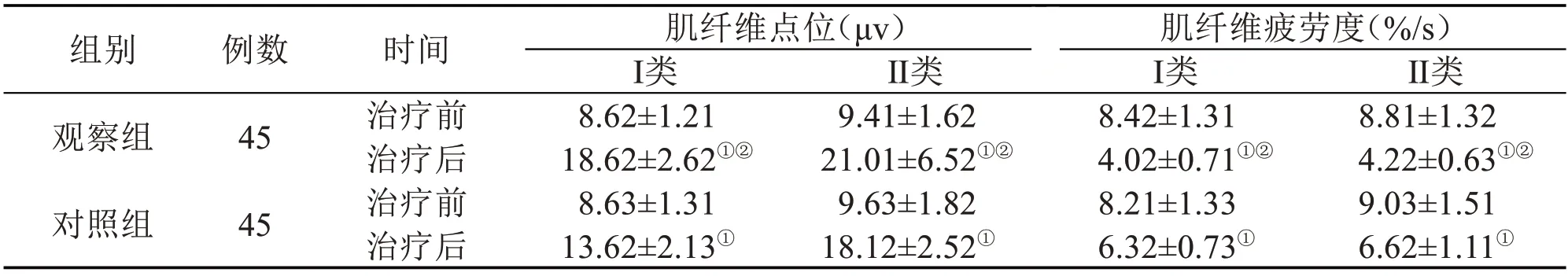
表2 兩組患者治療前后肌電活動和疲勞度比較(± s)
注:與治療前比較,①P<0.05;與對照組比較,②P<0.05
組別觀察組對照組例數45 45時間治療前治療后治療前治療后肌纖維點位(μv)I類8.62±1.21 18.62±2.62①②8.63±1.31 13.62±2.13①Ⅱ類9.41±1.62 21.01±6.52①②9.63±1.82 18.12±2.52①肌纖維疲勞度(%/s)I類8.42±1.31 4.02±0.71①②8.21±1.33 6.32±0.73①Ⅱ類8.81±1.32 4.22±0.63①②9.03±1.51 6.62±1.11①
2.3 ICI-Q-SF、POP-Q、性功能障礙評分 治療前,兩組患者的ICI-Q-SF、POP-Q、PISQ-12 差異無統計學意義(P>0.05)。治療后,兩組患者的ICI-QSF、POP-Q 均較治療前降低(P<0.05),PISQ-12 均較治療前升高(P<0.05),且觀察組治療后的ICIQ-SF、POP-Q 顯著低于對照組(P<0.05),PISQ-12高于對照組(P<0.05)。見表3。
表3 兩組患者治療前后ICI-Q-SF、POP-Q、PISQ-12比較(± s)

表3 兩組患者治療前后ICI-Q-SF、POP-Q、PISQ-12比較(± s)
注:與治療前比較,①P<0.05;與對照組比較,②P<0.05
組別觀察組對照組例數45 45時間治療前治療后治療前治療后ICI-Q-SF(分)15.33±3.57 8.56±2.51①②15.42±3.44 10.78±3.01①POP-Q(度)1.86±0.22 0.75±0.16①②1.84±0.24 1.05±0.20①PISQ-12(分)23.53±7.61 41.52±17.73①②23.51±6.67 32.54±17.74①
2.4 中醫癥候積分 治療前,兩組患者的中醫證候各項積分差異無統計學意義(P>0.05)。治療后,兩組患者的中醫證候各項積分均較治療前降低(P<0.05),且觀察組治療后的神疲、氣短、自汗評分及總積分顯著低于對照組(P<0.05)。見表4。
表4 兩組患者治療前后中醫證候積分比較(± s)
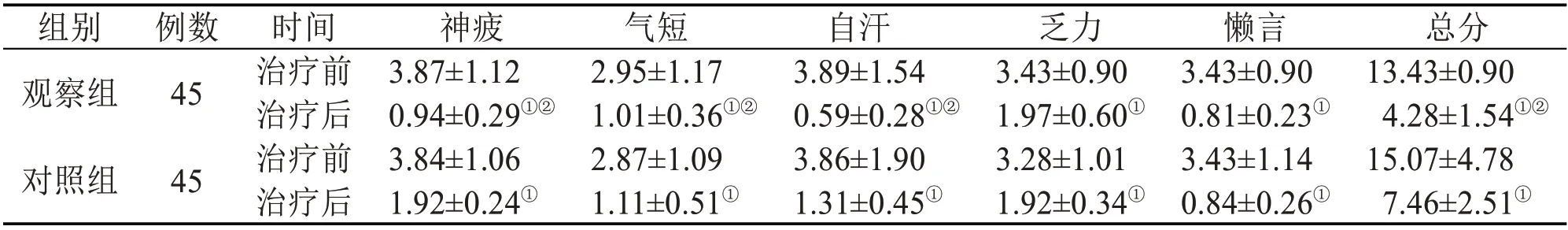
表4 兩組患者治療前后中醫證候積分比較(± s)
注:與治療前比較,①P<0.05;與對照組比較,②P<0.05
組別觀察組對照組總分13.43±0.90 4.28±1.54①②15.07±4.78 7.46±2.51①例數45 45時間治療前治療后治療前治療后神疲3.87±1.12 0.94±0.29①②3.84±1.06 1.92±0.24①氣短2.95±1.17 1.01±0.36①②2.87±1.09 1.11±0.51①自汗3.89±1.54 0.59±0.28①②3.86±1.90 1.31±0.45①乏力3.43±0.90 1.97±0.60①3.28±1.01 1.92±0.34①懶言3.43±0.90 0.81±0.23①3.43±1.14 0.84±0.26①
3 討論
女性盆底功能障礙性疾病目前發病機制尚不明確,多種因素錯綜復雜,其中妊娠、分娩時對運動祌經、肌肉和結締組織的損傷是導致PFD 產生最主要原因,其影響最大,持續作用時間最長。女性盆底肌肉是維持子宮、膀胱、直腸等盆腔器官正常解剖位置和形態的重要肌肉之一,可維持陰道肌肉緊張,促進排尿、排便[10]。妊娠期間體內激素水平的變化,子宮因胎兒發育造成的盆底組織、肌肉、筋膜過度伸展導致損傷、斷裂,以及分娩產力的加大,都不可避免對盆底肌肉功能造成受損、陰道松弛,進而導致PFD 的發生。尤其是隨著“三胎”政策的放開,女性妊娠及分娩次數增加,產后PFD 的發病率進一步上升,可以說其已成為影響婦女身心健康及生活質量的重要公共衛生疾病之一。因此,及時有效的盆底肌康復治療對PFD的發生具有重要意義。
目前臨床上主要采用生物電刺激等物理治療,擬通過物理刺激來恢復肌肉張力。生物電刺激療法是一種新的物理因子治療方法,其通過設置不同的頻率和脈寬,放置陰道電極來刺激盆底神經和肌肉,提高盆底肌群以及尿道周圍橫紋肌的收縮能力,促進尿道和膀胱頸的支持作用。該治療不僅可以增強盆底肌肉收縮彈性和強度,還可以通過專業設備模擬視覺或聽覺信號,通過圖式使患者及時獲得治療反饋信息,幫助患者更準確、及時地控制盆底肌肉收縮訓練,從而加強治療效果[11]。另外,其還可以通過促進排尿中心的反饋機制來穩定膀胱逼尿肌,以達到治療壓力性尿失禁的目的[12]。但因患者無法準確識別和自主收縮盆底肌肉,且無法堅持長期治療,導致盆底功能恢復不佳,影響預后。因此近年來,不少學者都提出了以中西醫結合治療盆底功能障礙性疾病的理念。
中醫認為PFD 屬“產后小便不禁(失禁)”、“陰挺”、“產腸不收”等范疇,病位在膀胱,與腎氣不固、脾氣下陷關系密切。《婦人大全良方》認為“產理不順,致傷膀胱”導致產后“遺尿無時”,《景岳全書》中記載“婦人……陰挺,此或因胞絡損傷……或因氣虛下脫。”,故中醫認為其病機主要在于脾腎氣虛和產傷胞絡,病位在脾、腎、胞絡,與素體虛弱、胎氣久壓、產時耗氣傷血或產程過長耗傷正氣有關,,妊娠、分娩耗氣動血,產后盆底功能障礙性疾病多以“虛”為本,因氣虛致固攝失調,因虛致陷,因陷致脫,主要癥候為壓力性尿失禁,伴有神疲、氣短、乏力、自汗、懶言等氣虛表現,部分患者兼有眩暈等癥狀。根據“虛則補之,實則瀉之”,故當以補中益氣固攝。
補中益氣湯出自金代名醫李東垣的《脾胃論》,具有補中健脾益氣、升陽舉陷的作用。黃芪為君藥,甘微溫,益氣健脾。黨參甘平,補中益氣,養血;白術味苦甘溫,健脾益氣,燥濕利水,止汗;炙甘草和中緩急,益氣補中又調和諸藥三藥共為臣藥,合用既補中益氣,又除水濕。陳皮辛散苦降而溫,理氣健脾,調中,燥濕,補而不滯;當歸甘補辛散溫通,營血和營;二藥共為佐藥。柴胡苦辛微寒,升提下陷;升麻辛微甘性涼,升散清泄;二藥共為使藥,助君藥升舉下陷之清陽。益母草、川芎調和,共奏補中益氣、升陽舉陷之效;同時,輔以益智仁、訶子、山萸肉、川斷補腎溫陽固脫。全方配伍,補中兼升,使中氣得健、清陽得升,共奏補中益氣、升陽舉陷之功,故善治脾胃虛弱、中氣下陷諸病證。
現代藥理學研究表明[13],黃芪不僅能通過改善網狀內皮系統的吞噬功能來增加血白細胞數量,提高巨噬細胞吞噬指數、吞噬細胞百分比,還能通過提高體液免疫和細胞免疫來降低毛細血管通透性,減少組織滲出和水腫,還能提高結締組織中韌帶和筋膜的膠原纖維含量,提高結締組織的抵抗力,維持盆底組織的正常位置及營養。另外在顯微鏡實驗中,發現黃芪可以促進DNA和蛋白質的合成,加快組織細胞的生長速度,從而減少和預防疾病的發展過程。人參能抑制組織中單氨氧化酶的活性,增強免疫力,促進代謝,加速炎癥病變的吸收。白術[14]可延長淋巴細胞的存活時間,提高其清除自由基的能力,并具有較強的抗氧化作用。甘草、當歸能刺激單核一巨噬細胞系統,改善機體功能。
有研究表明[15]補中益氣不僅能調節心肌、小腸等器官,還能調節子宮。通過實驗發現,該方可以選擇性地提高離體子宮及其周圍組織結構的興奮性,提高子宮及其周圍組織的收縮性。同時有研究表明[16],補中益氣能抑制子宮運動,增加子宮肌張力,對產時用力、產后過早負重引起的盆底器官脫垂具有良好的療效。
盆底I、II 類肌纖維肌力、疲勞度是反映盆底肌肉收縮的強度和耐力評價指標。本研究結果顯示,觀察組患者I、Ⅱ類肌纖維盆底肌電壓、盆底肌疲勞度值改善優于對照組(P<0.05),說明補中益氣湯配合生物電刺激治療能改善神經肌肉興奮性,喚醒肌肉收縮能力,恢復盆底彈性和肌張力,加速盆底肌靜脈回流。另外,觀察組能顯著改善患者手測盆底肌力、尿失禁、盆腔脫垂分期、性生活質量、中醫癥候積分(神疲、自汗、氣短),提示補中益氣湯從中醫的角度,治療PFD,以脾腎同補,補澀兼施為主,協同生物電刺激能夠幫助孕產婦更好的恢復盆底功能,并改善中醫證候,為臨床治療產后PFD提供了新思路。
綜上,在生物電刺激治療的基礎上,聯合補中益氣湯可顯著改善患者盆底肌力,改善患者尿失禁、盆腔脫垂、性生活質量,但因本研究樣本量不多、缺乏遠期觀察,結果可能存在一定偏倚,且缺乏產后盆底肌肉完全恢復至產前水平的觀察,因此今后需針對上述不足作進一步探討。