血清SAA、CysC、Hcy、SF表達與糖尿病周圍神經病變的相關性研究
肖俊銳,吳石貴,黃舒婕,吳邦泰,許旭昀,陳子睿
1.汕頭市中醫醫院檢驗科,廣東汕頭 515031;2.汕頭市中醫醫院內分泌科,廣東汕頭 515031
糖尿病周圍神經病變是糖尿病患者的常見慢性并發癥之一,累及患者的感覺神經、運動神經和自主神經。糖尿病周圍神經病變的發生主要是因機體長期代謝紊亂、氧化應激損傷導致血管性缺血缺氧和神經元生長因子不足,進而造成肢體遠端出現對稱性的功能障礙。據調查顯示,糖尿病患者中約有30%~50%伴有不同程度周圍神經受損,嚴重情況下會導致患者殘疾,致使其喪失行為能力和勞動能力。糖尿病周圍神經病變的起病較為隱匿,并且該病的發病機制較為復雜,如果患者出現了下肢麻木、疼痛、瘙癢、灼燒感等神經性癥狀時,則說明病情已經發展至終末期[1-3]。因此,對于此類患者,及早發現、及早診斷、及早治療是改善預后的關鍵所在,而尋找可以反映早期糖尿病周圍神經病變的特異性指標非常重要。通過總結既往研究,除血糖、血脂外,血清淀粉樣蛋白A、胱抑素C、同型半胱氨酸、鐵蛋白與周圍神經病變均有一定相關,為進一步探討具體的相關性,選取2020年8月—2021年12月汕頭市中醫醫院收治的200例2型糖尿病患者,開展本次研究,現報道如下。
1 資料與方法
1.1 一般資料
選取本院收治的200例2型糖尿病患者為研究對象,將閾值低于15 V的100例患者歸為單純糖尿病組,其中男54例,女46例;年齡40~78歲,平均(59.56±2.37)歲。將閾值高于15 V的100例患者歸為糖尿病周圍神經病變組,其中男56例,女44例;年齡42~76歲,平均(59.32±2.18)歲。再選取同期于本院體檢的100名健康人群作為對照組,其中男52名,女48名;年齡41~76歲,平均(59.13±2.22)歲。3組一般資料對比,差異無統計學意義(P>0.05),具有可比性。
1.2 納入與排除標準
納入標準:①糖尿病患者的空腹血糖均≥7.0 mmol/L,口服葡萄糖耐量試驗2 h血糖均≥11.1 mmol/L[4];②年齡18~84歲,且有獨立的行為能力;③依從性良好,可積極配合完成各項檢查,自愿參與,簽署知情同意書。
排除標準:①合并惡性腫瘤、系統性紅斑狼瘡、甲狀腺功能異常者;②合并其他神經病變者;③合并糖尿病其他并發癥者[5];④既往有腦梗、腦出血病史者。
1.3 方法
抽取3組受檢者5 mL清晨空腹肘部淺靜脈血,離心15 min,3 500 r/min,分離血清,將血清貯存在-20℃冰箱中待測。使用全血自動分析儀檢測空腹血糖、各項血脂、CysC、Hcy,采用高效液相層析法檢測糖化血紅蛋白,采用電化學發光法測定SF,采用膠體金法檢測血清SAA。
1.4 觀察指標
對3組的血糖、血脂、血清淀粉樣蛋白A(serum amyloid A,SAA)、胱抑素C(cystatin c,CysC)、同型半胱氨酸(homocysteine,Hcy)、鐵蛋白(serum ferritin,SF)檢測結果進行比較。
1.5 統計方法
采用SPSS 26.0統計學軟件處理數據,計量資料符合正態分布,以(±s)表示,組間差異比較采用F檢驗。相關性采用Pearson相關系數(r)表示。P<0.05為差異有統計學意義。
2 結果
2.1 3組血糖水平比較
糖尿病周圍神經病變組和單純糖尿病組的空腹血糖、糖化血紅蛋白均高于對照組,且糖尿病周圍神經病變組高于單純糖尿病組,差異有統計學意義(P<0.05),見表1。
表1 3組血糖水平比較(±s)
?
2.2 3組血脂水平比較
糖尿病周圍神經病變組和單純糖尿病組的總膽固醇、三酰甘油和低密度脂蛋白均高于對照組,且糖尿病周圍神經病變組患者的總膽固醇、三酰甘油和低密度脂蛋白均高于單純糖尿病組,差異有統計學意義(P<0.05)。3組高密度脂蛋白對比差異無統計學意義(P>0.05),見表2。
表2 3組血脂水平比較[(±s),mmol/L]
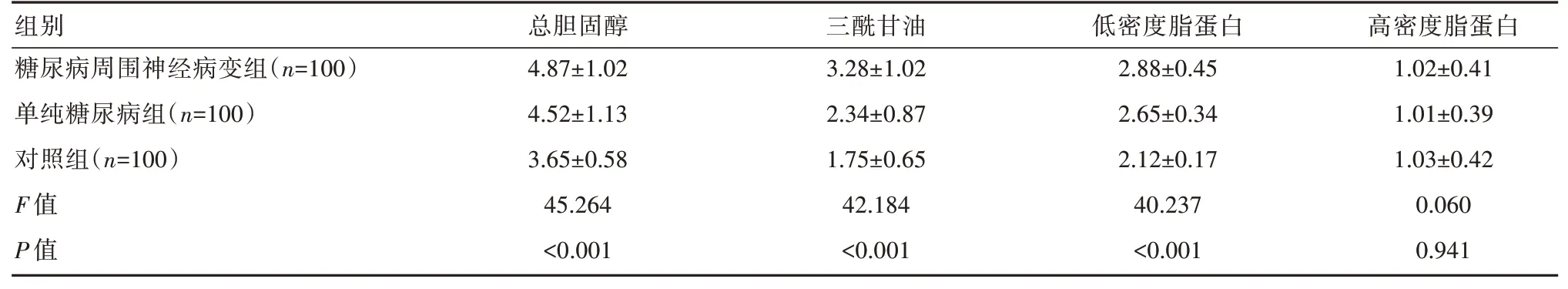
表2 3組血脂水平比較[(±s),mmol/L]
?
2.3 3組血清SAA、CysC、Hcy、SF表達比較
糖尿病周圍神經病變組和單純糖尿病組的血清SAA、CysC、Hcy、SF表達均高于對照組,且糖尿病周圍神經病變組高于單純糖尿病組,差異有統計學意義(P<0.05),見表3。
表3 3組血清SAA、CysC、Hcy、SF表達比較(±s)
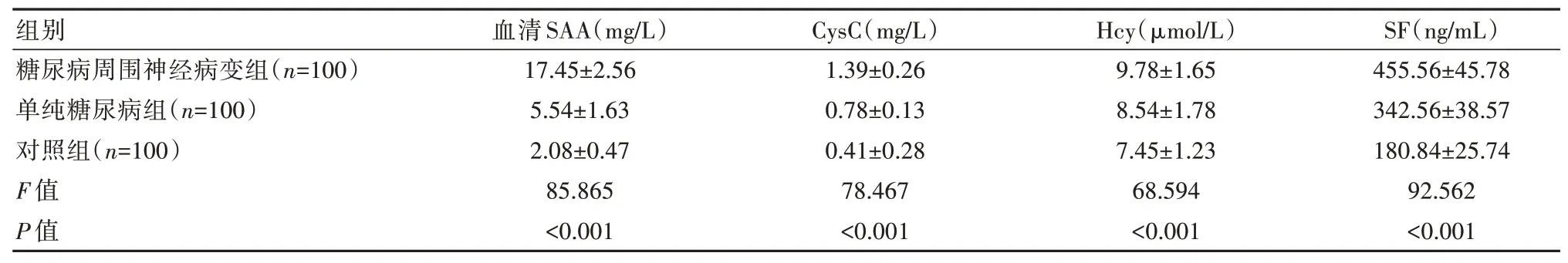
表3 3組血清SAA、CysC、Hcy、SF表達比較(±s)
?
2.4 相關性分析
血清SAA、CysC、Hcy、SF與糖化血紅蛋白呈正相關(r=25.458、23.261、28.585、16.597,P<0.001)。
3 討論
糖尿病是臨床上非常常見的慢性病,主要是機體胰島素分泌不足或胰島素抵抗所致的疾病,2型糖尿病的發生率高,約占糖尿病的90%以上,而2型糖尿病容易引發心腦、眼、腎、皮膚、神經等慢性并發癥,這些并發癥的發生是導致患者殘疾和死亡的主要原因。近年來,隨著人們生活方式的改變、飲食結構的調整,2型糖尿病的患病率不斷升高,對廣大患者的生活質量、身體與心理健康均造成了非常嚴重的影響[6-8]。
糖尿病周圍神經病變是糖尿病患者的常見并發癥,是糖尿病發生發展過程中出現的神經結構和周圍神經效能受損,從而出現與功能障礙相關的體征和臨床癥狀表現。現階段臨床上運用的篩查手段和診療標準存在一定的差異性。糖尿病周圍神經病變的患病率也有較大差異,并且該病的發生較為隱匿,缺乏典型的臨床癥狀表現,而一旦患者出現較為明顯的癥狀和體征時則說明患者的病情進入到晚期階段,最終有截肢、致殘的風險。近年來臨床上將生化指標運用在糖尿病周圍神經病變的臨床診斷上,生化指標的變化會導致局部氧化應激損傷程度加劇,進而促進細胞炎癥因子對周圍神經纖維的浸潤,造成患者病情的加重和進展[9-10]。因此,臨床上通過檢測患者的生化指標,開展生物學研究,可為患者的早期診斷、早期治療以及預后評估提供科學的參考依據。血糖和血脂檢測在臨床上應用較為廣泛,通過檢測患者的血糖水平和血脂水平能夠預測其發生并發癥的風險,但卻不能預測發生周圍神經病變的風險,因此單獨檢測患者血糖和血脂的漏診風險較高。
本研究除了對比糖尿病、糖尿病周圍神經病變與健康人的血糖和血脂水平之外,還對比了3類研究對象的血清SAA、CysC、Hcy、SF表達水平,研究結果顯示,糖尿病周圍神經病變組和單純糖尿病組的血清SAA、CysC、Hcy、SF表達均高于對照組,且糖尿病周圍神經病變組高于單純糖尿病組(P<0.05)。血清SAA是一種促炎性脂肪細胞因子,進入血液循環中能夠刺激內皮細胞分泌和單核細胞分泌出多種促炎性因子,造成巨噬細胞和單核細胞浸潤,從而促進白細胞的黏附作用,誘導血管活性物質產生。通過降低高密度脂蛋白可促進動脈硬化改變,進而導致糖尿病患者出現神經血管血流動力學改變。CysC是堿性非糖化蛋白質,在機體中表達較為穩定。生理狀態下的CysC的作用是抑制內源性半胱氨酸蛋白酶活性,而CysC和組織蛋白酶、同型半胱氨酸也會產生相互作用,參與到糖尿病周圍神經病變的發生發展過程中[11-12]。Hcy是蛋氨酸代謝的中間產物,在糖尿病周圍神經病變的發生和發展過程中Hcy表現為異常升高,可經多種途徑產生并誘發血管周圍神經病變[13-15]。SF是由肝臟合成的糖蛋白,是鐵儲存的最主要形式。如果機體內的鐵含量增加,則血清SF可攝取鐵并存儲。糖尿病患者多存在鐵高負荷,導致血清鐵蛋白升高,而發生周圍神經病變的糖尿病患者其血清鐵蛋白水平較單純糖尿病患者更高。
綜上所述,糖尿病周圍神經病變與血清SAA、CysC、Hcy、SF的表達均有一定相關性,通過檢測血清SAA、CysC、Hcy、SF表達水平以評估患者病情和預后,為臨床治療方案的制訂提供參考依據。

