Box-Behnken設計-效應面法優化巖黃連堿納米結構脂質載體處方工藝及體外藥效評價
蘇曉丹,麥琬婷,鐘華帥,曾勇珠,陸建媚,覃裕翠,黃秋潔,葉 勇, 3*
·藥劑與工藝·
Box-Behnken設計-效應面法優化巖黃連堿納米結構脂質載體處方工藝及體外藥效評價
蘇曉丹1,麥琬婷1,鐘華帥1,曾勇珠1,陸建媚1,覃裕翠1,黃秋潔2*,葉 勇1, 3*
1. 廣西醫科大學藥學院,廣西 南寧 530021 2. 廣西中醫藥大學藥學院,廣西 南寧 530001 3. 廣西生物活性分子研究與評價重點實驗室,廣西 南寧 530021
Box-Behnken設計-效應面法優化巖黃連堿納米結構脂質載體(dehydrocavidine nanostructured lipid carriers,DC-NLCs)處方,并進行體外藥效研究。采用溶劑蒸發法制備DC-NLCs。以包封率、載藥量和ζ電位為考察指標,采用單因素考察和Box-Behnken設計-效應面法優化DC-NLCs的處方。對DC-NLCs進行表征,并考察體外藥效作用。最佳處方為投藥量為10.0 mg、固-液脂質比為1∶8、卵磷脂用量為85.0 mg、表面活性劑為1%聚山梨酯-80。DC-NLCs測得包封率為(85.29±0.01)%,載藥量為(6.27±0.00)%,ζ電位為(?17.90±1.09)mV、粒徑為(188.50±11.77)nm,體外釋藥具有明顯的緩釋特征。體外藥效學實驗表明,DC-NLCs體外抑制肝纖維化的效果顯著。Box-Behnken設計-效應面法所建立的模型能較好地用于DC-NLCs處方優化,準確度高,預測效果較好,且優化制備的DC-NLCs具有顯著的抑制肝纖維化作用。
巖黃連堿;納米結構脂質載體;Box-Behnken設計-效應面法;緩釋;MTT法;藥效評價;溶劑蒸發法;肝纖維化
巖黃連又名石生黃堇、巖胡、土黃連,為罌粟科紫堇屬多年生草本植物巖黃連Bunting的全草[1],主要分布于廣西、貴州、云南等我國西南部地區。巖黃連作為廣西壯族傳統特色護肝藥物,常用于瘡疔腫毒、肝炎、肝硬化、肝癌[2-3]等疾病治療。
巖黃連堿是從巖黃連[4]中提取分離出來的1種季銨類生物堿。研究表明,巖黃連堿具有促進膠原溶解[5]、調節纖維化相關基因[5]、減少氧化應激[6]、減少肝臟丙二醛的形成[7]、提高超氧化物歧化酶(superoxide dismutase,SOD)、谷胱甘肽過氧化物酶(glutathione peroxidase,GSH-Px)和過氧化氫酶(catalase,CAT)活性[5]等藥理作用。目前以巖黃連堿作為主要質量控制指標的制劑有巖黃連注射液、巖黃連片劑[8]、巖黃連直腸栓[9]、巖黃連總堿膠囊[10]等,用于肝炎、肝硬化、肝癌等疾病的治療。然而,由于巖黃連堿存在溶解度差[11]、體外抗氧化活性能力低[12]藥物遞送率低等缺點,從而限制了其相關制劑的研發及臨床應用。因此,通過現代藥物制劑技術改善巖黃連堿溶解度及體外活性問題具有重要的現實意義。
據文獻報道,納米結構脂質載體(nanostructured lipid carriers,NLCs)是新一代脂質納米粒,也稱納米脂質載體[13]。NLCs存在液態油或混合基質打亂了固體脂質規整的晶型結構,以結晶缺陷型、無定形、液脂/固脂/水3者復合態等結構存在,可裝載更多藥物分子,提高包封率和載藥量[14],且具有改善藥物溶解度和緩控釋作用[15],能有效提高難溶性藥物在體內病灶的靶向性、吸收程度并延長藥效作用時間[16]。
基于此本研究利用單因素考察結合Box- Behnken設計-效應面法[17-18]進行實驗設計,以包封率、載藥量、ζ電位為考察指標,選擇巖黃連堿用量、固態與液態(固-液)脂質比、卵磷脂用量為主要影響因素,優化巖黃連堿-NLCs(dehydrocavidine- NLCs,DC-NLCs)的處方,并進行質量表征與體外藥效評價,以期為巖黃連堿新制劑的研發和臨床應用提供實驗依據和有價值的參考。
1 儀器與材料
1.1 儀器
Agilent 1200型高效液相色譜儀器,二極管陣列檢測器,美國Agilent公司;XS205DU型分析天平,梅特勒-托利多集團;KQ-500DB型數控超聲波清洗器,昆明市超聲儀器有限公司;HH-2型數顯電子恒溫水浴鍋,常州國華電器有限公司;Nano-ZS90型粒度分析儀,英國馬爾文公司;TG16-MS型高速離心機,賽默飛世爾有限公司;THZ-92C型臺式恒溫振蕩器,上海龍躍儀器設備有限公司;H-7650型透射電子顯微鏡(TEM),日本Htachi公司;Smart Lab-9kW型轉靶X-射線粉末衍射儀(XRD),瑞士梅特勒托利多公司;Nicolet IS20型傅里葉變換紅外光譜(FT-IR)儀,賽默飛世爾科技公司;超濾離心管,截留相對分子質量10 000,美國Millipore公司;Aynergy H1型酶標儀,美國伯騰儀器有限公司。
1.2 試藥
巖黃連堿原料藥,批號RP20201009,質量分數98.0%,購自成都麥德生科技有限公司;巖黃連堿對照品,批號111667-200401,質量分數99.6%,購自中國食品藥品檢定研究院;單硬脂酸甘油酯,批號L28N10S104297,購自源葉生物科技有限公司;油酸,批號k1929018,購自阿拉丁醫藥科技有限公司;聚山梨酯-80,批號70090050,購自Biosharp藥用輔料有限公司;磷酸,批號20201001,購自重慶川東華東有限公司;三乙胺,批號20210217,購自天津市大茂化學試劑廠;15-羥基硬脂酸聚乙二醇酯HS,批號73059868E0,購自德國巴斯夫化工有限公司;PBS緩沖液(批號20211210)、5-甲巰基-1-四氮唑(批號917Q054)、胰酶(批號20220221),購自北京索萊寶科技有限公司;MEM基礎培養基,批號WH0022X191,購自普諾賽生命科技有限公司;泊洛沙姆,批號GNC33221B,德國BASF有限公司;轉化生長因子-β1(transforming growth factor-β1,TGF-β1),批號?P01137?,派普泰克技術有限公司;LX-2細胞,廣西醫科大學藥學院林興課題組贈送。
2 方法與結果
2.1 DC-NLCs的制備工藝
稱取處方量的巖黃連堿原料藥、單硬脂酸甘油酯、油酸和卵磷脂置于燒杯中,加入無水乙醇4 mL,水浴加熱溶解得到澄清透明的有機相。將有機相緩慢滴入于70 ℃水浴的1%聚山梨酯-80中,以轉速為850 r/min磁力攪拌50 min后經0.45 μm微孔濾膜濾過,得DC-NLCs混懸液。
空白NLCs制備方法同DC-NLCs一致,但不加入巖黃連堿原料藥。
2.2 HPLC法測定巖黃連堿含量
2.2.1 色譜條件 色譜柱為6L Sciences ODS2 C18柱(250 mm×4.6 mm,5 μm);流動相為乙腈-0.2%磷酸三乙胺水溶液(30∶70);檢測波長為346 nm;體積流量為1.0 mL/min;柱溫為25 ℃。進樣后,巖黃連堿出峰位置在6.8 min左右(圖1),專屬性較高,理論塔板數以巖黃連堿計不低于12 000。

圖1 巖黃連堿對照品(A)和DC-NLCs (B)
2.2.2 線性關系考察 稱取巖黃連堿對照品2.5 mg至5 mL量瓶中,加入甲醇定容至刻度得500 μg/mL的巖黃連堿為母液。用巖黃連堿母液配制1、2、5、10、50、100、500 μg/mL系列質量濃度對照品溶液,進樣分析。以巖黃連堿的峰面積為縱坐標(),質量濃度為橫坐標(),進行線性回歸,得回歸方程=37.816+31.496,=0.999 8,可見,巖黃連堿在1~500 μg/mL線性關系良好。
2.2.3 供試品溶液制備 取DC-NLCs混懸液100 μL至5 mL量瓶中,加入甲醇定容至刻度后超聲(功率600 W)15 min,0.22 μm微孔濾膜濾過,即得DC-NLCs供試品溶液。
2.2.4 精密度考察 取低、中、高質量濃度(50、200、350 μg/mL)巖黃連堿溶液,連續進樣6次,記錄巖黃連堿色譜峰的峰面積,計算得巖黃連堿峰面積的RSD分別為0.22%、0.41%、0.09%,表明儀器精密度良好。
2.2.5 穩定性考察 取DC-NLCs供試品溶液,分別于制備后0、4、8、16、24 h進樣,記錄巖黃連堿色譜峰的峰面積,計算得巖黃連堿峰面積RSD為1.23%,表明供試品溶液在24 h內穩定性良好。
2.2.6 重復性考察 取DC-NLCs混懸液,按“2.2.3”項下方法處理,制備6份DC-NLCs供試品溶液,進樣,記錄巖黃連堿色譜峰的峰面積,計算得巖黃連堿質量濃度的RSD為1.15%,表明重復性良好。
2.2.7 加樣回收率考察 取DC-NLCs混懸液100 μL至10 mL量瓶中,分別加入500 μL巖黃連堿低、中、高質量濃度3組,每組3份。甲醇定容至刻度線后,取400 μL至超濾管中,以10 000 r/min離心(離心半徑7.5 cm)30 min。取續濾液,0.22 μm微孔濾膜濾過,進樣測定,計算得巖黃連堿的平均加樣回收率為105.18%,RSD分別為1.33%,表明該方法加樣回收率較高。
2.3 包封率、載藥量、粒徑及ζ電位的測定
取DC-NLCs混懸液100 μL至5 mL量瓶中,加入甲醇定容至刻度后超聲15 min,0.22 μm微孔濾膜濾過,進樣測定巖黃連堿總量(2)。另取DC-NLCs混懸液400 μL至超濾管中(截留相對分子質量10 000),10 000 r/min離心(離心半徑7.5 cm)30 min,取續濾液于10 mL量瓶中,甲醇定容至刻度線,進HPLC測定巖黃連堿游離藥量(1)。按照文獻方法分別計算包封率和載藥量。
包封率=(2-1)/2(1)
載藥量=(2-1)/(2+3) (2)
1為游離藥物的量,2為系統中藥物的總量,3為系統中輔料的量
取DC-NLCs混懸液0.4 mL,蒸餾水稀釋35倍后,置于粒度分析儀中,分別測定粒徑、多分散指數(polydispersity index,PDI)及ζ電位。
2.4 單因素考察DC-NLCs處方及制備工藝
2.4.1 巖黃連堿用量的考察 取處方量的單硬脂酸甘油酯、油酸、卵磷脂、巖黃連堿,在固-液脂質比為1∶8,聚山梨酯-80用量為1.0%,水浴溫度為70℃的條件下,考察巖黃連堿用量對DC-NLCs包封率、載藥量、粒徑等指標的影響,結果見表1。隨著巖黃連堿用量的增加,包封率總體呈現減小趨勢,這可能是在固-液脂質用量不變的情況下,其包載藥物的能力有限造成的。粒徑及PDI值均呈現先增加后減小趨勢,而載藥量呈增加趨勢,但ζ電位絕對值均大于20 mV。可見巖黃連堿用量對DC-NLCs的指標影響較大,當巖黃連堿用量為8 mg時包封率和載藥量相對較高,粒徑、PDI和ζ電位絕對值大小也相對理想。
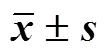
表1 巖黃連堿用量對DC-NLCs指標影響的考察(, n = 3)
2.4.2 固-液脂質比的考察 固定巖黃連堿用量為2 mg,取單硬脂酸甘油酯8 mg、油酸64 mg和處方量的卵磷脂置于燒杯,聚山梨酯-80用量為1.0%,水浴溫度為70 ℃,以轉速為850 r/min磁力攪拌50 min。考察不同固-液脂質比對DC-NLCs包封率、載藥量、粒徑等指標的影響,結果見表2。當固-液脂質比分別為1∶1、1∶4、1∶8、4∶1、8∶1時,包封率、載藥量和ζ電位絕對值先上升后下降,而粒徑和PDI值先下降后再上升。可見,固-液脂質比對DC-NLCs的影響較大,當固-液脂質比為1∶8時各指標相對較好。
2.4.3 卵磷脂用量的考察 固定巖黃連堿用量為2 mg,取單硬脂酸甘油酯8 mg、油酸64 mg和25、45、65、85、105、125 mg的卵磷脂置于燒杯,聚山梨酯-80用量為1.0%,水浴溫度為70 ℃,以轉速為850 r/min磁力攪拌50 min。考察不同卵磷脂用量對DC-NLCs包封率、載藥量、粒徑等指標的影響,結果見表3。當卵磷脂用量逐漸增加時,包封率和載藥量先上升后下降。當卵磷脂用量為65 mg時,包封率、載藥量和ζ電位較好。
2.4.4 攪拌時間的考察 固定巖黃連堿用量為2 mg,取單硬脂酸甘油酯8 mg、油酸64 mg和處方量的卵磷脂置于燒杯,聚山梨酯-80用量為1.0%,水浴溫度為70 ℃,以轉速為850 r/min,考察攪拌時間為10、30、50、70 min對DC-NLCs包封率、載藥量、粒徑等指標的影響,結果見表4。當攪拌時間逐漸增加時,載藥量先上升后下降的趨勢,包封率呈現增大趨勢。當攪拌時間為50 min時,包封率、載藥量和ζ電位較好。
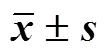
表2 固-液脂質比對DC-NLCs指標影響的考察(, n = 3)
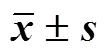
表3 卵磷脂用量對DC-NLCs指標影響的考察(, n = 3)
2.4.5 水浴溫度的考察 固定巖黃連堿用量為2 mg,取單硬脂酸甘油酯8 mg、油酸64 mg和處方量的卵磷脂置于燒杯,聚山梨酯-80用量為1.0%,考察水浴溫度為50、60、65、70、85 ℃,以轉速為850 r/min磁力攪拌50 min。考察不同攪拌溫度對DC-NLCs包封率、載藥量、粒徑等指標的影響,結果見表5。當水浴溫度逐漸增加時,包封率和載藥量大致先上升后下降的趨勢。當水浴溫度為70 ℃時,包封率、載藥量和ζ電位較好。
2.4.6 表面活性劑種類的考察 固定巖黃連堿用量為2 mg,取單硬脂酸甘油酯8 mg、油酸64 mg和處方量的卵磷脂置于燒杯,分別加入1%聚山梨酯-80、1%泊洛沙姆、1% 15-羥基硬脂酸聚乙二醇酯HS,以轉速為850 r/min磁力攪拌50 min。考察不同表面活性劑對DC-NLCs包封率、載藥量、粒徑等指標的影響,結果見表6。當表面活性劑為1%聚山梨酯-80時包封率、載藥量、粒徑、ζ電位、PDI較好。
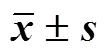
表4 攪拌時間對DC-NLCs指標影響的考察(, n = 3)
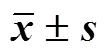
表5 水浴溫度對DC-NLCs指標影響的考察(, n = 3)
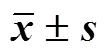
表6 表面活性劑種類對DC-NLCs指標影響的考察(, n = 3)
2.5 Box-Behnken響應面法優化處方
2.5.1 優化方案設計 包封率、載藥量、PDI、ζ電位是NLCs的重要指標,故選擇該4個指標進行Box-Behnken設計-響應面實驗。根據前期單因素考察,發現投藥量(1)、固-液脂質比(2)和卵磷脂用量(3)對DC-NLCs包封率(1)、載藥量(2)和ζ電位(3)的影響較大,各個因素的水平見表7。將包封率、載藥量和ζ電位歸一化為OD(overall desirability)值[19],作為Box-Behnken響應面設計的響應指標。
2.5.2 模型及方差分析 采用Design-Expert V 8.0.6軟件以綜合指標OD值對1、2、3進行擬 合,綜合考慮模型的擬合度及簡潔性,采用2次多項式進行擬合,得OD的2次多元回歸方程為1=0.47-0.301-0.0112+0.0123+0.1412-0.1213+0.26923+0.02212-0.08622-0.09532(2=0.929 0,<0.000 1)。
由2與值和可知,該預測模型擬合情況較好;且方程的失擬項值均大于0.05,差異不具有統計學意義,因此方程預測結果可靠性較高,可反映實際情況。對方程中各項系數進行了統計檢驗,OD值方差分析見表8,其中1、12、23有顯著或極顯著差異(<0.05、0.01)。

表7 Box-Behnken設計-響應面設計實驗因素水平及試驗結果
2.5.3 效應面評估與預測 采用Design Expert V 8.0.6繪制因變量對自變量的三維曲面圖。分別固定投藥量(1)、固-液脂質比(2)和卵磷脂用量(3)因素中之一,得到另外2個因素的交互作用對綜合指標OD值影響的結果見圖2。得出DC-NLCs最佳處方為投藥量為10.00 mg,固-液脂質比為1∶8,卵磷脂用量為65 mg,OD值為0.929 0,模型預測該處方的包封率為87.24%,載藥量為5.53%,ζ電位?16.50 mV。按照此處方平行制備3批DC-NLCs,結果見表9。測得其包封率為(85.29±0.01)%,載藥量為(6.27±0.00)%,ζ電位為(?17.90±1.09)mV分別與預測值較為接近,結果表明該方程預測結果較好。另測得DC-NLCs的粒徑為(188.50±11.77)nm,見圖3,結果表明DC-NLCs的粒徑較小;由圖4可見,DC-NLCs和空白NLCs溶液有明顯的丁達爾效應,但原料藥巖黃連堿溶液則沒有,進一步表明納米脂質載體的成功制備;由圖5可見,DC-NLCs的外觀形態圓整。

表8 方差分析結果
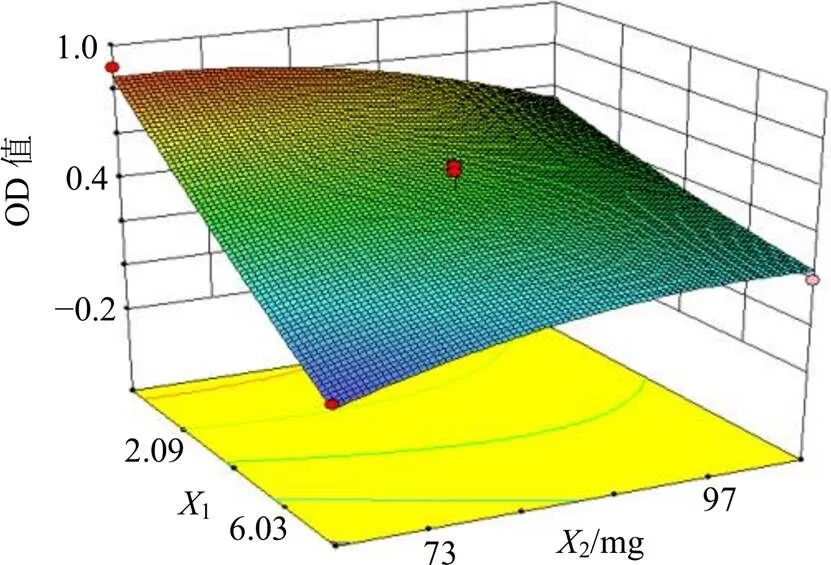
圖2 X2、X3對OD值的效應面圖
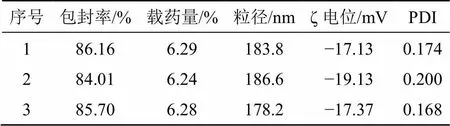
表9 DC-NLCs的包封率、載藥量、粒徑、ζ電位、PDI
2.6 體外釋放
取適量純化后的DC-NLCs至透析袋中扎緊兩端,釋放介質分別為30 mL的pH值為5.0、6.8、7.4的磷酸鹽緩沖液,溫度和轉速分別為(37±1)℃和100 r/min。分別在0.5、1.0、2.0、3.0、4.0、5.0、6.0、7.0、8.0、9.0、10.0、11.0、12.0、24.0、48.0 h分別取樣1 mL,并分別補液1 mL。各樣品均過0.22 μm微孔濾膜,進HPLC測定,結果見圖6。可見,巖黃連堿原料藥在2.0 h內釋藥較快,累積釋放率為97.52%,基本釋放完全。而DC-NLCs在前3 h釋放相較快,在4.0~48.0 h則表現出明顯的緩釋作用。
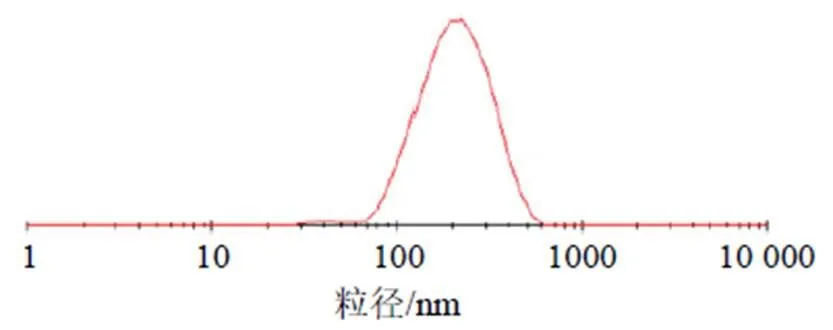
圖3 DC-NLCs的粒徑分布

圖4 巖黃連堿、DC-NLCs、空白NLCs溶液的外觀

圖5 DC-NLCs的TEM圖
2.7 DC-NLCs的質量評價
2.7.1 FT-IR分析 分別取適量純化的DC-NLCs凍干粉(所有樣品純化后均使用冷凍干燥機進行凍干成粉末)、空白NLCs凍干粉、巖黃連堿原料藥、空白NLCs凍干粉和巖黃連堿原料藥置于研缽中,加入適量溴化鉀研磨均勻后倒入模具中壓片。壓片完畢后分別進行FT-IR測定,結果見圖7。巖黃連堿、巖黃連堿原料藥和空白NLCs凍干粉的物理混合物在1650 cm?1都有C-N的特征吸收峰,而空白NLCs、DC-NLCs在1650 cm?1沒有IR吸收,2700~3100 cm?1是甲基、亞甲基及次甲基的伸縮振動,1650~1750 cm?1是羰基的特征吸收。結果表明,DC-NLCs成功制備。
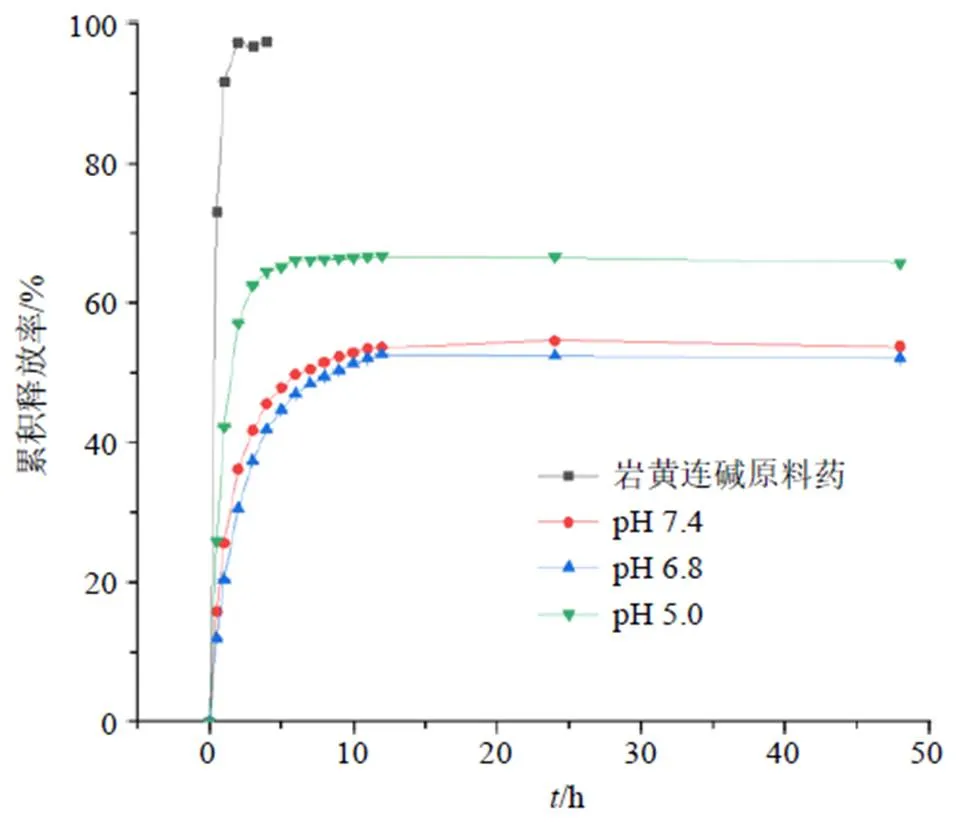
圖6 DC-NLCs和巖黃連堿在不同溶液中的累積釋放率(, n = 3)
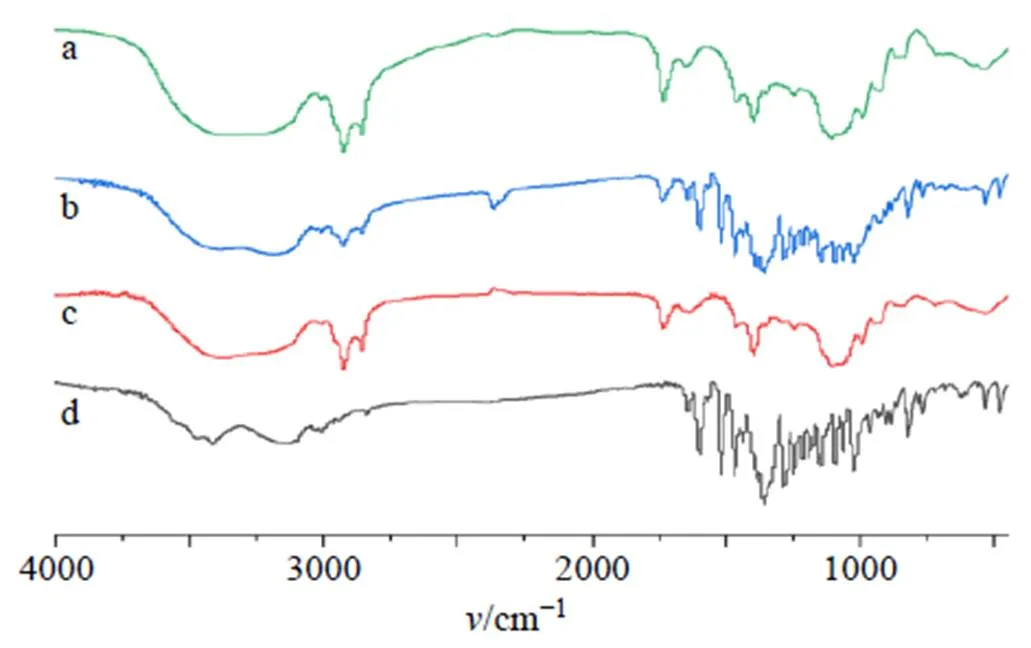
圖7 空白NLCs (a)、巖黃連堿+空白NLCs (b)、DC-NLCs (c)、巖黃連堿(d)的FT-IR圖譜
2.7.2 差示掃描量熱(DSC)分析 分別稱取適量巖黃連堿原料藥、空白NLCs凍干粉、DC-NLCs凍干粉、DC-NLCs凍干粉和巖黃連堿原料藥物理混合物置于鋁制樣品盤中壓制后,在DSC的樣品室中,以空鋁缽為參比進行測試。設置儀器參數為加熱速率10 ℃/min,掃描范圍30~300 ℃,結果見圖8。DC-NLCs和空白NLCs在175 ℃中有明顯的放熱峰,而沒有出現巖黃連堿在275 ℃的吸熱峰,這表明DC-NLCs成功制備。
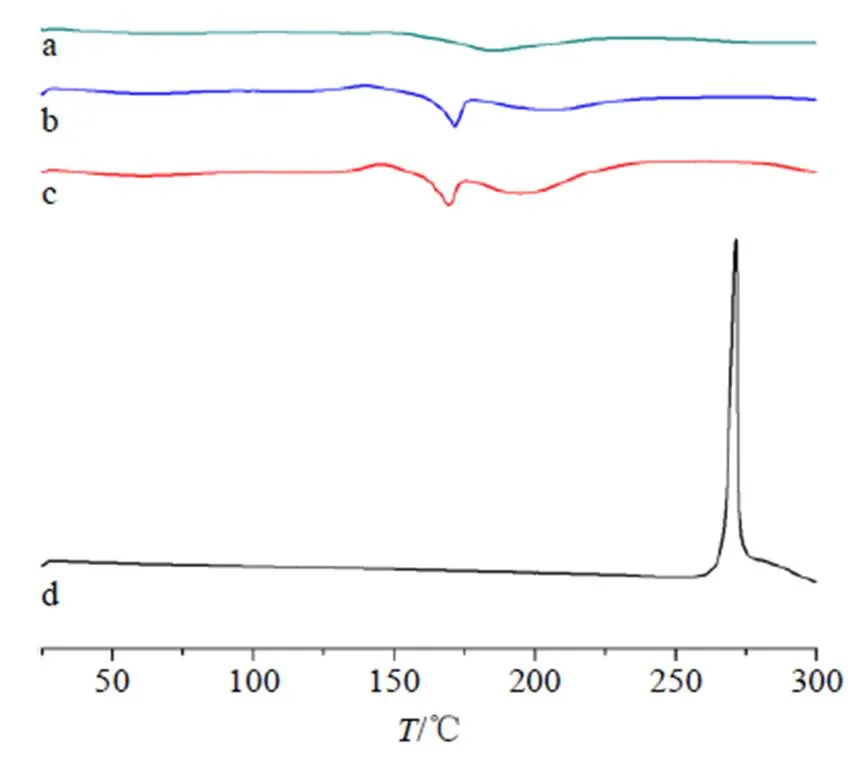
圖8 巖黃連堿+空白NLCs (a)、空白NLCs (b)、DC-NLCs (c)、巖黃連堿(d) 的DSC圖
2.7.3 X射線衍射(XRD)分析 分別稱取適量巖黃連堿原料藥、空白NLCs凍干粉、DC-NLCs凍干粉、DC-NLCs凍干粉和巖黃連堿原料藥物理混合物,將樣品粉末制成平整的試片,進行XRD測定。測定條件:Ni-濾液器,Cu-K α射線,輻射波長為0.154 056 nm,掃描范圍5°~45°,掃描速度5°/min、采樣時間l s,步長0.05°進行掃描,分別繪制XRD圖,結果見圖9。巖黃連堿自身有很多衍射峰,而制備成DC-NLCs后,所有的衍射峰都減弱了,且與空白NLCs具有相同的衍射的情況;由巖黃連堿與+空白NLCs凍干粉的物理混合物比較可見,在相同位置中都出現了相同的衍射峰。結果表明,DC- NLCs制備成功。
2.8 DC-NLCs對肝纖維化細胞體外藥效研究
2.8.1 MTT實驗檢測細胞增殖抑制活性 將LX-2細胞接種于96孔板內,并使每孔含有細胞懸液100 μL。將96孔板放入細胞培養箱內培養24 h,至細胞單層平鋪孔底,棄去原培養基。再加入100 μL制備好5 ng/mL的TGF-β1繼續刺激24 h后,棄去培養基,分別加入質量濃度為1.2、2.4、4.8、9.6、19.2 μg/mL的巖黃連堿或DC-NLCs,選取未加入藥物作為對照組,每組設3個復孔。置于條件為37 ℃、5% CO2培養箱內培養24 h,結果見圖10和表10。由圖10可見,未活化的LX-2細胞成梭形,經過TGF-β1活化后,明顯出現星狀化;表10結果表明,與巖黃連堿相比,DC-NLCs在1.2、2.4、4.8、9.6、19.2 μg/mL對LX-2細胞的抑制率具有顯著性差異(<0.01),且4.8 μg/mL的DC-NLCs在24 h后對細胞的抑制率達到50.57%。

圖9 空白NLCs (a)、DC-NLCs (b)、巖黃連堿+空白NLCs (c)、巖黃連堿(d)的XRD圖

圖10 未活化(A) 和活化(B)的LX-2細胞
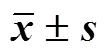
表10 巖黃連堿和DC-NLCs對LX-2細胞的抑制率
與巖黃連堿組比較:**<0.01
**< 0.01dehydrocavidine group
2.8.2 劃痕實驗檢測細胞遷移能力 將30%~40%密度的LX-2細胞接種于96孔細胞培養板中,每個樣品3個復孔,每孔100 μL完全培養基細胞培養箱內靜置培養。再加入100 μL制備好5 ng/mL TGF-β1繼續刺激24 h后,棄去培養基24 h后,用10 μL無菌槍頭在每孔培養板底劃線條粗細均勻的豎線后,吸去培養基,200 μL PBS洗2次,再加入100 μL質量濃度為4.8 μg/mL的巖黃連堿或DC-NLCs。在倒置顯微鏡下拍照,拍照結束后,置于培養箱,繼續培養48 h后,繼續拍照。計算遷移率,結果見圖11和表11。結果表明,DC-NLCs可明顯抑制LX-2細胞的遷移。
遷移率=(0 h劃痕寬度-48 h劃痕寬度)/0 h劃痕寬度
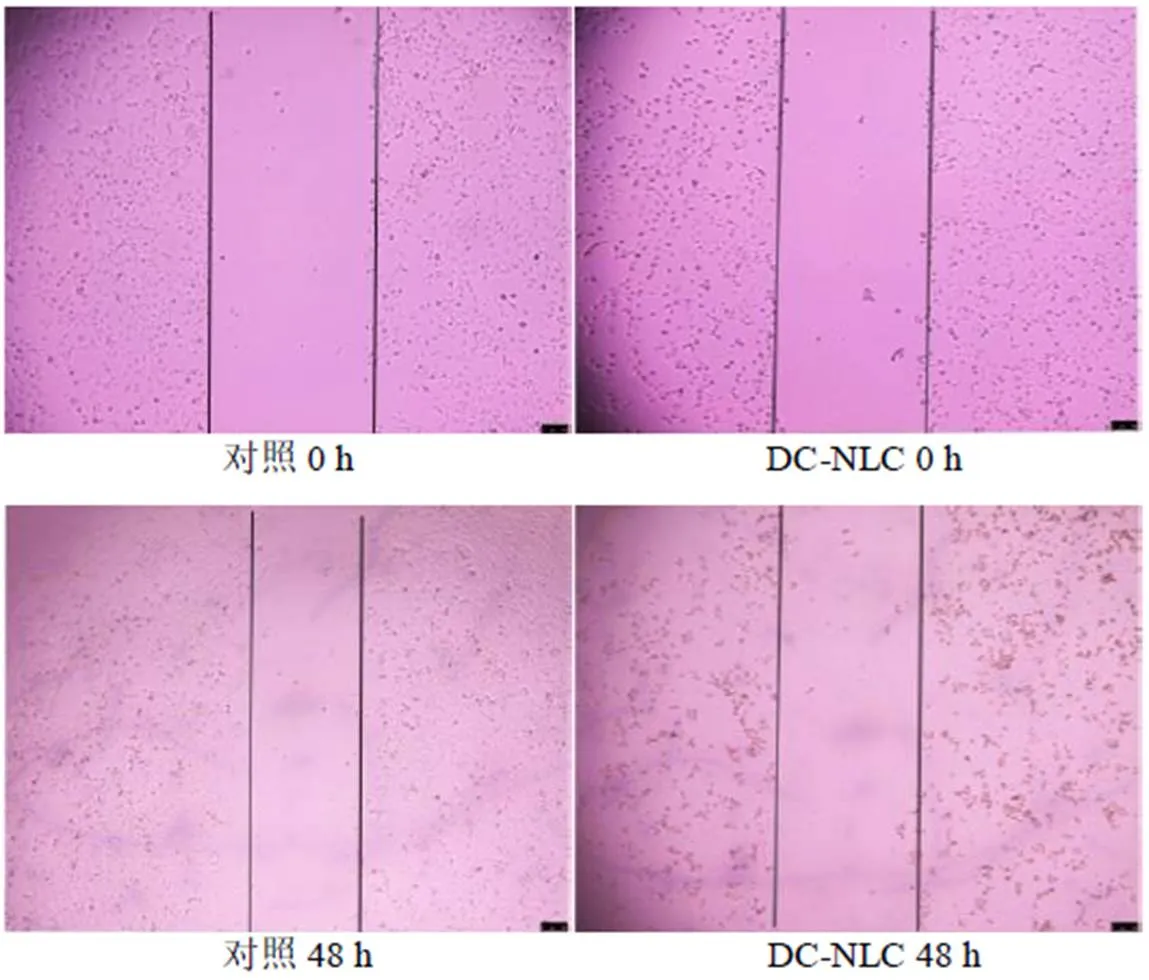
圖11 DC-NLCs對LX-2細胞的遷移影響

表11 DC-NLCs對LX-2細胞的遷移率
3 討論
巖黃連堿作為一種具有藥理活性的季銨堿化合物,越來越多研究表明巖黃連堿具有較好的肝纖維化治療潛力。然而巖黃連堿的水溶性差、半衰期短、生物利用度低等缺點嚴重限制了其臨床應用。NLCs是將固體脂質與液體脂質混合,并加入含有表面活性劑或表面活性劑混合物的水相,以形成與藥物結合的第二代脂質納米顆粒[20]。由于固體和液體脂類的分子大小和構象形狀不同,使載藥基質不能形成完美晶格,產生了空隙。這增加了溶解性、滲透性、降低了代謝、p-糖蛋白外排,從而增加了溶性差藥物的生物利用度[21]。因此,在本研究中,利用單因素考察結合Box-Behnken設計-效應面法成功優化了DC-NLCs處方,并評估了其在提高藥物成藥性能以及對體外細胞藥效作用的影響。
在確定處方選用液態脂質油酸,固態脂質單硬脂酸甘油酯的前期,分別固定液態和固態脂質,以包封率、粒徑等為評價指標進行了大量的處方篩選。結果發現,單硬脂酸甘油酯和油酸制得的納米結構脂質載體包封率相對較高,且粒徑相對較小。因此,處方輔料選用單硬脂酸甘油酯和油酸。同時,研究油酸總量對DC-NLCs中藥物包封效率的影響。結果表明,DC-NLCs包封率從69.32%增加到86.75%,油酸質量從20 mg增加到100 mg。這可能是由于液體脂質摻入固體脂質,導致了大量的晶體順序干擾,晶格中較大的缺陷留下了足夠空間來容納藥物分子,這最終提高了載藥能力和包封率[22]。在含有100 mg的油酸配方中,包封率最高,但粒徑、PDI較大,因此,綜合各因素處方選用油酸為64 mg的配比。單因素中考察了不同表面活性劑對包封率、載藥量、粒徑、ζ電位、PDI的影響,發現聚山梨酯-80所制備得到的DC-NLCs載藥量、包封率更高,可能由于聚山梨酯-80增溶及乳化效果更好,因此選用聚山梨酯-80作為表面活性劑。由于聚山梨酯-80的用量過大,會對紅細胞造成溶血現象[23],對后續的大鼠尾靜脈注射實驗造成影響,故選用1%聚山梨酯- 80進行單因素實驗。
有研究發現,腫瘤環境中由于癌細胞的有氧糖酵解增加導致癌細胞外pH值6.5~7.2低于正常組織[24],DC-NLCs在釋放度實驗中,藥物在pH值5.0中釋放最快,在pH值6.8中釋放最慢。這可能表明DC-NLCs在腫瘤環境中更適合緩慢釋放從而達到長效作用。此外,有文獻報道[25],加入凍干保護劑形成的NLCs呈無定型狀態,而不含凍干保護劑的NLCs凍干后有一定的結晶結構存在。在進行DSC實驗中,空白NLCs、DC-NLCs只出現1個較弱的放熱峰,而巖黃連堿出現了1個較強的吸熱峰,可能是冷凍干燥時加入少量的蔗糖造成的。此外,巖黃連堿與空白NLCs的物理混合物沒有呈現任何的放熱、吸熱峰,有可能是物理混合物加大了兩者的不定型狀態造成的。
本研究所制備的DC-NLCs大小在150~200 nm,適合細胞攝取。在體外藥效研究發現,DC-NLCs對LX-2細胞在24、48 h都具有明顯的抑制作用,且與游離巖黃連堿抑制率的比較具有顯著性差異(<0.01),這表明DC-NLCs對肝纖維化疾病治療有巨大的應用前景。這些結果與納米結構脂質載體在給藥方面的優勢相一致[19,26]。考慮到腫瘤組織和腫瘤微環境之間的聯系,需要通過更準確和有效的藥物傳遞來解決日益增長的癌癥負擔。在過去的20年里,納米技術在癌癥的診斷和靶向治療領域中做出了巨大貢獻[27]。然而,納米技術藥物傳遞相關的效率和毒性問題仍需要解決[28]。因此,后續研究將進行DC-NLCs的體內藥效學、藥動學評價,并進一步完善質量表征,為DC-NLCs的開發應用提供更為全面的研究資料。
利益沖突 所有作者均聲明不存在利益沖突
[1] 張曉, 李保宏, 張永康, 等. 巖黃連的化學成分及生物活性研究進展 [J]. 中草藥, 2022, 53(9): 2861-2871.
[2] 金書屹, 李紅婷, 汪萬利, 等. 紫堇屬巖黃連的化學成分及藥理作用研究進展 [J]. 中成藥, 2022, 44(5): 1545-1552.
[3] 陳萍, 鞠霖杰, 成俊, 等. 巖黃連總堿對代謝相關脂肪性肝病小鼠的治療作用及分子機制研究 [J]. 藥物評價研究, 2021, 44(3): 468-477.
[4] 廣西科學院廣西植物研究所. 廣西植物志 [M]. 南寧: 廣西科學技術出版社, 1991: 410.
[5] Wang T, Sun N L, Zhang W D,. Protective effects of dehydrocavidine on carbon tetrachloride-induced acute hepatotoxicity in rats [J]., 2008, 117(2): 300-308.
[6] 石永輝, 黃光業, 薛照蕓, 等. 脫氫卡維丁對H2O2處理成骨前體細胞MC3T3-E1增殖及凋亡的影響 [J]. 中藥材, 2020, 43(2): 457-463.
[7] Fu P, Zhang Q, Yi D Y,. Dehydrocavidine attenuates d-galactose induced learning and memory impairment in rats [J]., 2018, 665: 200-205.
[8] 黃雪梅, 黃興振, 劉雪萍, 等. 巖黃連片質量標準研究 [J]. 中國藥房, 2007, 18(12): 916-918.
[9] 諸葛明麗, 農慧亮, 黃興振, 等. 巖黃連直腸栓質量標準研究 [J]. 中國藥業, 2013, 22(12): 87-89.
[10] 戴國梁, 歐陽冰琛, 王一清, 等. 巖黃連總堿膠囊在健康受試者體內的藥動學研究 [J]. 中國醫院藥學雜志, 2022, 42(7): 702-706.
[11] 薛斐倩, 王績英. 脫氫卡維丁的藥理作用及其相關機制研究進展 [J]. 世界最新醫學信息文摘, 2017, 17(95): 58-60.
[12] 何志超, 王冬梅, 李國成, 等. 巖黃連生物堿類成分及其抗氧化活性研究 [J]. 中草藥, 2014, 45(11): 1526- 1531.
[13] Patel D, Dasgupta S, Dey S,. Nanostructured lipid carriers (NLC)-Based gel for the topical delivery of aceclofenac: Preparation, characterization, andevaluation [J]., 2012, 80(3): 749-764.
[14] Mishra N, Yadav N P, Rai V K,. Efficient hepatic delivery of drugs: Novel strategies and their significance [J]., 2013, 2013: 382184.
[15] 周劍雄, 吳送姑, 龔俊波, 等. 小檗堿的藥理活性以及提升其口服生物利用度的策略 [J]. 藥學學報, 2022, 57(5): 1263-1272.
[16] 董丹丹, 焦紅軍, 郝海軍, 等. 吳茱萸堿納米結構脂質載體處方優化和SD大鼠體內口服藥動學研究 [J]. 中草藥, 2022, 53(1): 60-70.
[17] 尹元元, 耿燕娜, 范明松. Box-Behnken設計-效應面法優化延胡索乙素聚乳酸-羥基乙酸共聚物納米粒處方和體外釋藥行為研究 [J]. 中草藥, 2021, 52(22): 6806- 6815.
[18] 楊金枝, 趙興業, 周開, 等. Box-Behnken設計-效應面法優化根皮素納米結構脂質載體處方研究 [J]. 中國醫院藥學雜志, 2021, 41(20): 2076-2081.
[19] 麥琬婷, 鐘華帥, 蘇曉丹, 等. Box-Behnken響應面優化蛇葡萄素納米結構脂質載體處方工藝及體外評價 [J]. 中草藥, 2022, 53(16): 4982-4991.
[20] Patel P, Patel M. Nanostructured lipid carriers-A versatile carrier for oral delivery of lipophilic drugs [J]., 2021, 15(2): 154-164.
[21] Harde H, Das M, Jain S. Solid lipid nanoparticles: An oral bioavailability enhancer vehicle [J]., 2011, 8(11): 1407-1424.
[22] Patel D, Dasgupta S, Dey S,. Nanostructured lipid carriers (NLC)-Based gel for the topical delivery of aceclofenac: Preparation, characterization, andevaluation [J]., 2012, 80(3): 749-64.
[23] 魏寒梅. Angiopep-2修飾吐溫80包裹環維黃楊星D脂質體的制備及評價[D]. 廣州: 廣州中醫藥大學, 2018.
[24] Guo X, Shi C L, Wang J,. pH-triggered intracellular release from actively targeting polymer micelles [J]., 2013, 34(18): 4544-4554.
[25] Hisaka T, Sakai H, Sato T,. Quercetin suppresses proliferation of liver cancer cell lines[J]., 2020, 40(8): 4695-4700.
[26] Yin J, Hou Y, Yin Y,. Selenium-coated nanostructured lipid carriers used for oral delivery of berberine to accomplish a synergic hypoglycemic effect [J]., 2017, 12: 8671-8680.
[27] 楊冰, 陸洋, 杜守穎, 等. 基于“鼻-腦”通路細胞模型組探索相對分子質量及粒徑因素對藥物制劑經鼻入腦的影響 [J]. 中草藥, 2020, 51(22): 5748-5753.
[28] Ashdaq U A, Riaz M, Yasmeen E,. Recent advances in nanoparticle-based targeted drug-delivery systems against cancer and role of tumor microenvironment [J]., 2017, 34(4): 317-53.
Formulation optimization of dehydrocavidine nanostructured lipid carriers by Box-Behnken design response surface method and pharmacodynamic studies
SU Xiao-dan1, MAI Wan-ting1, ZHONG Hua-shuai1, ZENG Yong-zhu1, LU Jian-mei1, QIN Yu-cui1, HUANG Qiu-jie2, YE Yong1, 3
1. School of Pharmacy, Guangxi Medical University, Nanning 530021, China 2. School of Pharmacy, Guangxi University of Traditional Chinese Medicine, Nanning 530001, China 3. Guangxi Key Laboratory of Bioactive Molecules Research and Evaluation, Nanning 530021, China
To optimize the formulation of dehydrocavidine nanostructured lipid carriers (DC-NLCs) by Box-Behnken design response surface method, and studypharmacodynamics.Preparation of DC-NLCs by solvent evaporation. Encapsulation efficiency, drug loading and potential were used as evaluation index, single factor investigation method and Box-Behnken response surface method (BBD-RSM) were used to investigate the optimal prescriptions of DC-NLCs. The DC-NLCs were characterized andefficacy results were compared.The optimal formulation: dehydrocavidine dosage was 10.0 mg, solid-liquid lipid ratio was 1∶8, lecithin dosage was 85.0 mg, surfactant was 1% polysorbate-80. Envelopment efficiency, drug loading, potential and particle size of DC-NLCs were (85.29 ± 0.01)%, (6.27 ± 0.00)%, (?17.90 ± 1.09) mV and (188.50 ± 11.77) nm, respectively.drug release has obvious sustained-release characteristics.pharmacodynamic experiments showed that DC-NLCs had significant inhibitory effect on liver fibrosis.It is feasible to apply BBD-RSM for the formulation optimization of DC-NLCs, and DC-NLCs had significant inhibitory effect on liver fibrosis.
dehydrocavidine; nanostructured lipid carriers; Box-Behnken design-response surface method; sustained release; MTT colorimetric method; pharmacodynamic evaluation; solvent evaporation method; liver fibrosis
R283.6
A
0253 - 2670(2022)22 - 7019 - 10
10.7501/j.issn.0253-2670.2022.22.005
國家自然科學基金資助項目(81960756);國家自然科學基金資助項目(81360689);廣西自然科學基金資助項目(2022GXNSFDA 035063);廣西自然科學基金資助項目(2018GXNSFAA050078);廣西自然科學基金資助項目(2015GXNSFAA139173);廣西高校中青年教師科研基礎能力提升基金資助項目(2019KY0148);廣西高校中青年教師科研基礎能力提升基金資助項目(2019KY0315)
蘇曉丹(1996—),女,碩士研究生,研究方向為中藥新劑型與新技術。
黃秋潔(1979—),女,副教授,主要從事中藥新劑型與新技術研究。Tel: 13737172226 E-mail: hqj8@163.com
葉 勇(1979—),男,博士,副教授,主要從事民族藥藥效物質及其新制劑研究。Tel: 13978679458 E-mail: yong-ye@163.com
[責任編輯 鄭禮勝]

