水系鋅二次電池MnO2正極的晶體結(jié)構(gòu)、反應(yīng)機(jī)理及其改性策略
陳鮮紅,阮鵬超,吳賢文,梁叔全,2,周江,2,*
1中南大學(xué)材料科學(xué)與工程學(xué)院,長沙 410083
2中南大學(xué)電子封裝及先進(jìn)功能材料湖南省重點(diǎn)實(shí)驗(yàn)室,長沙 410083
3吉首大學(xué)化學(xué)化工學(xué)院,湖南 吉首 416000
1 引言
當(dāng)前,能源危機(jī)和環(huán)境污染等問題日益突出,開發(fā)可持續(xù)發(fā)展的新能源成為當(dāng)務(wù)之急。而太陽能、潮汐能、風(fēng)能及生物能源等可再生能源易受環(huán)境影響,具有間歇性和不可控性。電化學(xué)儲能技術(shù)作為新一代綠色能源技術(shù),無需使用化石燃料,可有效減少溫室氣體的排放,是目前全球科研界的聚焦點(diǎn)之一。其中水系二次電池由于成本低、安全性高、毒性小,環(huán)境友好等優(yōu)勢受到廣泛關(guān)注1。相較于眾多金屬如鈉2、鈣3、鋰4,5等,金屬鋅在水系電解液中具有更高的可逆性和穩(wěn)定性6,同時,鋅還具有豐度高、理論容量高(820 mAh·g?1)及氧化還原電位低(?0.763 V vs.標(biāo)準(zhǔn)氫電極)等優(yōu)勢,在規(guī)模儲能領(lǐng)域中展現(xiàn)出廣闊的發(fā)展前景7,8。
水系鋅二次電池的電化學(xué)性能與正極材料的結(jié)構(gòu)和形貌特征息息相關(guān)9,10,開發(fā)容量高、電化學(xué)穩(wěn)定的正極材料是發(fā)展高性能鋅二次電池儲能器件的關(guān)鍵因素之一。現(xiàn)已報道的正極材料有錳基氧化物11,12、釩基氧化物13,14、普魯士藍(lán)類似物15、有機(jī)化合物16、層狀硫化物17、聚陰離子化合物18及chevrel相化合物19,20等(圖1a)。其中MnO2具有種類豐富、毒性小、成本低、容量高(616 mAh·g?1,基于2個電子轉(zhuǎn)移數(shù))、放電平臺高(大于1.35 V vs.Zn2+/Zn)等諸多優(yōu)勢,被作為正極材料廣泛地應(yīng)用于水系鋅二次電池中21。然而,目前報道的水系鋅錳電池仍無法達(dá)到預(yù)期的要求,其不令人滿意的電化學(xué)性能以及多樣的儲能機(jī)制在很大程度上取決于MnO2的晶體結(jié)構(gòu)(α、β、γ、δ、λ和R態(tài)等,圖1b)22,23和電解液條件24,25。

圖1 (a)鋅電池具有代表性的正極材料的工作電壓和比容量20;(b) α-MnO2,β-MnO2,γ-MnO2,λ-MnO2,δ-MnO2和R-MnO2的晶體結(jié)構(gòu)示意圖23Fig. 1 (a) The working voltage and specific capacity of representative cathode materials for zinc battery 20.(b) Schematic diagram of crystal structures of α-MnO2, β-MnO2, γ-MnO2, λ-MnO2, δ-MnO2 and R-MnO2 23.
本文主要總結(jié)了MnO2的晶體結(jié)構(gòu)和儲能機(jī)制,以及針對MnO2主要的兩類儲能機(jī)制(嵌入-脫出和溶解-沉積機(jī)制)工作時所存在的電池容量低、循環(huán)壽命短等問題所提出的優(yōu)化策略,為高性能鋅錳二次電池的發(fā)展提供參考。
2 二氧化錳的晶體結(jié)構(gòu)
二氧化錳具有多種晶體結(jié)構(gòu),如α-MnO2,β-MnO2,γ-MnO2,λ-MnO2,δ-MnO2和R-MnO2。在這些晶體結(jié)構(gòu)中,每個Mn4+離子被6個相鄰的氧離子包圍,形成基本八面體單元MnO6,這些單元通過周期性共享頂點(diǎn)/邊緣而形成不同的晶體結(jié)構(gòu)類型(鏈/隧道/層狀),被作為正極材料廣泛應(yīng)用于水系鋅二次電池中22。本節(jié)將詳細(xì)介紹不同類型MnO2的晶體結(jié)構(gòu)特征(表1)。
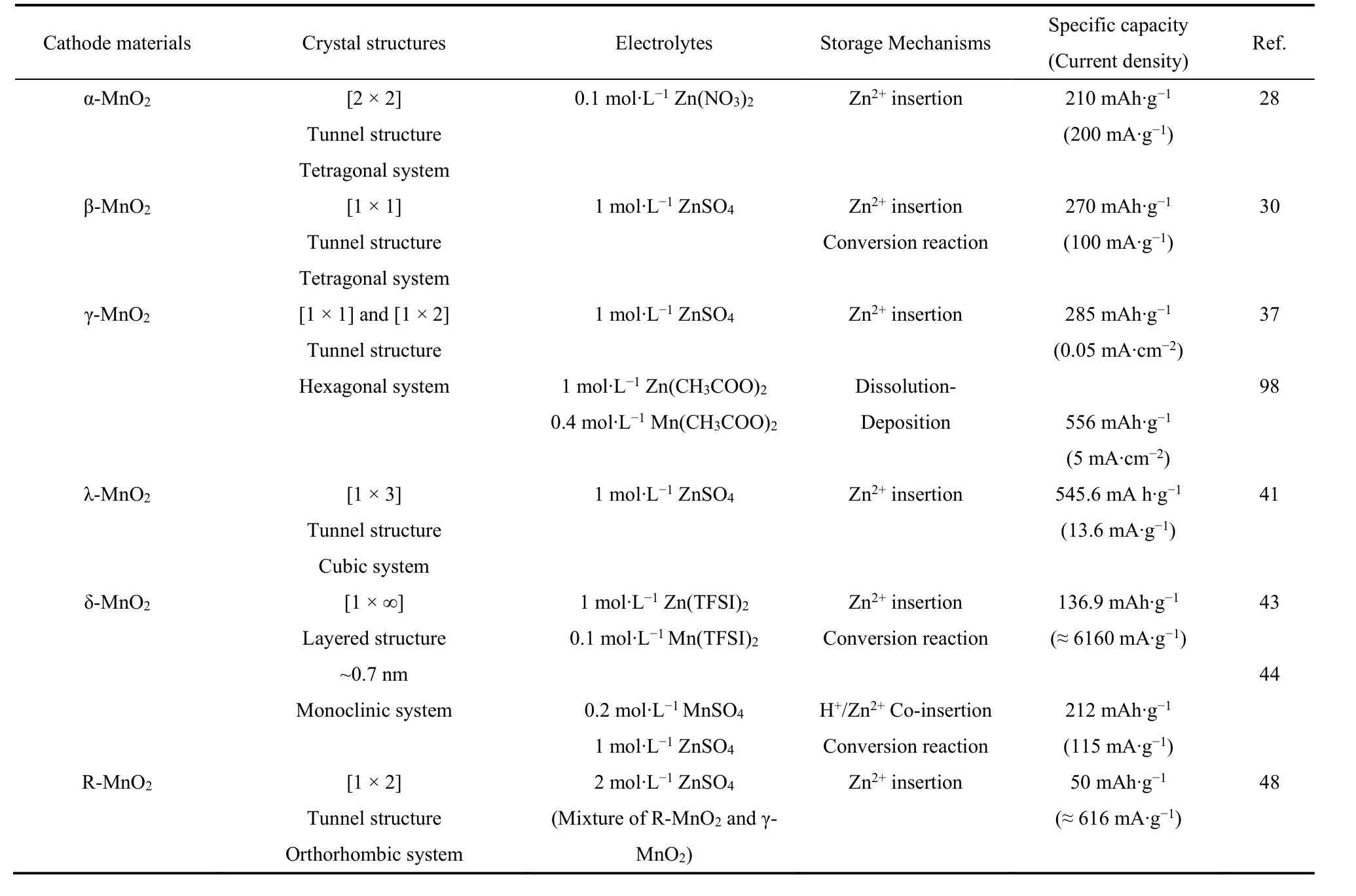
表1 不同晶型MnO2的晶體結(jié)構(gòu)、儲能機(jī)制及其性能Table 1 The crystal structure, energy storage mechanism and performance of different crystalline MnO2.
2.1 α-MnO2
α-MnO2具有[2 × 2,~0.46 nm × 0.46 nm]隧道結(jié)構(gòu),屬于體心四方晶系,空間群為I4/m,其基本八面體單元MnO6通過共享角形成雙鏈結(jié)構(gòu)。α-MnO2較寬的隧道結(jié)構(gòu)可允許Zn2+沿z軸快速嵌入/脫嵌26。納米尺寸的α-MnO2直徑小,具有較大的比表面積和更高的電解液可及性,能有效地提高電池的容量27。2009年Xu等28報道了α-MnO2在弱酸性Zn(NO3)2電解液中Zn2+的嵌入/脫嵌行為,之后又證明了放電時Zn2+會嵌入α-MnO2正極中形成ZnMn2O4,充電過程為其逆反應(yīng),從而實(shí)現(xiàn)了210 mAh·g?1的高容量(電流密度為200 mA·g?1),表明在α-MnO2中Zn2+嵌入-脫嵌行為的高度可逆性29。
2.2 β-MnO2
β-MnO2具有[1 × 1,~0.23 nm × 0.23 nm]隧道結(jié)構(gòu),屬于正方晶系,為金紅石結(jié)構(gòu)22,其晶胞中的氧原子呈緊密排列的六角形結(jié)構(gòu),其中錳原子占據(jù)八面體的中心,氧原子分別占據(jù)八面體的六個頂點(diǎn)。β-MnO2的隧道結(jié)構(gòu)較窄,其熱力學(xué)穩(wěn)定,理論上不利于Zn2+的嵌入。但I(xiàn)slam等30設(shè)計了一種暴露(101)面的β-MnO2納米棒,這種獨(dú)特的棒狀形態(tài)有助于Zn2+嵌入/脫嵌。利用原位X射線衍射技術(shù)(in situ XRD)可觀察到β-MnO2在首次經(jīng)歷Zn2+嵌入時,(101)晶面的峰值會略微向較低的角度移動,并在完全充電后恢復(fù),不存在明顯的結(jié)構(gòu)畸變。這種改性的電極材料在100 mA·g?1電流密度下實(shí)現(xiàn)了270 mAh·g?1的高比容量。同時,近年來,研究人員利用缺陷工程、復(fù)合材料等策略,通過改變材料晶格結(jié)構(gòu)或調(diào)節(jié)活性位點(diǎn)等方式,顯著提高了β-MnO2的電化學(xué)性能31,32。
2.3 γ-MnO2
γ-MnO2由交替生長的[1 × 1,~0.23 nm × 0.23 nm,鐵礦巖]和[1 × 2,~0.23 nm × 0.46 nm,菱巖]隧道組成,屬于六方晶系33。γ-MnO2隧道結(jié)構(gòu)的無序性導(dǎo)致其具有較低的結(jié)晶度,同時存在較多缺陷,包括孿平面(Tw或Mt)、Mn(III)取代Mn(IV)和Mn空位等34。1986年γ-MnO2首次被作為正極應(yīng)用于弱酸性水系鋅二次電池中35,之后Kumar等36將一種聚(偏氟乙烯)-三氟酸鋅凝膠聚合物作為電解液,嘗試進(jìn)一步分析Zn2+在γ-MnO2的嵌入/脫嵌行為,遺憾的是其深入機(jī)理未能明晰。直到2015年,Alfaruqi等37研究表明,Zn2+嵌入γ-MnO2時會發(fā)生相變,形成層狀L-ZnyMnO2、ZnMn2O4和γ-ZnxMnO4,放電時又重新恢復(fù)成γ-MnO2,闡明了充放電循環(huán)時γ-MnO2的具體儲能過程。此外,有報道指出,可通過調(diào)節(jié)溫度來控制γ-MnO2向γ/β-MnO2發(fā)生結(jié)構(gòu)轉(zhuǎn)變,而γ/β-MnO2具有比γ-MnO2更優(yōu)異的電化學(xué)性能,這可為設(shè)計高性能二氧化錳材料提供參考38。
2.4 λ-MnO2
λ-MnO2具有[1 × 3]隧道結(jié)構(gòu),是一種典型的尖晶石結(jié)構(gòu),Mn和O離子分別占據(jù)八面體的16d位和32e位39。1981年Hunter成功制備λ-MnO2,即先采用前驅(qū)體法制備錳酸鋰,再利用酸性溶液處理,使其發(fā)生氧化脫鋰反應(yīng),最后生成λ-MnO240。λ-MnO2隧道結(jié)構(gòu)尺寸有限,在一定程度上會阻礙Zn2+的快速嵌入/脫嵌,但Yuan等41將由稀酸溶液處理LiMn2O4所制備的λ-MnO2作為正極,在13.6 mA·g?1的電流密度下實(shí)現(xiàn)了545.6 mAh·g?1的高放電容量,表明λ-MnO2材料可允許一定量的Zn2+嵌入-脫嵌。
2.5 δ-MnO2
δ-MnO2具有層間距較大的二維層狀結(jié)構(gòu)(~0.7 nm),其由共角的MnO6八面體構(gòu)成,屬于單斜晶系,P2/m空間群21。Alfaruqi等42研究了Zn2+在層狀的納米δ-MnO2中的充放電行為,發(fā)現(xiàn)Zn2+嵌入時δ-MnO2會轉(zhuǎn)變成尖晶石型ZnMn2O4和層狀δ-ZnxMnO2,證實(shí)了δ-MnO2在循環(huán)過程中會經(jīng)歷相的轉(zhuǎn)變。之后,Jin等43證明了在Zn(TFSI)2電解液中,首次快速充電時Zn2+會嵌入δ-MnO2中,但并不會引起明顯的相變。而后續(xù)的反應(yīng)過程是由有H+參與的轉(zhuǎn)換反應(yīng)主導(dǎo),這種機(jī)制實(shí)現(xiàn)了電池穩(wěn)定的高容量(4000次循環(huán)后仍有93%的容量保持率)。此外,δ-MnO2結(jié)構(gòu)的質(zhì)子吸附能較低,可允許H+與Zn2+共嵌入電極結(jié)構(gòu)中,同時其較大的層間距可滿足Zn2+更快的擴(kuò)散和儲存,被作為電極材料廣泛應(yīng)用44。其他隧道結(jié)構(gòu)的MnO2(如α-,β-,γ-和λ-MnO2)在循環(huán)時會發(fā)生由隧道結(jié)構(gòu)向?qū)訝罱Y(jié)構(gòu)的轉(zhuǎn)變,影響電池的穩(wěn)定性29,37,41,45,而δ-MnO2這種從“層狀到層狀”的轉(zhuǎn)變在動力學(xué)上更有利于Zn2+的存儲46。
2.6 R-MnO2
R-MnO2的[1 × 2]隧道框架由共享角的雙鏈結(jié)構(gòu)構(gòu)成,而雙鏈結(jié)構(gòu)由共享邊緣的MnO6八面體組成,屬于一種藍(lán)寶石結(jié)構(gòu)47。R-MnO2具有較寬的隧道結(jié)構(gòu),可滿足載流子快速嵌入-脫嵌,并實(shí)現(xiàn)較高的電池容量48。
3 二氧化錳的反應(yīng)機(jī)制
MnO2的儲能機(jī)理非常復(fù)雜,目前對于其電化學(xué)反應(yīng)機(jī)制仍然存在爭議49。根據(jù)目前的研究進(jìn)展,本文總結(jié)了以下四種不同的MnO2儲能機(jī)制:(1) Zn2+的嵌入機(jī)制;(2)共嵌入機(jī)制;(3) H+嵌入引發(fā)的轉(zhuǎn)化反應(yīng)機(jī)制;(4)溶解-沉積機(jī)制。對于前兩種機(jī)制,不同晶型的MnO2在經(jīng)歷Zn2+嵌入時會發(fā)生不同的電化學(xué)反應(yīng)和結(jié)構(gòu)轉(zhuǎn)變,且H+作為微酸水系電解液中的組分,理論上可與Zn2+共同參與離子反應(yīng)。這兩種機(jī)制均表現(xiàn)出相似的充放電曲線和電壓平臺。而轉(zhuǎn)換反應(yīng)機(jī)制是一種H+參與的可逆電化學(xué)反應(yīng)實(shí)現(xiàn)充放電的儲能機(jī)制,Zn2+無需嵌入到MnO2隧道中,而是以化合物的形式在MnO2表面生成。至于溶解-沉積機(jī)制,其主要是基于在相對高電壓區(qū)發(fā)生的氧化還原反應(yīng),利用MnO2可逆的溶解/沉積進(jìn)行儲能,與電解液的pH值有關(guān)50。對于嵌入-脫嵌儲能機(jī)理,電池容量衰減的主要原因是循環(huán)過程中發(fā)生活性材料的溶解、嚴(yán)重的相變和結(jié)構(gòu)的崩塌,而溶解-沉積機(jī)制所使用的酸性電解質(zhì)會加速鋅負(fù)極的腐蝕和析氫反應(yīng),且發(fā)生H+或Zn2+的嵌入會降低電池能量效率。不同晶體結(jié)構(gòu)的MnO2所發(fā)生的基本反應(yīng)不同,其內(nèi)在復(fù)雜機(jī)理仍需要繼續(xù)探索。
3.1 Zn2+的嵌入機(jī)制
Zn2+的嵌入機(jī)制是Zn2+在正極材料中發(fā)生可逆的嵌入-脫嵌進(jìn)行儲能。在弱酸性的Zn(NO3)2水系電解液中,放電時,Zn會快速溶解到電解液中形成Zn2+,此時溶液中的Zn2+會嵌入α-MnO2的隧道中形成ZnMn2O4(Zn2++ 2e?+ 2MnO2→ Zn Mn2O4),同時Mn會經(jīng)歷由+4價到+3價氧化還原態(tài)的轉(zhuǎn)變;充電時為放電反應(yīng)的逆過程,即Zn2+從正極中脫嵌,并重新沉積到負(fù)極上29。但不同晶體結(jié)構(gòu)的MnO2在Zn2+嵌入-脫嵌時發(fā)生的結(jié)構(gòu)轉(zhuǎn)變類型不同,其反應(yīng)過程有很大的差異。如,Zhang等45所報道的以Zn(CF3SO3)2和Mn(CF3SO3)2作為電解液的水系鋅錳電池(圖2a),在第一次放電過程中,Zn2+會嵌入β-MnO2隧道中,經(jīng)歷不可逆相變形成層狀Zn-buserite (B-ZnxMnO2·nH2O),隨后Zn2+會在該結(jié)構(gòu)內(nèi)進(jìn)行可逆的嵌入-脫嵌。γ-MnO2在Zn2+嵌入過程中也會發(fā)生相的轉(zhuǎn)變,依次轉(zhuǎn)變成尖晶石型ZnMn2O4、隧道型γ-ZnxMnO2和層狀LZnxMnO2,同時伴隨錳還原,分別從Mn(IV)態(tài)還原成Mn(III)和Mn(II)態(tài),在Zn2+完全嵌入階段,ZnMn2O4、γ-ZnxMnO2和L-ZnxMnO2共存(圖2b)37。需要注意的是,這些在循環(huán)過程中發(fā)生的相結(jié)構(gòu)轉(zhuǎn)變可能是導(dǎo)致電極結(jié)構(gòu)崩塌和容量衰減的主要因素51。
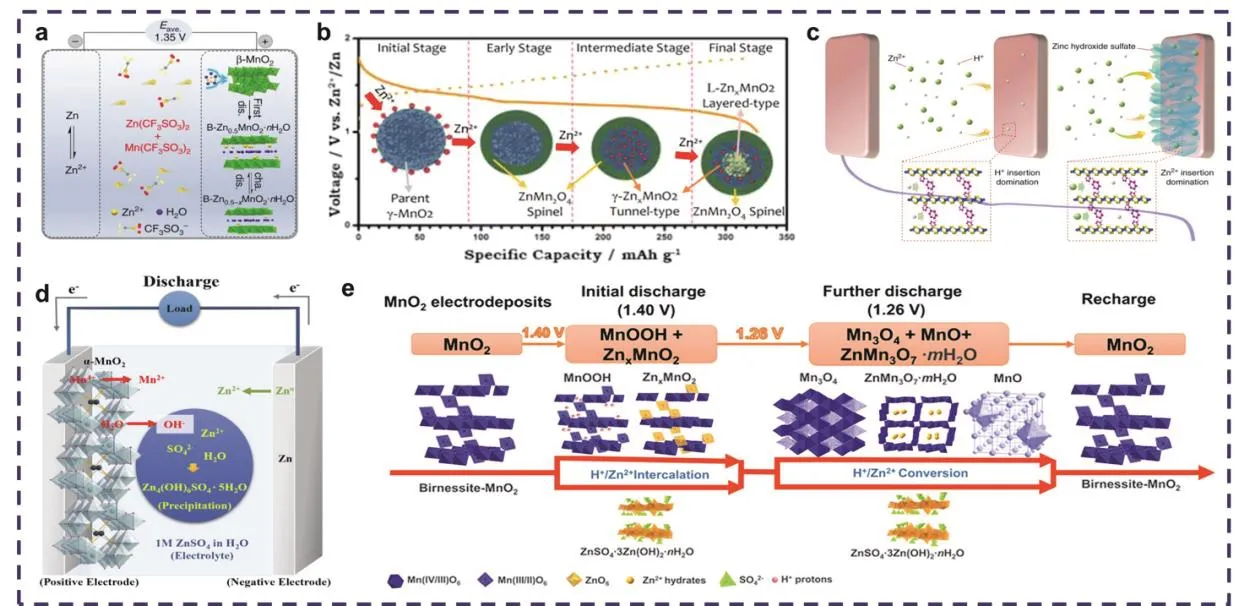
圖2 (a)基于CF3電解液的可充電鋅錳電池反應(yīng)機(jī)理示意圖45;(b) Zn2+嵌入γ-MnO2正極的反應(yīng)路徑示意圖37;(c)在層狀MnO2中共嵌入H+/Zn2+示意圖54;(d)在ZnSO4電解液中Zn//α-MnO2電池放電過程示意圖57;(e)在Zn|0.2 mol·L?1 MnSO4(aq),1 mol·L?1 ZnSO4(aq)|Carbon black電池中發(fā)生的氧化還原反應(yīng)及相應(yīng)化合物結(jié)構(gòu)轉(zhuǎn)變示意圖44Fig. 2 (a) Schematic diagram of the rechargeable Zn//MnO2 battery using CF3-based electrolyte 45; (b) Schematic diagram of the reaction pathway of Zn-insertion in γ-MnO2 cathode 37; (c) Schematic diagram of co-insertion H+/Zn2+ in layered MnO2 54; (d) Schematic diagram of showing the reactions during the discharge process for Zn//α-MnO2 battery using aqueous ZnSO4 electrolyte 57. (e) Schematic diagram of the redox reactions and crystal structures of related compounds in the Zn|0.2 mol·L?1 MnSO4 (aq), 1 mol·L?1 ZnSO4 (aq)| carbon black battery 44.
3.2 共嵌入機(jī)制
H+的離子半徑較小,與Zn2+之間的靜電相互作用較弱,且H+作為微酸水系電解液中的關(guān)鍵組分,理論上可參與離子的嵌入-脫嵌反應(yīng)。Sun等52報道了H+和Zn2+共嵌入儲能機(jī)制,證實(shí)了第一個放電平臺(~1.4 V vs. Zn2+/Zn)和第二個放電平臺(~1.3 V vs. Zn2+/Zn)分別與H+的嵌入和Zn2+的嵌入有關(guān),同時,放電過程中副產(chǎn)物MnOOH和ZnMn2O4的出現(xiàn)再次印證了H+和Zn2+的共嵌入。值得一提的是,由于H+和Zn2+存在動力學(xué)和熱力學(xué)上的差異,有報道稱H+和Zn2+的共嵌入比單一嵌入Zn2+具有更大的離子擴(kuò)散速度和更低的嵌入電阻,即水系鋅錳二次電池更傾向于有H+參與的共嵌入53。同時,Huang等54報道了一種有“自我調(diào)節(jié)機(jī)制”的共嵌入反應(yīng)(圖2c),在初始放電階段,主要發(fā)生H+的連續(xù)嵌入,這會提高溶液中OH?的局部濃度,但尚不足以形成片狀Zn4(OH)6SO4·nH2O(ZHS)。隨著二氧化錳表面的H+濃度持續(xù)降低,電池的放電平臺降低,此時主要發(fā)生Zn2+的嵌入,溶液中的OH-則會與Zn2?、和水發(fā)生反應(yīng),誘導(dǎo)ZHS在正極表面形成。Zn2+和H+的同時嵌入會進(jìn)一步促進(jìn)片狀ZHS的形成。需要注意的是,ZHS的形成會消耗多余的OH?,平衡溶液pH值,這有利于提高電池的循環(huán)穩(wěn)定性。此外,Li等44闡明了在不同電壓下Zn//MnO2電池發(fā)生的氧化還原反應(yīng)和化合物的晶體結(jié)構(gòu)轉(zhuǎn)變(圖2e),初始放電到1.40 V時,發(fā)生H+/Zn2+共嵌入反應(yīng),MnO2會轉(zhuǎn)變成MnOOH和Zn0.125MnO2,當(dāng)放電到1.26 V時,則發(fā)生H+/Zn2+轉(zhuǎn)換反應(yīng),MnOOH和Zn0.125MnO2會進(jìn)一步轉(zhuǎn)變成Mn3O4、MnO和ZnMn3O7·2H2O,充電時又重新恢復(fù)成MnO2,需要注意的是,由于反應(yīng)體系的復(fù)雜性,在反應(yīng)過程發(fā)生一些難以避免的副反應(yīng),導(dǎo)致ZnSO4·3Zn(OH)2·nH2O副產(chǎn)物的生成。
近期Wang等55提出了一種H+/NH4+共嵌入機(jī)制,即H+和NH4+可以同時嵌入到MnO2隧道中。嵌入的H+會與MnO2中的O2?結(jié)合形成O-H鍵,O-H鍵與Mn-O鍵的競爭效應(yīng)會增大后者氧原子的電子密度,而NH4+的嵌入會增強(qiáng)NH4+與MnO2之間的氫鍵,從而增大Mn3+O6八面體結(jié)構(gòu)的穩(wěn)定性。同時,H+和NH4+之間的協(xié)同作用可有效地提高載流子的擴(kuò)散動力學(xué)。根據(jù)Bader電荷分析,H+/NH4+共嵌入狀態(tài)下的電荷轉(zhuǎn)移數(shù)小于僅嵌入H+或NH4+,并經(jīng)計算發(fā)現(xiàn),共嵌入的擴(kuò)散能壘約為0.37 eV,低于僅嵌入H+或NH4+(0.51或0.43 eV)。這種共嵌入機(jī)制有效提高了鋅錳電池的電化學(xué)性能,實(shí)現(xiàn)了在4 A·g?1的電流密度下經(jīng)過4000次循環(huán)后仍能保持93.3%的容量。然而,目前MnO2中載流子的反應(yīng)路徑仍存在爭議,研究策略不夠全面,需要對不同晶型的MnO2的質(zhì)子反應(yīng)機(jī)制做出更加全面系統(tǒng)的研究。
3.3 轉(zhuǎn)化反應(yīng)機(jī)制
與傳統(tǒng)的Zn2+嵌入/脫出機(jī)制不同,Pan等56報道了一種電解液中的H+參與α-MnO2電化學(xué)反應(yīng)的機(jī)制。在弱酸性的ZnSO4+MnSO4電解液中,α-MnO2會與水中的H+形成MnOOH,而為了平衡溶液電荷,在放電時多余的OH-會與ZnSO4和H2O反應(yīng),在正極表面生成ZnSO4[Zn(OH)2]3·xH2O。充電時,ZnSO4[Zn(OH)2]3·xH2O會逐漸溶解,同時MnOOH也會恢復(fù)為原始的MnO2。其正負(fù)極的電極反應(yīng)情況可由下式表示:


基于上述討論,轉(zhuǎn)化反應(yīng)理論上與MnO2的晶體結(jié)構(gòu)和電解液的條件(如離子濃度)有關(guān)。隨后,Lee等57通過研究循環(huán)過程中離子的傳輸與反應(yīng)行為,發(fā)現(xiàn)在放電過程中錳會發(fā)生歧化溶解到電解液中,提高了電解液的pH值,導(dǎo)致Zn2+會以Zn4(OH)6(SO4)·5H2O的形式在α-MnO2表面沉積(圖2d)。但該化合物可以通過酸洗去除,說明Zn2+并未嵌入到α-MnO2隧道中,這與傳統(tǒng)觀念中的Zn2+嵌入機(jī)制不同。之后,Yang等58通過對放電后的正極形態(tài)和結(jié)構(gòu)進(jìn)行研究,證明了電池的放電過程為α-MnO2和MnOOH之間的轉(zhuǎn)化反應(yīng),無需Zn2+嵌入隧道中形成ZnMn2O4或ZnxMnO2。值得一提的是,目前對轉(zhuǎn)換反應(yīng)機(jī)理的研究不多,相關(guān)報道較少,仍以傳統(tǒng)的嵌入-脫出為主。
3.4 溶解-沉積機(jī)制
相比于傳統(tǒng)的嵌入-脫嵌機(jī)制在Mn4+/Mn3+氧化還原過程中只利用了1個有效電子轉(zhuǎn)移,基于2個有效電子轉(zhuǎn)移數(shù)的溶解-沉積機(jī)制有效提高了電池的比容量和輸出電壓,其理論容量和理論電壓分別可達(dá)616 mAh·g?1和1.991 V vs. Zn2+/Zn59,60。根據(jù)方程2可知,溶解-沉積機(jī)制與溶液的pH值密切相關(guān),MnO2/Mn2+之間的轉(zhuǎn)化會隨著pH值的降低而逐漸加強(qiáng)61。Chao等62通過添加H2SO4將電解液pH值降低至1左右,實(shí)現(xiàn)了MnO2/Mn2+較為充分的可逆轉(zhuǎn)化(圖3a)。在充電過程中,游離的Mn2+在正極集流體表面失去兩個電子轉(zhuǎn)變成了二氧化錳,在這個過程中會不斷地生成H+。而在放電時,正極表面的二氧化錳獲得兩個電子重新轉(zhuǎn)變?yōu)镸n2+。整個反應(yīng)過程如下述方程所示:

得益于這種獨(dú)特的機(jī)理,所制備的Zn//MnO2電池在高酸度環(huán)境下實(shí)現(xiàn)了很高的比容量(~570 mAh·g?1)、優(yōu)異的輸出電壓(~1.95 V vs. Zn2+/Zn)和卓越的能量密度(1100 Wh·kg?1) (圖3b)。

圖3 (a)基于溶解-沉積機(jī)制的鋅電池示意圖以及(b)其恒流放電曲線62;(c)基于溶解-沉積機(jī)制和嵌入-脫嵌機(jī)制的鋅電池示意圖以及(d)ZHS在放電過程中的作用機(jī)制50;(e)完全放電(D)和充電(C)狀態(tài)下的Mn熒光圖63Fig. 3 (a) Schematic diagram of zinc battery based on dissolution-deposition mechanism and (b) its Galvanostatic discharge curves 62. (c) Schematic diagram of zinc battery based on dissolution-deposition mechanism and intercalation mechanism and (d) the role of ZHS in the discharge process 50. (e) Mn fluorescence maps at fully discharged (D) and charged (C) states 63.
這種溶解-沉積儲能機(jī)制除了在酸性電解液中有過報道外,近期有研究人員也在弱酸性電解液中觀察到了二氧化錳的溶解-沉積過程。如Guo等50認(rèn)為,Zn//MnO2電池在首次放電過程中,MnO2與H2O反應(yīng)生成Mn2+和OH?而提高電解液的pH值,此時OH?會立即與周圍的ZnSO4發(fā)生反應(yīng)生成Zn4(OH)6SO4·4H2O;充電時Zn4(OH)6SO4·4H2O則會與Mn2+反應(yīng)生成bimeessite-MnO2,后續(xù)的充放電過程為bimeessite-MnO2的溶解-沉積過程(圖3c),此過程即為Zn//MnO2電池的放/充電過程。有趣的是,Zn4(OH)6SO4·4H2O會通過控制活性水的方式抑制Mn的溶解沉積行為(圖3d),但同時又會消耗掉電解液中多余的OH?,促進(jìn)循環(huán)反應(yīng)的持續(xù)進(jìn)行,其復(fù)雜的作用機(jī)制仍待探索。值得一提的是,H+/Zn2+的嵌入-脫出仍會發(fā)生在未充分溶解的MnO2中,只是對容量的貢獻(xiàn)值較小。同時,Wu等63利用X射線熒光映射,分析了在弱酸性電解液中錳基的具體溶解-沉積行為(圖3e)。放電時,MnO2正極會溶解成Mn2+,而充電時,MnO2則會重新沉積在正極上,但同時可觀察到一種嵌鋅的層狀錳化物(ZnMn3O7·3H2O)的存在。這種MnO2的溶解-沉積和H+/Zn2+的嵌入-脫嵌出共存的現(xiàn)象說明了這兩種機(jī)制可能普遍共同存在于水系鋅二次電池體系,只是對于容量的貢獻(xiàn)值不同。
目前MnO2的儲能機(jī)制主要以離子的嵌入-脫嵌和錳基的溶解-沉積機(jī)制為主。以電荷載流子在正極材料中嵌入-脫嵌進(jìn)行充放電循環(huán)是鋅錳二次電池典型的儲能機(jī)制,其有效轉(zhuǎn)移電子數(shù)為1,電解液通常為弱酸性。在充放電過程中發(fā)生的活性材料溶解、不可逆相變以及相變過程中造成的結(jié)構(gòu)崩塌是導(dǎo)致這類機(jī)制容量快速衰減的主要原因64。盡管對于二氧化錳的儲能機(jī)理已經(jīng)研究多年,但到目前為止,由于水系電池體系中復(fù)雜的pH值變化和存在各種副反應(yīng)等問題,隧道型、層狀和尖晶石狀等不同晶體相的MnO2的基本反應(yīng)機(jī)制仍不明晰,對其充放電行為的理解仍存在爭議,需要進(jìn)行進(jìn)一步全面且統(tǒng)一的研究。此外,一種MnO2與電解液中的H+之間發(fā)生轉(zhuǎn)化反應(yīng)的儲能機(jī)制被提出,化合物的生成-溶解即為電池的充放電過程,其與傳統(tǒng)的Zn2+嵌入-脫嵌MnO2隧道實(shí)現(xiàn)電池循環(huán)的觀念不同56。但目前對于這種機(jī)制的報道較少,有待更加深入的研究。近期,不斷有學(xué)者提出了具有2個有效轉(zhuǎn)移電子數(shù)的MnO2溶解-沉積儲能機(jī)制,并成功應(yīng)用于水系鋅錳二次電池中,該機(jī)制深受電解液中pH值的影響61,通常需要酸性電解液來實(shí)現(xiàn)充分的溶解/沉積反應(yīng)。H+的濃度在電化學(xué)反應(yīng)中起到至關(guān)重要的作用。相比于傳統(tǒng)的嵌入-脫嵌機(jī)制,溶解-沉積儲能機(jī)制合理地利用了難以避免的錳溶解的問題。值得一提的是,Xue等49指出電解液添加劑MnSO4的作用可能并不是抑制MnO2的溶解,而是促進(jìn)MnO2/Mn2+更充分可逆的沉積-溶解,從而提高電池的循環(huán)穩(wěn)定性和比容量。實(shí)際上,嵌入-脫出機(jī)制與溶解-沉積機(jī)制在水系鋅錳二次電池中應(yīng)該都是普遍存在的,但由于兩種機(jī)制的轉(zhuǎn)移電子數(shù)不同,在基于溶解-沉積機(jī)制的電池體系中發(fā)生H+/Zn2+的嵌入可能會降低電池的比容量。因此,如何明晰這兩種機(jī)制的反應(yīng)路徑,并有效地結(jié)合兩者的優(yōu)勢,突破現(xiàn)有容量瓶頸,開發(fā)出高性能水系鋅錳二次電池,是目前所需要深入研究的問題。
4 二氧化錳的優(yōu)化措施
目前,對于嵌入-脫嵌機(jī)制,需要解決循環(huán)過程中發(fā)生的活性材料溶解、本征電導(dǎo)率低、不可逆相變和結(jié)構(gòu)崩塌,以及由于Zn2+與宿主材料之間的強(qiáng)靜電相互作用而導(dǎo)致的離子擴(kuò)散動力學(xué)行為變差,和電極添加劑(如PVDF)的使用會阻礙載流子的傳輸?shù)葐栴}。而溶解-沉積機(jī)制當(dāng)前仍處于探索階段,其內(nèi)在機(jī)理并未明晰。在該體系下電池的高容量和高電壓平臺依賴于充分可逆的錳溶解。此外,反應(yīng)過程中發(fā)生的不可避免的H+/Zn2+嵌入以及強(qiáng)酸性的電解液會加速金屬鋅負(fù)極的腐蝕和析氫等問題,都會造成Zn//MnO2電池較差的循環(huán)穩(wěn)定性和庫倫效率。為了有效提高Zn//MnO2電池的各項(xiàng)電化學(xué)性能,下文將針對MnO2主要的儲能機(jī)制(嵌入-脫嵌和溶解-沉積機(jī)制),總結(jié)MnO2正極材料現(xiàn)有的優(yōu)化策略。
4.1 針對嵌入-脫嵌機(jī)制的優(yōu)化策略
4.1.1 復(fù)合材料改性
復(fù)合材料改性策略可通過結(jié)合碳基材料、有機(jī)物等來提高電極材料導(dǎo)電性,同時提供更大的比表面積和更多的活性位點(diǎn),并有效防止相變造成的結(jié)構(gòu)崩塌,進(jìn)而提升水系鋅錳二次電池電化學(xué)性能64。
常用于復(fù)合的碳材料有碳纖維、石墨烯、碳納米管等。其中碳纖維具有特殊的離子/電子傳輸通道和收集定向電子的功能,且對于水介質(zhì)具有較低的電化學(xué)活性和較寬的電化學(xué)窗口。同時碳纖維還可起到支撐作用,防止發(fā)生結(jié)構(gòu)崩塌,提高電池的循環(huán)穩(wěn)定性。Chen等65合成了一種在碳納米纖維(CNFs)表面原位生長出的垂直排列的MnO2納米片結(jié)構(gòu)(MOC,圖4a),導(dǎo)電的CNFs與MnO2的緊密聯(lián)系形成的互連網(wǎng)絡(luò)顯著提高了正極材料的離子/電子轉(zhuǎn)移動力學(xué),且層間的結(jié)晶水起到了結(jié)構(gòu)支架的作用,維持了活性材料內(nèi)部結(jié)構(gòu)的穩(wěn)定。同時,超薄的MnO2納米片增大了電極與電解液界面的接觸面積,有效增加了反應(yīng)活性位點(diǎn)。此外,通過測定由不同KMnO4/CN質(zhì)量比F (0,5 : 1,15 : 1)制備的MOC在不同電流密度下的比容量(圖4b),發(fā)現(xiàn)其中MOC-5在200 mA·g?1電流密度下實(shí)現(xiàn)了297 mAh·g?1的高放電容量,且當(dāng)電流密度從3000 mA·g?1回到200 mA·g?1后,容量仍能保持在283 mAh·g?1,表現(xiàn)出了高達(dá)95%的容量保持率,同時其在200 mA·g?1的電流密度下經(jīng)過700次循環(huán)后仍保留有221 mAh·g?1的高容量(圖4c)。碳布是一種重量輕、抗彎折能力強(qiáng)、電導(dǎo)率高和化學(xué)穩(wěn)定性強(qiáng)的材料,在其表面電沉積MnO2可以制備出高性能電極材料,有效提高離子/電子的傳輸速率,表現(xiàn)出良好的導(dǎo)電性和電化學(xué)穩(wěn)定性66。除了碳布外,經(jīng)過優(yōu)化改性制備的碳材料能夠顯著提高自身的物理化學(xué)性能,可應(yīng)用于改善電池性能。如氮摻雜碳納米片(N-CNSs)網(wǎng)絡(luò)由具有豐富的納米孔結(jié)構(gòu)的N-CNS相互連接而成,該多孔骨架框架能增大材料比表面積,并提供更多的離子/電子傳輸通道,同時摻雜N時所形成的缺陷能夠有效提高反應(yīng)活性,是良好的導(dǎo)電材料67。Fu等68通過金屬-有機(jī)框架模板策略制備出了具有多孔骨架的氮摻雜錳基正極材料(MnOx@N-C),得益于材料的多孔性、獨(dú)特滲氮導(dǎo)電碳網(wǎng)絡(luò)結(jié)構(gòu)和電解質(zhì)中Zn2+和Mn2+的協(xié)同作用,其表現(xiàn)出了優(yōu)良的電化學(xué)性能。同時,還可利用三維多孔泡沫骨架具有高電導(dǎo)率的優(yōu)勢以提高電子轉(zhuǎn)移和離子擴(kuò)散速率,如一種由α-MnO2和具有三維多孔泡沫結(jié)構(gòu)的碳納米管(CNTs)復(fù)合而成的薄膜材料α-MnO2@CNT,其能有效改善離子/電子擴(kuò)散動力學(xué),賦予了電極材料更快的離子擴(kuò)散速率和更優(yōu)異的導(dǎo)電性,在0.97C(1C = 308 mA·g?1)的 電 流密度 下 實(shí)現(xiàn)了 308.5 mAh·g?1的放電比容量69。

圖4 (a) MOC的合成示意圖;(b)以MOC-5,MOC-15和MO分別作為正極,2 mol·L?1 ZnSO4和0.1 mol·L?1 MnSO4作為電解液的的鋅離子電池在不同電流密度下的倍率性能以及(c)在0.2 A·g?1電流密度下的循環(huán)性能65;(d) MnO2@PEDOT樣品的高分辨透射電鏡(HRTEM)圖像以及(e)柔性準(zhǔn)固態(tài)Zn//MnO2@PEDOT電池在1.86 A·g?1電流密度下經(jīng)過300次循環(huán)后的循環(huán)性能和庫倫效率;(f)三個柔性準(zhǔn)固態(tài)Zn//MnO2@PEDOT電池供電的由45個發(fā)光二極管組成的霓虹燈以及(g)電池為手表上的LED燈供電的圖片72Fig. 4 (a) Schematic diagram of the synthetic procedure of MOC. (b) The rate performance of zinc ion battery with MOC-5, MOC-15 and MO as positive electrodes and 2 mol·L?1 ZnSO4 and 0.1 mol·L?1 MnSO4 as electrolyte at different current densities and (c) the cycle performance at current density of 0.2 A·g?1 65. (d) HRTEM images of MnO2@PEDOT sample and (e) Cycling performance and Coulombic efficiency collected at 1.86 A·g?1 for 300 cycles of flexible quasi-solidstate Zn//MnO2@PEDOT battery. (f) Photographs of a neon sign composed of 45 light-emitting diodes powered by three flexible quasi solid Zn// MnO2@PEDOT battery devices and (g) a watch with LED lights powered by three devices 72.
正極表面的涂層可形成穩(wěn)定的固體電解質(zhì)界面(簡稱SEI膜),能有效抑制Mn2+的溶解,增強(qiáng)電極表面穩(wěn)定性,從而提高電池循環(huán)性能。已報道的涂層材料可分為有機(jī)物和無機(jī)物兩大類。作為最典型的例子,Wu等70提出了一種石墨烯(rGO)均勻包覆的α-MnO2(MGS)正極材料。利用電感耦合等離子體(ICP)分析在2 mol·L?1ZnSO4電解液中錳的溶解行為,發(fā)現(xiàn)在放電過程中,Zn//MGS電池電解液中Mn的濃度比在原始Zn//MnO2電池中要低,說明rGO涂層的存在有效抑制了電池循環(huán)過程中MnO2的溶解。因此,Zn//MGS電池能在0.3 A·g?1條件下經(jīng)過100次循環(huán)后仍具有406.6 Wh·kg?1(382.2 mAh·g?1)的高能量密度。但石墨烯的高昂成本也大大限制了其大規(guī)模商業(yè)化的發(fā)展。除了石墨烯,其他碳材料如無定形碳等,其獨(dú)有的多孔性不僅能有效提高離子/電子的傳輸速率,還能建立穩(wěn)定的電極結(jié)構(gòu),實(shí)現(xiàn)優(yōu)異的電化學(xué)性能68。此外,研究人員還報道了利用原位電化學(xué)法在二氧化錳表面形成CaSO4·2H2O的SEI薄膜保護(hù)層的策略,有效提高電池電化學(xué)穩(wěn)定性,延長使用壽命71。需要注意的是,由于非導(dǎo)電涂層會降低載流子的擴(kuò)散速率,在設(shè)計時應(yīng)考慮正極界面處離子傳輸和電解液可及性的問題。
導(dǎo)電聚合物不僅具有較高的導(dǎo)電性、優(yōu)異的化學(xué)穩(wěn)定性和較強(qiáng)的電荷儲存能力的優(yōu)勢,還具有環(huán)境友好、成本低廉等特性,可作為活性材料的理想保護(hù)涂層。Zeng等72報道了一種用于修飾MnO2界面的聚3,4-乙基二氧硫吩(PEDOT)涂層(圖4d),PEDOT緩沖涂層在抑制錳溶解和結(jié)構(gòu)崩塌的同時保證了較高的載流子傳輸速率。同時,MnO2@PEDOT可直接在柔性碳布上制備,避免使用粘結(jié)劑。以PVA/ZnCl2/MnSO4凝膠作為電解液,所制備出的柔性準(zhǔn)固態(tài)電池Zn//MnO2@PEDOT具有良好的循環(huán)性能和庫倫效率(圖4e),可為發(fā)光二極管供電(圖4f),并作為柔性電源為手表供電(圖4g),表明其在可穿戴電子產(chǎn)品中具有廣闊的應(yīng)用前景。此外,有研究人員提出聚吡咯(PPy)和聚苯胺(PANI)等導(dǎo)電聚合物也可以充當(dāng)二氧化錳的涂層以緩解在充放電過程中活性材料的溶解73,74。
4.1.2 納米結(jié)構(gòu)優(yōu)化
蘇:豪邁!羌族沙朗舞的這種感染力讓人心里很舒服,就會使我情不自禁地加入當(dāng)中去。在各種豐收、節(jié)慶的日子里,不論男女老少都要跳。沙朗舞的風(fēng)格比較淳樸,節(jié)奏比較輕快,動作比較粗獷,具有強(qiáng)烈的民族藝術(shù)感染力,容易吸引大家的注意力和興趣,充分顯示出我們的羌族文化氣息及獨(dú)特的藝術(shù)風(fēng)格。
納米尺寸的電極材料具有較大的表面積和優(yōu)異的尺寸效應(yīng)(包括微小尺寸效應(yīng)與真實(shí)尺寸效應(yīng))。納米材料有更大的電解液接觸面積,載流子容易在納米結(jié)構(gòu)表面擴(kuò)散,這顯著提高了電池的倍率性能。此外,納米材料還可緩解體積膨脹問題,維持結(jié)構(gòu)穩(wěn)定,從而實(shí)現(xiàn)長循環(huán)壽命75。根據(jù)公式τeq= L2/2D (τeq為擴(kuò)散時間,L為材料尺寸,D為擴(kuò)散系數(shù))可知,合成納米尺寸的電極材料(即降低L)可有效降低離子的τeq,從而提高電池充放電速率。
MnO2的晶體形態(tài)很大程度上決定Zn2+的存儲性能22,目前,不同晶體結(jié)構(gòu)和形貌的納米MnO2在水系鋅錳二次電池中得到廣泛的研究。Kim等76報道的3D分層介孔γ-MnO2納米球(UW-MO)結(jié)構(gòu)具有比本體γ-MnO2更優(yōu)異的循環(huán)穩(wěn)定性和電荷容量,在50個循環(huán)后UW-MO仍有400 mAh·g?1的比容量,而MO逐漸下降到180 mAh·g?1。此外,與其他隧道型的MnO2晶型相比,β-MnO2具有較窄的隧道結(jié)構(gòu),不利于Zn2+的存儲。而Lslam等30采用微波輔助水熱合成法制備了暴露(101)平面的β-MnO2納米棒,并將其作為水系鋅錳二次電池的正極材料(圖5a),其中,(101)峰在Zn2+嵌入β-MnO2后會向更低的角度轉(zhuǎn)變,這歸因于錳的還原導(dǎo)致Mn―O鍵的延伸(圖5b)。Zn2+嵌入-脫嵌過程中,β-MnO2納米棒電極分別在0.15、0.25和0.3 nm處表現(xiàn)出三個不同的傅里葉變化(FT)峰,分別對應(yīng)Mn―O,共享邊緣的Mn―Mn和共享角的Mn―Mn。將β-MnO2納米棒沿a軸旋轉(zhuǎn)約90°后,可以看到納米棒中的[1 ×1]開放隧道,這種獨(dú)特的一維棒狀形態(tài)增大了電極與電解液的接觸面積,有利于Zn2+在β-MnO2結(jié)構(gòu)內(nèi)的嵌入-脫嵌。所制備的電池在100 mA·g?1電流密度下實(shí)現(xiàn)了高達(dá)270 mAh·g?1的放電比容量,以及經(jīng)過200次循環(huán)后仍保持75%的容量保持率和100%的庫倫效率(200 mA·g?1電流密度)。納米結(jié)構(gòu)的優(yōu)異性還體現(xiàn)在其他晶型當(dāng)中,如Liu等77提出的具有(1D-3D)混合網(wǎng)絡(luò)結(jié)構(gòu)的δ-MnO2納米線正極,這種獨(dú)特的結(jié)構(gòu)增大了電極與電解質(zhì)的接觸面積,提供了更多活性位點(diǎn)和快速的離子傳輸通道。以及Alfaruqi等78報道的一種納米α-MnO2正極,其具有優(yōu)異的結(jié)構(gòu)穩(wěn)定性,顯著提高了Zn2+嵌入正極的可逆性。

圖5 (a) β-MnO2納米棒樣品的晶體結(jié)構(gòu)以及(b) β-MnO2結(jié)構(gòu)內(nèi)(101)晶格平面示意圖;(c) Zn//MnO2經(jīng)歷充放電后β-MnO2納米棒的EXAFS光譜30;(d) δ-MnO2納米片的形成示意圖;(e) δ-MnO2納米片與微球電極的Nyquist示意圖(黑線為擬合線) 79;(f)不同合成階段的α-MnO2 NFs和α-MnO2/CNT HMs的制備示意圖和相應(yīng)產(chǎn)物的SEM圖像以及(g)將α-MnO2 NFs和α-MnO2/CNT HMs作為電極制備的鋅離子電池(ZIBs)在電壓范圍為1.2–1.85 V時的速率能力比較81Fig. 5 (a) Schematic diagram of crystal structure of β-MnO2 nanorod sample and (b) (101) lattice planes in the β-MnO2 structure. (c) EXAFS spectra of the β-MnO2 nanorod cathode collected after discharging/charging 30.(d) Schematic diagram of the formation of δ-MnO2 nanosheets. (e) Nyquist diagram of δ-MnO2 nano sheet and microsphere electrode (black line is fitting line) 79. (f) Preparation diagrams of α-MnO2 NFs and α-MnO2/CNT HMs at different synthesis stages and SEM images of corresponding products and (g) rate capability comparison at voltage cutoffs of 1.2–1.85 V of ZIBs with α-MnO2 NFs and α-MnO2/CNT HMs 81.
納米尺寸的電極材料會縮短離子擴(kuò)散的距離,縮小擴(kuò)散時間,改善電化學(xué)反應(yīng)動力學(xué)75。Guo等79制備了一種超薄δ-MnO2納米片結(jié)構(gòu)(圖5d),通過對超薄δ-MnO2納米片和納米球結(jié)構(gòu)進(jìn)行電化學(xué)阻抗譜測試(EIS) (圖5e),可發(fā)現(xiàn)具有納米片結(jié)構(gòu)的δ-MnO2的電荷轉(zhuǎn)移電阻為46 ?,遠(yuǎn)小于納米球δ-MnO2的223 ?,這可能是因?yàn)殡x子在厚度為2–4 nm的薄納米片中的擴(kuò)散路徑小于在50 nm厚的納米球中,因此所需的擴(kuò)散時間更短。此外,Wang等80所報道的2D單原子層納米MnO2作為正極會在水平和垂直方向上提供相互交聯(lián)的離子傳輸通道,相較于多層納米MnO2,單層納米MnO2具有更短的離子擴(kuò)散路徑,可實(shí)現(xiàn)更快的電子/離子傳輸速率。這基本上可以說明更小尺寸的納米結(jié)構(gòu)具有更快的電化學(xué)反應(yīng)速率。此外,具有納米尺寸的活性材料更容易適應(yīng)離子嵌入-脫嵌時所發(fā)生的體積變化,有效防止相變造成的結(jié)構(gòu)坍塌,表現(xiàn)出優(yōu)異的循環(huán)穩(wěn)定性。如Liu等81利用電化學(xué)沉積法制備了α-MnO2與納米纖維/碳納米管的復(fù)合材料(α-MnO2/CNT HMs) (圖5f),其獨(dú)特的復(fù)合結(jié)構(gòu)有助于提高電極材料的電化學(xué)穩(wěn)定性。再加上納米纖維α-MnO2(α-MnO2NFs)與CNTs之間形成了一種緊密排列的網(wǎng)絡(luò)結(jié)構(gòu),兩者之間的協(xié)同作用提供了更多可快速轉(zhuǎn)移電荷的通道和豐富的活性反應(yīng)位點(diǎn),有效改善了活性材料的電荷轉(zhuǎn)移動力學(xué),從而提高了電池的倍率性能(圖5g)。
需要注意的是,盡管納米材料具有諸多優(yōu)勢,但仍存在諸如熱穩(wěn)定性下降、表面副反應(yīng)多等問題75。如納米顆粒由于具有非常高的比表面積和表面能,會傾向于形成團(tuán)聚體,導(dǎo)致接觸電阻升高,或在循環(huán)過程中發(fā)生電化學(xué)團(tuán)聚現(xiàn)象,降低電池容量,同時還會增加電極與電解液之間發(fā)生副反應(yīng)的概率。此外,納米結(jié)構(gòu)的電極材料相比于普通電極具有更窄的電化學(xué)穩(wěn)定窗口。因此,在設(shè)計納米結(jié)構(gòu)改性電極材料時,需綜合考慮納米材料的優(yōu)劣勢來設(shè)計高性能鋅錳二次電池正極材料。
4.1.3 客體預(yù)嵌策略
不可逆的非平衡相變以及嵌入層結(jié)構(gòu)的不穩(wěn)定性會導(dǎo)致電池容量衰減,影響電池性能82。通過在具有層狀結(jié)構(gòu)的MnO2中預(yù)嵌入客體,如水分子83、有機(jī)分子84和無機(jī)金屬離子85等,能夠?yàn)閆n2+/H+的嵌入-脫嵌提供穩(wěn)定的內(nèi)部結(jié)構(gòu),緩解其在嵌入-脫出過程中引起的結(jié)構(gòu)崩塌,優(yōu)化晶體結(jié)構(gòu),同時減弱Zn2+離子與MnO2之間的靜電相互作用,提高載流子的擴(kuò)散速率。相比于其他具有隧道結(jié)構(gòu)的MnO2晶型,δ-MnO2具有較寬的層間距,更適合預(yù)嵌入客體,是大多數(shù)預(yù)嵌入策略的選擇。

圖6 (a) PANI-MnO2納米層結(jié)構(gòu)示意圖;(b)經(jīng)過400 °C熱處理去除PANI后的PANI-MnO2納米層結(jié)構(gòu)的HR-TEM圖像54;(c) cw-MnO2的XRD圖案和晶體結(jié)構(gòu);(d)左圖:Zn插層結(jié)構(gòu)和所需的相應(yīng)能量;右圖:鋅的球內(nèi)絡(luò)合效應(yīng)導(dǎo)致面向錳的突出,形成放大的Zn-Mn啞鈴結(jié)構(gòu)(數(shù)字代表原子間的距離) 83;(e)預(yù)嵌Na+和水分子的δ-MnO2充放電工作示意圖;(f) δ-NMOH電極的非原位XRD圖87Fig. 6 (a) Schematic diagram of PANI-MnO2 nanolayers structure. (b) HR-TEM image of PANI-MnO2 nanolayers structure after removing PANI by heat treatment at 400 °C 54. (c) XRD pattern and crystal structure of cw-MnO2.(d) Left: Zn-intercalation structure and corresponding energy; Right: the inner-sphere complexation of zinc leads to the protrusion of the facing Mn, constituting a Zn-Mn dumbbell structure as zoomed (numbers represents the distance between atoms) 83. (e) Schematic diagram of pre-intercalated Na+ and water molecules δ-MnO2 during charging and discharging.(f) ex situ XRD pattern of δ-NMOH electrode 87.
將金屬陽離子K+、Ba2+、Na+、Co2+/3+作為客體嵌入MnO2會占據(jù)特定的晶格位點(diǎn),或增大電極的晶格間距,并與Zn2+發(fā)生相互作用,從而改變正極的導(dǎo)電性。如Zhang等88提出了一種預(yù)嵌La3+的納米δ-MnO2電極材料(LMO),預(yù)嵌的La3+可有效降低Zn2+與MnO2間的相互作用力,改善Zn2+的嵌入-脫嵌動力學(xué)行為,使得LMO具有更大的儲鋅容量、更快的反應(yīng)速率和可逆的氧化還原反應(yīng),同時La3+還能對晶體結(jié)構(gòu)起到支撐作用,防止在循環(huán)過程中發(fā)生結(jié)構(gòu)的崩塌,最終Zn//MnO2全電池展現(xiàn)了超高的容量密度375.9 Wh·kg?1(100 mA·g?1電流密度)。
雖然客體嵌入MnO2被普遍認(rèn)為可以擴(kuò)大層間距、促進(jìn)載流子的嵌入/脫出,并提高結(jié)構(gòu)穩(wěn)定性82。然而,有報道指出發(fā)現(xiàn)引入的金屬陽離子會通過物理阻塞和靜電排斥作用阻礙載流子在隧道中的擴(kuò)散89,說明當(dāng)隧道被預(yù)先填充了不輕易去除的金屬陽離子時,可能會大大降低載流子嵌入/脫出速率。因此,在設(shè)計客體預(yù)嵌改性MnO2正極時,應(yīng)綜合考慮外來離子對于載流子運(yùn)輸?shù)淖璧K作用和其對于穩(wěn)定材料結(jié)構(gòu)的貢獻(xiàn)等方面,從而開發(fā)出更優(yōu)異的電極材料。
4.1.4 缺陷工程
電化學(xué)反應(yīng)與電極材料的電子結(jié)構(gòu)有密切的關(guān)系,其可決定載流子的擴(kuò)散速率,而晶體結(jié)構(gòu)中的缺陷會影響電子結(jié)構(gòu)的分布。晶體中缺陷的類型主要有點(diǎn)缺陷(如空位)、線缺陷(如位錯)、面缺陷(如晶界)和體缺陷(如雜質(zhì)引起的晶格無序狀態(tài))。缺陷的存在可提供更多載流子的儲存/吸附/活性位點(diǎn),有效減小離子間的靜電斥力,克服遷移和擴(kuò)散障礙,并降低反應(yīng)勢壘,從而提高離子的嵌入/脫出速率90。
在MnO2中摻雜異質(zhì)元素會導(dǎo)致在原帶隙上產(chǎn)生新的缺陷態(tài)(如空位),處于缺陷態(tài)上的電子結(jié)構(gòu)會發(fā)生改變,降低鋅嵌入的能壘,從而實(shí)現(xiàn)更優(yōu)異的電化學(xué)性能。通過摻雜異質(zhì)元素所形成的氧空位能有效調(diào)控其表面化學(xué)和幾何構(gòu)型,如Lian等91報道了一種Ti摻雜α-MnO2,雖然Ti的摻雜會導(dǎo)致層間收縮,但由于錳價態(tài)的降低,會產(chǎn)生氧空位進(jìn)行電子補(bǔ)償。而氧空位會打開[MnO6]八面體壁,導(dǎo)致晶體結(jié)構(gòu)中電荷分布不均和局部電場不平衡,從而加速離子/電子的擴(kuò)散速率,實(shí)現(xiàn)高倍率性能和長循環(huán)穩(wěn)定性。同時,F(xiàn)ang等92報道了一種K+摻雜與氧缺陷復(fù)合材料(K0.8Mn8O16,KMO)。與原始的α-MnO2相比,KMO具有更快的H+擴(kuò)散速度,有效提高了電化學(xué)反應(yīng)動力學(xué)(圖7a)。這是因?yàn)檠跞毕菽苡行Ы档脱趸€原反應(yīng)過程中電子運(yùn)輸和電荷轉(zhuǎn)移的能量勢壘,并打開了α-MnO2中[MnO6]多面體壁,促進(jìn)H+的擴(kuò)散(圖7b)。所制備的Zn//K0.8Mn8O16電池實(shí)現(xiàn)了398 Wh·kg?1的高能量密度,在經(jīng)過1000次充放電循環(huán)后仍無明顯的容量衰減(圖7c),顯示出了缺陷工程在發(fā)展高性能正極材料方向上的潛力。此外,Kim等31報道了一種摻雜氟(F)的β-MnO2交錯球狀納米片正極材料,這種F摻雜策略有效擴(kuò)大了β-MnO2的晶格尺寸,提供了更多的電化學(xué)反應(yīng)活性位點(diǎn)。同時因摻雜而引入的氧缺陷不僅會通過改變局部電子結(jié)構(gòu)來提高電導(dǎo)率,還能降低鋅嵌入的能量勢壘,進(jìn)而促進(jìn)鋅離子的嵌入/脫嵌行為。結(jié)合交錯穩(wěn)定的內(nèi)部網(wǎng)絡(luò)結(jié)構(gòu),實(shí)現(xiàn)了優(yōu)異的循環(huán)穩(wěn)定性和倍率性能,在1800 W·kg?1功率密度下實(shí)現(xiàn)158 Wh·kg?1的高能量密度,且在經(jīng)過150次循環(huán)后容量保持率仍達(dá)85%。

圖7 (a)KMO和α-MnO2電極在不同放電/充電狀態(tài)下的GITT曲線和相應(yīng)的H+擴(kuò)散系數(shù);(b) H+在KMO的完整結(jié)構(gòu)及含氧缺陷結(jié)構(gòu)中擴(kuò)散示意圖;(c) KMO和α-MnO2電極在1000 mA·g?1下的長壽命循環(huán)性能和KMO電極的最后十條充放電曲線92;(d) β-MnO2和Ce摻雜β-MnO2的晶體結(jié)構(gòu);(e) β-MnO2和0.1 mmol Ce摻雜β-MnO2的EIS奈奎斯特圖和等效電路85Fig. 7 (a) GITT curves and corresponding H+ diffusion coefficients of KMO and α-MnO2 electrodes under different discharge/charge states. (b) Schematic diagram of H+ diffusion in the complete structure and oxygen defect structure of KMO. (c) Long cycle performance of KMO and α-MnO2 electrode and the last ten charge/discharge curves of KMO electrode at 1000 mA·g?1 92. (d) Crystal structure of β-MnO2 and Ce doping β-MnO2;(e) EIS Nyquist diagram and equivalent circuit of the β-MnO2 and 0.1 mmol Ce doping cathode 85.
4.1.5 元素?fù)诫s
異質(zhì)元素與MnO2具有不同的電子構(gòu)型,可以調(diào)節(jié)材料的表面形態(tài),誘導(dǎo)結(jié)構(gòu)發(fā)生轉(zhuǎn)變,極大地影響電極材料的結(jié)構(gòu)和電化學(xué)性能。此外,利用Mn與異質(zhì)元素的鍵合作用,可增強(qiáng)晶體結(jié)構(gòu)穩(wěn)定性,防止其在相變過程中發(fā)生坍塌,提高M(jìn)nO2正極的電荷存儲性能93。
稀土元素具有特殊的4f電子構(gòu)型,可與MnO2相互作用,調(diào)節(jié)其表面形態(tài)。結(jié)合納米結(jié)構(gòu)與金屬元素?fù)诫s的優(yōu)異性,Wang等85提出了一種通過水熱法合成的Ce摻雜MnO2納米棒正極材料,Ce的摻雜誘導(dǎo)MnO2從原來的β相轉(zhuǎn)變成新的α相(圖7d),出現(xiàn)了[2 × 2]隧道結(jié)構(gòu)。其循環(huán)伏安(CV)曲線表明,Ce摻雜β-MnO2的正極峰和負(fù)極峰中心之間的電壓差明顯小于未摻雜的β-MnO2。且Ce摻雜β-MnO2的電荷轉(zhuǎn)移電阻遠(yuǎn)低于本體β-MnO2,表明前者具有更優(yōu)異的導(dǎo)電性(圖7e)。基于改性β-MnO2制備的Zn//MnO2電池能在5C (1C = 308 mA·g?1)的電流密度下實(shí)現(xiàn)134 mAh·g?1的高容量。除了稀土元素外,Alfaruqi等94報道了一種利用氧化還原反應(yīng)制備的V摻雜MnO2納米正極,這種V摻雜MnO2的平均晶粒尺寸小于原始的MnO2,增大了活性材料的比表面積,且增加了反應(yīng)活性位點(diǎn),有效提高了材料的導(dǎo)電性。相比于原始MnO2,其具有更高的放電容量(266 vs. 213 mAh·g-1)。此外,摻雜微量元素(如N、La、Ca等)也可以降低電荷轉(zhuǎn)移電阻,從而改善MnO2的導(dǎo)電性,進(jìn)而提升電池的電化學(xué)性能95,96。
氟摻雜是一種常見的改善電極電化學(xué)儲能的方法98。它不僅可以誘導(dǎo)缺陷的生成和提供更多的Zn2+電化學(xué)活性位點(diǎn),其極高的電負(fù)性和對離子的吸附能力還能有效調(diào)節(jié)電極性能,從而促進(jìn)Zn2+的嵌入/脫嵌行為。同時,Liu等93還提出了一種Mn-F鍵的引起的“釘扎效應(yīng)”,這種效應(yīng)構(gòu)建了一種活性高且穩(wěn)定的晶格框架,并提供快速的離子傳輸通道,在0.6C (1C = 308 mA·g?1)的電流密度下實(shí)現(xiàn)了高達(dá)311.6 mAh·g?1的比容量,以及在5C下經(jīng)過1200次循環(huán)后仍無明顯的容量衰減。值得一提的是,氧具有高電負(fù)性,采用低電負(fù)性元素如S和C等取代氧從而降低Zn2+在晶體結(jié)構(gòu)中的擴(kuò)散勢壘似乎可以實(shí)現(xiàn)。但目前少有對陰離子摻雜的研究報道,有待進(jìn)一步研究。
4.2 針對溶解-沉積機(jī)制的優(yōu)化措施
近年來,溶解-沉積機(jī)制由于其高放電電壓、高能量密度等優(yōu)勢受到了研究人員的大量關(guān)注。Chao等62在水系鋅錳二次電池中提出了這種具有雙電子轉(zhuǎn)移的氧化還原反應(yīng),基于此機(jī)制所制備的Zn//MnO2電池的理論容量可達(dá)616 mAh·g?1,這是單電子氧化還原反應(yīng)容量(308 mAh·g?1)的兩倍,同時,其理論電壓可達(dá)1.991 V vs. Zn2+/Zn,能量密度可超過1100 Wh·kg?1。當(dāng)前,基于溶解-沉積機(jī)制已經(jīng)能成功制備出接近理論容量的高容量電池。但仍存在反應(yīng)路徑尚未明晰(如無法明確放電平臺降低的原因)、酸性的電解液會對負(fù)極有腐蝕作用以及MnO2難以充分溶解等問題。目前所報道的優(yōu)化措施主要有調(diào)節(jié)電解液成分、活性催化以及制備解耦體系、液流體系電池等。
通過改變電解液成分,可有效調(diào)控MnO2的溶解沉積行為,并控制鋅負(fù)極腐蝕和析氫等問題。Zeng等98報道了一種以接近中性的Zn(CH3COO)2和Mn(CH3COO)2作為電解液的Zn//MnO2電池(圖8a)。CH3COO?是一種典型的弱酸離子,具有強(qiáng)極化性和高電負(fù)性。電解液中的CH3COO?會吸附在MnO2表面的Mn位點(diǎn),這顯著削弱了其與水的結(jié)合作用,改變了MnO2正極的表面性質(zhì),進(jìn)而降低Mn溶解的能量勢壘(圖8b)。同時,接近中性的電解液可抑制鋅負(fù)極析氫和腐蝕的問題,并提供了556 mAh·g?1的高比容量和1.5 V的工作電壓。此外,Lei等99提出了一種碘化物(I?)介質(zhì)調(diào)節(jié)策略,即I?會將固態(tài)的MnO2還原成Mn2+,同時自身被氧化成I3?,并在后續(xù)的充電過程中重新還原成I?。這種I3?/I?對MnO2//Mn2+的協(xié)同作用可提高未充分溶解的MnO2的活性,使其具備循環(huán)溶解-沉積的能力。同時,Zheng等100報道了一種溴(Br?)介質(zhì)調(diào)節(jié)的Zn-Br2//MnO2電池,這種溴介質(zhì)可以有效促進(jìn)MnO2溶解的可逆性,并在一定程度上提高電池的面積比容量(5.8 mAh·cm?2,靜態(tài)條件)。

圖8 (a)醋酸基電解質(zhì)中Zn//MnO2電池示意圖;(b) MnO2與裸露的表面和含有豐富的醋酸表面發(fā)生溶解反應(yīng)的原子結(jié)構(gòu)98。(c) Zn//MnO2解耦電池的充放電示意圖以及(d)電極氧化的MnO2(101)和(e) Ni-MnO2(101)的電子密度差示意圖106;(f) Mn(Ac)2(左上角)和MnSO4電解液(右上角)的電化學(xué)機(jī)制;(g)電解液為0.5 mol·L?1 Mn(Ac)2 +0.5 mol·L?1 Zn(Ac)2 + 2 mol·L?1 KCl的液流電池的充放電曲線以及(h)在40 mA·cm-2電流密度下的循環(huán)性能109Fig. 8 (a) Schematic diagram of Zn//MnO2 battery in acetate electrolyte. (b) Atomic structures for the dissolution reaction on MnO2 with a bare surface and with an acetate-rich surface 98. (c) Schematic illustration of Zn//MnO2 in the hybrid electrolytes during charge/discharge and electron density difference between (d) electrooxidized MnO2 (101) and(e) Ni-MnO2 (101) 106. (f) Electrochemical mechanism of Mn(AC)2 (top left corner) and MnSO4 electrolyte(top right corner). (g) The charge/discharge curve of the flow battery with electrolyte of 0.5 mol·L?1 Mn(AC)2 + 0.5 mol·L?1 Zn(AC)2 + 2 mol·L-1 KCl and (h) the cycle performance at current density of 40 mA·cm?2 109.
金屬元素對電化學(xué)反應(yīng)有催化作用,可促進(jìn)活性錳的沉積作用,有效提高電池的反應(yīng)動力學(xué)。Zhong等101報道了一種Co修飾的δ-MnO2正極材料,其中Mn(IV)和Co(III)的雙催化作用促進(jìn)了活性Mn的可逆沉積。其催化途徑如下:

Co誘導(dǎo)的共催化有效促進(jìn)了Mn的電化學(xué)沉積能力,因此,所制備的電池具有超過500 mAh·g?1的高比容量,且在經(jīng)過5000次循環(huán)后仍保持63%的容量。
由于酸性電解液中存在大量質(zhì)子,會促進(jìn)析氫反應(yīng)(HER),而析氧反應(yīng)(OER)在堿性電解液中更容易發(fā)生102,103。在解耦電池體系中,離子交換膜能分離正/負(fù)極電解液,可同時實(shí)現(xiàn)正極電解液呈酸性,負(fù)極電解液呈堿性,這有效抑制了OER和HER的發(fā)生,從而擴(kuò)大電化學(xué)窗口104。Zhong等105報道了一種電壓平臺高、反應(yīng)速率快的Zn//MnO2解耦電池,負(fù)極的堿性電解液和正極的酸性電解液被一個中性室(K2SO4溶液)分隔,避免了酸性和堿性電解液的中和。得益于解耦電池獨(dú)特的分離體系,其開路電壓可達(dá)2.83 V,比能量密度為1621.7 Wh·kg?1。隨后,Chao等106提出了一種將含Ni2+的電解液添加劑加入到解耦電池的正極電解液中的策略(圖8c),利用強(qiáng)電負(fù)性金屬Ni的催化作用(圖8d和e),增強(qiáng)了活性電子態(tài)和電荷離域,即引入Ni會降低O的電子密度,電荷局部化作用減弱,改善了活性O(shè) 2p電子態(tài),促進(jìn)電荷轉(zhuǎn)移,使得整個反應(yīng)都在能壘較低的勢能表面進(jìn)行,進(jìn)一步提高電池性能。這種Ni催化的解耦電池實(shí)現(xiàn)了高達(dá)50 mA·cm?2(50C,放電60 s,1C = 1 mA·cm?2)的反應(yīng)動力學(xué)以及超高的電壓平臺2.44 V (1C)。此外,Huang等107提出了兩性水系電解液解耦體系與鋅錳電池的集成,HER和OER過程可分別在高電流密度下(高達(dá)1 A·cm?2)和低電流密度下進(jìn)行,高/低電流密度可分別由高功率風(fēng)能和低功率太陽能驅(qū)動,為未來可再生能源的存儲/轉(zhuǎn)換提供有效策略。需要注意的是,由于正/負(fù)極電解液的酸堿度不同,會不可避免地發(fā)生離子交叉,這在一定程度上降低倍率性能和能量密度。同時,昂貴的離子交換膜也會限制其大規(guī)模應(yīng)用。
近年來,液流電池由于其高安全性、長循環(huán)壽命,以及能夠完全釋放發(fā)生結(jié)構(gòu)崩塌時所產(chǎn)生的壓力等優(yōu)勢,受到了廣泛的關(guān)注108。Xie等109報道了一種高度可逆的中性Zn-Mn液流電池(圖8f)。與MnSO4電解液相比,二氧化錳在含醋酸根(Ac?)的電解液中的氧化還原電位降低了530 mV,這是由于Ac?與Mn2+的配位作用造成的。在充電過程中,Mn(Ac)2轉(zhuǎn)變成MnO2時會伴隨著HAc生成,而HAc的吉布斯自由能比H+要小,驅(qū)動該反應(yīng)所需的能量較少,從而降低了MnO2/Mn2+的電極電位。同時,Ac?的配位作用可使Mn2+直接轉(zhuǎn)變成MnO2,而不會發(fā)生Mn3+的歧化,減少了副反應(yīng)的發(fā)生,大大提高了循環(huán)穩(wěn)定性。但由于電池庫倫效率無法達(dá)到100%,放電時所產(chǎn)生的多余的游離H+會與Ac?結(jié)合產(chǎn)生醋酸,進(jìn)而減弱Ac?的配位作用。而液流電池裝置會不斷更新電解液,穩(wěn)定電解液中Ac?的濃度,在一定程度上保證了配位作用的實(shí)現(xiàn)。以0.5 mol·L?1Mn(Ac)2+ 0.5 mol·L?1Zn(Ac)2+ 2 mol·L?1KCl作為電解液制備的液流電池實(shí)現(xiàn)了優(yōu)異的充放電性能(圖8g)和循環(huán)性能(圖8h)。此外,Li等110報道的一種無隔膜的液流Zn//MnO2電池,正極(Mn2+/MnO2)和負(fù)極(Zn2+/Zn)在同一種電解液中,無需使用離子交換膜,有效降低了成本。并且指出,需開發(fā)出一種具有良好的親水性、優(yōu)良的導(dǎo)電率和更大表面積的正極集流體,以實(shí)現(xiàn)較高的面積容量,為未來規(guī)模儲能系統(tǒng)的發(fā)展奠定基礎(chǔ)。
5 總結(jié)與觀點(diǎn)
新一輪能源革命的核心為可再生能源發(fā)電與規(guī)模儲能,在眾多電化學(xué)儲能技術(shù)中,水系鋅二次電池由于其兼具經(jīng)濟(jì)性、安全性、生態(tài)友好以及高能量和高功率密度等優(yōu)勢而備受關(guān)注,成為儲能領(lǐng)域的理想選擇之一。電池的性能很大部分取決于電極材料,MnO2因其儲量豐富、低成本、低毒性的優(yōu)勢,成為水系鋅二次電池最佳候選正極。因此,Zn//MnO2電池的電極材料特性、儲能機(jī)制以及針對容量低、循環(huán)壽命短等問題提出的優(yōu)化措施被廣泛研究。本文總結(jié)了當(dāng)前主要的兩類儲能機(jī)理(嵌入-脫出和溶解-沉積機(jī)理)的特征及區(qū)別,以及針對這兩種反應(yīng)機(jī)制所提出的優(yōu)化策略,為進(jìn)一步推動具有高能量密度和長循環(huán)壽命的水系鋅錳二次電池的開發(fā)提供研究方向。
5.1 嵌入-脫嵌機(jī)制與溶解-沉積機(jī)制的區(qū)別
近年來Zn//MnO2電池優(yōu)異的電化學(xué)性能引起了廣泛關(guān)注。目前主流的反應(yīng)機(jī)理主要有嵌入-脫嵌機(jī)制和溶解-沉積機(jī)制兩大類。嵌入-脫嵌機(jī)制主要在弱酸性的條件下發(fā)生。這種H+、Zn2+等離子嵌入-脫嵌行為會導(dǎo)致晶格間發(fā)生膨脹/收縮,并發(fā)生不可逆相變,生成副產(chǎn)物如ZnxMnO4、MnOOH、ZnMn3O7·3H2O和Zn2Mn3O8等,且活性材料還會溶解到電解液中,減小充放電容量。同時,Zn2+的高電荷密度會使Zn2+與MnO6晶格之間產(chǎn)生強(qiáng)靜電反應(yīng),導(dǎo)致本征的離子擴(kuò)散動力學(xué)較差,且由于反應(yīng)機(jī)制和晶體結(jié)構(gòu)的復(fù)雜性,難以確定Zn2+合適的調(diào)節(jié)位點(diǎn)。再加上嵌入-脫出機(jī)制的Mn4+/Mn3+氧化還原反應(yīng)只利用了1個有效電子轉(zhuǎn)移,限制了電池的容量和輸出電壓。這些問題大大影響錳基水系鋅二次電池的發(fā)展。
近些年提出的溶解-沉積機(jī)制,是基于MnO2可逆溶解/沉積的行為實(shí)現(xiàn)電池的充放電,此過程與電解液的pH值有密切關(guān)系。該機(jī)制的電化學(xué)反應(yīng)過程轉(zhuǎn)移的有效電子數(shù)為2,其理論容量和理論電位均高于嵌入-脫出機(jī)制。Chao等62通過分析放電曲線中三個電化學(xué)窗口不同區(qū)域,解釋了ZnSO4+MnSO4電解質(zhì)中Zn//MnO2電池的儲能機(jī)理。第一個區(qū)域(2–1.7 V)控制MnO2/Mn2+反應(yīng),第二個區(qū)域(1.7–1.4 V)和第三個區(qū)域(1.4–0.8 V)分別反映H+和Zn2+嵌入MnO2的結(jié)果。通過調(diào)控H2SO4的濃度,可控制D1高電壓區(qū)的容量百分比,當(dāng)H2SO4的濃度達(dá)到0.1 mol·L?1時,電池儲能過程主要由溶解-沉積機(jī)制主導(dǎo),實(shí)現(xiàn)了可觀的放電電壓和能量密度。然而,目前溶解-沉積機(jī)制復(fù)雜的內(nèi)在反應(yīng)路徑尚未明晰,還無法實(shí)現(xiàn)錳基完全充分可逆的溶解-沉積,同時在酸性電解液中發(fā)生的鋅腐蝕和析氫等問題會降低Zn沉積/剝離效率,這些問題仍待進(jìn)一步研究。此外,一些報道曾提到在中性或弱酸性電解液中也能發(fā)生錳基可逆的溶解-沉積50,或在液流電池中也能觀察到H+/Zn2+和MnO2共存現(xiàn)象110,說明溶解-沉積反應(yīng)和H+/Zn2+的嵌入可能普遍存在于水系鋅二次電池體系。
5.2 MnO2正極優(yōu)化措施的特點(diǎn)
當(dāng)前,蓬勃發(fā)展的儲能市場使得對高性能電子設(shè)備和柔性可穿戴設(shè)備的需求愈發(fā)迫切,這極大推動了高能量密度和高安全的可充電電池的發(fā)展。本節(jié)總結(jié)了錳基電極優(yōu)化措施的特點(diǎn)及其未來的發(fā)展方向。(1)針對嵌入-脫嵌機(jī)制:①采用涂覆涂層的方法,形成穩(wěn)定SEI膜,抑制活性材料的溶解,或利用三維多孔網(wǎng)絡(luò)結(jié)構(gòu)為離子傳輸提供更多更穩(wěn)定的通道,提高離子的嵌入-脫嵌速率;②與具有多孔結(jié)構(gòu)的納米材料進(jìn)行復(fù)合,不僅能提高活性材料的比表面積,增大電極與電解液的接觸面積,增加活性反應(yīng)位點(diǎn),從而提高電池的反應(yīng)速率,還能避免添加劑的使用,實(shí)現(xiàn)更快的電子/離子傳輸速率;③材料在電池循環(huán)過程中會發(fā)生難以避免的內(nèi)部結(jié)構(gòu)崩塌現(xiàn)象,客體預(yù)嵌在擴(kuò)大層狀材料層間距的同時,還有助于穩(wěn)定電極結(jié)構(gòu),并降低離子的擴(kuò)散勢壘,更有利于離子的嵌入/脫嵌;④離子參與氧化還原反應(yīng)需要克服能量勢壘,勢壘越高,則發(fā)生反應(yīng)時所需的能量越大,阻礙高功率、高能量密度電池的發(fā)展。異質(zhì)元素具有與MnO2不同的電子構(gòu)型,摻雜異質(zhì)元素可誘導(dǎo)缺陷的形成,并調(diào)節(jié)MnO2的電子結(jié)構(gòu)分布,從而減小離子間的靜電斥力,降低電化學(xué)反應(yīng)勢壘,進(jìn)而提高離子的嵌入/脫出速率。(2)針對溶解-沉積機(jī)制:通過調(diào)節(jié)電解液的組分或pH值,以降低能量勢壘、促進(jìn)錳基可逆溶解或提高未充分溶解的MnO2的活性的方法來調(diào)控MnO2的溶解-沉積行為。同時,金屬元素對電化學(xué)反應(yīng)的催化作用可有效提高二氧化錳溶解-沉積的可逆性。此外,解耦體系電池對正負(fù)極電解液的分離有效抑制了OER和HER,極大地提高了電池的電化學(xué)穩(wěn)定性。同時,液流體系電池可通過消除濃度極化來維持電解液離子濃度的穩(wěn)定,也能保證外來離子介質(zhì)與Mn2+的協(xié)同作用的穩(wěn)定實(shí)現(xiàn),且流動的電解液在一定程度上抑制了鋅枝晶的生成,進(jìn)一步提高了電池的綜合性能。除了對正極材料和電解液的研究,對于負(fù)極的析氫和腐蝕的影響也應(yīng)該被考慮。
高性能水系鋅二次電池在大規(guī)模電網(wǎng)儲能領(lǐng)域具有廣泛的發(fā)展前景,持續(xù)優(yōu)化水系鋅二次電池性能,進(jìn)一步提高其能量密度、長循環(huán)穩(wěn)定性、低成本及可回收利用性,推動其商業(yè)化進(jìn)程。然而,目前Zn//MnO2電池領(lǐng)域仍存在如嵌入-脫嵌和溶解-沉積的內(nèi)在機(jī)制未明晰,無法實(shí)現(xiàn)高能量密度等問題。如何有效結(jié)合兩種機(jī)制,探討高性能錳基電極的研發(fā),制備出具有高能量密度和優(yōu)異循環(huán)穩(wěn)定性的實(shí)用水系鋅二次電池,需要更加深入的研究。

