β-氨基酸聚合物用于協(xié)同增效逆轉(zhuǎn)白色念珠菌對(duì)伊曲康唑的耐藥性
馬凱茜, 張東輝, 施 超, 顧佳蔚, 劉潤(rùn)輝
(華東理工大學(xué)生物反應(yīng)器工程國(guó)家重點(diǎn)實(shí)驗(yàn)室, 超細(xì)材料制備與應(yīng)用教育部重點(diǎn)實(shí)驗(yàn)室,教育部醫(yī)用生物材料工程研究中心, 材料科學(xué)與工程學(xué)院, 上海 200237)
微生物感染嚴(yán)重威脅著人類(lèi)的生命健康,同時(shí)抗生素的濫用導(dǎo)致微生物不斷出現(xiàn)耐藥性,造成了巨大的社會(huì)問(wèn)題和經(jīng)濟(jì)損失[1-7],而其中的真菌感染問(wèn)題已經(jīng)日益嚴(yán)峻[8]。近些年,全球范圍內(nèi)的真菌感染發(fā)病率顯著上升,并且系統(tǒng)性真菌感染常常伴隨著高死亡率,其中感染白色念珠菌(C. albicans)的死亡率通常可超過(guò)50%[9-12]。白色念珠菌是一種機(jī)會(huì)性致病菌,在人體黏膜和環(huán)境中廣泛存在。當(dāng)人體健康時(shí),即使攜帶白色念珠菌也往往不會(huì)出現(xiàn)任何癥狀,而一旦體內(nèi)微生物群發(fā)生紊亂或免疫系統(tǒng)出現(xiàn)異常時(shí),其便可能表現(xiàn)出毒力[13,14]。在各類(lèi)抗真菌藥物中,伊曲康唑(Itraconazole)由于具有廣譜抗真菌活性、低毒性、能夠進(jìn)行系統(tǒng)性給藥、便宜易得等優(yōu)勢(shì),在臨床中被廣泛使用[15-17]。然而,由于唑類(lèi)藥物的濫用,白色念珠菌對(duì)伊曲康唑的耐藥性已經(jīng)非常嚴(yán)重[18-20]。
伊曲康唑主要通過(guò)與靶酶-甾醇14α-去甲基化酶(由ERG11基因編碼)特異性結(jié)合從而抑制膜上麥角甾醇的合成來(lái)發(fā)揮抗真菌作用。真菌對(duì)伊曲康唑產(chǎn)生耐藥性的主要原因包括ERG11基因的過(guò)表達(dá)提高了胞內(nèi)靶酶的豐度,以及藥物外排泵的過(guò)表達(dá)降低了胞內(nèi)的有效藥物濃度[21-23]。這啟發(fā)我們用能夠干擾菌膜的聚合物協(xié)助伊曲康唑,提高真菌對(duì)其攝取效率和胞內(nèi)藥物濃度,通過(guò)協(xié)同增效來(lái)逆轉(zhuǎn)真菌對(duì)伊曲康唑的耐藥性,而具有抗真菌活性的聚合物是實(shí)現(xiàn)協(xié)同增效的理想選擇。許多天然宿主防御肽具有抗真菌活性,這些抗真菌肽通常具有正電荷和疏水性?xún)捎H性結(jié)構(gòu),其作用方式主要是針對(duì)帶有負(fù)電性的真菌細(xì)胞膜[24-30]。然而宿主防御肽成本高昂、不耐蛋白酶水解等缺點(diǎn)限制了其應(yīng)用[31-35]。β-氨基酸聚合物是宿主防御肽的模擬物,通過(guò)合理設(shè)計(jì)可實(shí)現(xiàn)抗真菌活性,同時(shí)具有穩(wěn)定性高、生物相容性好、合成方法簡(jiǎn)單、價(jià)格低廉的突出優(yōu)勢(shì)[36-38]。
本文設(shè)計(jì)了β-氨基酸聚合物來(lái)研究其與伊曲康唑的協(xié)同抗真菌活性。前期研究證實(shí)聚N(α)-Z-DL-2,3-二氨基丙酸N-羧基硫代羰基環(huán)內(nèi)酸酐(Poly-DAP)具有高效抗真菌性質(zhì)[39]。本文采用DAP作為模擬宿主防御肽的正電荷部分、DL-β-正亮氨酸N-羧基硫代羰基環(huán)內(nèi)酸酐(Bu)作為疏水性部分,通過(guò)本課題組近期建立的反應(yīng)條件溫和、對(duì)水分不敏感的β-氨基酸N-硫代羧基酸酐(β-NTA)開(kāi)環(huán)聚合的方法獲得了β-氨基酸聚合物((DAPxBuy)n)[40]。抗菌測(cè)試、溶血測(cè)試和細(xì)胞毒性測(cè)試表明,(DAPxBuy)n聚合物能實(shí)現(xiàn)高效協(xié)同增效,逆轉(zhuǎn)了真菌對(duì)伊曲康唑的耐藥性,且聚合物本身基本不引起明顯的溶血和細(xì)胞毒性,展示出其在真菌感染治療領(lǐng)域的應(yīng)用潛力。
1 實(shí)驗(yàn)部分
1.1 原料和試劑
DAP、Bu按文獻(xiàn)[40]合成;石油醚(PE)、四氫呋喃(THF)、N,N-二甲基甲酰胺(DMF)、三氟乙酸(TFA)、溴化氫的醋酸溶液(w= 33%, HBr-HOAc)、甲基叔丁基醚(MTBE)、甲醇(MeOH)、二甲基亞砜(DMSO)、聚乙二醇辛基苯基醚(TX-100):上海泰坦科技股份有限公司;3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴鹽(MTT)、氯化鈉、三羥甲基氨基甲烷(Tris)、對(duì)叔丁基芐胺(tBuBz-NH2)、伊曲康唑:上海阿拉丁生化科技有限公司;洛斯維帕克紀(jì)念研究所1640培養(yǎng)基(RPMI 1640):賽默飛世爾科技(中國(guó))有限公司;3-嗎啉丙磺酸(MOPS):Sigma Aldrich;酵母浸出粉胨葡萄糖培養(yǎng)基(YPD):青島海博生物技術(shù)有限公司;達(dá)爾伯克改良伊格爾培養(yǎng)基(DMEM):GE醫(yī)療;氘代試劑重水(D2O):上海笛柏化學(xué)品技術(shù)有限公司;超純水和去離子水由彤迪科學(xué)儀器(上海)有限公司生產(chǎn)的MING-CHE-24 UV系列純水機(jī)制備。
1.2 測(cè)試與表征
核磁共振波譜(NMR):瑞士Bruker公司Ascend 600 MHz型儀器,D2O作為溶劑;酶標(biāo)儀:美國(guó)Molecular Devices公司,型號(hào)為SpectraMax M2。
1.3 實(shí)驗(yàn)步驟
1.3.1 (DAPxBuy)n聚合物的合成 采用本課題組文獻(xiàn)[40]的β-NTA開(kāi)環(huán)聚合方法,合成了一系列正電荷兩親性聚合物(DAPxBuy)n(x、y分別為單體DAP、Bu的投料摩爾分?jǐn)?shù),x+y=1,n=20)。以(DAP0.5Bu0.5)20的合成為例,合成路線(xiàn)如圖1所示。在氮?dú)獗Wo(hù)的手套箱內(nèi),稱(chēng)量單體DAP (14.02 mg,0.05 mmol)、Bu (9.36 mg,0.05 mmol)及引發(fā)劑tBuBz-NH2(0.82 mg,0.005 mmol),用總共0.5 mL的DMF溶解后在室溫下反應(yīng),通過(guò)柱層析硅膠板監(jiān)測(cè)反應(yīng)。反應(yīng)結(jié)束后使用1.5 mL THF潤(rùn)洗反應(yīng)瓶并轉(zhuǎn)移至50 mL離心管,加滿(mǎn)-20 ℃ PE離心、沉淀,倒掉上清液并重復(fù)此操作兩次。將固體置于真空皿中真空干燥后,加入4 mL HBr-HOAc和TFA的混合溶液(體積比為1∶1)脫保護(hù)12 h,吹干溶劑,用1 mL甲醇溶解,加入49 mL、-20 ℃ MTBE沉淀、離心,重復(fù)3次,真空干燥。將固體用超純水溶解,0.45 μm過(guò)濾頭過(guò)濾后凍干,即得聚合物(DAP0.5Bu0.5)20。(DAPxBuy)n聚合物的核磁共振氫譜表征結(jié)果如圖2所示。
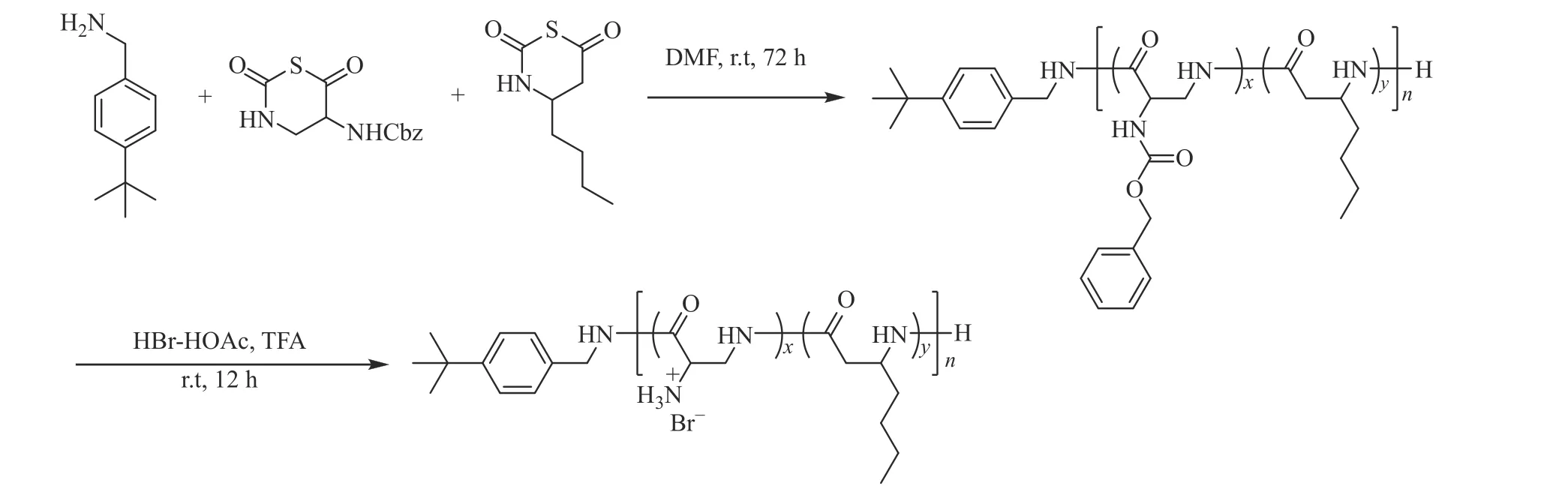
圖 1 (DAPx Buy)n系列β-氨基酸聚合物的合成Fig. 1 Synthetic route of (DAPx Buy)n series of β-amino acid polymers
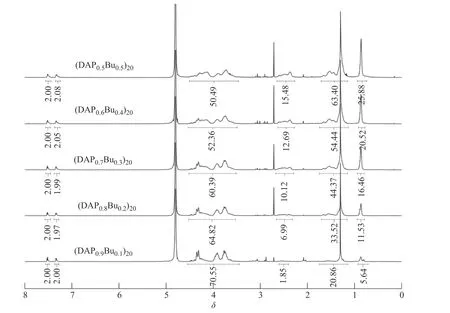
圖 2 系列聚合物的1H-NMR圖譜Fig. 2 1H-NMR spectra of series of polymers
1.3.2 (DAPxBuy)n聚合物的最低抑菌濃度測(cè)試 配制YPD肉湯。稱(chēng)量50 g YPD固體于1 L去離子水中,115 ℃滅菌15 min。
配制RPMI 1640培養(yǎng)基。稱(chēng)量30.34 g MOPS,加入一包RPMI 1640粉末,溶于1 L去離子水中,0.22 μm過(guò)濾頭過(guò)濾。
從C. albicans(K1菌株)涂板的瓊脂上取一個(gè)菌落于10.0 mL YPD中,倒入滅過(guò)菌的錐形瓶,置于30 ℃搖床中培養(yǎng)15 h,用RPMI 1640清洗一次后,稀釋至2.5×103CFU/mL待用。將聚合物用超純水配成1 mg/mL,在96孔板中用RPMI 1640以?xún)杀短荻认♂尩姆椒▽⒕酆衔锵♂尩阶罱K質(zhì)量濃度為0.1~25 μg/mL,將伊曲康唑用DMSO稀釋至8 mg/mL,兩倍梯度稀釋至最終質(zhì)量濃度為0.1~200 μg/mL,每個(gè)孔的液體體積為100 μL。再取100 μL待用菌液分別加入到稀釋好的聚合物和伊曲康唑中。另外96孔板最后一列不加藥物,前4個(gè)孔加純RPMI 1640作為陰性對(duì)照,后4個(gè)孔加等體積的RPMI 1640和菌液作為陽(yáng)性對(duì)照。將96孔板置于30 ℃培養(yǎng)箱孵育24 h,之后肉眼觀察實(shí)驗(yàn)結(jié)果,恰好看不到有真菌生長(zhǎng)的最低濃度即為樣品的最低抑菌濃度(MIC)[37]。每個(gè)樣品至少在不同的時(shí)間重復(fù)測(cè)試2次。
1.3.3 棋盤(pán)格協(xié)同抗真菌測(cè)試 待用菌液的配制同“1.3.2”節(jié)部分。將聚合物用超純水配成1 mg/mL,在96孔板中用RPMI 1640橫向以?xún)杀短荻认♂尩姆椒▽⒕酆衔锵♂尩阶罱K質(zhì)量濃度為0.1~25 μg/mL,每個(gè)孔的液體體積為50 μL。伊曲康唑用DMSO稀釋至2 mg/mL,在96孔板中用RPMI 1640縱向兩倍稀釋至最終質(zhì)量濃度為0.1~50 μg/mL。保持方向不變,轉(zhuǎn)移50 μL稀釋好的伊曲康唑到稀釋聚合物的96孔板中。然后加入100 μL待用菌液,最終每個(gè)孔的體積為200 μL。每塊96孔板的最后一列前4個(gè)孔和后4個(gè)孔分別作為陰性和陽(yáng)性對(duì)照。將96孔板置于30 ℃培養(yǎng)箱孵育24 h,之后肉眼觀察實(shí)驗(yàn)結(jié)果,記錄樣品的MIC。每個(gè)樣品至少在不同時(shí)間重復(fù)測(cè)試2次。
協(xié)同活性用協(xié)同指數(shù)(FICI)進(jìn)行判斷。FICI按照式(1)進(jìn)行計(jì)算:

式中,A和B分別代表兩種藥物,combined和alone分別代表聯(lián)合使用兩種藥物和單獨(dú)使用一種藥物。當(dāng)FICI ≤ 0.5時(shí),表示兩種藥物存在協(xié)同作用;當(dāng)0.5 < FICI ≤ 4時(shí),表示兩種藥物不存在相互作用;當(dāng)FICI > 4時(shí),表示兩種藥物存在拮抗作用。
1.3.4 (DAPxBuy)n聚合物的溶血率測(cè)試 稱(chēng)取0.61 g Tris和4.39 g氯化鈉,溶于500 mL去離子水中,121 ℃滅菌15 min,即制得TBS緩沖液。
向1 mL新鮮人血中加入19 mL TBS緩沖液,輕輕混勻后以4 000 r/min離心3 min,倒掉上清液,重復(fù)操作3次。最后用TBS將人血稀釋至體積分?jǐn)?shù)5%得到待用血紅細(xì)胞懸液。在96孔板中,用TBS將聚合物以?xún)杀短荻认♂尩姆椒ㄏ♂屩磷罱K質(zhì)量濃度為12.5~400 μg/mL,最后一列加入等體積的TBS和體積分?jǐn)?shù)0.1%的TX-100分別作為陰性和陽(yáng)性對(duì)照。然后向每個(gè)孔中加入等體積的血紅細(xì)胞懸液,在37 ℃的培養(yǎng)箱中孵育1 h。取出96孔板,以3 700 r/min的轉(zhuǎn)速離心5 min,然后吸出80 μL上清液用酶標(biāo)儀讀光密度(OD)值(405 nm)并計(jì)算溶血率。 每個(gè)樣品重復(fù)3組實(shí)驗(yàn)。
1.3.5 (DAPxBuy)n聚合物的細(xì)胞毒性測(cè)試 稱(chēng)量0.5 g的MTT,溶于100 mL磷酸鹽緩沖溶液(PBS),制得MTT溶液。
NIH3T3(小鼠胚胎成纖維細(xì)胞系)用DMEM培養(yǎng)基于37 ℃ CO2培養(yǎng)箱中培養(yǎng),當(dāng)培養(yǎng)皿中的細(xì)胞達(dá)到90%~95%的黏附率時(shí),吸走DMEM培養(yǎng)基,用PBS潤(rùn)洗,再用胰蛋白酶和DMEM處理。以1 340 r/min離心、清洗,并用DMEM將細(xì)胞稀釋至1.0×105cell/mL待用。在96孔板中加入100 μL細(xì)胞懸液,置于CO2培養(yǎng)箱,24 h后除去培養(yǎng)基。將聚合物兩倍梯度稀釋至最終質(zhì)量濃度為6.25~400 μg/mL,轉(zhuǎn)移100 μL到除去培養(yǎng)基的96孔板中,對(duì)照組加入100 μL DMEM,其中不含細(xì)胞的作為陰性對(duì)照,含有細(xì)胞的作為陽(yáng)性對(duì)照,置于37 ℃CO2培養(yǎng)箱中。24 h后,向板中加入10 μL MTT溶液,在CO2培養(yǎng)箱孵育。4 h后,去除培養(yǎng)基,然后加入150 μL DMSO,置于搖床中搖晃。15 min后,用酶標(biāo)儀讀OD值(570 nm)并計(jì)算細(xì)胞存活率。每個(gè)樣品重復(fù)3組實(shí)驗(yàn)。
2 結(jié)果與討論
2.1 聚合物的協(xié)同抗菌活性
(DAPxBuy)n聚合物及伊曲康唑?qū). albicans(K1菌株)的抑菌活性、聯(lián)合使用聚合物與伊曲康唑的MIC值,以及通過(guò)計(jì)算得到的協(xié)同指數(shù)FICI,如表1所示。結(jié)果表明,單獨(dú)使用聚合物時(shí),其抑菌活性隨著主鏈?zhǔn)杷鶊F(tuán)Bu比例的增多而降低,單獨(dú)使用伊曲康唑時(shí),即使藥物質(zhì)量濃度達(dá)到200 μg/mL也無(wú)法完全抑制C.albicans的生長(zhǎng)。當(dāng)聯(lián)合使用時(shí),所有(DAPxBuy)n聚合物與伊曲康唑的FICI均小于0.5,表明這5種(DAPxBuy)n聚合物與伊曲康唑均存在協(xié)同效應(yīng),伊曲康唑的MIC可從單獨(dú)使用時(shí)的大于200 μg/mL降低到協(xié)同后的3.1 μg/mL,說(shuō)明(DAPxBuy)n聚合物可通過(guò)協(xié)同增效有效逆轉(zhuǎn)C. albicans對(duì)伊曲康唑的耐藥性,使伊曲康唑抗真菌活性從無(wú)效轉(zhuǎn)變?yōu)楦咝А?/p>
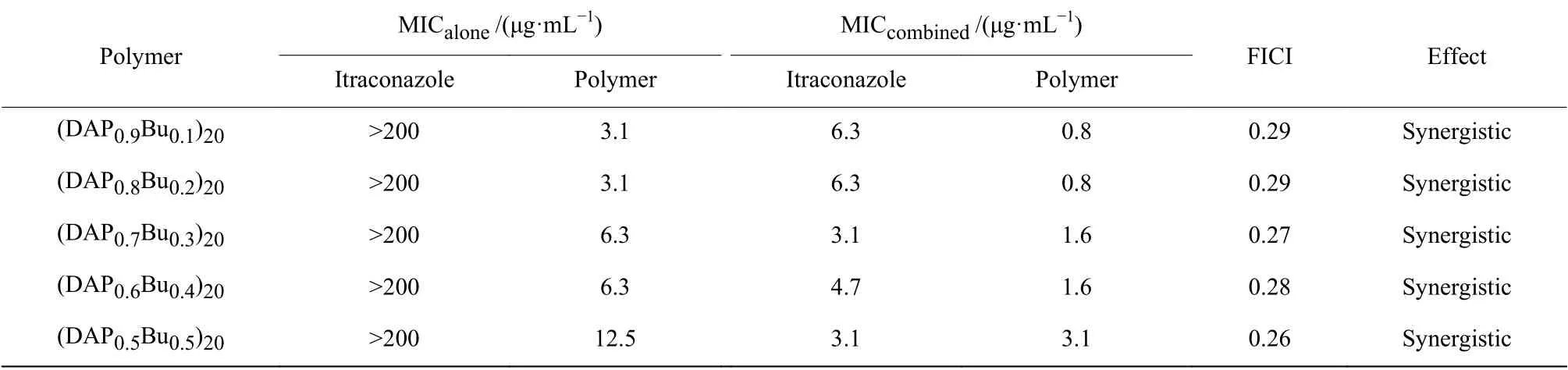
表 1 聚合物與伊曲康唑的MIC、FICI及相互作用模式Table 1 Interaction modes of polymers and itraconazole and their MIC and FICI values
C. albicans在不同質(zhì)量濃度藥物聯(lián)合使用下的生長(zhǎng)情況如圖3所示。白色代表此質(zhì)量濃度下兩次實(shí)驗(yàn)均無(wú)肉眼可見(jiàn)的真菌生長(zhǎng),淺藍(lán)色代表有一次實(shí)驗(yàn)有真菌生長(zhǎng),深藍(lán)色代表兩次實(shí)驗(yàn)均有真菌生長(zhǎng)。從圖中可以明顯看出,聯(lián)合使用(DAPxBuy)n聚合物和伊曲康唑后,兩者可以在各自最多四分之一MICalone的條件下成功抑制真菌生長(zhǎng)。
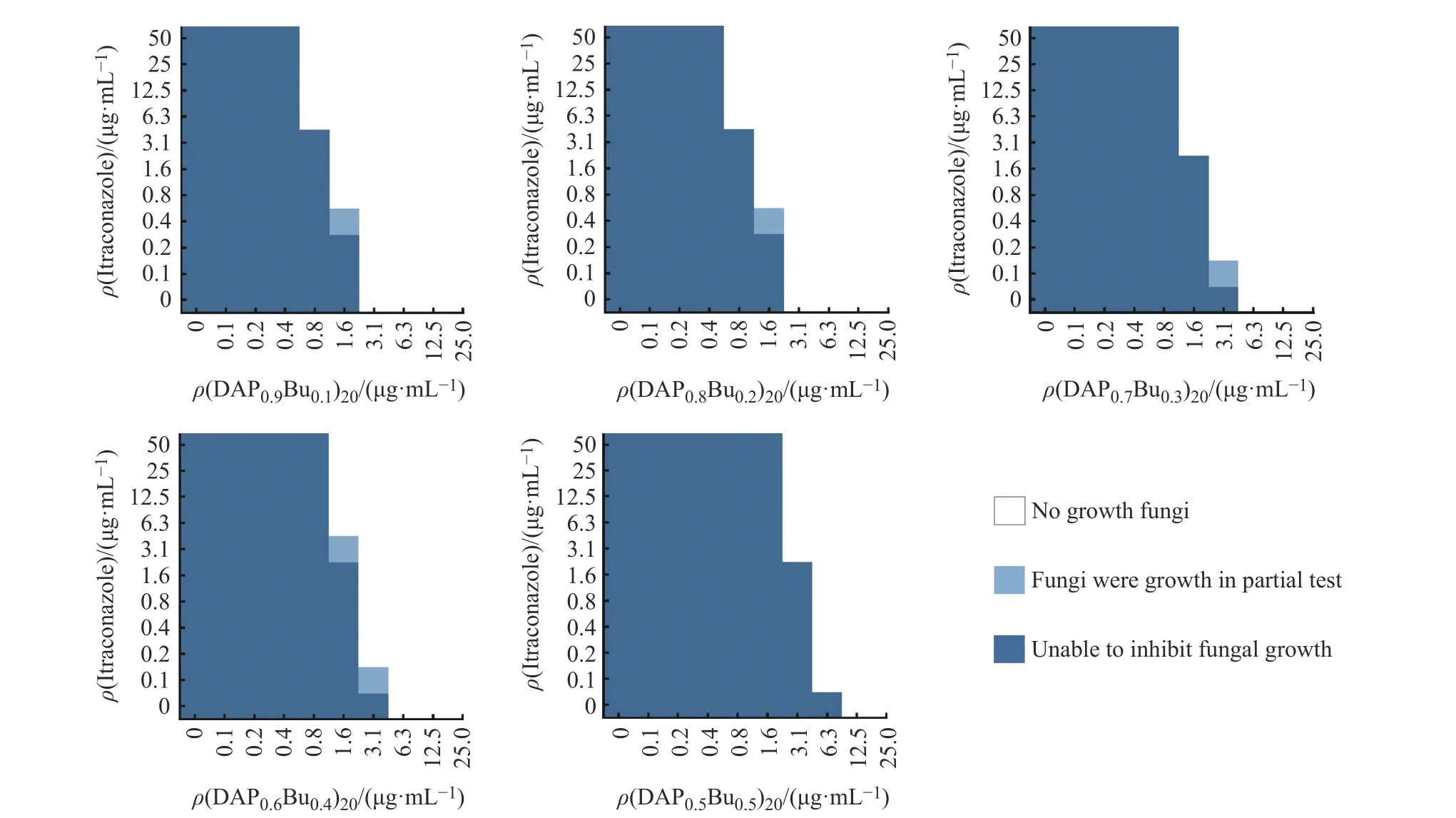
圖 3 C. albicans (K1菌株)在不同質(zhì)量濃度藥物聯(lián)合作用下的生長(zhǎng)情況Fig. 3 Growth of C. albicans (strain K1) incubated with different mass concentrations of polymers and itraconazole
有報(bào)道提出,宿主防御肽的正電荷和疏水性?xún)捎H性特性使它能夠改變微生物細(xì)胞膜的通透性,從而使更多抗菌藥物進(jìn)入胞內(nèi),宿主防御肽進(jìn)而得以發(fā)揮協(xié)同增效作用[41,42]。結(jié)合由于真菌靶酶基因及藥物外排泵基因過(guò)表達(dá)而導(dǎo)致其對(duì)伊曲康唑產(chǎn)生耐藥性的機(jī)理,我們推測(cè)宿主防御肽模擬物(DAPxBuy)n聚合物可能表現(xiàn)出類(lèi)似的協(xié)同機(jī)理,即通過(guò)改變真菌細(xì)胞膜通透性使更多伊曲康唑進(jìn)入胞內(nèi),從而實(shí)現(xiàn)逆轉(zhuǎn)真菌對(duì)伊曲康唑的耐藥性。
2.2 聚合物的溶血率
(DAPxBuy)聚合物的溶血率如圖4所示。4組樣品的50%溶血時(shí)的藥物濃度(HC50)均大于400 μg/mL,溶血率較低,血液安全性良好,(DAP0.6Bu0.4)20的HC50為200 μg/mL,溶血率較其他樣品略微增強(qiáng)。同時(shí),除(DAP0.5Bu0.5)20外,其余樣品的溶血率隨疏水基團(tuán)Bu含量的提高而變大。(DAP0.5Bu0.5)20的反常現(xiàn)象仍在研究中。
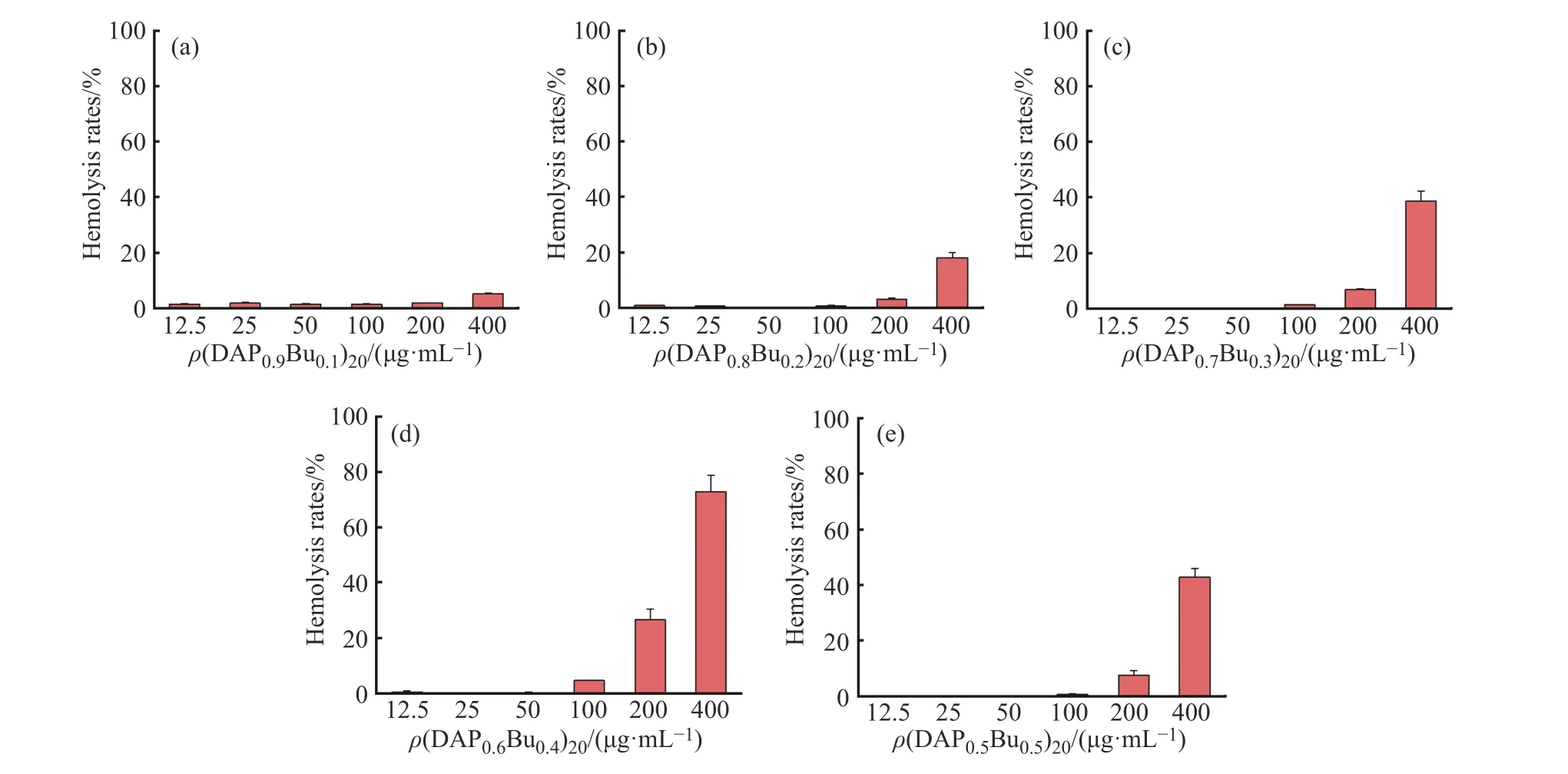
圖 4 系列聚合物的溶血率Fig. 4 Hemolysis rates of series of polymers
2.3 聚合物的細(xì)胞毒性
聚合物的細(xì)胞毒性實(shí)驗(yàn)結(jié)果如圖5所示。從圖5可以看出,(DAPxBuy)n聚合物的質(zhì)量濃度在6.25~400 μg/mL,均沒(méi)有產(chǎn)生明顯的細(xì)胞毒性。所有聚合物的抑制50% NIH 3 T3成纖維細(xì)胞生長(zhǎng)的質(zhì)量濃度(IC50)都在400 μg/mL以上。綜合考慮“2.1”節(jié)中各聚合物的MIC及“2.2”節(jié)中的溶血率,認(rèn)為(DAPxBuy)n聚合物對(duì)真菌和哺乳動(dòng)物細(xì)胞具有比較好的選擇性。
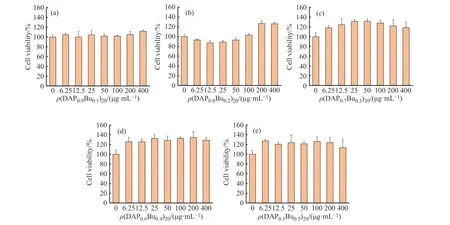
圖 5 聚合物的細(xì)胞毒性Fig. 5 Cytotoxicity of polymers
3 結(jié) 論
(1)(DAPxBuy)n聚合物能實(shí)現(xiàn)高效協(xié)同增效,逆轉(zhuǎn)了C. albicans對(duì)伊曲康唑的耐藥性,使伊曲康唑的抗真菌最低抑制濃度從單藥的高于200 μg/mL降低至協(xié)同后的3.1 μg/mL,即從原先的無(wú)效逆轉(zhuǎn)為高效抗真菌活性。
(2)(DAPxBuy)n聚合物在400 μg/mL的質(zhì)量濃度下基本不會(huì)造成明顯人血紅細(xì)胞溶血和細(xì)胞毒性。

