基于核心素養的有機結構與性質高考題命題特點及解題策略
湖北 熊云貴
一、命題特點
核心素養背景下,有機結構與性質考題備受命題者青睞。這類考題,一般給出科學家合成的具有重要作用的某有機物的結構簡式,考查該有機物的分子式、基團或者官能團的數目、手性碳原子數目、分子中的某原子共面或者共線情況、能夠發生反應的類型、與某物質反應的數量關系等。題干部分創設真實情境,指出科學家合成的該有機物具有重要作用,體現了學科價值,起到學科育人功能,有利于培養學生的“科學態度與社會責任”;選項中涉及的問題,考查學生觀察結構、根據結構推測物質性質的能力,有利于培養學生的“證據推理與模型認知”。
【考題示例1】(2022年全國甲卷,8題)輔酶Q10具有預防動脈硬化的功效,其結構簡式如圖1。下列有關輔酶Q10的說法正確的是

圖1
( )
A.分子式為C60H90O4
B.分子中含有14個甲基
C.分子中的四個氧原子不在同一平面
D.可發生加成反應,不能發生取代反應
【答案】B
【分析】本題給出輔酶Q10的結構簡式,考查分子式、分子中甲基數目、分子中的氧原子共面情況、是否發生加成反應和取代反應。
【考題示例2】(2022年海南卷,12題)化合物“E7974”具有抗腫痛活性,結構簡式如圖2,下列有關該化合物說法正確的是

圖2
( )
A.能使Br2的CCl4溶液褪色
B.分子中含有4種官能團
C.分子中含有4個手性碳原子
D.1 mol該化合物最多與2 mol NaOH反應
【答案】AB
【分析】本題給出“E7974”的結構簡式,考查能否使Br2的CCl4溶液褪色、官能團的數目、手性碳原子數目、1 mol該化合物最多與NaOH反應的物質的量。
二、解題策略
(一)深刻領會有機物的結構特點
1.有機物分子式
確定有機物分子式,首先要把碳原子數目數對,氧原子、氮原子、鹵素原子一般較少,比較容易確定。關鍵是氫原子,由于氫原子一般會在結構簡式中省略,所以,我們要根據碳的成鍵原則,補充相關氫原子,確定總的氫原子數目。也可以根據相關通式,確定氫原子數目。如烷烴通式CnH2n+2,如果其中含有單鍵氧原子,不改變氫原子數目;如果其中含有鹵素原子,則氫原子數目與鹵素原子數目之和等于2n+2;如果其中含有單鍵氮原子,則氫原子數目比相應烷烴的氫原子數目多一個。如果出現一個雙鍵或者一個環,氫原子數目比相應烷烴減少2個;如果出現一個三鍵,氫原子數目比相應烷烴減少4個;如果出現一個苯環,氫原子數目比相應烷烴減少8個。
考題示例1的A項,碳原子數目應該為59,所以A錯。氫原子數目是90,可以按照碳的成鍵原則補充相關氫原子后直接數,也可以按照通式計算:59×2+2-15×2=90。氧原子4個,一目了然。
2.手性碳原子
手性分子是指含有手性碳原子的分子,由于4個原子或原子團在空間的排列不同,形成了如同左手與右手一樣互為鏡像,卻在三維空間里不能重疊的分子。具有手性的分子,一般在一個C原子上按四面體方式連接上4個互不相同的原子或基團,如圖3所示中左右兩只手托出的兩個呈鏡像關系的乳酸分子。
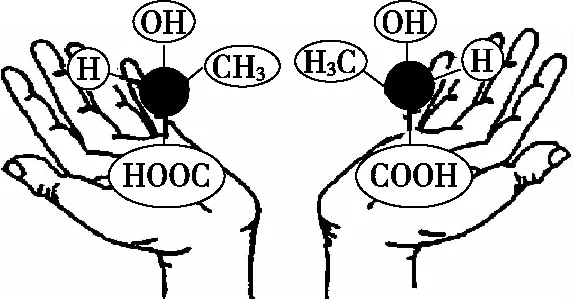
圖3
3.有機物原子的共面、共線
原子的雜化方式決定了分子的空間構型,是解決共面、共線問題的根本核心,同時可以借助分子模型加以理解。
①甲烷及烷烴
甲烷分子中碳原子采用sp3雜化,為正四面體構型的分子,鍵角為109°28′。在甲烷分子中,一個碳原子和任意兩個氫原子可確定一個平面,其余兩個氫原子分別位于平面的兩側,即甲烷分子中有且只有三原子共面(稱為三角形規則)。當甲烷分子中某氫原子被其他原子或原子團取代時,取代該氫原子的原子可看作是在原來氫原子的位置。有機物分子中只要含有飽和碳原子,該碳原子采用sp3雜化,則所有原子不可能在同一平面。甲烷分子構型及球棍模型如圖4和圖5所示。

圖4

圖5
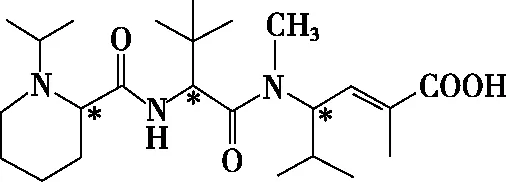
②乙烯及烯烴

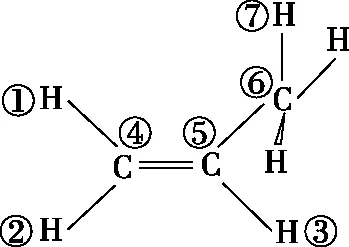
圖6

③苯及芳香烴
苯分子中碳原子均以sp2雜化方式成鍵,如圖7,苯分子中共有12個原子共面。當苯分子中的一個氫原子被其他原子或原子團取代時,取代該氫原子的原子一定在苯分子所在平面內。甲苯中甲基碳原子采用sp3雜化,所有原子不可能在同一平面。哪些原子可以在一個平面上呢?如圖8,7個碳原子(苯環上的6個碳原子和甲基上的一個碳原子)、5個氫原子(苯環上的5個氫原子)這12個原子一定共面。此外甲基上1個氫原子(①H,②C,③C構成三角形)也可以旋轉到這個平面上,其余兩個氫原子分布在平面兩側。故甲苯分子中最多可能是13個原子共面。
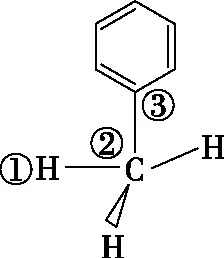
圖8
④乙炔及炔烴

⑤多個平面(直線)連接

(二)全面掌握有機物結構與性質的關系
有機化學中結構決定性質體現得非常充分。教學中應該引導學生從定性、定量、定位、辯證等多角度全面掌握有機物結構與性質的關系。
1.從定性看
從物理性質看:烴一般是非極性或弱極性的分子。分子間的作用力比較小,因此烴的熔點、沸點比較低,碳原子數小于等于4的烴常溫下為氣態,烴一般難溶于強極性的溶劑水中;烴的衍生物隨著官能團極性的增強,分子間作用力增大,其熔點、沸點都比相對分子質量相當的烴類要高,如乙醇的沸點為78℃,比相對分子質量相當的丙烷高出120.07℃;具有強極性的烴的衍生物,容易溶解在強極性的溶劑水中,如低碳原子的醇、醛、酸能與水互溶。

考題示例1的D項,分子中有碳碳雙鍵,能發生加成反應,分子中含有甲基,能發生取代反應,D錯誤。考題示例2的A項,根據結構,“E7974”含有碳碳雙鍵,可使Br2的CCl4溶液褪色,A正確。
2.從定量看
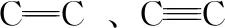
3.從定位看
對于給定有機物,我們有時候還要從定位角度進行思考,知道該有機物發生反應的部位以及原子或者原子團加到反應物的相關部位。
【考題示例3】(2022年浙江6月卷,15題)染料木黃酮的結構如圖9,下列說法正確的是
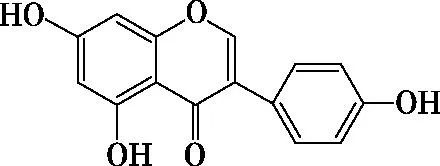
圖9
( )
A.分子中存在3種官能團
B.可與HBr反應
C.1 mol該物質與足量溴水反應,最多可消耗4 mol Br2
D.1 mol該物質與足量NaOH溶液反應,最多可消耗2 mol NaOH
【答案】B
【分析】根據該物質結構簡式可知分子中含有酚羥基、羰基、醚鍵和碳碳雙鍵,共四種官能團,A錯誤;該物質含有碳碳雙鍵,能與HBr發生加成反應,B正確;該分子中含有3個酚羥基,所以最多消耗3 mol NaOH,D錯誤。而解答C項時,要從定位角度考慮,該分子中酚羥基含有四種鄰位或對位H,另外碳碳雙鍵能和單質溴發生加成反應,所以最多消耗單質溴5 mol,C錯誤。
在有機學習中,我們還可以找到不少的這種定位思考。如醇類能催化氧化為醛、發生消去生成碳碳雙鍵,但(CH3)3C—OH不能氧化成醛,CH3—OH、(CH3)3C—CH2—OH不能發生消去生成碳碳雙鍵。這是因為醇的催化氧化是去掉—OH的氫以及和—OH相連碳上的一個氫。連有—OH的碳上有2個或2個以上氫原子時被氧化為醛,有1個氫原子時可被氧化為酮,(CH3)3C—OH中連有—OH的碳上不含 氫原子,不能發生催化氧化。醇發生消去反應時,與 —OH 相連的碳原子的鄰位碳原子上必須有氫原子。(CH3)3C—CH2—OH中與羥基相連碳原子的鄰位碳原子上沒有氫原子,故不能發生消去反應。
4.從辯證看
結構決定性質,相同結構的有機物具有相似的性質,但由于有機物化學性質的“多面性”,具有相同結構的有機物在不同條件下可能發生不同的反應。所以分析有機反應,在首先考慮內因即物質結構的同時,還必須充分考慮外因,即反應條件對有機反應的影響。這種同時考慮內因和外因的思維就是辯證的思維。如乙醇與濃H2SO4共熱至170℃,發生消去反應,主要生成乙烯;但若是140℃,則主要發生取代而得到乙醚。又如苯與Cl2在鐵為催化劑時發生取代得到氯苯,但在紫外線照射時,則發生加成生成“六六六”(六氯環己烷)。鹵代烴在NaOH醇溶液并加熱時發生消去反應生成烯烴,但在NaOH水溶液并加熱時發生水解反應生成醇。
甲醇、乙醇等易溶于水,苯酚不溶于冷水、可溶于熱水,碳原子數較多的一元醇則不溶于水。從結構上來看,它們都含有羥基,羥基是親水基團,有使它們溶于水的可能;但烴基是疏水基團,隨著碳原子數的增多,疏水基團影響增大,使得碳原子數較多的一元醇不溶于水。這也包含著量變最終引起質變的辯證思維。

