miRNA和甲基化酶抑制劑在支氣管哮喘中對(duì)Th細(xì)胞的影響
張茹 卜倩 賈宏林 梁曉鷹 高麗 姜孝芳
支氣管哮喘(bronchial asthma, BA)是以發(fā)作性喘息伴呼吸困難為主要癥狀[1]且與微小RNA(microRNA, miRNA)有關(guān)[2]的疾病。miRNA可下調(diào)靶向轉(zhuǎn)錄的蛋白質(zhì)來(lái)調(diào)控病理生理改變[3],并可調(diào)控BA的發(fā)展[4]。DNA甲基化是不改變DNA序列而調(diào)控基因產(chǎn)生可遺傳性改變[5-6]。在哮喘中發(fā)現(xiàn)DNA甲基化的變異,這將推進(jìn)闡明BA在表觀遺傳學(xué)中的機(jī)制[7]。本研究旨在探究BA中miR-126、miR-326和miR-155的表達(dá)以及甲基化酶抑制劑對(duì)BA的調(diào)控作用。
資料與方法
一、主要實(shí)驗(yàn)材料與試劑
5-氮雜胞苷(A2385,Sigma),TRIzol裂解液(152104,Invitrogen),HISTOPAQUE?-1077 (RNBF2219,Sigma),磁珠抗體(557787,BD),兔超敏二步法免疫組化檢測(cè)試劑盒(PV-6001,中杉金橋),IFN-γ、GATA3、ROR-γ、Foxp3抗體(A2385、AF6233、DF3196、AF6544)均定購(gòu)于Affinity,miScript Ⅱ RT Kit(218161)、miScript SYBR Green PCR kit(1046470)、miScript miRNA-126 Primer Assay(MS00003430)、Hs-miR-326 miScript Primer Assay (MS00003948)、Rn-miR-326 miScript Primer Assay (MS00027342)Hs-miR-155 miScript Primer Assay (MS00008778)、Hs-RNU6 miScript primer assay(MS00033740)均定購(gòu)于QIAGEN,實(shí)驗(yàn)所需引物序列見(jiàn)表1。

表1 引物序列信息表
二、研究對(duì)象
1 哮喘患者
病例為自2015年10月到2017年12月就診于新疆醫(yī)科大學(xué)第一附屬醫(yī)院、新疆維吾爾自治區(qū)人民醫(yī)院及新疆醫(yī)科大學(xué)附屬中醫(yī)醫(yī)院的哮喘急性發(fā)作期患者(48例),并符合2016年發(fā)布的《支氣管哮喘防治指南(2016年版)》[8]里的診斷要點(diǎn),排除嚴(yán)重的循環(huán)系統(tǒng)、內(nèi)分泌系統(tǒng)疾病、系統(tǒng)性疾病及妊娠,排除采血一周內(nèi)服用抗組胺藥物、免疫抑制劑等。對(duì)照組在新疆醫(yī)科大學(xué)第一附屬醫(yī)院、新疆維吾爾自治區(qū)人民醫(yī)院及新疆醫(yī)科大學(xué)附屬中醫(yī)醫(yī)院的健康志愿者(48例)中選擇。對(duì)照組排除近期有感染史、哮喘、類風(fēng)濕性關(guān)節(jié)炎及其他免疫性疾病患者,排除前一個(gè)月內(nèi)服用過(guò)三環(huán)類抗抑郁藥、β受體阻滯劑或抗組胺藥等的患者以及有親屬患有過(guò)敏性疾病和哮喘病史的人群。本研究獲新疆醫(yī)科大學(xué)第一附屬醫(yī)院、新疆維吾爾自治區(qū)人民醫(yī)院及新疆醫(yī)科大學(xué)附屬中醫(yī)醫(yī)院倫理委員會(huì)批準(zhǔn)(20120220-144),患者或近親親屬對(duì)研究方案簽署知情同意書(shū)。
2 動(dòng)物模型
于新疆醫(yī)科大學(xué)動(dòng)物實(shí)驗(yàn)中心選購(gòu)180~240 g的無(wú)病原體SPF級(jí)SD雄性大鼠,并清潔飼養(yǎng)。隨機(jī)將大鼠分為4組,每組10只,分組為:正常組、哮喘模型(BA)組、5-aza低劑量(5-aza-L)組、5-aza高劑量(5-aza-H)組。
三、研究方法
1 臨床標(biāo)本的采集及CD4+T細(xì)胞的分離
在無(wú)菌條件下對(duì)病例組和對(duì)照組取靜脈血5mL,使用HISTOPAQUE?-1077分離淋巴細(xì)胞。將分離的淋巴細(xì)胞用500 μL磷酸緩沖鹽水培養(yǎng)液處理,與45 μL磁珠抗體混合,得到CD4+T細(xì)胞。CD4+T細(xì)胞保存在-80℃?zhèn)浯妫糜诤罄m(xù)實(shí)驗(yàn)。
2 動(dòng)物造模
動(dòng)物致敏:動(dòng)物實(shí)驗(yàn)的第1、7、14天對(duì)大鼠進(jìn)行基礎(chǔ)致敏,除正常對(duì)照組外其他組在實(shí)驗(yàn)的第1天使用10%的OVA溶液(10%的Al(OH)3為佐劑)1 mL腹腔注射進(jìn)行基礎(chǔ)致敏,第7天和第14天再次腹腔注射1 mL上述溶液,正常對(duì)照組用生理鹽水代替致敏溶液進(jìn)行注射,部位、劑量及方法與其他實(shí)驗(yàn)組相同。
動(dòng)物激發(fā):第一天致敏在腹腔內(nèi)注射10 %OVA和Al(OH)3混合液1 mL,待第7日重復(fù)1次以加強(qiáng)致敏,第14天基礎(chǔ)致敏后將大鼠置入自制透明霧化吸入箱激發(fā),按3 %的濃度OVA霧化吸入(霧粒直徑3~5 μm),每日1次,每次30 min,連續(xù)15日。正常組予等量生理鹽水腹腔注射以及霧化吸入,其余方法同哮喘模型組。激發(fā)過(guò)程中大鼠出現(xiàn)呼吸加快、口唇發(fā)紺、點(diǎn)頭呼吸、短氣喘息、二便失禁及站立不穩(wěn)等表現(xiàn)為激發(fā)成功。
動(dòng)物給藥:第31日起藥物干預(yù),腹腔注射5-aza-L(0.5 mg/kg)和5-aza-H(5 mg/kg),連續(xù)給藥7天,每次給藥前30min進(jìn)行OVA霧化30min。
3 CD4+T細(xì)胞和大鼠模型RNA的提取
分離出的T細(xì)胞,采用TRIzol法提取總RNA后逆轉(zhuǎn)錄,用于RT-PCR檢測(cè)。按照試劑盒說(shuō)明手冊(cè)進(jìn)行操作,用Nanodrop 2000測(cè)定RNA的濃度。取各組大鼠右肺約50 mg,放入液氮中研磨組織,與T細(xì)胞提取總RNA相同。
4 實(shí)時(shí)熒光定量RT-PCR檢測(cè)miRNA 以及Th細(xì)胞相關(guān)因子mRNA的表達(dá)
按照逆轉(zhuǎn)錄試劑盒說(shuō)明書(shū)操作,將RNA置于MyCyclerTM Thermal Cycler 中進(jìn)行逆轉(zhuǎn)錄,逆轉(zhuǎn)錄反應(yīng)條件為:37 ℃,15 min;85 ℃,5 s;4 ℃,+∞;得到cDNA,然后于PCR儀器中進(jìn)行擴(kuò)增,反應(yīng)體系:2× Master Mix 10 μL、10× PCR Universal Primer 2 μL、10×PCR Primer Assay 2 μL、cDNA 模板2 μL、滅菌水補(bǔ)充至20 μL。擴(kuò)增反應(yīng)程序:95 ℃, 15 min;94 ℃, 15 s;55 ℃, 30 s;70 ℃, 34 s;循環(huán)數(shù):40。最后用2-△△Ct法計(jì)算各組mRNA相對(duì)表達(dá)量。
5 HE染色及免疫組化檢測(cè)大鼠肺組織中蛋白表達(dá)
造模結(jié)束后取大鼠肺組織,進(jìn)行包埋、切片,HE染色,一抗孵育過(guò)夜、顯色、二抗孵育、復(fù)染封片。在光鏡下觀察肺組織氣道的變化,每組選取6個(gè)樣本,每個(gè)樣本選取5個(gè)不重疊視野,測(cè)定平均吸光度用軟件Image-Pro Plus進(jìn)行分析。
四、統(tǒng)計(jì)學(xué)方法
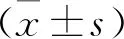
結(jié) 果
一、哮喘組與正常組中miR-126、miR-326和miR-155 mRNA的相對(duì)表達(dá)量
miR-126 、miR-326和miR-155在哮喘組表達(dá)水平高于正常組,差異有統(tǒng)計(jì)學(xué)意義。(表2)
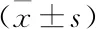
表2 哮喘患者組與正常組miR-126、miR-326、miR-155的表達(dá)水平
二、哮喘組與正常組中IFN-γ、GATA3、ROR-γ、Foxp3 mRNA的相對(duì)表達(dá)量
IFN-γ和 Foxp3在哮喘組表達(dá)水平明顯低于正常組,差異有統(tǒng)計(jì)學(xué)意義;ROR-γ在哮喘組表達(dá)水平顯著高于正常組,差異有顯著統(tǒng)計(jì)學(xué)意義。(表3)
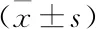
表3 哮喘患者組與正常組IFN-γ、GATA3、ROR-γ、Foxp3的表達(dá)水平
三、 哮喘患者miR-126、miR-326和miR-155 mRNA與IFN-γ、GATA3、ROR-γ、Foxp3 mRNA的相關(guān)性分析
Pearson相關(guān)性分析顯示在哮喘患者中miR-126 、miR-326和 miR-155 與IFN-γ、GATA3 、ROR-γ和Foxp3表達(dá)無(wú)明顯相關(guān)性(見(jiàn)表4)。
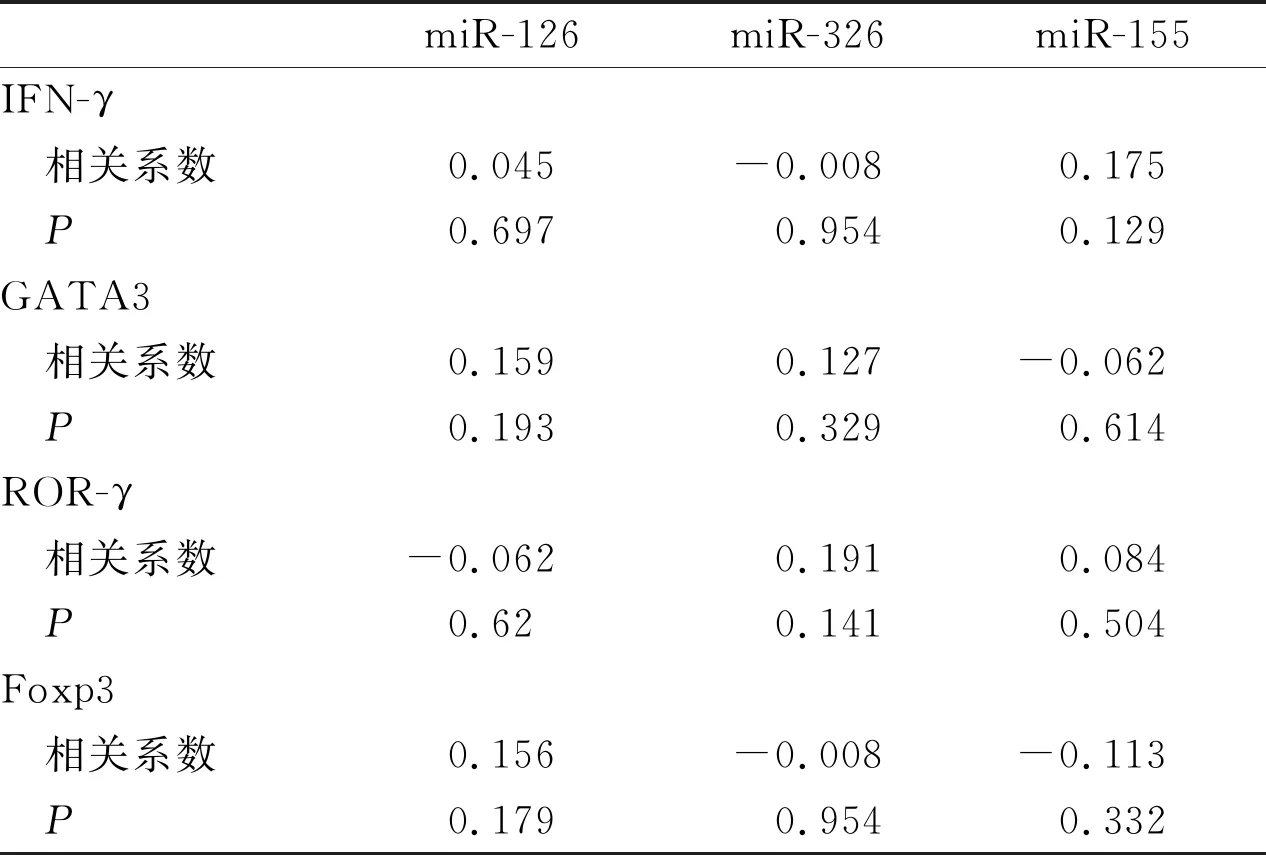
表4 哮喘患者miR-126、miR-326和miR-155 mRNA與IFN-γ、GATA3、ROR-γ、Foxp3 mRNA的相關(guān)性分析
四、各組大鼠肺組織病理學(xué)變化
光鏡下觀察顯示: 正常組支氣管平滑肌細(xì)胞、黏膜皺襞無(wú)增生,無(wú)炎性滲出物,杯狀細(xì)胞無(wú)增生,氣道內(nèi)無(wú)明顯炎性細(xì)胞; 哮喘組氣管壁周圍有大量炎性細(xì)胞浸潤(rùn),部分肺泡壁斷裂,杯狀細(xì)胞出現(xiàn)增生,支氣管黏膜皺襞增多延長(zhǎng),管腔縮窄; 5-aza-L組、5-aza-H組周圍有少量炎性細(xì)胞浸潤(rùn),支氣管黏膜皺襞少許增多,杯狀細(xì)胞少量增生,管腔有些輕微縮窄。(圖1)
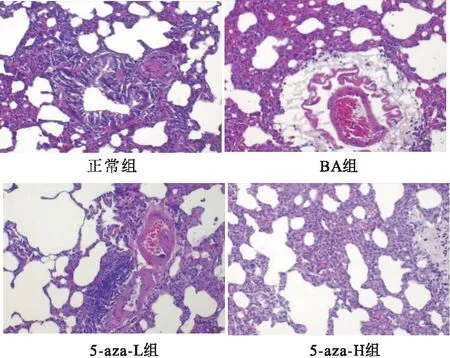
圖1 HE染色觀察大鼠肺組織病理改變(×200)
五、5-aza干預(yù)大鼠模型對(duì)miR-126、miR-326和miR-155 mRNA表達(dá)的影
miR-126在哮喘組表達(dá)水平高于正常組,在5-aza-L組和5-aza-H組表達(dá)水平低于哮喘組,差異有統(tǒng)計(jì)學(xué)意義;miR-326在5-aza-L組表達(dá)水平低于哮喘組,差異有顯著統(tǒng)計(jì)學(xué)意義; miR-155在5-aza-L組表達(dá)水平低于哮喘組,差異有統(tǒng)計(jì)學(xué)意義。(表5-6)
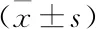
表5 大鼠正常組與哮喘組miR-126、miR-326、miR-155的表達(dá)水平
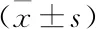
表6 大鼠模型各組miR-126、miR-326、miR-155的表達(dá)水平
六、5-aza干預(yù)大鼠模型對(duì)IFN-γ、GATA3、ROR-γ、Foxp3 mRNA 表達(dá)的影響
IFN-γ在5-aza-H組表達(dá)水平低于哮喘組,差異有顯著統(tǒng)計(jì)學(xué)意義; GATA3在哮喘組表達(dá)水平明顯高于正常組,在5-aza-H組表達(dá)水平低于哮喘組,差異有統(tǒng)計(jì)學(xué)意義;ROR-γ在哮喘組表達(dá)水平明顯高于正常組,在5-aza-L組和5-aza-H組表達(dá)水平明顯低于哮喘組,差異有顯著統(tǒng)計(jì)學(xué)意義;Foxp3在哮喘中表達(dá)低于正常組,在5-aza-L組表達(dá)水平明顯高于哮喘組,差異有顯著統(tǒng)計(jì)學(xué)意義。(表7-8)
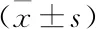
表7 大鼠正常組和哮喘組IFN-γ、GATA3 、ROR-γ、Foxp3的表達(dá)水平
七、5-aza干預(yù)大鼠模型對(duì)IFN-γ、GATA3、ROR-γ、Foxp3 蛋白 表達(dá)的影響
免疫組化檢測(cè),計(jì)算平均光密度進(jìn)行相對(duì)表達(dá)分析,IFN-γ在哮喘組的表達(dá)水平低于正常組,在5-aza-L組表達(dá)水平高于哮喘組,差異有顯著統(tǒng)計(jì)學(xué)意義;GATA3在哮喘組的表達(dá)水平高于正常組,5-aza-L組和5-aza-H組表達(dá)水平低于哮喘組,差異有顯著統(tǒng)計(jì)學(xué)意義; ROR-γ在哮喘組表達(dá)水平明顯高于正常組,5-aza-L組和5-aza-H組表達(dá)水平低于哮喘組,差異有顯著統(tǒng)計(jì)學(xué)意義;Foxp3在哮喘組表達(dá)水平明顯低于正常組,5-aza-L組和5-aza-H組表達(dá)水平高于哮喘組,差異有顯著統(tǒng)計(jì)學(xué)意義。(圖2,表9-10)
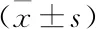
表9 大鼠正常組和模型組中IFN-γ、GATA3 、ROR-γ、Foxp3蛋白的平均吸光度值
圖2 大鼠模型各組IFN-γ、GATA3、ROR-γ、Foxp3的蛋白表達(dá)水平(×400)
表8 大鼠模型各組IFN-γ、GATA3 、ROR-γ、Foxp3的表達(dá)水平
討 論
CD4+T可分為Th1、Th2、Th17以及Treg四個(gè)亞群,Th1細(xì)胞分泌干擾素-γ(interferon-γ, IFN-γ),參與細(xì)胞免疫和遲發(fā)性超敏炎癥反應(yīng)[9]; Th2細(xì)胞的轉(zhuǎn)錄因子GATA結(jié)合蛋白3 ( GATA binding protein 3, GATA3)具有促炎作用[10-11]。Treg細(xì)胞負(fù)責(zé)維持自身耐受并抑制自身免疫, 而Th17細(xì)胞參與炎癥反應(yīng)[12]。Th1/Th2、Th17/Treg細(xì)胞平衡在哮喘發(fā)病中起重要作用[13],免疫失衡易引起氣道炎癥疾病,以BA最常見(jiàn)[14]。哮喘發(fā)作時(shí),GATA3表達(dá)迅速升高,促進(jìn)氣道高反應(yīng)性和氣道壁重塑[15]。本研究結(jié)果表明,與正常組相比較,IFN-γ和叉頭翼狀螺旋轉(zhuǎn)錄因子3(winged-helix transcription factor 3, Foxp3)在人體外周血中哮喘組表達(dá)水平明顯降低,而哮喘組維甲酸相關(guān)孤兒受體(retinoic acid receptor-related orphan receptor-γ,ROR-γ)表達(dá)水平明顯升高,與此前研究一致。本研究大鼠模型中, GATA3和ROR-γ在哮喘組表達(dá)水平升高,這與此前研究一致。
表10 大鼠模型各組中IFN-γ、GATA3、ROR-γ、Foxp3蛋白的平均吸光度值
近年來(lái),研究發(fā)現(xiàn)BA發(fā)病與miRNA有關(guān)[16],可能通過(guò)影響炎癥因子釋放參與BA的病理改變[17]。miRNA是CD4+T細(xì)胞分化的重要調(diào)節(jié)因子[18],有研究發(fā)現(xiàn)調(diào)節(jié)miR-126[19]和miR-155[20]可以調(diào)節(jié)Th細(xì)胞因子平衡[21]。因此,miRNA與Th細(xì)胞因子在BA中的作用成為哮喘新的研究方向。miR-126定位于9號(hào)染色體類表皮生長(zhǎng)因子樣結(jié)構(gòu)域7基因7號(hào)內(nèi)含子中,能調(diào)控Th2細(xì)胞因子表達(dá)[22],參與機(jī)體炎癥反應(yīng)及免疫應(yīng)答[23], miR-126 表達(dá)降低可調(diào)控GATA-3表達(dá)進(jìn)而使Th2 細(xì)胞減少釋放炎性介質(zhì),改善氣道炎癥反應(yīng)[24],緩解哮喘小鼠氣道炎癥反應(yīng)[25]。本研究結(jié)果表明, miR-126在哮喘患者組表達(dá)水平升高,在大鼠模型中,miR-126在哮喘組表達(dá)水平升高,ROR-γ表達(dá)水平升高,與此前研究一致。從本研究結(jié)果來(lái)看,在大鼠模型中,哮喘組miR-126表達(dá)水平升高,GATA3和ROR-γ表達(dá)水平升高,推測(cè)miR-126與GATA3和ROR-γ可能存在負(fù)調(diào)控關(guān)系。miR-326位于人體11號(hào)染色體,之前研究發(fā)現(xiàn)miR-326在變應(yīng)性鼻炎CD4+T淋巴中高表達(dá)且與低表達(dá)的IFN-γ負(fù)相關(guān),推測(cè)miR-326可能影響Th1細(xì)胞因子IFN-γ的表達(dá)[26],miR-326先前也已被證明通過(guò)誘導(dǎo) Th17 分化和成熟在免疫發(fā)病機(jī)制中發(fā)揮作用[27]且miR-326在哮喘中調(diào)控氣道平滑肌細(xì)胞[28]從而參與哮喘的發(fā)生發(fā)展。本研究結(jié)果表明,哮喘患者組miR-326表達(dá)水平升高,與此前研究一致,哮喘患者組同時(shí)ROR-γ表達(dá)水平升高,IFN-γ和Foxp3表達(dá)水平降低。進(jìn)行大鼠造模,結(jié)果顯示,在大鼠哮喘組中GATA3和 ROR-γ表達(dá)水平升高,與此前研究一致。miR-155位于人體21號(hào)染色體上, 具有維持人類免疫系統(tǒng)功能[29]。有研究發(fā)現(xiàn),BA患者血清miR-155水平顯著增加[30], 且與其肺功能呈顯著負(fù)相關(guān)性,而且miR-155能夠抑制CD4+T細(xì)胞中IFN-γ信號(hào)轉(zhuǎn)導(dǎo)[31],促進(jìn)miR-155的表達(dá),IFN-γ表達(dá)水平明顯降低而GATA3表達(dá)水平升高[32],推測(cè)miR-155可以負(fù)調(diào)控IFN-γ和正調(diào)控GATA3的表達(dá)。在本實(shí)驗(yàn)中,哮喘患者組miR-155表達(dá)水平升高,ROR-γ表達(dá)水平升高,IFN-γ和Foxp3表達(dá)水平降低,與此前研究一致,本研究在哮喘患者組和正常組中miR-126、miR-326和miR-155與IFN-γ、GATA3、 ROR-γ和Foxp3呈弱相關(guān)性,考慮原因有三,一可能與病人過(guò)敏源不同有關(guān),二可能與疾病發(fā)展階段有關(guān),三可能與哮喘復(fù)雜機(jī)制有關(guān),因其多種基因多種通路調(diào)控,所以此后應(yīng)針對(duì)以上原因細(xì)化研究方案,探究它們具體調(diào)控關(guān)系。
DNA甲基化可以通過(guò)調(diào)控Th細(xì)胞因子失衡進(jìn)而調(diào)控炎癥因子的基因表達(dá)[33],比如DNA甲基化通過(guò)調(diào)控Th細(xì)胞因子失衡參與了類風(fēng)濕炎早期炎癥的發(fā)生發(fā)展[34]。5-aza作為一種甲基化酶抑制劑,它被證明可以通過(guò)調(diào)節(jié)甲基化來(lái)調(diào)節(jié)miRNA的轉(zhuǎn)錄[35]及下調(diào)Th2表達(dá)抑制炎癥反應(yīng),減輕鼻黏膜損傷,緩解AR大鼠過(guò)敏性癥狀[36],例如之前發(fā)現(xiàn)miR-126在甲基化酶抑制劑作用下表達(dá)降低[37]。本研究用5-aza干預(yù)大鼠后顯示大鼠模型中5-aza低劑量組miR-126、miR-326和miR-155表達(dá)水平降低,所以5-aza作為甲基化酶抑制劑還可以調(diào)控miR-126、miR-326和miR-155的表達(dá)水平,且調(diào)控作用與5-aza劑量正相關(guān)。此外,免疫組化結(jié)果顯示,與哮喘組相比,IFN-γ蛋白表達(dá)水平在5-aza低劑量組表達(dá)升高而5-aza高劑量組中并未升高,這表明5-aza對(duì)IFN-γ的調(diào)控作用是雙向的;GATA3和ROR-γ表達(dá)水平在哮喘組表達(dá)升高在5-aza 干預(yù)之后下降;Foxp3表達(dá)水平在5-aza 干預(yù)之后升高,因此,5-aza作為甲基化酶抑制劑可以調(diào)控IFN-γ、GATA3、ROR-γ和Foxp3基因甲基化的表達(dá)。
綜上所述,在哮喘中,甲基化酶抑制劑5-aza可以調(diào)控miR-126、miR-326和miR-155的表達(dá);甲基化酶抑制劑5-aza可以下調(diào)細(xì)胞因子GATA3、ROR-γ的表達(dá)以及上調(diào)Foxp3的表達(dá),同時(shí)可通過(guò)調(diào)整5-aza的劑量雙向調(diào)節(jié)IFN-γ的表達(dá)。 miR-326與 GATA3和 ROR-γ表達(dá)呈正相關(guān); miR-326和 miR-155 與 Foxp3表達(dá)呈負(fù)相關(guān),所以 miR-326、miR-155以及Th細(xì)胞因子可能存在交互關(guān)系,為表觀遺傳藥物治療哮喘提供了新的思路,miRNA和甲基化酶抑制劑可以作為BA和氣道敏感反應(yīng)的有效切入點(diǎn),為哮喘中表觀遺傳藥物的研究開(kāi)闊了思路。

