Cu/Mg 含量對2024 鋁合金耐蝕性能的影響
吳學昆,羅兵輝,柏振海,鄧 攀,莫文鋒
(中南大學 材料科學與工程學院,長沙 410083)
Al-Cu-Mg 系合金具有高比強度、高延展性,廣泛應用于航空航天領域[1]。時效過后的相組成大致由Cu/Mg 含量比值決定(Cu 與Mg 的質量分數比值表示為Cu/Mg):當Cu/Mg>8 時,合金的主要強化相為θ′相;當4<Cu/Mg<8 時,合金的主要強化相為θ′相和S 相;當1.5<Cu/Mg<4 時,合金的主要強化相為S 相[2]。2024 鋁合金的主要添加元素為Cu、Mg。合金中Cu 是形成主要強化相θ′相(Al2Cu)和S 相(Al2CuMg)的主要元素之一,可以增加鋁合金的強度、硬度和耐熱性能。而Mg 的存在不僅會對晶粒尺寸大小有影響,還會影響鋁合金的屈服強度和拉伸性能。資料顯示Cu 和Mg 對于鋁合金的性能的貢獻表現出一定的協同作用[3]。目前,關于Cu/Mg 的研究主要集中在力學性能方面。但關于Cu/Mg 對合金耐蝕性影響的報道相對較少。晶間腐蝕作為一種典型的局部腐蝕,主要發生在晶界處。崔繼紅等[4]發現鋁合金的晶間腐蝕是由局部點蝕引起的,特別是合金中S 相的溶解在整個過程中起到至關重要的作用。化學銑切(簡稱化銑)是利用試劑對合金表面進行溶解,提高表面平整度的重要方法[5]。這種表面處理方法不需要刀具,不會存在機加工產生的應力。因此,這種加工方式常用于結構復雜的零部件。特別是針對超大、超薄、易變形的蒙皮加工具有很大的優勢[6],彌補了傳統機械加工的不足。
本文在保證合金強度的基礎上,研究Cu/Mg 對合金晶間腐蝕,以及化銑表面粗糙度的影響。
1 試驗材料與方法
1.1 試驗材料
試驗材料由實驗室熔鑄制備。使用的原材料為純Al、純Mg、純Zn 和Al-50Cu、Al-10Mn、Al-4Ti 等中間合金。熔煉在井式電阻爐中進行,在760 ℃熔化后降溫至720~730 ℃進行澆鑄,合金成分見表1。鑄錠尺寸為35 mm×80 mm×270 mm,鑄錠經過498 ℃×18 h 均勻化處理后,軋制成2 mm 厚的板材,板材經498 ℃×1 h 固溶處理后進行人工時效。
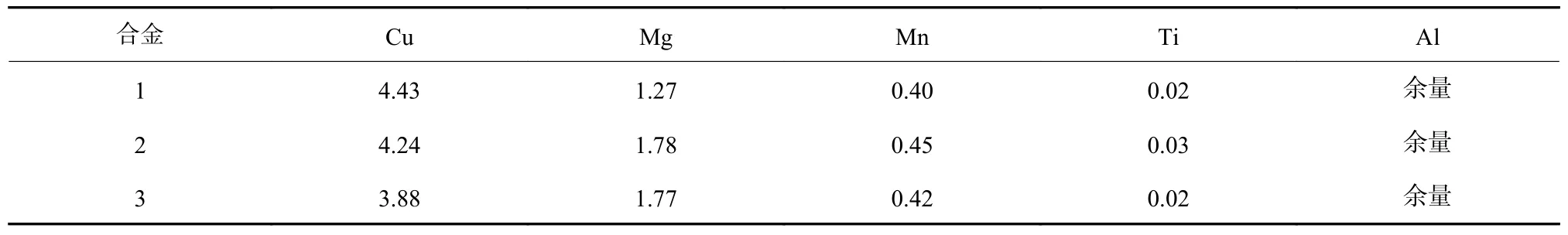
表1 三種合金成分 (質量分數/%)Tab.1 Compositions of the three alloys (mass fraction/%)
1.2 試樣制備及測試方法
電化學試樣的制備:將試樣加工成面積為1 cm×1 cm 的試樣塊,并用自凝型義齒基托樹脂對試樣進行鑲嵌,經1 000#金相砂紙細磨拋光后作為工作電極備用。使用Chi660H 工作站進行電化學測試。電化學阻抗(electrochemical impedance spectroscopy,EIS)測試頻率范圍為10-2~105Hz。振幅信號為10 mV,用Zview 軟件進行等效電路擬合。極化曲線測量的范圍為-1.2~-0.4 V,掃描速率為1 mV/s。晶間腐蝕測試及評定結果按照國家標準GB/T 7998—2005 進行,腐蝕液由57 g NaCl+10 mL H2O2+1 L H2O 組成,試驗溫度為35 ℃,時間為6 h。結束后在距離腐蝕面底部5 mm 處截取試樣,在金相顯微鏡下觀察截面腐蝕深度。利用Tescan MIRA3 掃描電子顯微鏡(scanning electron microscope,SEM)觀察腐蝕形貌。元素成分用配套的Genesis-60s 能譜儀(energy disperse spectroscopy,EDS)進行分析。
沿軋向取化銑試樣,尺寸為30 mm×25 mm×2 mm。用質量分數為40% 的NaOH 水溶液對試樣進行預處理,然后水洗晾干。采用HH968-2 可剝涂料作為保護涂層,待固化后用刻刀剝出待化銑表面。將化銑試樣放入80 ℃的化銑液[2]中,化銑后取出干燥。采用JB-4C 表面粗糙度儀對試樣的表面粗糙度進行測量。
2 試驗結果與分析
在NaCl 水溶液中,2024 鋁合金的氧化膜成分相對比較復雜,其氧化膜的形成與溶解是一個動態的過程[7],反應式為:
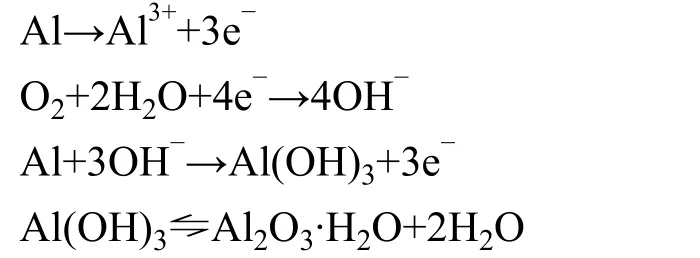
從上述反應式中可以看出,2024 鋁合金的表層以Al 的水合氧化物作為保護合金基體的主要物質。在整個腐蝕滲透過程中,Cl-會在電場作用下吸附在水合氧化物的表面,置換界面中的OH-,然后與其中的陽離子(Al3+)結合形成可溶于水的氯化物(AlCl3),破壞合金氧化層,加快局部腐蝕的發生[8]。圖1 為在3.5% NaCl 水溶液中浸泡3 h 后的合金表面。對比合金的EDS 結果可以看出,隨著表面氧化層的破壞,合金首先發生溶解的位置為S 相,隨后沿周邊晶界擴展造成晶間腐蝕,對合金造成更加嚴重的破壞[9]。

圖1 合金3 在3.5%NaCl 水溶液中浸泡3 h 后的表面形貌及成分分析結果Fig.1 Surface morphologies and composition analysis results of alloy 3 after soaking in 3.5% Nacl solution for 3 h
晶間腐蝕作為一種局部腐蝕,主要發生在晶界及其周邊區域。對于鋁合金而言,作為第二相的金屬間化合物在熱處理過程中會在晶界處發生選擇性沉淀。這些中間相與鋁基體之間存在電勢差,從而引起腐蝕反應發生[10]。這種晶界處的腐蝕行為雖然不會引起金屬整體的大量損失,但這種局部腐蝕發生的區域更容易形成裂紋,導致合金力學性能下降[11]。圖2 顯示了在光學顯微鏡下三種合金在腐蝕液中腐蝕后的截面情況,表2 為最大晶間腐蝕深度結果。當Cu/Mg=2.19 時,合金3 的最大晶間腐蝕深度為182 μm,抗晶間腐蝕性能最差。當Cu/Mg=3.39 時,合金1 最大晶間腐蝕深度為152 μm,晶間腐蝕的敏感性相對較低。當Cu/Mg=2.38 時,合金2 最大晶間腐蝕深度為134 μm,此時合金的耐蝕性最好。

表2 三種合金晶間腐蝕深度Tab.2 Intergranular corrosion depth of the three alloys

圖2 三種合金晶間腐蝕截面形貌Fig.2 Intergranular corrosion cross section morphology of the three alloys
圖3 顯示了不同Cu/Mg 的極化曲線,由極化曲線得到的電化學腐蝕參數見表3。一般來說,自腐蝕電勢取決于材料的屬性,是材料本身各種氧化還原反應綜合表現后的穩定值[12]。而腐蝕電流密度反映出材料在發生腐蝕反應后腐蝕過程的快慢。特別是2024 鋁合金這樣無明顯鈍化狀態的材料首要考慮的就是腐蝕電流密度。從表3 中可以看出Cu/Mg不同對其中的電化學腐蝕參數有著很大的影響。根據Tafel 外推法測量了腐蝕電勢,陰極和陽極的Tafel 斜率以及腐蝕電流密度。并根據公式計算出腐蝕速率[13]。
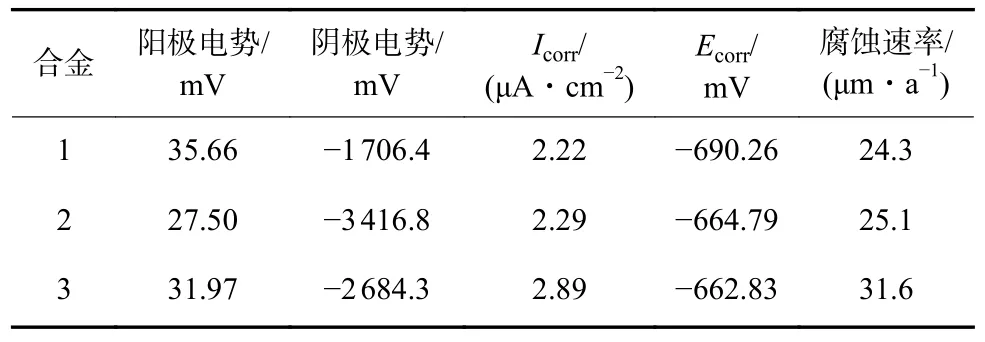
表3 三種合金的極化曲線參數Tab.3 Polarization curve parameters of the three alloys
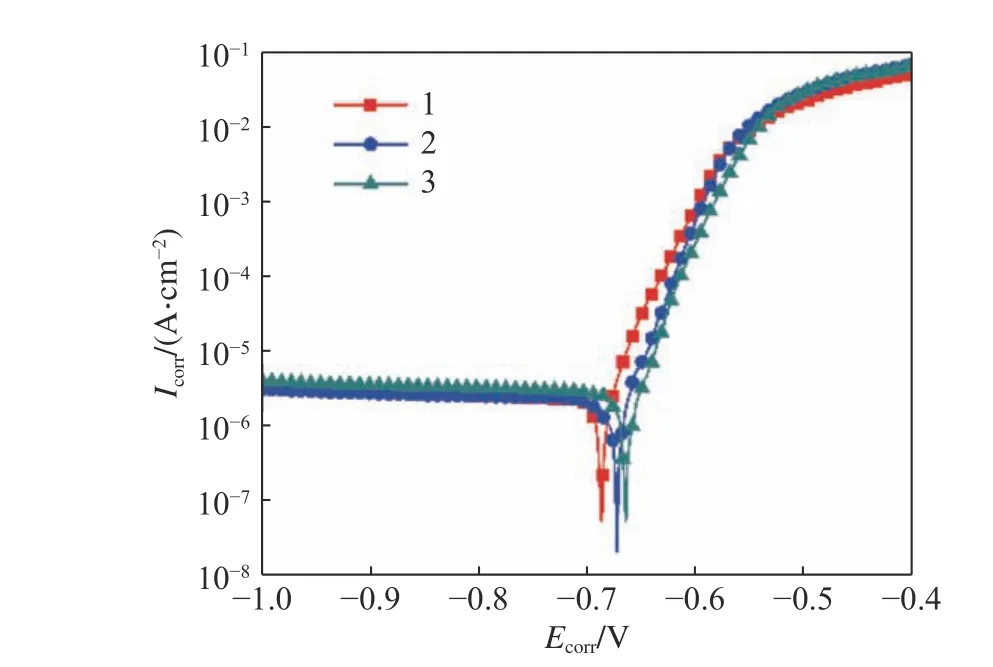
圖3 三種合金的極化曲線Fig.3 Polarization curves of the three alloys

式中:K為法拉第常數;Icorr為腐蝕電流密度;ρ為合金密度;ni為第i種元素在腐蝕反應過程中的價態(有效價態);fi為第i種元素的質量分數;Wi為第i種元素的相對分子質量。
通常腐蝕電流密度越低,腐蝕電勢越高的材料耐蝕性越好。合金1 具有更負的腐蝕電勢。這表明合金1 在電化學反應中具有較低的腐蝕反應臨界值,易發生腐蝕反應。對比表4 發現,合金1 具有更小的腐蝕電流密度,說明合金1 在腐蝕過程中具有較低的腐蝕速率。較低的電流密度使得合金1 具有較好的耐蝕性。當Cu/Mg=2.19 時,合金具有更正的腐蝕電勢。盡管合金1 的電化學反應的熱力學趨勢高于合金3,但合金3 具有更高的腐蝕電流密度,在達到臨界值后能快速反應,腐蝕敏感性較高。

表4 三種合金的EIS 擬合參數Tab.4 EIS fitting parameters of the three alloys
EIS 廣泛用于腐蝕領域。EIS 作為一種研究腐蝕性環境中金屬表面狀況的有效方法,在電化學測量方面可用于表征發生在電極/電解質界面處的反應過程。圖4 是由EIS 譜圖得到的Bode 圖和Nyquist 圖。從圖4 中可以看出,三種Cu/Mg 合金在3.5%NaCl 水溶液中具有不同的表面特性。對鋁合金而言,其基體表面有一層致密的氧化膜,所以在Bode 圖的高頻區存在一個時間常數。而低頻區的時間常數通常受局部點蝕的影響[14]。
通過圖4(b)中等效電路的擬合數據可以發現,三種合金的CPE1 比較接近理想電容。合金3 表面存在大量的腐蝕產物,導致合金3 具有較高的Yo-1,為6.73×10-5S·cm-2·s-n。此外,合金3 擁有更小的電荷轉移電阻13 496 Ω/cm2。與合金3 相比,合金2 具有較小的Yo-2 和較大的電荷轉移電阻。較大的電荷轉移電阻表明金屬表面存在更加穩定的氧化膜阻礙了Cl-以及腐蝕產物對合金基體的滲透。在Nyquist 圖中表現為,在低頻區電荷轉移部分與實軸夾角更加接近45°。而Yo-1 值與合金氧化膜的水化作用相關。與理想電容相比,合金表面的狀態比較復雜(不均勻的電流分布,表面粗糙度的變化,漏電電容的存在)。利用公式計算出材料的真實電容[15]:

圖4 三種合金的EIS 圖譜Fig.4 EIS spectra of the three alloys

式中:C為真實電容;Yo為CPE 常數;n為彌散系數;ω*為特征頻率。
對每個試樣的真實電容依據式(2)進行計算,結果如圖5 所示。當Cu/Mg=3.49 時,合金的真實電容最低為1.14 μF/cm2,其次為1.46 μF/cm2。當Cu/Mg=2.19 時真實電容最高,為1.87 μF/cm2。對于2024 鋁合金而言,這種現象的出現說明在3.5%NaCl 水溶液中,當Cu/Mg=2.19 時,合金表面可能更易發生脫合金現象[16],使得合金表面結構更加復雜,使真實電容升高。對于鋁合金而言,氧化膜的穩定性和厚度通常直接關系到合金的耐蝕性。利用下式對氧化膜的厚度h進行估算[17]。式中:ε為介電常數;ε0為真空中的介電常數;C為真實電容。從圖5 中可以看出,當Cu/Mg=3.49 時,合金氧化膜厚度最大為7.25 nm,當Cu/Mg=2.38 時,合金氧化膜厚度為5.56 nm;當Cu/Mg=2.19 時,合金氧化膜厚度最低為4.42 nm。由于缺乏足夠厚的氧化膜對合金基體進行保護,腐蝕性介質更容易穿過氧化膜對合金基體造成破壞,使合金的耐蝕性大大降低。

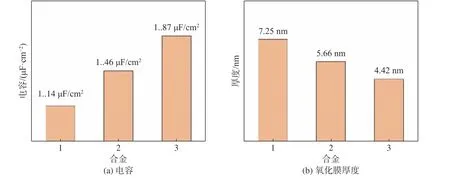
圖5 三種合金的真實電容及氧化膜厚度Fig.5 Capacitance and oxide film thickness of the three alloys
化學銑切作為一種特殊的表面腐蝕加工手段,常用作蒙皮材料的加工。2024 鋁合金作為蒙皮材料,其表面不允許出現較大的加工痕跡。這種條件通常選擇表面粗糙度與輪廓最大高度對表面粗糙度進行綜合評判,其結果見表5。圖6 為合金3 化銑后的表面情況,從表5 中可以看出,合金2 的表面粗糙度最低,為0.75 μm,而合金3 和合金1 的表面粗糙度分別為1.22 μm 和1.33 μm。對比三種合金輪廓的峰值和谷值,合金1 具有更大的表面輪廓差值,合金2 和合金3 相對差值較小。要想獲得更加平整的表面,需要合金在化銑溶液中能夠均勻腐蝕。從圖6 中可以看出,在化銑后的樣品表面出現了大量的腐蝕坑,而且發生了腐蝕坑的聚集。對其進行EDS 分析,發現在腐蝕坑當中的粒子主要是殘余的S 相。據研究表明,在化銑過程中雖然主要參加反應的是鋁基體,但合金中析出相會與鋁基體產生局部的電化學反應,使得化銑結果更加不可控[18]。化銑過程中,S 相優先發生選擇性溶解,使合金中的Cu 富集。Cu 的加入會使周邊鋁基體優先溶解,隨著反應的進行,這些第二相粒子發生脫落導致表面產生深淺不一的腐蝕坑,對合金表面粗糙度造成嚴重的影響。

表5 三種合金化銑后的表面粗糙度Tab.5 Surface roughness of the three alloys after chemical milling

圖6 合金3 化銑后表面形貌及成分分析結果Fig.6 Surface morphologies and composition analysis results of alloy 3 after chemical milling
3 結論
本文研究了三種Cu/Mg 對2024 鋁合金耐蝕性能及化銑后合金表面粗糙度的影響。得到結論如下:
(1)合金氧化層的厚度隨Cu/Mg 的增大而增大,Cu/Mg=3.49 時,氧化膜厚度最大為7.25 nm。
(2)對于2024 鋁合金,腐蝕電流影響要大于腐蝕電勢的影響,當Cu/Mg=2.19 時具有較高的腐蝕速率,為31.6 μm/a。Cu/Mg=3.49 時,合金腐蝕速率最低,為24.3 μm/a。綜合比較三種合金,合金2 的耐蝕性最好。
(3)S 相是造成合金化銑表面腐蝕坑的主要原因,Cu/Mg=2.38 時化銑表面粗糙度為0.75 μm,此時合金的表面平整度最高。

