缺血性腦卒中分子流行病學篩查及其危險因素分析
閆 雯,趙于飛,宮玉哲,張小珍,韓樹珍,李興杰
蘭州大學第二醫院 健康管理中心,甘肅 蘭州 730000
缺血性腦卒中是以局灶性神經功能缺失為共同特征的急性腦血管疾病,占腦卒中總發病率的80%[1]。有研究報道,缺血性腦卒中發病是遺傳和環境因素共同作用的結果,高血壓、糖尿病、冠心病、高同型半胱氨酸血癥是其明確的危險因素[2-3]。但仍有許多影響因素與其發病關系尚未明確。近年來,全基因組關聯分析作為分析人類復雜疾病的一種重要手段,已識別出眾多與缺血性腦卒中或其危險因素相關的候選基因[4]。缺血性腦卒中涉及的易感基因較多,其發生、發展往往由多個基因共同作用。因此,臨床對缺血性腦卒中遺傳易感性的研究難以有突破性的進展。CDKN2B-AS1基因表達與心腦血管疾病關系密切[5],但目前尚缺乏缺血性腦卒中分子流行病學的相關數據。本研究以缺血性腦卒中遺傳學背景作為切入點,構建聚合酶鏈式反應-高分辨熔解曲線(PCR-HRM)對缺血性腦卒中患者進行基因分型,獲取缺血性腦卒中遺傳學數據,同時探索能夠預測缺血性腦卒中發病的相關臨床檢測指標,篩選缺血性腦卒中的危險因素,為缺血性腦卒中的早期篩查提供依據。現報道如下。
1 對象與方法
1.1 研究對象 選取自2020年3月至2022年1月蘭州大學第二醫院收治的250例缺血性腦卒中患者納入B組,另選取同期250例健康體檢者納入A組。納入標準:(1)B組患者符合《2014年中國急性缺血性腦卒中診治指南》[6]中缺血性腦卒中的診斷標準,首次發病,且經顱腦CT或磁共振確診;(2)年齡18~80歲;(3)所有研究對象均知情同意。排除標準:(1)心源性腦栓塞、瘤性腦卒中、煙霧病或靜脈竇血栓形成引起的腦卒中;(2)惡性腫瘤;(3)合并心、肝、腎重要臟器疾病;(4)認知功能障礙及凝血功能障礙;(5)臨床資料缺失,未完成本研究。本研究經蘭州大學第二醫院倫理委員會批準。
1.2 研究方法
1.2.1 特異性引物設計 篩選易感基因。在NCBI的數據庫(http://www.ncbi.nlm.nih.gov)SNP子庫內對SNP位點全序列信息進行查詢,標注該位點上下游200 bp內所有其他的突變,避開這些突變位點進行引物設計。引物設計使用在線軟件Primer-BLAST,引物的有效性、特異性、可辨性和具體的Tm值(℃)通過Two-state melting、Primer-BLAST、Oligo Analyzer和uMelt等在線軟件進行評價,初步評價可用后,由上海生工生物工程有限公司進行合成。引物的特異性和有效性通過后續預實驗PCR擴增驗證,擴增效果不理想時及時修正,最終獲得最佳特異性引物。
1.2.2 PCR-HRM檢測體系的建立與優化 基因組DNA提取使用Ezup柱式動物基因組DNA抽提試劑盒,嚴格按照說明書操作。提取的基因組DNA具體純度和濃度采用微量蛋白核酸檢測儀(Nano-drop 2000)進行檢測,使用瓊脂糖凝膠電泳檢測DNA的完整性。PCR擴增和HRM檢測使用梯度PCR儀(北京東勝創新生物科技有限公司,型號EDC-810)及高分辨的實時熒光定量PCR儀(美國凱杰公司,Rotor-Gene Q)完成,通過預實驗優化反應條件,擴增完成后通過瓊脂糖凝膠電泳和全自動凝膠成像儀進行PCR產物的特異性檢測。
1.2.3 PCR-HRM檢測體系檢驗性能評價 通過靈敏度、特異性、重復性、再現性和準確性對上述檢測方法進行檢驗性能評價。通常將突變基因型定義為陽性,野生基因型定義為陰性。隨機挑選50例標本進行PCR-HRM基因分型,通過Sanger測序評估其準確性,并計算特異性和靈敏度。采用批內10次重復實驗評估重復性,即選取確定的純合突變型和野生型標本各2例,每個標本在同1個批次內重復10管;采用批內10次重復實驗評估再現性,即隨機挑選10個樣本,每天1次,不間斷地實施10 d檢測;計算2種基因型的Tm值平均值、變異系數(CV)和標準差。
特異性=真陰性/(假陽性+真陰性)×100%
靈敏度=真陽性/(真陽性+假陰性)×100%
1.3 觀察指標 評價遺傳分子標志物的疾病預測價值,通過多因素Logistic回歸分析篩選出缺血性腦卒中的危險因素,分析SNP基因型突變與缺血性腦卒中的相關性。比較各基因型缺血性腦卒中指標,包括空腹血糖、甘油三酯、糖化血紅蛋白。
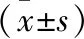
2 結果
2.1 單因素分析結果 兩組性別、職業比較,差異無統計學意義(P>0.05)。兩組年齡、體質量指數、高血壓史、糖尿病史、高脂血癥、腦卒中家族史、基因型分布比較,差異有統計學意義(P<0.05)。見表1。
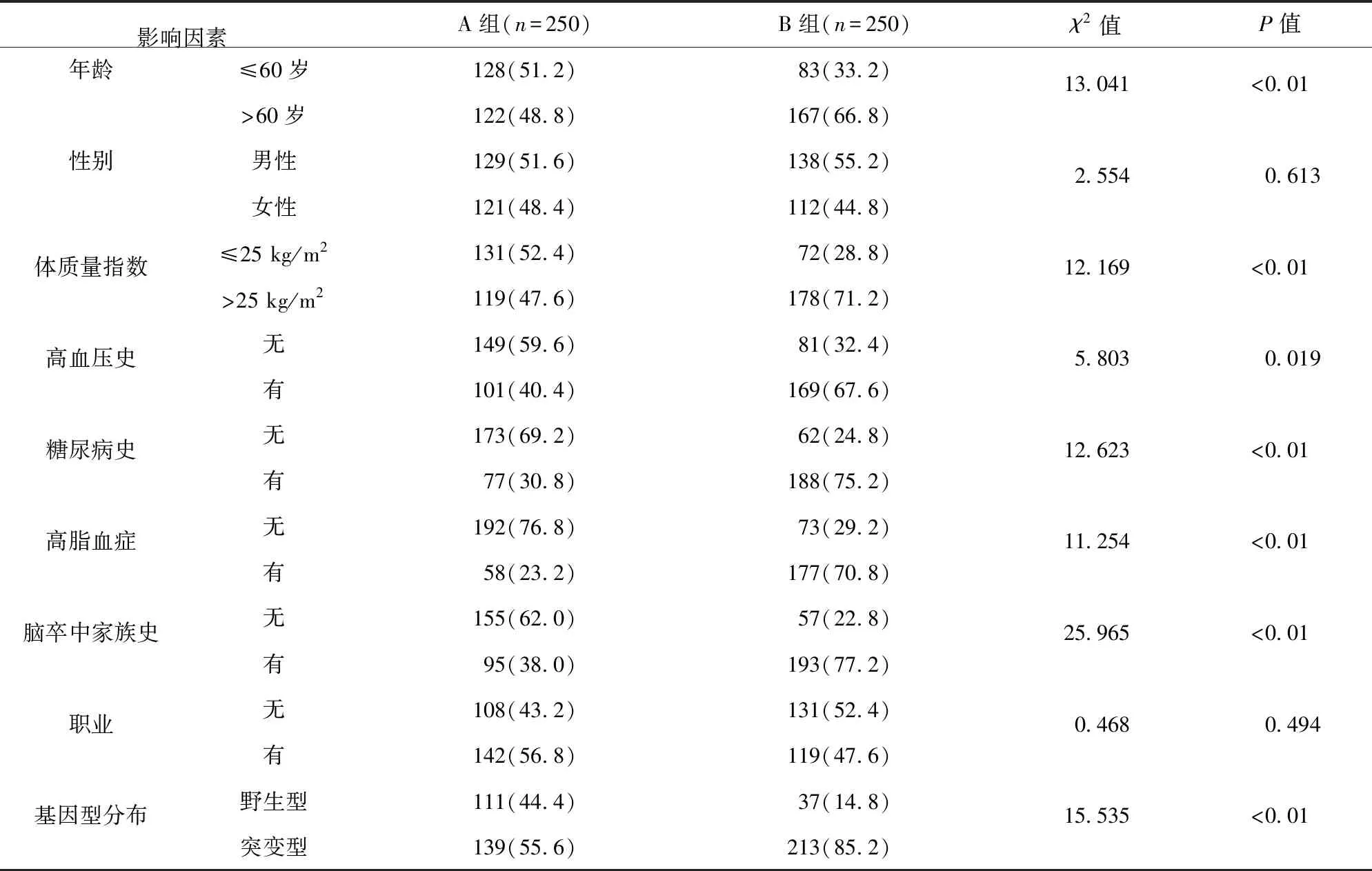
表1 單因素分析結果/例(百分率/%)
2.2 多因素Logistic回歸分析結果 以年齡、體質量指數、高血壓史、糖尿病史、高脂血癥、腦卒中家族史、基因型分布為自變量,以是否有缺血性腦卒中為因變量,進行多因素Logistic回歸分析。高血壓、高脂血癥、腦卒中家族史及基因型分布是缺血性腦卒中的獨立危險因素(P<0.05)。見表2。
2.3 Hardy-Weinberg遺傳平衡檢驗CDKN2B-AS1基因的10個SNP位點(包括rs10116277、rs10738607、rs564398、rs10757269、rs496892、rs4977574、rs1537375、rs2184061、rs7044859和rs2383207)均有3個基因型(GG、GA、AA;AA為野生型,GA為雜合突變型,GG為純合突變型)。兩組上述位點各基因型的期望值與觀測值均符合Hardy-Weinberg平衡定律(P>0.05)。
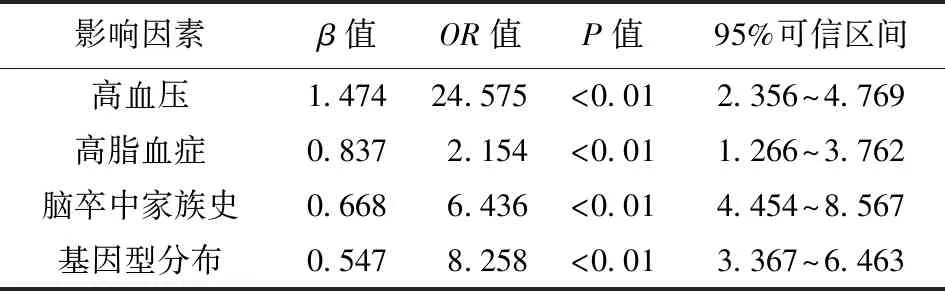
表2 多因素Logistic回歸分析結果
2.4CDKN2B-AS1基因多態性與缺血性腦卒中的相關性 兩組CDKN2B-AS1基因rs10116277、rs10738607、rs564398、rs10757269、rs496892、rs4977574、rs1537375、rs2184061和rs2383207位點基因型分布比較,差異均無統計學意義(P>0.05);而CDKN2B-AS1基因rs7044859位點多態性與缺血性腦卒中具有相關性(P<0.05),其共顯性模型(GG/AA)、顯性模型(GG/GA+AA)與隱性模型(AA/GA+GG)的粗OR(ORc)分別為2.486(95%可信區間1.368~4.453)、1.873(95%可信區間1.179~2.975)、0.525(95%可信區間0.313~0.882)。
2.5CDKN2B-AS1基因多態性rs7044859位點突變頻率分析 兩組 rs7044859的GG、AA基因型分布頻率比較,差異均有統計學意義(P<0.05);兩組rs7044859的GA基因型分布頻率比較,差異無統計學意義(P>0.05);B組等位基因G頻率為89.2%(223/250),明顯高于A組的68.4%(171/250),差異有統計學意義(P<0.05)。見表3。
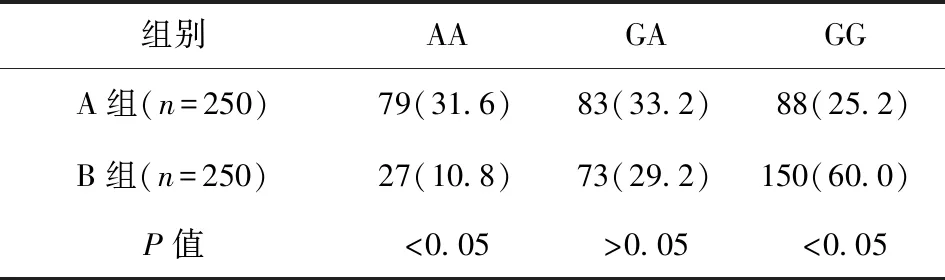
表3 兩組rs7044859位點基因型比較/例(百分率/%)
2.6 rs7044859位點基因型與缺血性腦卒中的相關性 以突變基因型為自變量,Logistic回歸分析結果顯示,rs7044859位點基因多態性與缺血性腦卒中獨立相關(P<0.05)。見表4。

表4 rs7044859位點基因型與缺血性腦卒中的相關性
2.7 各基因型缺血性腦卒中指標比較 AA型甘油三酯水平低于GG型、GA型,且GA型低于GG型,差異均有統計學意義(P<0.05)。AA型糖化血紅蛋白水平高于GG型,差異有統計學意義(P<0.05)。見表5。
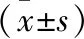
表5 各基因型缺血性腦卒中指標比較
3 討論
腦卒中是腦部血管突然破裂或腦部血管阻塞造成血液循環障礙引起的腦組織損傷,包括出血性腦卒中和缺血性腦卒中[7]。其中,缺血性腦卒中發病快速且兇險,預后不良,嚴重威脅患者生命健康[8]。缺血性腦卒中發病危險因素分為可干預因素與不可干預因素,可干預因素包括血糖、血脂異常、高血壓、冠心病、高同型半胱氨酸血癥、不良生活習慣與飲食習慣等[9];不可干預的因素包括年齡、性別、種族和遺傳因素[10]。對缺血性腦卒中進行早期預防,是降低患者發病率和病死率的根本途徑。
本研究結果顯示,高血壓、高脂血癥、腦卒中家族史及基因型分布是缺血性腦卒中的獨立危險因素(P<0.05)。高脂血癥患者脂質沉積于血管壁,會加速血管粥樣硬化斑塊的產生,使血管更為狹窄,最終造成血栓形成[11-12]。長期的高血壓會損害腦血管,導致血管發生玻璃樣變,誘發腦梗死[13-15]。此外,腦卒中家族史提示此疾病具有顯著性基因風險。
PCR-HRM作為一種突變掃描和基因分型技術,不受突變的位點及類型限制,靈敏度和特異性較高,無需特異性的探針,操作簡便、快速高效、成本低廉且全程閉管操作,是疾病遺傳學研究的理想方法。CDKN2B-AS1基因表達與心腦血管疾病的發病相關。在外周血的單核巨噬細胞中,CDKN2B-AS1基因的高表達能夠加速細胞增殖,并增加其粘附力,導致動脈粥樣硬化的風險增加。本研究篩選10個CDKN2B-AS1基因位點,發現rs7044859位點多態性與缺血性腦卒中具有相關性(P<0.05);兩組rs7044859的GG、AA基因型分布頻率比較,差異均有統計學意義(P<0.05);B組等位基因G頻率明顯高于A組,差異有統計學意義(P<0.05)。這提示,CDKN2B-AS1基因位點rs7044859多態性和缺血性腦卒中關系密切,攜帶等位基因G的人群更易患缺血性腦卒中。此外,rs7044859多態性與血糖水平關系密切,高空腹血糖會增加缺血性腦卒中的發病風險。有研究報道,糖代謝異常是缺血性腦卒中發病的獨立危險因素[16-17]。相關研究證實,在缺血性腦卒中的診治期間,糖化血紅蛋白、甘油三酯等生化指標可有效地預測、評估缺血性腦卒中嚴重程度和預后[18]。另有研究發現,攜帶等位基因G的患者更易出現血糖水平升高[19],CDKN2B-AS1基因rs4977574位點和血糖代謝相關,提示等位基因G可能會影響缺血性腦卒中的發病[20]。
綜上所述,高血壓、高脂血癥、腦卒中家族史及基因型突變型分布是缺血性腦卒中的危險因素,CDKN2B-AS1基因位點rs7044859基因型與缺血性腦卒中具有相關性,臨床可參考基因型分布特點積極預測并干預缺血性腦卒中。

