高強度聚焦超聲治療淺表組織的仿真研究
劉 力,劉 闖,朱巧苗,李雁浩,2*
(1.重慶醫科大學 生物醫學工程學院 超聲醫學工程國家重點實驗室,重慶 400016;2.超聲醫療國家工程研究中心,重慶 401121)
高強度聚焦超聲(High-Intensity Focused Ultrasound,HIFU)是近年來發展迅速的一種無創局部高溫治療技術,該技術將體外發射的多組超聲波聚焦于腫瘤細胞組織[1],聚焦超聲在生物組織中形成的凝固性壞死區域被定義為生物學焦域[2],聲能量的吸收不僅代表了能量的耗散,還會導致靶組織溫度升高和熱量的沉積,基于聚焦超聲在生物學焦域處能量疊加產生的生物學效應(由HIFU 誘導的組織消融的主要機制包括熱效應、空化效應和機械效應[3-4]),使得腫瘤組織溫度瞬間上升到65 ℃以上,從而導致蛋白質變性產生不可逆的細胞損傷,達到消融腫瘤細胞的目的。
目前,HIFU 技術在淺表組織的臨床治療領域已得到越來越廣泛的應用,其在治療外陰白色病變[5]、宮頸炎[6]和皮膚美容[7]等領域已經積累了豐富的臨床治療經驗。在淺表組織的臨床治療過程中,存在由于皮膚組織的物理特性會使皮膚表面沉積過多能量導致發生皮膚灼傷的情況,因此臨床醫師在術前選擇合適的治療參數和制定治療方案對確保治療過程的安全性和有效性十分重要。溫度作為在臨床治療過程中最直觀的可觀測物理參數使得在治療過程中獲取組織的溫度場特性極為重要[8],對臨床醫師選擇合適的治療參數具有重要意義,因此在制定術前治療計劃前對靶組織熱場分布和損傷面積的預測是不可或缺的一步。
數值仿真工具的廣泛應用使得在術前對治療過程的模擬和參數預測更加簡便,常詩卉等[9]構建了一種三維數值仿真模型探究在疊加雙焦點的情況下調控信號激勵時間差和幅值對HIFU 焦域溫度場分布和焦域形狀大小的影響。Meaney 等[10]構建了一種三維有限元模型計算得到聚焦超聲消融病變組織過程中的溫度場分布,結合熱計量算法預測病變組織形狀。張千等[11]采用數值仿真方法計算經顱骨治療的溫度場分布,并研究了治療參數(輸入聲強、輻照時間)及換能器與顱骨相對距離對顱內形成焦域體積的影響。
本文基于K-wave 仿真工具包構建了高頻聚焦超聲換能器三維仿真模型,模擬高頻聚焦超聲換能器輻照淺表組織的實際治療過程,分別利用Westervelt 方程和Pennes 生物傳熱方程求解聲場和溫度場分布。介質物理屬性在空間域中的分布并非為理想的均勻分布條件,因此比較了介質物理屬性在均勻和非均勻分布條件下求解的聲場和溫度場差異性,分析介質分布條件對聲場和溫度場的影響,此外采用3 種輻照模式探究了激勵時間和間歇時間對溫度場變化的影響,且預測了在換能器不同輻照模式下靶組織的凝固性壞死面積,為臨床醫師在制定術前方案時提供了可參考的治療參數。
1 數值仿真理論
1.1 Westervelt 方程
本研究采用Westervelt 方程計算基波和諧波聲場的分布,該方程考慮了聲波在傳播過程中的衰減、非線性效應、波散射和反射的影響[12],能夠較為精確地計算有限振幅聲波的非線性傳播[13]
式中:? 代表拉普拉斯算子;p 為聲壓;c 為聲波傳播介質的聲速;聲擴散率,α 代表聲波傳播介質的聲吸收系數,角頻率ω=2πf,f 代表聚焦超聲換能器的激勵信號頻率;β 為聲傳播介質的非線性系數;ρ 為聲傳播介質密度。超聲波聚焦在靶組織處時由于組織對聲波的粘滯吸收,部分聲能量會轉換為熱量成為聚焦超聲的加熱熱源,靶組織在單位時間內單位體積吸收的聚焦超聲加熱熱源可由聲強梯度空間公式Q=-?·I 計算得到[14],其中聲強,本文取n=4計算到最高四次諧波的聲場分布,此時Q 可表示為
1.2 Pennes 生物傳熱方程
物體一般的傳熱方程
其物理意義是熱傳遞物體內熱量積累的總效果等于該物體控制邊界熱流流入、流出的積分[15]。在該方程的基礎上考慮生物組織的血流灌注作用,在式(3)中加入血液灌注項得到Pennes 生物傳熱方程[16]
式中:ρ0為組織密度;C 為組織比熱;T 為組織溫度;λ為組織導熱系數;Wb為血液灌注率;Cb為血液比熱;Ta和Tv分別為動脈血溫度與靜脈血溫度;Q 為高頻聚焦超聲換能器產生的加熱熱源。
1.3 等效熱計量
用等效熱計量的方法可以預測靶組織凝固性壞死面積,計算公式如下[17]
式中:T 為輻照過程中t 時刻的組織溫度;R 為常數,取值隨著組織溫度的變化而變化,R=0.5(T≥43),R=0.25(T<43)。本文將等效熱計量大于240 min 的區域定義為治療結束后靶組織的凝固性壞死區域。
2 仿真模型構建與仿真參數
2.1 仿真模型
基于K-wave 仿真工具構建中心開孔的聚焦超聲換能器三維仿真模型,如圖1 所示。仿真模型由換能器、脫氣水和兩層淺表組織組成,模擬聚焦超聲換能器在脫氣水環境下發射超聲波經過皮膚到達脂肪組織的過程,其中換能器焦距F 為9.5 mm,換能器外孔徑a 和中心開孔內徑b 分別為12.2 mm 及5.6 mm,換能器陣元表面距離組織的距離c 為3 mm,皮膚厚度d 為2 mm,脂肪厚度e 為6.8 mm,組織寬度g 為14.1 mm。
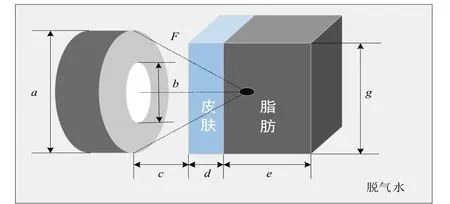
圖1 仿真模型示意圖
2.2 仿真參數
仿真模型計算中使用的介質屬性參數見表1,基波與諧波對應不同介質的聲吸收常數見表2。

表1 介質屬性參數
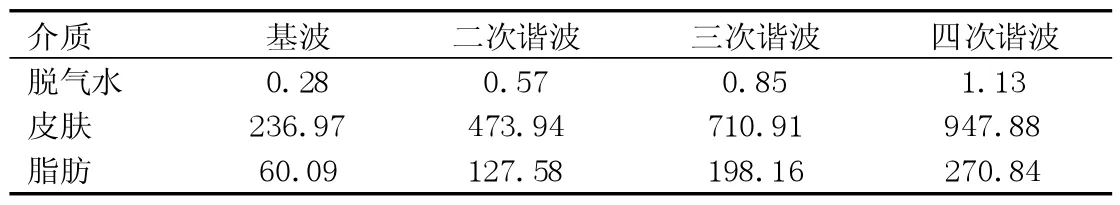
表2 介質聲吸收常數Np·m-1
3 仿真結果
在仿真計算中,選擇頻率為11.2 MHz 的正弦波作為換能器的激勵信號,以換能器陣元幅值為0.1 MPa的表面初始壓力表征換能器輻照組織時的輸出能量大小,設置換能器以不同輻照模式(T1:2s-1s-5c,T2:2s-2s-5c,T3:3s-1s-5c,激勵時間-間歇時間-治療回合)輸出信號,分析在不同仿真條件下換能器輻照域內的聲場和溫度場分布特性,計算靶組織聲軸面方向凝固性壞死面積。
3.1 聲場計算結果
由于換能器激發的聲波聚焦在組織處會使得焦域處聲壓的幅值變得較高,導致聲波的傳播過程不再是線性的,會在聲傳播過程中產生高次諧波,而高次諧波對計算溫度場產生的影響是不可忽略的,因此在計算聲場分布時需要考慮聲波傳播過程的非線性效應[18]。如圖2 和圖3 所示,計算了介質物理屬性在均勻和非均勻分布條件下沿換能器輻照域聲軸面方向基波及諧波聲場的分布,圖4 為2種介質分布條件下沿換能器聲軸線方向的聲壓幅值分布。

圖2 介質均勻分布條件下沿聲軸面方向聲場計算結果

圖3 介質非均勻分布條件下沿聲軸面方向聲場計算結果
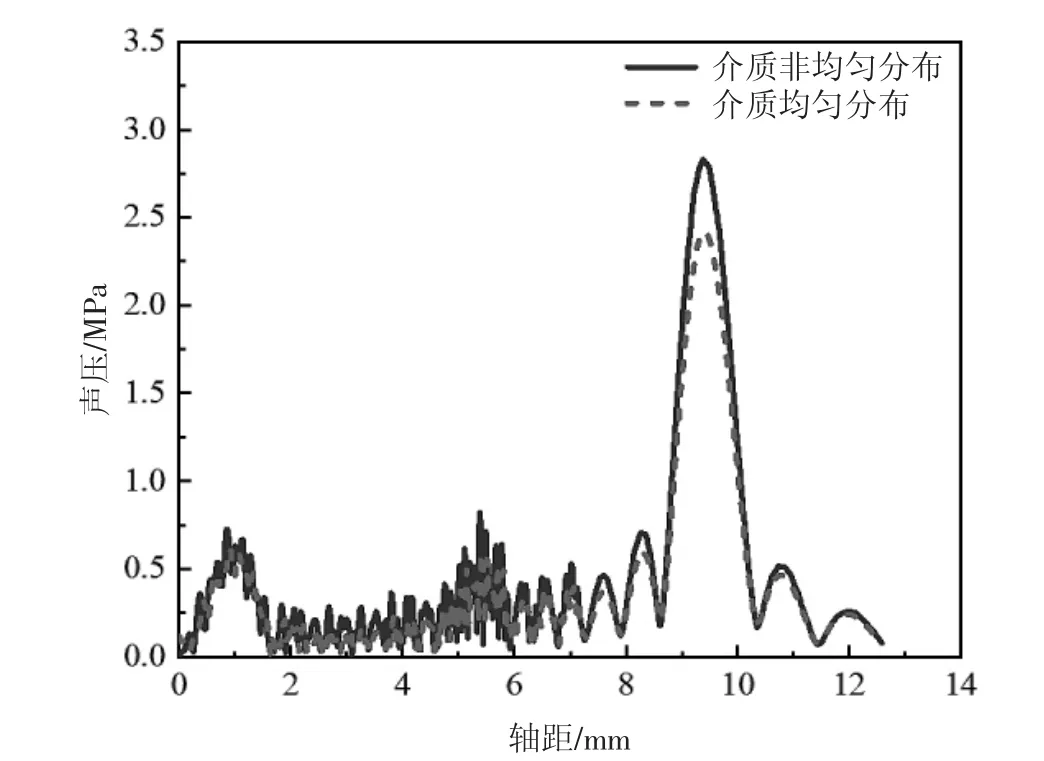
圖4 2 種介質分布條件下沿換能器聲軸線方向的聲壓幅值分布
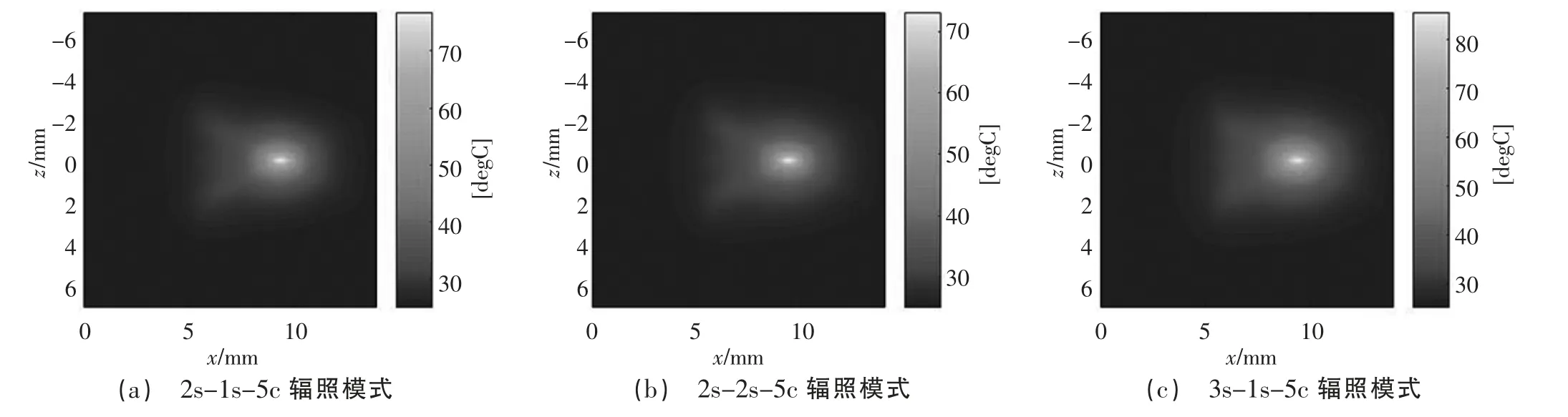
圖5 介質均勻分布條件下不同輻照模式治療結束時刻溫度場分布
如圖2 和圖3 所示,換能器激勵信號產生的聲能量聚焦在焦域處產生的非線性效應會導致諧波的產生,從而會影響溫度場的計算結果。基波同高次諧波相比,在焦點處的聲壓幅值最大,因此基波沉積的聲能量作為高頻聚焦超聲的加熱熱源主要輸入項,此外二次諧波和三次諧波對溫度場的溫度計算也需考慮,四次諧波聲壓幅值已相對較小,因此在計算聲場時考慮到計算域的空間采樣率和時間步長大小選擇最高計算到四次諧波。
圖4 分析了在不同介質分布條件下沿換能器聲軸線方向的聲壓幅值分布情況,在聲軸線方向上介質非均勻分布條件下的聲壓幅值普遍高于均勻分布,且在換能器幾何焦點處最為明顯。聲能量主要分布集中在換能器輻照域的幾何焦點處,此外在換能器陣元及皮膚組織界面處有一部分聲能量被反射和吸收導致聲壓幅值較高,因此在構建仿真模型時應考慮實際治療環境中組織的幾何特性和物理特性,提高仿真模型的精確性,避免在臨床治療過程中由于皮膚組織的粘滯吸收導致聲能量轉換為熱能引起皮膚灼傷。
3.2 溫度場計算結果
以Westervelt 方程計算得到的換能器幾何焦點處的時變聲壓作為輸入項帶入式(2)可得到加熱熱源Q,利用Pennes 生物傳熱方程計算溫度場的分布。圖5 至圖8 為2 種介質分布條件在換能器不同輻照模式下的溫度場計算結果。圖9 和圖10 為在溫度場的計算結果基礎上得到的輻照域內靶組織凝固性壞死面積。
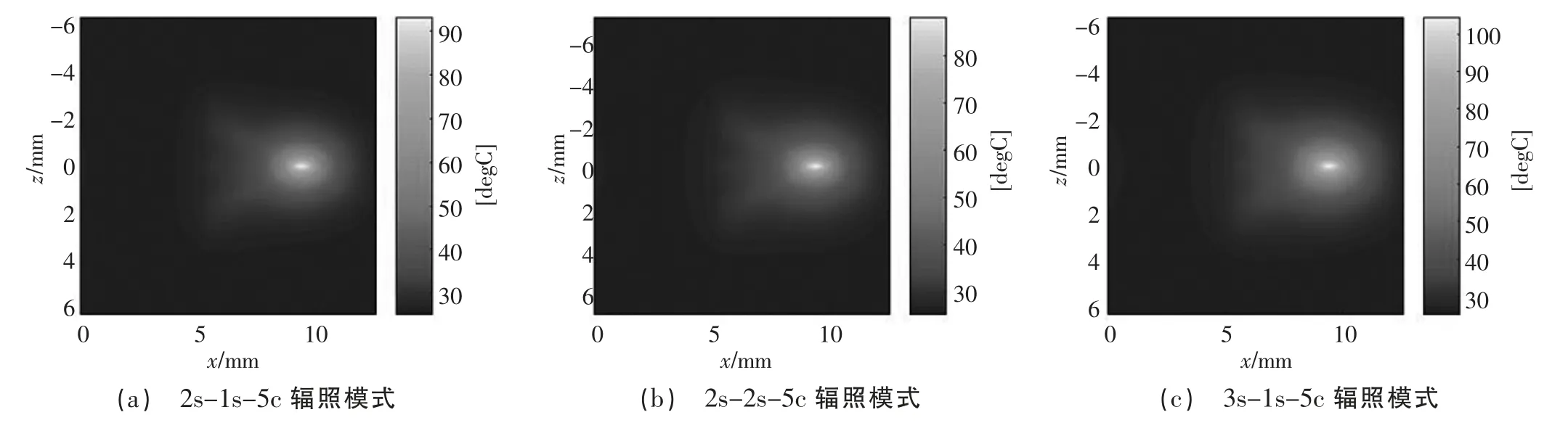
圖6 介質非均勻分布條件下不同輻照模式治療結束時刻溫度場分布
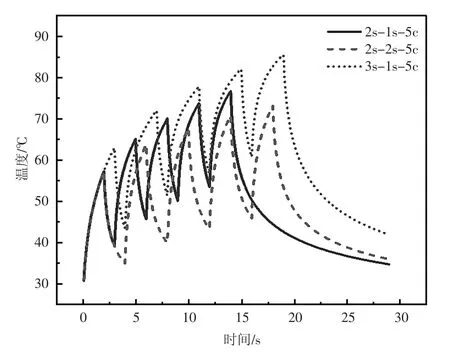
圖7 介質均勻分布條件下不同輻照模式焦點處的溫度變化曲線
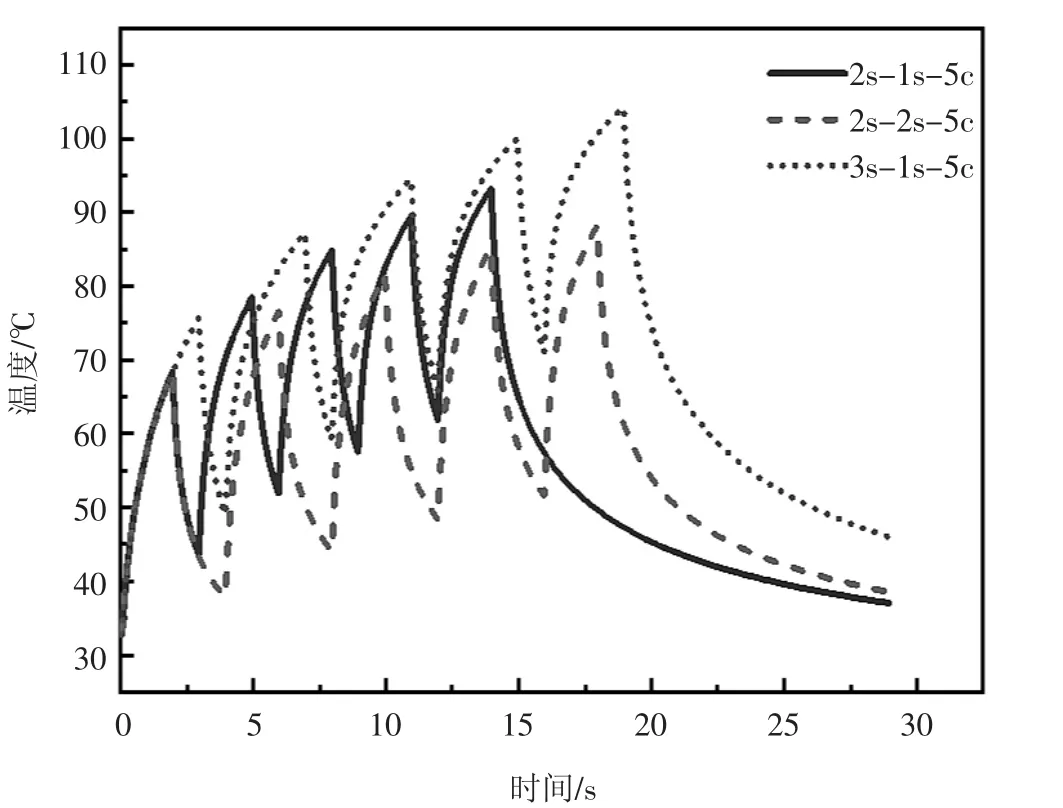
圖8 介質非均勻分布條件下不同輻照模式焦點處的溫度變化曲線
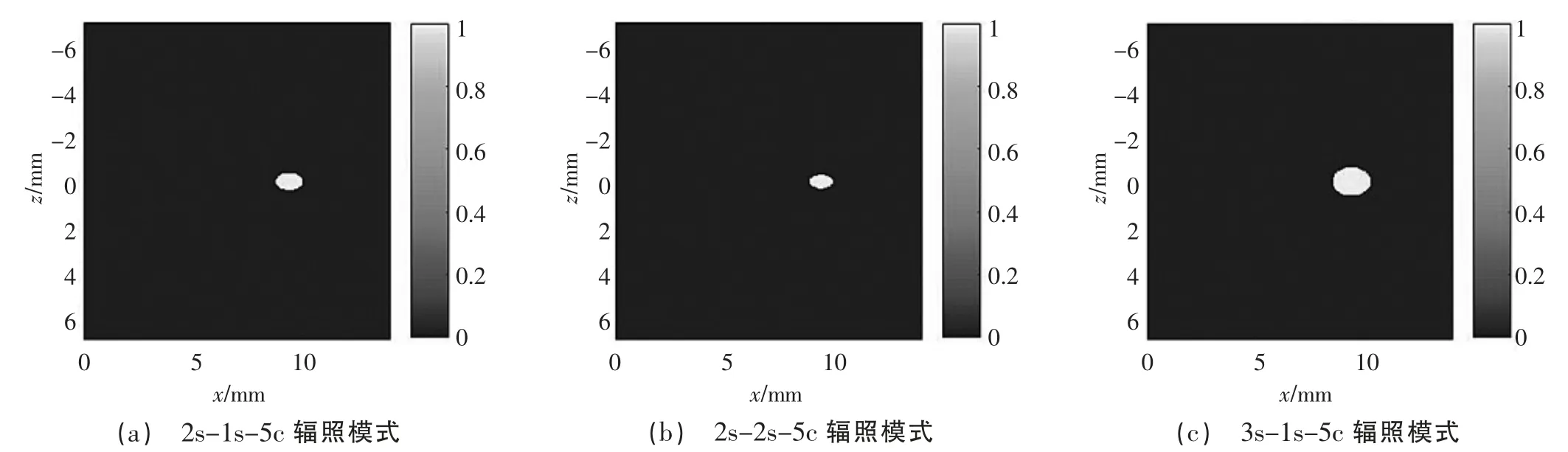
圖9 介質均勻分布條件下不同輻照模式形成的凝固性壞死區域

圖10 介質非均勻分布條件下不同輻照模式形成的凝固性壞死區域
如圖5 及圖6 所示,熱沉積能量主要集中于換能器焦點附近,溫升最明顯區域與圖2、圖3 中聲壓幅值大小的分布情況相對應。由圖7 和圖8 可知,隨著激勵時間的增加,溫度上升幅度相對較高,可見激勵時間和間歇時間的變化對溫度場有較大影響。因此在臨床治療過程中可根據所需消融的病變組織大小選擇合適的治療參數,對所需治療體積較大的病變組織可采用稍長的激勵時間消融大部分所需治療區域,再結合較長的間歇時間治療模式消除小部分未消融病變組織區域,避免由于在組織中沉積過多的熱量損傷周圍健康組織。如圖9 及圖10 所示,計算了在整個治療過程結束后由于熱量沉積導致組織溫升后產生的凝固性壞死區域,在T1、T2、T3輻照模式下,介質在均勻和非均勻分布條件下的靶組織凝固性壞死面積分別為0.759 mm2和1.578 mm2、0.513 mm2和1.145 mm2、1.169 mm2和3.179 mm2,可見即使在相同仿真條件下,介質分布條件的改變對仿真模型預測凝固性壞死面積有較大的影響,因此在構建仿真模型時應充分考慮治療過程中的組織差異性,提高仿真模型對模擬實際治療過程的精確性和有效性。
4 結論
本文基于K-wave 仿真工具包構建了聚焦超聲換能器輻照淺表組織的三維仿真模型,仿真模型考慮了聲傳播過程中的非線性效應,研究介質物理屬性均勻和非均勻的分布特性對聲場和溫度場的影響,采用有限元法結合Westervelt 方程求解換能器輻照域內靶組織的聲場,得到了換能器輻照區域中聲軸面方向基波同諧波聲場的分布及沿聲軸線方向的聲壓幅值分布。基于所求得的聲場分布結果,通過Pennes 生物傳熱方程求解溫度場,比較了3 種不同輻照模式對溫度場變化的影響,并在此基礎上預測了換能器輻照域中的靶組織凝固性壞死面積。結果表明,相對于非均勻分布,介質在均勻分布狀態下聚焦區域的聲壓幅值及溫升幅度都較小,從而導致在2 種不同介質分布特性下預測的凝固性壞死面積也存在較大差異。此外,仿真模型對換能器激勵時間和間歇時間敏感性較高,在較短時間內可使組織上升到所需的治療溫度,選擇合適的輻照模式可更好地控制組織凝固性壞死面積。本文建立的仿真模型對聲傳播過程和治療過程中溫度場的變化進行了研究,為臨床醫師制定術前治療計劃和選擇合適的治療參數提供了參考。

