基于主成分分析和相關性檢驗的多通道胎心率提取
鞠文博, 袁 林, 李 慶, 楊 波
(1.成都信息工程大學電子工程學院/物理場生物效應及儀器四川省高校重點實驗室,四川 成都 610225;2.成都信息工程大學計算機學院,四川 成都 610225)
0 引言
胎心監護是正確評估胎兒宮內狀態的重要檢測手段,對及時診斷胎心失常、降低圍產兒死亡率有極其重要的意義[1]。20 世紀中葉,臨床使用胎兒心電圖(fetal electrocardiogram,FECG)觀察胎兒心臟信息。測量FECG 的最準確方法是將頭皮電極直接置于孕婦體內進行胎兒心電圖監測,得到的信號較為純凈,但這僅適用在分娩中監測,不能反復使用[2-4]。并且侵入式的監測會導致未確診的胎兒缺氧,因此,無害的、非侵入式的監護方法顯得尤為重要。腹部心電圖技術直接將母體腹部電信號作為測量信號,與傳統的胎心監護手段相比,這種方法操作簡單,可以在孕后期使用,孕婦主觀上更容易接收,能更好保護孕婦及胎兒。
非侵入式測量操作更加簡便,但會受到其他生理信號和噪聲的干擾,如:母體心電(maternal electrocardiogram,MECG)、基線漂移、肌電干擾和50Hz 工頻干擾及其諧波干擾等。非侵入式方法檢測得到母體心電信號幅值一般為0.5 ~2 mV,胎兒心電信號幅值約為10 ~50 μV,MECG 幅值遠大于FECG 且頻譜上也存在重疊,傳統的濾波方法難以去除[5-6],因此在臨床研究中去除母體心電干擾是重要也是必要的一步。為解決無創提取胎兒心電這一難題,人們相繼提出了自適應濾波器;線性分解,如小波分解[7]、奇異值分解[8]、盲或半盲源分離[9];非線性分解如子空間分離[10]等方法。其中盲源分離(blind source separation,BSS)引申出獨立成分分析的快速不動點(FastICA)和特征矩陣的聯合近似對角化(JADE)兩種算法,JADE 在準確性方面優于FastICA,但在計算時間方面卻不盡人意;而FastICA 可以通過許多微調步驟得到與JADE 相當的結果且受輸入信號質量的影響較低[11],更加符合臨床實驗場景。兩種方法的共性均是首先從AECG 信號中移除MECG 和增強FECG,再從剩余分量中提取FECG[12],而肌電干擾噪聲會降低算法性能。
本文提出一種基于主成分分析(principal component analysis,PCA)和相關性檢驗多通道提取胎心率算法。首先通過樣本熵對多通道原始信號進行質量評估,去除質量較差的通道信號;然后利用PCA 從評估后的混合信號中提取主成分得到最優AECG;其次,Pan-Tompkins 初步定位R 峰位置,并通過極性檢測消除因波形倒置而出現的誤檢與漏檢,對母體R 峰位置進行校正,利用相干平均法對母體R 峰位置序列進行重構,構造長度為兩個R-R 間期的梯形窗,使之能包括一個完整的QRS 波群,對質量評估后滿足條件的每路AECG 進行加窗處理,重采樣至長度與重構后的母體QRS 波群相同,并在規定閾值范圍內進行序列微調,以實現與MECG 最相關;最后,將AECG 與MECG相減得到的殘差即為FECG,檢測胎兒QRS 波群進而計算得到胎兒心率,通過分析相關性能指標結果,本方法適用于多通道腹部信號胎心電提取。
1 方法
1.1 數據集
數據來自于PhysioNet 提供的開源數據庫Challenge 2013 Traning Set A。包括75 組胎兒心電圖記錄,每條記錄包含4 路無創孕婦腹部電信號,均以每秒1000 樣本點采樣,并對每個胎兒的QRS 波群進行參考標注。
1.2 方法描述
算法流程如圖1 所示。該方法由4 個主要步驟組成:(1)腹部心電信號預處理;(2)母體QRS 波群定位;(3)母體ECG 信號抵消;(4)胎兒QRS 波群檢測。其中步驟(1)數據預處理階段包括樣濾波與信號質量評估;步驟(2)和步驟(3)可以拆分為主成分分析提取母體ECG、母體R 峰檢測與校正以及母體ECG 信號重構;相關性檢驗校正胎兒QRS 波群在步驟(4)中進行。
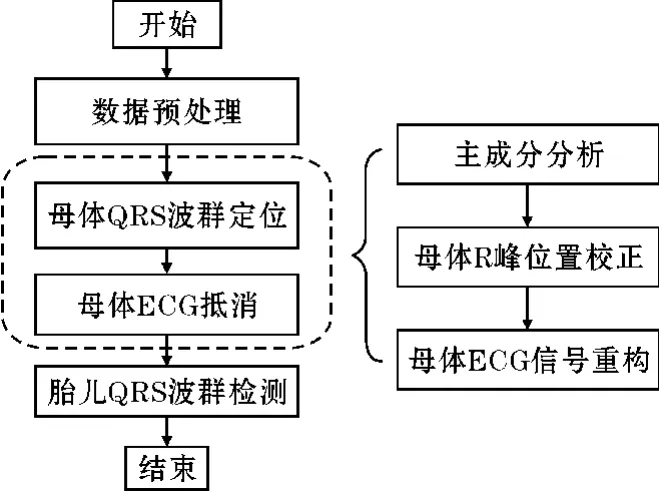
圖1 算法流程圖
2 預處理
2.1 去噪
使用50 Hz 陷波濾波器消除工頻干擾;基線漂移是由孕婦呼吸或運動引起的,使用巴特沃斯低通濾波器去除5 Hz以下的基線漂移干擾以及母體心電信號中的P、T波[13],實驗證明去除P 波和T 波并不影響R 峰的檢測;肌電屬于高頻干擾,使用小波去噪去除信號中的高頻噪聲[14]。腹部心電信號預處理前后對比如圖2 所示。
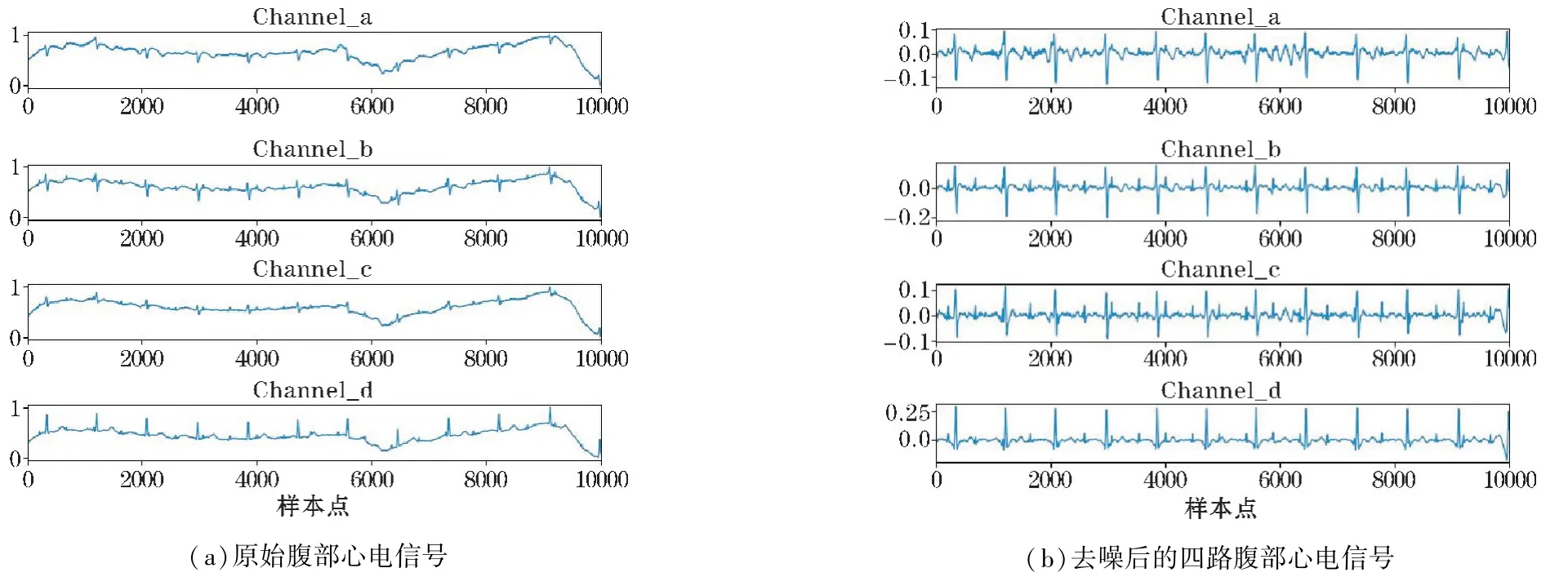
圖2 腹部心電預處理前后對比圖
2.2 信號質量評估
信噪比(SNR)通常是作為評估信號質量好壞的指標之一,狹義上定義為輸出信號的功率與同時輸入的噪聲功率之比。但檢測信號為胎兒心電信號、母體心電信號與其他噪聲的混合,且FECG 與MECG 頻譜上存在重疊,因此使用信噪比無法準確判斷各個通道信號質量的好壞。
近似熵(approximate entropy,ApEn)與樣本熵(sample entropy,SampEn)是通過度量信號中產生新模式的概率大小來衡量時間序列復雜性[15],新模式產生的概率越大,序列的復雜性越高。熵值結果越低,序列的自我相似性就越低,信號就越簡單;相反,熵值結果越高,信號就越復雜。
定義一個由N個數據組成的等樣時間序列{x(n)}=x(1),x(2),…,x(n), 算法相關參數m,r,其中,m為整數,表示重構的維度;r為實數,表示“相似度”的度量值。樣本熵的計算步驟如下:
(1)重構m維向量Xm(1),…Xm(N-m+1),其中Xm(i)=[x(i),x(i+1),…x(i+m-1)]T,1≤i≤N-m+1
(2)統計滿足Xm(i)與Xm(j)之間的距離d小于等于r的j(1≤j≤N-m,j≠i)的數目,并記作Bi,則對于1≤i≤N-m定義:
其中,距離d由Xm(i)與Xm(j)對應元素中最大的差值的絕對值決定,即:
(3)求(r)對于所有i值的平均值,記為Bm(r),即
(4)增加維度到(m+1)維,重復步驟(2)將滿足條件的個數記為Ai,則Ai(r)定義為
(5)定義Am(r)為
由于在實際計算應用過程中,N不可能為∞,因此當N取有限值時,樣本熵估計為
式中,嵌入維數m一般取1 或2;相似度r的選擇在很大程度上取決于實際應用場景,通常選擇r=0.1·std ~0.25·std,其中std 表示原時間序列的標準差。在本次實驗中取m=2,r=0.25·std。
設定一個恒定的樣本熵閾值為1.5,每個通道的樣本熵值與該閾值相比,將值小于1.5認定為質量良好的信號,用于后續分析;舍棄熵值大于1.5的通道信號,如果認定的質量良好的信號數量少于2 個,則保留熵值最小的2 個通道信號以供進一步分析[16]。a19 樣本中4 路信號的熵值如表1 所示,4 路AECG 分別在10 s內的樣本熵值如圖3 所示。

表1 4 路信號樣本熵值
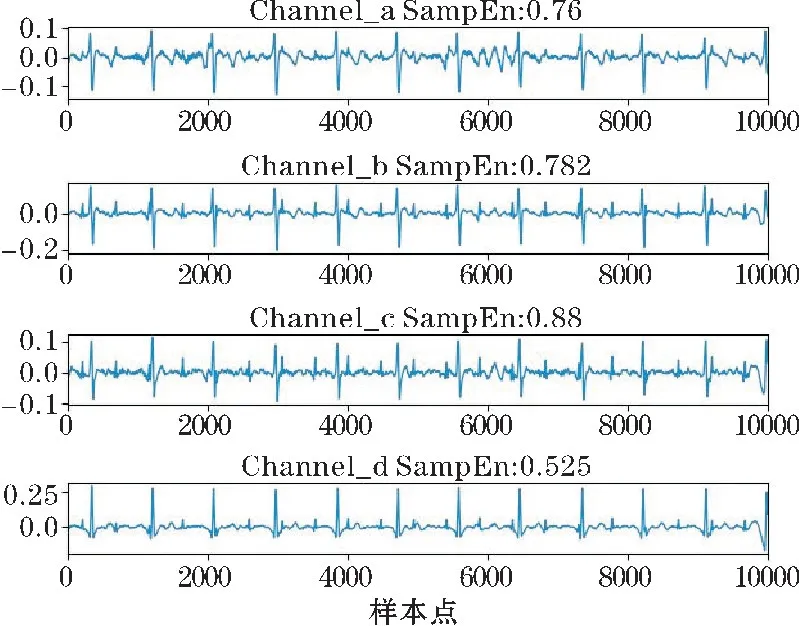
圖3 4 路AECG 分別在10 s 內的樣本熵值
3 MECG 提取與重構
3.1 主成分分析
經過信號質量評估篩選后的AECG 全部用于PCA,自動保留了3 個成分,其各分量的方差貢獻率分別為51.02%、47.15%和1.61%,這意味著幾乎保留了原始信號的所有信息,且第一分量作為主分量包含信息最大。母體QRS 波群與胎兒QRS 波群在不同分量中的表現如圖4 所示(紅色框內為母體QRS 波群,黃色框內為胎兒QRS 波群)。在不失真的情況下,選擇第一分量作為最優參考信號。
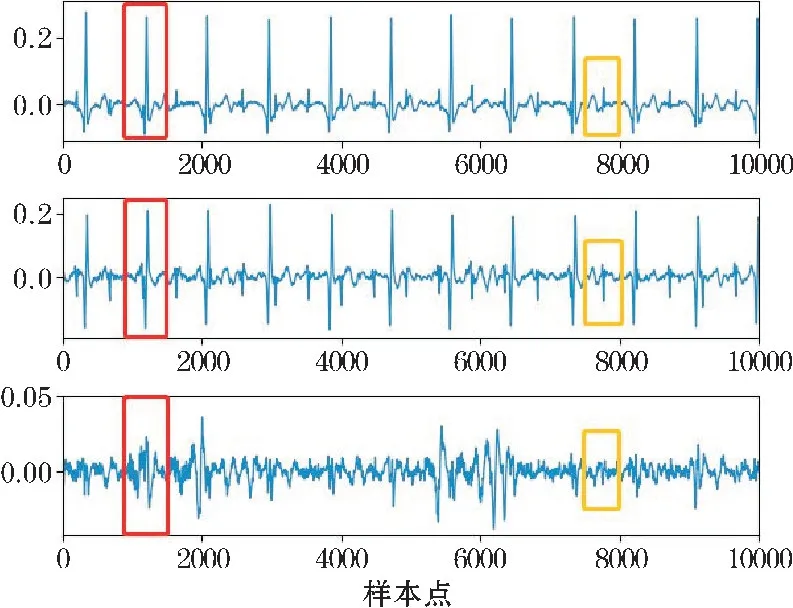
圖4 不同分量下的MQRS 與FQRS
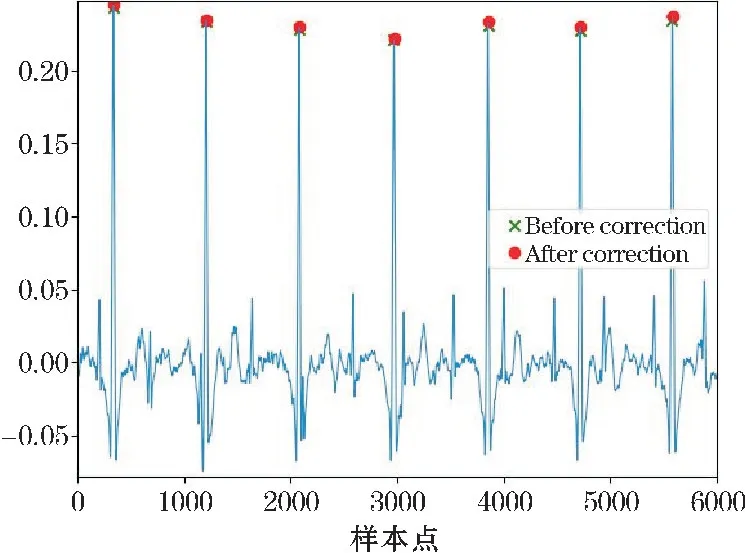
圖5 校正前后R 峰位置對比
3.2 R 峰位置定位與校正
母體R 峰的檢測方法主要用Pan-Tompkins 算法[17],相比于Q 波、P 波,R 波所在位置斜率最大。該方法首先對心電信號進行差分求導,然后進行平方,銳化信號。定義差分平方后的心電序列為X、長度為N、采樣率fs,閾值thre 的計算方法為將心電按采樣頻率分為等長序列X(1),X(2),…,X(k),計算每個序列的均值記為m(1),m(2),…,m(k),取最小均值的0.3倍作為閾值,即:
thre=min{m(1),m(2),…,m(k)}×0.3,k=fs
在每一個長度為i的序列范圍內,將大于閾值點中的最大值作為R 波的初步參考位置,然后擬合相同長度的拋物線用于增強QRS 波,便于尋找在以R 峰為中心220 ms范圍內的最大值作為QRS 波群R 峰位置[18]。
3.3 MECG 重構
基于得到的母體QRS 波群,使用相干平均法構建每個MECG 模板[19]。首先,2 個連續R 峰間期構成完整的R-R 間期,使之能夠包括一個心跳過程所產生的所有事件;然后,將每個R-R 間期重采樣至恒定的1K采樣率,以提供與AECG 平均處理;最后,將MECG 模板重新拉伸到每個周期的實際長度,再將它們逐拍連接,獲得重構的MECG 信號。
4 胎兒心率檢測
4.1 相關性檢驗校正
在MECG 重構之后,基于相關性檢驗來實現預處理后的AECG 和重構的MECG 信號之間的最佳匹配,實現過程如圖6 所示。首先,將重構后的MECG 信號和預處理后的AECG 信號都使用原始采樣頻率的10倍進行重采樣,即10 KHz上采樣;其次,構建一個幅值為1,時間長度為440 ms的矩形窗,使其能包括一個完整的母體QRS 波段;然后,基于相關性檢驗執行窗內匹配操作,通過尋找最大相關系數找到MECG 和AECG 的最佳匹配位置。
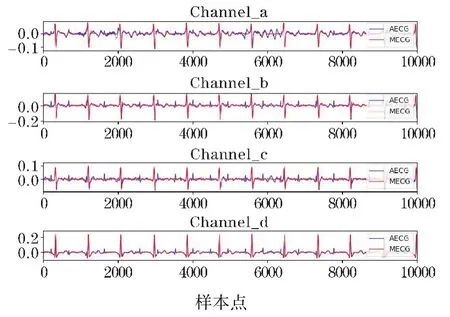
圖6 MECG 匹配抵消實現過程
匹配操作首先設定一個微調閾值,步長為10 個樣本點,然后將MECG 信號向左或向右移動,計算MECG和AECG 的相關系數,以達到最大相關度,從而確保從AECG 中減去重構的母體心電模板后,可以獲得更清晰的胎兒心電信號。圖7 顯示了對于來自記錄a19 的2 個QRS 波段的相關性校正過程,并給出沒有通過校正的例子。
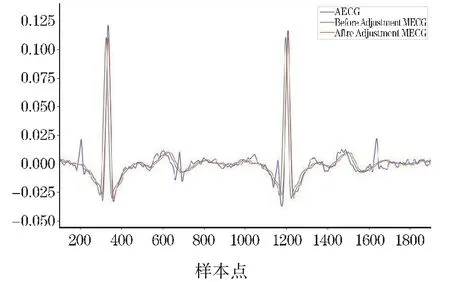
圖7 2 個QRS 波段相關性校正前后MECG 與原始AECG 信號對比
4.2 FECG 檢測
從AECG 信號中抵消MECG 得到的殘差中,MECG的殘留成分已經很少,因此將殘差信號作為最終胎兒心電結果。由于胎兒心跳周期為母體的1.5 ~2 倍,相比于檢測母體QRS 波群使用的220 ms,胎兒QRS 波群恒定時間范圍修改為150 ms[16],再用Pan-Tompkins 算法檢測校正胎兒QRS 波群,得到胎兒R 峰序列。
5 結果
提取出數據集中的fQRS 文件中的專家標注信息作為參考,與實驗結果得到的胎兒R 波位置計算的F1測量值與靈敏度Se 作為評估該算法精度的兩項指標,并分別列出校正前后F1和Se 的值,如表2 所示。F1測量值與Se 計算方法如下:
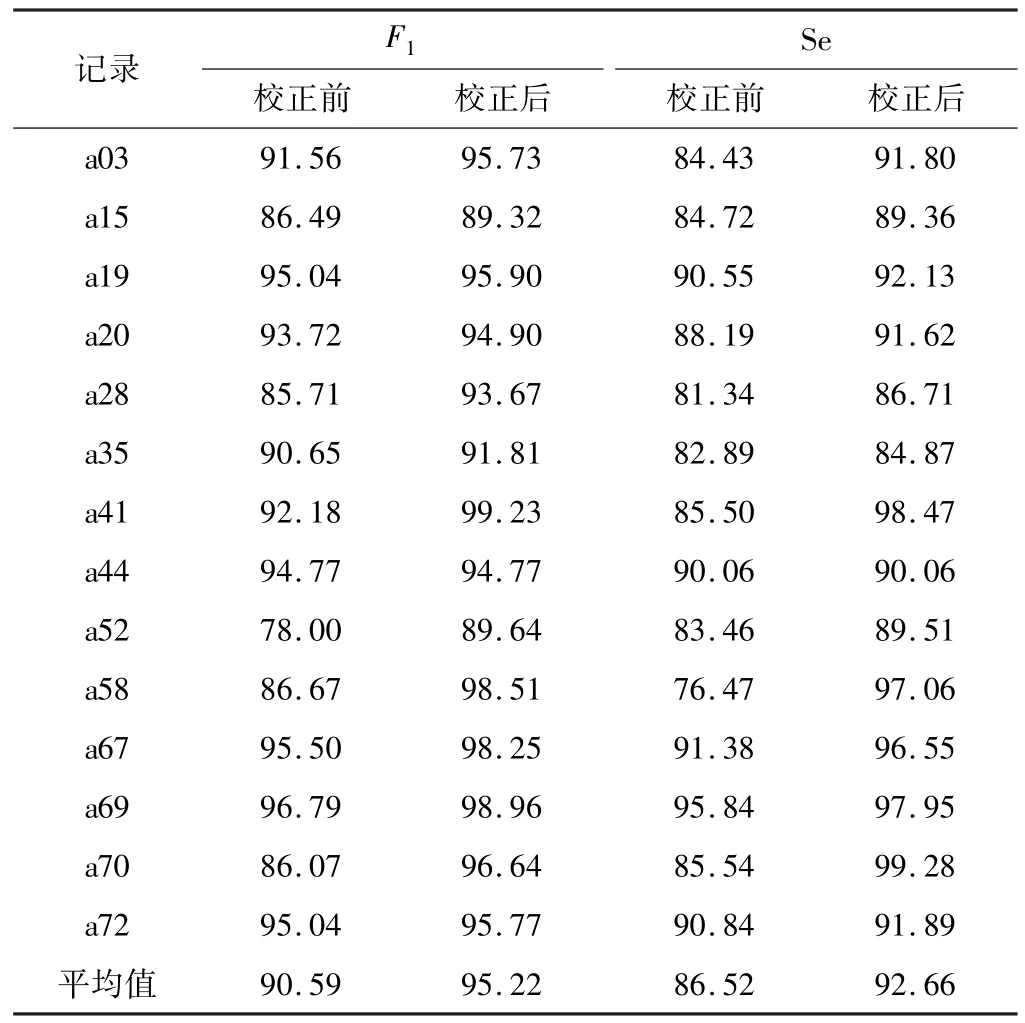
表2 基于數據庫Challenge 2013 Set A 相關性檢驗校正前后的各項指標結果對比 單位:%
其中,TP 是記錄標注的與實驗檢測相匹配的QRS 波群數量,FP 是假陽性(誤檢的QRS 波群)數量,FN 是假陰性(漏檢的QRS 波群)數量。考慮標注信息的誤差,實驗結果在50 ms范圍內均是認為與標注結果匹配[20]。
6 結束語
提出基于主成分分析和相關性檢驗的腹部胎心點提取方法。首先對4 路原始信號進行預處理,通過樣本熵值評估信號質量,符合條件的信號用于后續提取主成分;然后,將第一主成分作為最優參考信號,使用斜率法檢測其QRS 波群以及R 峰位置,為增加R 峰位置的準確性,對原始信號的導數進行平方處理,初步得到的R 峰位置索引,再在區間內尋找幅值最大的位置,即R 峰校正后的位置;其次,利用相干平均法重構每個MECG 模板,在以每個母體R 峰位置為中心220 ms內的矩形窗內進行相關性檢驗,通過尋找最大相關系數找到MECG 和AECG 的最佳匹配位置;最后,從預處理后的每路AECG 中減去各自的MECG 信號,達到去除MECG 干擾的目的,得到的殘差中包含了FECG 與少量噪聲混合,再用主成分分析提取較為純凈的FECG。
本文對胎兒心電的提取思想仍然是目前流行的模板相減法,優點是能夠以無監督的方式提供較好的檢測結果。該方法改善了使用獨立成分分析算法時肌電干擾噪聲對提取的信號質量影響較大的問題,并在此基礎上進行了相關性檢驗校正,極大消除了在模板抵消時由于時域不同步而出現的誤差,提高了胎兒心率檢測的準確性。

