促性腺激素釋放激素激動劑聯合滋陰疏肝方加減治療女童特發性中樞性性早熟的療效觀察
馬夢瑾,周川,李志潔*
鄭州大學第二附屬醫院,1 社區及預防保健科,2 新生兒科,鄭州 450000
性早熟是指女童在8 歲前、男童在9 歲前呈現出第二性征[1],按照發病機制和臨床表現可分為中樞性(促性腺激素釋放激素依賴性)性早熟和外周性(非促性腺激素釋放激素依賴性)性早熟,以往分別稱為真性性早熟和假性性早熟[2-3]。其中女童以特發性性早熟為多,占中樞性性早熟的80%~90%[4]。特發性中樞性性早熟(idiopathic central precocious puberty,ICPP)是一種內分泌紊亂性疾病,大多由下丘腦-垂體-性腺軸激素分泌過多導致功能亢進,進而使患兒過早出現第二性征發育,臨床常見身高、體重、骨骼生長超出正常指標,女性患兒出現乳房和陰毛的生長,甚至月經過早來潮。促性腺激素釋放激素激動劑(gonadotropin releasing hormone agonist,GnRH-a)可延緩過度發育,但會影響患兒糖脂代謝,且臨床療效不夠理想[5-6]。中醫藥理論認為,性早熟屬于肝腎病變,在病理上表現為腎陰陽失調、相火亢盛、腎水不足,造成陰虛火旺的現象[7]。滋陰疏肝方為本院自擬方,由六味地黃丸和逍遙散化裁而來,具有滋水涵木、疏肝解郁之效,可治肝木失其柔潤之體,相火萌動,子盜母氣而致的陰虛火旺。基于此,本研究探討了GnRH-a 聯合滋陰疏肝方加減治療女童ICPP 的臨床療效與安全性,現報道如下。
1 資料與方法
1.1 一般資料
選取某院2020年1月~2022年2月生長發育門診收治的106 例女性患兒為研究對象,采用隨機數字表法分為觀察組與對照組,每組53 例。對照組:年齡7~9 歲,平均年齡(8.02±0.83)歲;身高120.00~154.00cm,平均身高(140.36±3.12)cm;出現月經初潮者33 例;出現腋毛者20 例。觀察組:年齡7~9 歲,平均年齡(8.05±0.81)歲;身高120.00~154.00cm,平均身高(140.38±3.16)cm;出現月經初潮者34 例;出現腋毛者19 例。兩組一般資料比較均無統計學差異(P>0.05),具有可比性。本研究經醫學倫理委員會批準(倫理批號:2020-KY-012)。
診斷標準:①西醫診斷符合《女性性早熟的診治共識》(2018 版)[8]中關于女童ICPP 的診斷標準:8 歲之前出現第二性征發育,10 歲之前出現月經初潮;B 超檢查可見卵巢及子宮容積增大,出現多個卵泡,且直徑均超過4mm;骨齡超過實際年齡1年及以上;線性生長速度加快;GnRH 激發試驗顯示,促黃體生成素激發峰值>5.0U/L,促黃體生成素激發峰值/促卵泡生成素峰值>0.6。②中醫診斷符合《中醫兒科臨證指南·性早熟(修訂)》[9]中關于臨床表現為陰虛火旺兼肝郁化火的診斷標準,包括:月經提前來潮,乳房發育,陰唇發育,色素沉著,伴隨五心煩熱、潮熱、顴紅、盜汗、煩躁易怒,咽干口苦,小便短黃,大便干結,舌紅絳,少苔或無苔,脈細數。
納入標準:①年齡為7~9 歲者。②依從性良好者。③患兒家屬同意并簽署知情同意書。④性腺增大或女童在B 超下見卵巢容積>1ml 且可見多個直徑>4mm 的卵泡者。⑤血清性激素和促性腺激素達到青春期水平者。排除標準:①中樞器質性病變所致的性早熟者。②單側乳房發育和單側陰唇陰毛發育者。③假性性早熟和其他遺傳內分泌疾病所致性早熟者。④患有先天性心臟病等臟器疾病者。
1.2 治療方法
對照組采用GnRH-a 治療,給予注射用醋酸曲普瑞林(Ipsen Pharma Biotech,注冊證號H20140298,規格3.75mg)肌內注射,初始劑量為3.75mg/次,1 個月1 次;自第2 個月起按照0.05~0.1mg/kg 進行減量注射,4 周注射1次;治療4 個月后,根據患兒的身高和體重調整為0.06~0.08mg/kg,依舊間隔4 周注射1 次,維持身高生長速率>4cm/年,連續治療6 個月。
觀察組在對照組治療基礎上加用滋陰疏肝方加減,方劑組成:熟地黃15g、山茱萸10g、山藥10g、澤瀉10g、牡丹皮10g、茯苓5g、柴胡10g、當歸5g、白芍5g、白術5g、炙甘草5g。煎煮前加入1000ml 水浸泡30min,隨后煎煮濃縮至250ml,早晚分服,連續治療6 個月。
1.3 觀察指標
①性激素水平。治療前后抽取兩組患兒空腹靜脈血5ml,采用L400 型臺式低速自動平衡離心機(廣州葆科鍵醫療器械有限公司,r=10cm)以2500r/min 離心10min,取上層血清備用。采用酶聯免疫吸附法檢測黃體生成素(luteinizing hormone,LH)、促卵泡激素(follicle-stimulating hormone,FSH)、雌二醇(estradiol,E2)、胰島素樣生長因子-1(insulin-like growth factor-1,IGF-1)水平,相關檢測試劑盒由上海酶聯生物科技有限公司提供(批號:ml026275、ml048650、ml077368、ml037425)。②身體指標。分別在治療前后計算兩組的骨齡指數、預測成年身高及身高標準差分值。③子宮、卵巢容積及直徑>4mm 的卵泡數量。采用BLS-X8B 超診斷儀(徐州貝爾斯電子科技有限公司)檢測兩組治療前后的子宮、卵巢容積和卵泡直徑。④臨床療效。根據《24 個專業105個病種中醫診療方案》(第2 版)中的性早熟中醫診療方案(試行)[10]的療效標準進行判斷。其中,痊愈:患兒乳房縮小至青春期前期,陰道分泌物和陰道出血消失,月經消失,陰毛和腋毛停止生長,骨齡與身高相匹配,B 超檢查卵巢容積<1ml;好轉:乳房顯著縮小,陰道分泌物與出血消失,腋毛和陰毛生長緩慢,骨齡與實際年齡相匹配,B 超檢查卵巢容積為1~2ml;未愈:乳房未有明顯變化,陰道分泌物及出血依舊不變,腋毛和陰毛生長繼續,骨齡超過實際年齡1年及以上,B 超檢查卵巢容積>2ml。治療總有效率=(痊愈+好轉)例數/總例數×100%。⑤不良反應發生情況。觀察并記錄兩組惡心嘔吐、頭暈頭痛、腹瀉、肌肉疼痛等不良反應的發生情況。
1.4 統計學方法
采用SPSS20.0 進行統計分析。計量資料以±s 表示,兩組間比較采用獨立樣本t檢驗,多組間比較采用單因素方差分析;計數資料以n(%)表示,組間比較采用χ2檢驗。P<0.05 為具有統計學差異。
2 結果
2.1 性激素水平
治療前,兩組LH、E2、FSH、IGF-1、LH/FSH 水平比較均無統計學差異(P>0.05)。治療后,兩組LH、E2、FSH、IGF-1、LH/FSH 水平均降低,且觀察組低于對照組(P<0.05)(表1)。
表1 兩組性激素水平比較 n=53,±s

表1 兩組性激素水平比較 n=53,±s
LH:黃體生成素;E2:雌二醇;FSH:促卵泡激素;IGF-1:胰島素樣生長因子-1。a:與同組治療前比較,P<0.05,下同
組別LH(U/L)E2(pg/ml)FSH(mIU/ml)IGF-1(ng/ml)LH/FSH治療前 治療后治療前治療后 治療前 治療后 治療前 治療后 治療前 治療后觀察組10.81±0.11 2.03±0.02a 45.06±3.42 23.08±2.41a 3.89±0.41 1.83±0.28a 339.85±20.48 206.36±13.52 a 0.31±0.03 0.13±0.02 a對照組10.80±0.12 2.09±0.04a 45.11±3.43 29.48±2.48a 3.90±0.40 2.11±0.31a 340.89±20.03 219.08±14.09 a 0.30±0.04 0.24±0.03a t 值0.4479.7670.07513.4730.1274.8790.2644.7421.45622.21 P 值0.6560.0000.9400.0000.8990.0000.7920.0000.1480.000
2.2 身體指標
治療前,兩組骨齡指數、預測成年身高、身高標準差分值比較均無統計學差異(P>0.05)。治療后,兩組骨齡指數、身高標準差分值絕對值水平均降低,且觀察組低于對照組;而兩組預測成年身高均有所提高,且觀察組高于對照組(P<0.05)(表2)。
表2 兩組身體指標比較 n=53,±s
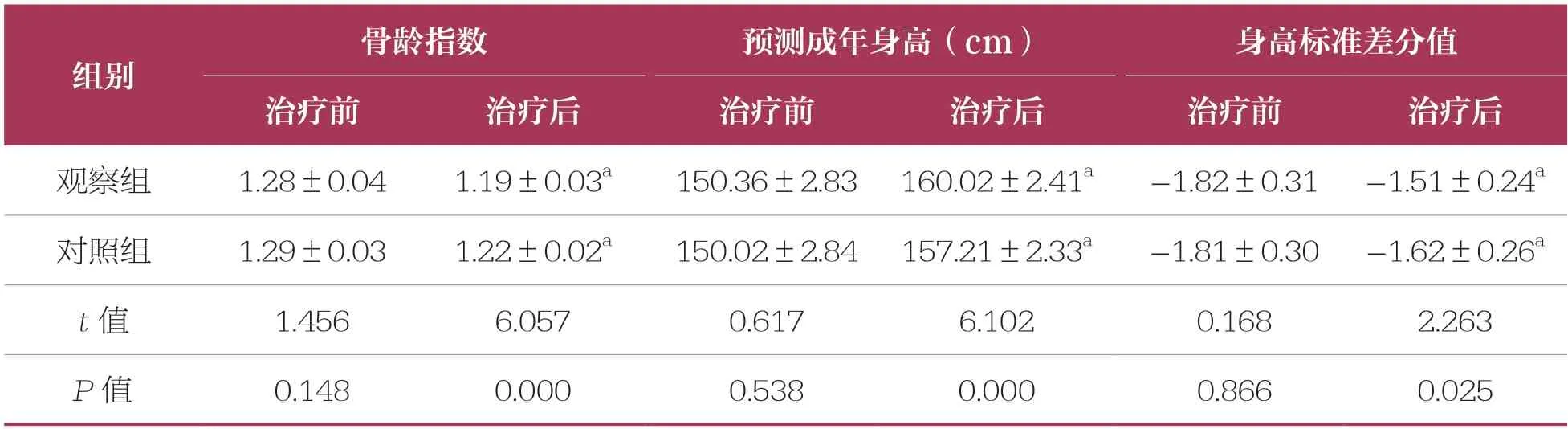
表2 兩組身體指標比較 n=53,±s
組別骨齡指數預測成年身高(cm)身高標準差分值治療前治療后治療前治療后治療前治療后觀察組1.28±0.041.19±0.03a150.36±2.83 160.02±2.41a-1.82±0.31 -1.51±0.24a對照組1.29±0.031.22±0.02a150.02±2.84 157.21±2.33a-1.81±0.30 -1.62±0.26a t 值1.4566.0570.6176.1020.1682.263 P 值0.1480.0000.5380.0000.8660.025
2.3 子宮、卵巢容積及直徑>4mm 的卵泡數量
治療前,兩組子宮、卵巢容積及直徑>4mm 的卵泡數量比較均無統計學差異(P>0.05)。治療后,兩組子宮、卵巢容積及直徑>4mm 的卵泡數量均降低,且觀察組低于對照組(P<0.05)(表3)。
表3 兩組子宮、卵巢容積及直徑>4mm 的卵泡數量比較 n=53,±s
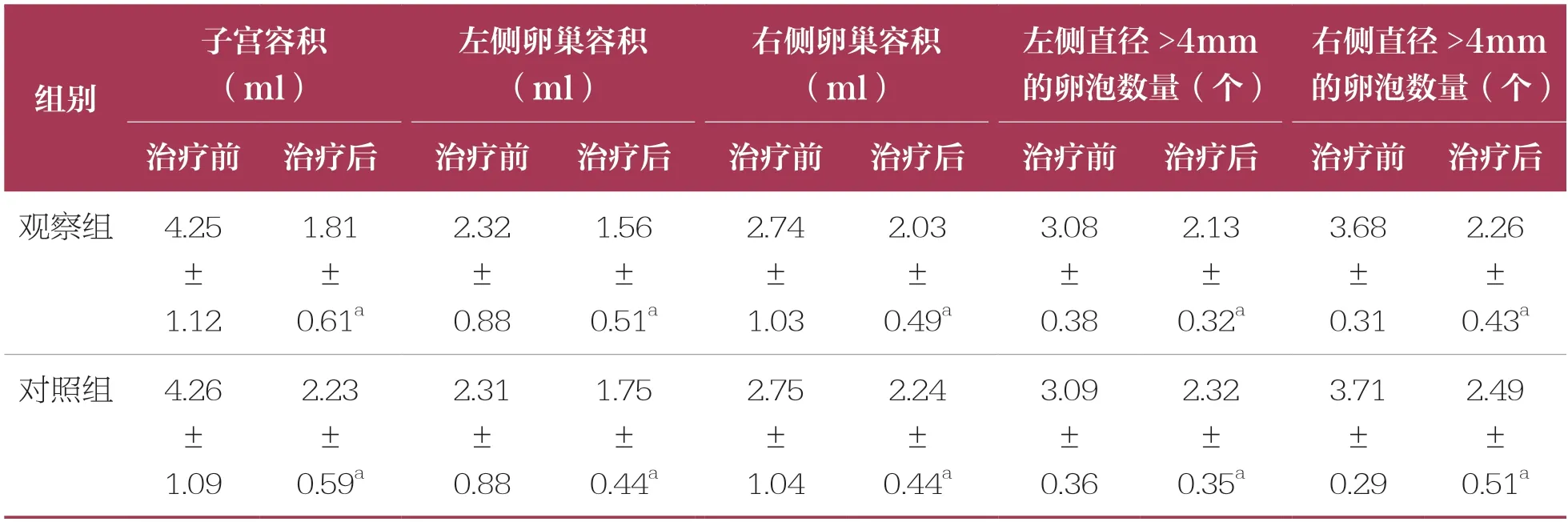
表3 兩組子宮、卵巢容積及直徑>4mm 的卵泡數量比較 n=53,±s
右側直徑>4mm的卵泡數量(個)治療前 治療后治療前 治療后治療前 治療后治療前 治療后治療前 治療后觀察組4.25±1.12組別子宮容積(ml)左側卵巢容積(ml)右側卵巢容積(ml)左側直徑>4mm的卵泡數量(個)1.81±0.61a 2.32±0.88 1.56±0.51a 2.74±1.03 2.03±0.49a 3.08±0.38 2.13±0.32a 3.68±0.31 2.26±0.43a對照組4.26±1.09 2.23±0.59a 2.31±0.88 1.75±0.44a 2.75±1.04 2.24±0.44a 3.09±0.36 2.32±0.35a 3.71±0.29 2.49±0.51a
續表
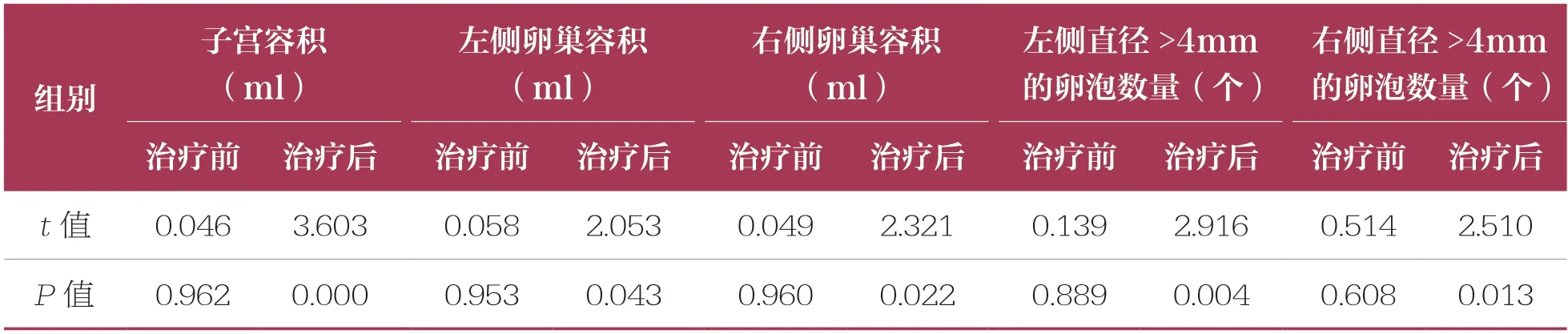
表3 兩組子宮、卵巢容積及直徑>4mm 的卵泡數量比較 n=53,±s
右側直徑>4mm的卵泡數量(個)治療前 治療后治療前 治療后治療前 治療后治療前 治療后治療前 治療后t 值0.046 3.603 0.058 2.053 0.049 2.321 0.139 2.916 0.514 2.510 P 值0.962 0.000 0.953 0.043 0.960 0.022 0.889 0.004 0.608 0.013組別子宮容積(ml)左側卵巢容積(ml)右側卵巢容積(ml)左側直徑>4mm的卵泡數量(個)
2.4 臨床療效
觀察組治療總有效率(96.23%)高于對照組(81.13%,χ2=6.014,P=0.014)(表4)。
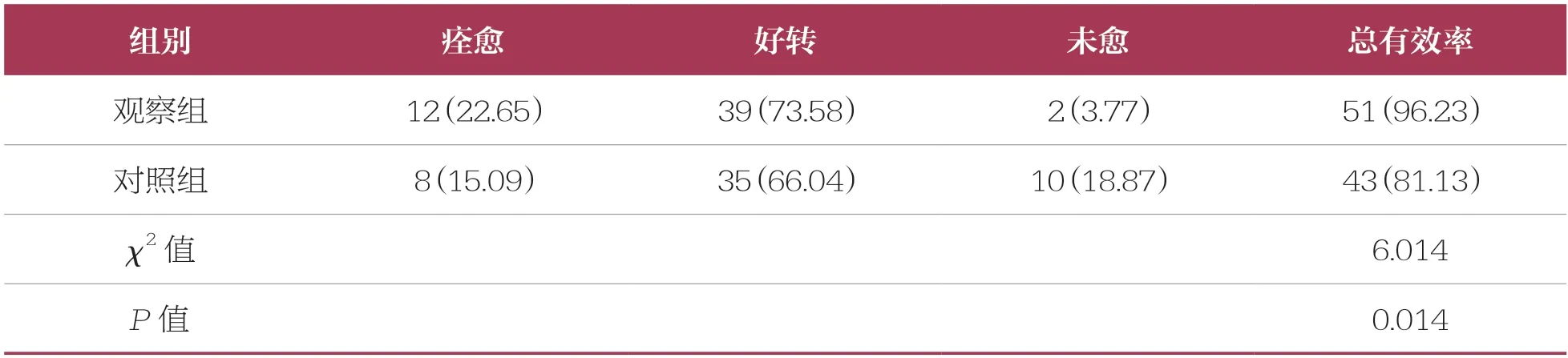
表4 兩組臨床療效比較 n=53,n(%)
2.5 不良反應發生率
觀察組不良反應發生率(3.78%)略低于對照組(7.56%),但無統計學差異(χ2=0.706,P=0.401)(表5)。
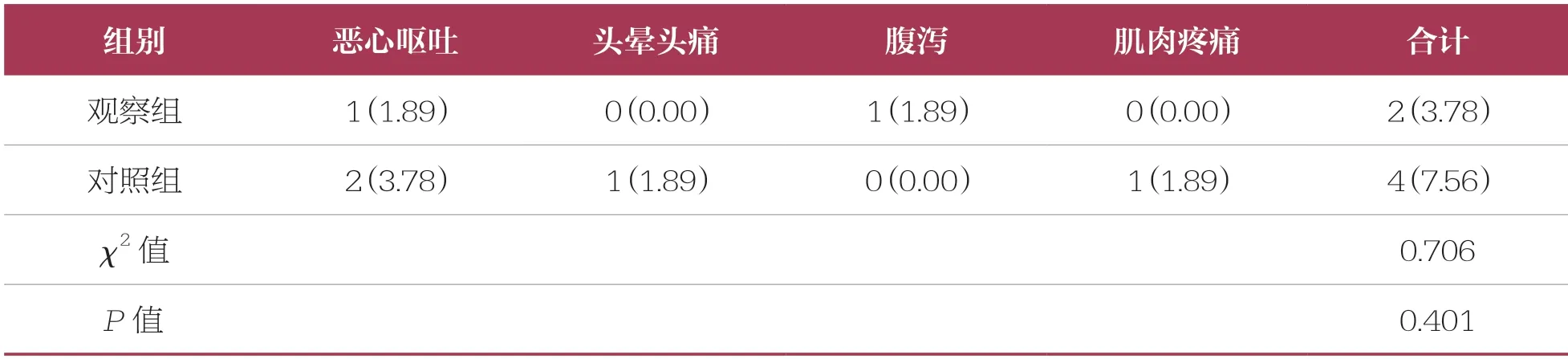
表5 兩組不良反應發生率比較 n=53,n(%)
3 討論
ICPP 可損害兒童心理,易誘發煩惱、焦慮等情緒,且在生理上可導致患兒身高低于同齡人[11]。目前,性早熟逐漸受到越來越多的重視,如何早發現早診治已成為重要的醫學難題之一。
西醫常用的治療手段大多以應用GnRH-a 為主,但相關藥品價格昂貴,患兒家屬經濟負擔重,且治療時間長,不良反應較大,因此該療法在臨床難以進行推廣[12-13]。中藥治療女童ICPP 因具有療效較佳、不良反應較小且價格較低等多重優勢而逐漸應用于臨床。
中醫理論認為,女性性發育與肝腎聯系密切。中醫基礎理論中描述“腎藏精,主生殖”,古代醫家認為“腎無實,不可瀉”,腎封藏失職,就會出現帶下、陰道出血不止。腎中精氣能助長發育,上通于腦、下連于沖任二脈而系胞宮,可調節機體的生殖功能[14]。結合小兒“肝常有余,而腎常不足”的特點,腎功能易失常則出現腎陽偏亢、腎水不足的現象,腎陰不足、水不涵木則肝失疏泄,臨床上可表現為生殖系統調節失司,表現為性早熟[15]。腎陽虛可致生殖功能衰退;腎陰虛而相火旺則可致生殖功能亢進。腎的陰陽失衡可影響患兒的性發育,性早熟屬于生殖功能亢進,提示為腎陰虛而相火旺[16],即ICPP 屬腎陰虛癥。中醫基礎理論中的肝腎同源學說指出,腎精依賴肝血不斷補充,肝血依賴腎精的滋養。精能生血,血能化精,肝血與腎精可以相互滋生、相互轉化。因此治療肝郁化火或陰虛火旺、相火妄動應以滋腎陰、降肝火為主要治則。
本研究中采用滋陰疏肝方加減治療ICPP。方中,熟地黃、山茱萸為君藥。熟地黃可補血滋陰、益精填髓,《珍珠囊》中指出其可“大補血虛不足,通血脈,益氣力”[17];山茱萸可補益肝腎、收澀固脫,正如《本草新編》中言:“山茱萸,味酸澀,氣平、微溫,無毒。入腎、肝二經。溫肝經之血,補腎臟之精……暖腰膝而助陽氣,經候可調。”[18]山藥、澤瀉、茯苓、牡丹皮為臣藥。山藥具有補脾養胃、生津益肺、補腎澀精的作用;澤瀉可利水滲濕,《本草綱目》[19]中提到其可“益腎氣,強陰,補不足,除邪濕”;茯苓藥性平和,利濕而不傷正氣;牡丹皮具有清熱涼血、活血化瘀的作用,《本草綱目》[19]記載可“和血、生血、涼血,治療血中伏火,除煩熱”,且有研究表明其具有瀉腎中之火的療效[20]。柴胡、當歸、白芍、白術為佐藥。柴胡歸肝、膽、肺經,可疏散退熱、疏肝解郁、升舉陽氣,用于肝郁氣滯、月經不調[21];當歸具有補血和血、調經止痛、潤腸通便的功效,現代藥理學研究提示其可保肝利膽、改善血液微循環[22];白芍具有養血調經、柔肝止痛、平抑肝陽的功效;白術具有健脾益氣、燥濕利水的功效,可用于脾虛食少、腹脹泄瀉。炙甘草為使藥,以補陰補血為主,有調和作用,在方中起著緩急和中的效果。全方共奏滋陰降火之功。
FSH、LH、E2可有效反映患兒性激素水平,常用于評估內分泌代謝情況[23];IGF-1 為一條單鏈堿性蛋白,在骨骼生長中可發揮重要作用,在正常青春期中會隨著性激素和生長激素的升高而升高,可用于ICPP 患者的診斷[24]。本研究結果顯示,治療后觀察組FSH、LH、E2、IGF-1 的水平均低于對照組,提示與單獨使用GnRH-a 比較,GnRH-a聯合滋陰疏肝方加減能更有效降低患兒的性激素水平。本研究中,治療后觀察組的骨齡低于對照組,且更符合患兒的身高與年齡對應水平[25]。子宮和卵巢容積的檢查對早期ICPP 患兒具有一定的診斷治療價值[26],進入青春期或早熟時子宮和卵巢體積均會逐漸增大,卵泡數目逐漸增多。本研究中,觀察組子宮、卵巢容積及直徑>4mm 的卵泡數量均低于對照組,提示GnRH-a 聯合滋陰疏肝方加減能有效縮小子宮、卵巢容積,減少直徑>4mm 的卵泡數量。
綜上所述,GnRH-a 聯合滋陰疏肝方加減能有效降低ICPP 患兒的FSH、LH、E2水平、改善患兒性早熟的臨床癥狀、緩解青春期的提前到來、恢復性激素水平。但本研究尚存在不足之處,例如選取樣本量較少、觀察時間較短、未能長期對患兒的性激素水平進行測定、遠期療效不能明確等,未來仍需進一步研究證實。

