薯蕷皂苷通過調控PDCD4對高糖誘導的血管內皮細胞增殖和凋亡的影響
李亞南 劉小勇
(1河南省中醫(yī)院周圍血管科,河南 鄭州 450003;2洛陽市第一中醫(yī)院周圍血管科)
糖尿病血管病變是一種高血糖持續(xù)的慢性血管系統(tǒng)疾病,長期在高糖條件下,血管內皮細胞功能代謝紊亂,與糖尿病的并發(fā)癥和發(fā)病機制密切相關,如神經病變、腎病、心力衰竭和視網膜病變等〔1,2〕。糖尿病引起的血管內皮細胞凋亡是糖尿病性周圍血管病變疾病發(fā)生的重要原因,長期血糖濃度不穩(wěn)定,易造成血管內皮結構破壞,影響其正常功能〔3〕。薯蕷皂苷(DIO)具有護肝、調節(jié)糖尿病性周圍血管病變功能、降血脂、抗炎和抗腫瘤等藥理疾病〔4〕。DIO可以通過抑制Wnt通路進而影響脂多糖誘導對大鼠系膜細胞MC增殖的作用〔5〕。蘇健等〔6〕研究結果顯示,DIO可以抑制氧化低密度脂蛋白誘導的血管內皮細胞EC的凋亡,進而起到保護的作用,但是在人臍靜脈內皮細胞(HUVECs)中的研究機制尚不清楚。程序性細胞死亡(PDCD)4位于染色體10q24上,是細胞凋亡因子,可以抑制細胞的凋亡〔7〕,PDCD4在高糖誘導的血管內皮細胞HUVEC中表達上調,下調PDCD4可以促進高糖誘導的血管內皮細胞中增殖,抑制其細胞凋亡〔8〕。本研究通過選取HUVECs建立高糖模型,研究薯蕷皂苷通過調控PDCD4對高糖誘導的血管內皮細胞增殖、凋亡的影響。
1 材料與方法
1.1細胞與主要試劑 HUVECs購自中國科學院上海細胞研究所;胎牛血清、DMEM培養(yǎng)基購自美國Gibco公司;DIO購自廣州左克生物公司;葡萄糖購自北京百歐博偉公司;LipofectamineTM2000轉染試劑盒購自美國Invitrogen公司;噻唑藍(MTT)試劑盒購、凋亡試劑盒自上海碧云天生物公司;PDCD4抗體、p21抗體、B細胞淋巴瘤(Bcl)-2抗體、Bcl-2相關X蛋白(Bax)抗體和GAPDH抗體購自美國Cell Signaling Technology公司;Trizol試劑盒購自北京索萊寶公司;反轉錄試劑盒、熒光定量試劑盒購自日本TaKaRa公司。si-NC、si-PDCD4、pcDNA和PDCD4購自廣州瑞博公司;引物購自上海吉瑪公司。
1.2細胞培養(yǎng)與分組 HUVECs常規(guī)復蘇后,置于培養(yǎng)箱內37 ℃、5%CO2進行培養(yǎng),且含有10%胎牛血清的DMEM培養(yǎng)基,并加入胰蛋白酶消化傳代培養(yǎng)。取對數(shù)生長期的HUVECs調整密度至5×105個/ml后,接種到96孔板中,然后將HUVECs分組,分為對照組(加入葡萄糖濃度為5 mmol/L處理)、高糖組(加入葡萄糖濃度為30 mmol/L處理)、高糖+DIO-L組(加入DIO 5 μg/ml,進行高糖處理)、高糖+DIO-M組(加入DIO 15 μg/ml,進行高糖處理)、高糖+DIO-H組(加入DIO 30 μg/ml,進行高糖處理),高糖+si-NC組(轉染si-NC后進行高糖處理)、高糖+si-PDCD4組(轉染si-PDCD4后進行高糖處理)、高糖+DIO+pcDNA組(轉染pcDNA后進行高糖和DIO 30 μg/ml處理)、高糖+DIO+PDCD4組(轉染PDCD4后進行高糖和DIO 30 μg/ml處理)。HUVECs細胞轉染參照LipofectamineTM2000轉染試劑盒說明書操作進行,轉染48 h,收集HUVECs進行后續(xù)實驗使用。
1.3MTT檢測細胞活力 收集HUVECs,加入胰蛋白酶消化后,將重懸的細胞調整密度至5×104個/ml,接種到96孔板中,繼續(xù)培養(yǎng)48 h后,每孔以20 μl加入MTT溶液,然后繼續(xù)培養(yǎng)4 h,繼續(xù)加入二甲基亞砜(DMSO)溶液150 μl,震蕩后在酶標儀490 nm波長處檢測細胞的光度值,并計算細胞活力。
1.4流式細胞術檢測細胞凋亡 收集HUVECs,消化重懸細胞后,調整細胞濃度至2×105/ml,然后加入500 μl磷酸鹽緩沖液。參照凋亡試劑盒說明書,分別加入5 μl膜聯(lián)蛋白Ⅴ-異硫氰酸熒光素(Annexin Ⅴ-FITC)和10 μl碘化丙啶(PI),15 min后在流式細胞儀檢測細胞凋亡率。
1.5Western印跡檢測PDCD4、p21、Bax和Bcl-2蛋白表達 收集HUVECs,加RIPA蛋白裂解液,冰上反應30 min后,提取各組細胞總蛋白,采用二喹啉甲酸(BCA)試劑檢測蛋白的濃度。然后將蛋白樣品上樣凝膠電泳處理后,轉膜后,脫脂牛奶封閉培養(yǎng)1.5 h。加入一抗PDCD4抗體、p21抗體、Bax抗體、Bcl-2抗體和GAPDH抗體,孵育過夜后,加入二抗,孵育2 h后,加入電化學發(fā)光液,顯影。通過Quatity One軟件蛋白條帶灰度值。
1.6實時熒光定量聚合酶鏈反應(qRT-PCR)檢測PDCD4 mRNA的表達 收集HUVECs,通過Trizol法提取細胞的總RNA,檢測其RNA濃度,反轉錄合成cDNA,然后以cDNA模板按照熒光定量試劑盒進行PCR擴增。以GAPDH為內參,通過2-△△Ct計算PDCD4 mRNA表達。
1.7統(tǒng)計學方法 采用SPSS22.0軟件進行方差分析。
2 結 果
2.1DIO對高糖誘導HUVECs增殖的影響 與對照組相比,高糖組細胞活力明顯降低,p21蛋白表達明顯增加(均P<0.05);與高糖組相比,高糖+DIO-L組、高糖+DIO-M組和高糖+DIO-H組細胞活力均明顯增加,p21蛋白表達均明顯降低(均P<0.05),見圖1、表1。

表1 DIO對高糖誘導HUVECs增殖的影響

1~4:對照組、高糖組、高糖+DIO-L組、高糖+DIO-M組、高糖+DIO-H組;圖2同圖1 DIO對高糖誘導HUVECs細胞的p21蛋白的影響
2.2DIO對高糖誘導HUVECs凋亡的影響 與對照組相比,高糖組細胞凋亡率、Bax蛋白表達均明顯增加,Bcl-2蛋白表達明顯降低(均P<0.05);與高糖組相比,高糖+DIO-L組、高糖+DIO-M組和高糖+DIO-H組細胞凋亡率、Bax蛋白表達均明顯降低,Bcl-2蛋白表達均明顯增加(均P<0.05),見圖2、圖3、表2。因此,本研究以DIO濃度選取30 μg/ml進行后續(xù)實驗。

表2 DIO對高糖誘導HUVECs凋亡的影響

圖2 DIO對高糖誘導HUVECs細胞凋亡的影響

1~5:對照組,高糖組,高糖+DIO-L組,高糖+DIO-M組,高糖+DIO-H組圖3 Western印跡檢測各組Bax、Bcl-2蛋白表達
2.3DIO對高糖誘導HUVECs PDCD4表達的影響 與對照組相比,高糖組PDCD4 mRNA和蛋白表達均明顯增加(P<0.05);與高糖組相比,高糖+DIO組PDCD4 mRNA和蛋白表達均明顯降低(P<0.05),見圖4、表3。

表3 DIO對高糖誘導HUVECs PDCD4表達的影響

圖4 DIO對高糖誘導HUVECsPDCD4蛋白表達的影響
2.4抑制PDCD4對高糖誘導HUVECs增殖的影響 與對照組相比,高糖組的PDCD4、p21蛋白表達均明顯增加,細胞活力明顯降低(均P<0.05);與高糖+si-NC組相比,高糖+si-PDCD4組的PDCD4、p21蛋白表達均明顯降低,細胞活力明顯增加(均P<0.05),見圖5、表4。
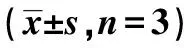
表4 抑制PDCD4對高糖誘導HUVECs增殖的影響

圖5 抑制PDCD4對高糖誘導HUVECsPDCD4、p21蛋白表達的影響
2.5抑制PDCD4對高糖誘導HUVECs凋亡的影響 與對照組相比,高糖組細胞凋亡率、Bax蛋白表達均明顯增加,Bcl-2蛋白表達明顯降低(均P<0.05);與高糖+si-NC相比,高糖+si-PDCD4組細胞凋亡率、Bax蛋白表達均明顯降低,Bcl-2蛋白表達明顯增加(均P<0.05),見圖6、表5。
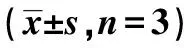
表5 抑制PDCD4對高糖誘導HUVECs凋亡的影響

1~4:對照組、高糖組、高糖+si-NC組、高糖+si-PDCD4組

2.6過表達PDCD4可以逆轉DIO對高糖誘導HUVECs增殖、凋亡的影響 與高糖組相比,高糖+DIO組PDCD4蛋白表達、細胞凋亡率、p21和Bax蛋白表達均明顯降低,細胞活力、Bcl-2蛋白表達明顯增加(均P<0.05);與高糖+DIO+pcDNA組相比,高糖+DIO+PDCD4組PDCD4蛋白表達、細胞凋亡率、p21和Bax蛋白表達均明顯增加,細胞活力、Bcl-2蛋白表達明顯降低(均P<0.05),見圖7、表6。

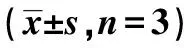
表6 過表達PDCD4可以逆轉DIO對高糖誘導HUVECs細胞增殖、凋亡的影響

1~4:高糖組、高糖+DIO組、高糖+DIO+pcDNA組、高糖+DIO+PDCD4組
3 討 論
糖尿病受遺傳、環(huán)境和飲食習慣等因素的影響,糖尿病引起的一系列糖尿病性周圍血管病變系統(tǒng)疾病并發(fā)癥嚴重威脅著人類的生命健康〔9,10〕。目前,中國糖尿病的患病率是世界上排行最高的,1990~2016年中國糖尿病患病率由3.7%上升至6.6%〔11〕。血管內皮細胞在細胞增殖和凋亡中處于一個動態(tài)平衡的狀態(tài),如果血管內皮細胞凋亡超過負荷,造成血管內皮細胞抗凝功能受阻,導致血管內皮細胞功能紊亂,是糖尿病血管疾病發(fā)病的主要原因〔12,13〕。DIO藥用價值很高,廣泛存在于薯蕷科、石竹科和百合科等植物中,在薯蕷科根莖中含量最高,具有消食利水、祛痰和舒筋活血等功效〔14〕。DIO在降低血糖方面效果作用明顯,研究結果顯示,DIO可以降低鏈脲佐菌素誘導的大鼠糖尿病血脂和氧化應激,提高促胰液素GLP-1釋放〔15〕。吳貴福等〔16〕研究發(fā)現(xiàn),DIO可以明顯抑制高糖誘導的大鼠視網膜血管內皮細胞HUVEC凋亡和氧化損傷。本研究結果說明,DIO可以促進高糖誘導的HUVECs的增殖和抑制其細胞凋亡。
PDCD4在糖尿病性周圍血管病變疾病、癌癥中廣泛表達,是一種促凋亡的基因,可以通過基因轉錄或翻譯抑制疾病的生長和凋亡等過程〔17〕。鄭華峰等〔18〕研究結果顯示,miR-155通過調控PDCD4表達調控高糖誘導的血管內皮細胞的凋亡。在男性糖尿病并發(fā)癥的研究中發(fā)現(xiàn),PDCD4在高糖誘導的大鼠海綿體組織中高表達,下調PDCD4表達可以抑制海綿體平滑肌細胞凋亡和促進其細胞增殖〔19〕,這與本研究結果相似。Zhang等〔20〕研究結果顯示,敲減PDCD4可以改善高糖誘導的糖尿病性周圍血管病變大鼠的胰島素抵抗和功能障礙,抑制心肌細胞的凋亡和炎癥反應。敲低PDCD4可以明顯促進高糖誘導的胰島β細胞的增殖,抑制其細胞凋亡和氧化應激〔21〕,這與本研究結果相似。本研究結果說明PDCD4在糖尿病中發(fā)揮著重要的作用。DIO可以通過調控PDCD4影響高糖誘導的HUVECs增殖和凋亡。

