精喹禾靈脅迫下萱草光合速率、葉綠素含量及根活力影響
余月書,遲法安,張 寶,朱 音,吳子凡,張志國
(1.上海應用技術大學 生態技術與工程學院,上海 201418;2.威海永達綠色技術有限公司,山東 威海 264200)
萱草是一種多年生的宿根花卉,其花色豐富、花期長、花型多,是園林綠化上常用的觀花類植物[1],但萱草田雜草種類繁多,嚴重影響萱草生長。化學除草是控制農田雜草的有效方法[2]。李金霞等[3]研究表明,20%氯氟吡氧乙酸對大花萱草田雜草防效達98%以上,且對萱草安全。萱草定植后使用33%二甲戊樂靈乳油、72%異丙甲草胺乳油對萱草田雜草有良好的控制作用[4]。同時,有研究報道滅草松與莠去津對大花萱草株高有明顯的抑制作用,使用莠去津60 d 后大花萱草植株全部死亡[3]。精喹禾靈是一種低毒型選擇性除草劑,常用于田間禾本科雜草防除。研究表明稻田與蠶豆田使用精喹禾靈能對水稻生長、酶系統、抗氧化系統及蠶豆根瘤與生長產生影響[5-6],但對萱草生長影響未見報道。本文以精喹禾靈為研究對象,萱草光合速率、葉綠素及根活力為指標,探索精喹禾靈田間使用對萱草生理生化產生的影響,以期為精喹禾靈在萱草田間使用提供理論依據。
1 材料與方法
1.1 材料
除草劑:精喹禾靈,安徽四達農藥化工有限公司生產,由上海應用技術大學萱草種植基地提供。萱草:萱草是上海應用技術大學培育的新品種,編號12010。
1.2 試驗方法
1.2.1 萱草栽培
3 月初,將越冬后的萱草從田間取出,去除枯葉,以清水洗凈泥土。自然晾干后,栽植于裝有營養土(蛭石:珍珠巖:草炭=1∶1∶3)的塑料盆(盆口直徑25 cm,高度30 cm)中,每盆2 株。室外自然條件下生長,常規管理。
1.2.2 試驗方法
萱草培育45 d 后,以10%精喹禾靈乳油400、800、1 200 mg/kg 噴霧處理。分別于處理后6、10、13、17 d 測定光合速率等光合參數;藥后8、11、14 d 測定葉綠素含量;藥后6、10、13 d 測定萱草根活力。以清水處理做對照。每處理重復3 次,每重復3 盆。
1.3 測定方法
光合參數以CI-340 光合儀(上海澤泉科技有限公司)測定。葉綠素含量以分光光度法測定,具體參考沈娟等方法[7]。根活力采用氯化三苯基四氮唑(triphenyltetrazolium chloride,TTC)法測定[8]。以SPSS12.0 進行試驗數據分析,以EXCEL 作圖。
2 結果與分析
2.1 精喹禾靈對萱草光合參數影響研究
藥后同一時間下,萱草光合速率在處理與對照之間不存在顯著差異(見表1)。藥后第6、10、13 d,較低濃度(400、800 mg/kg)精喹禾靈處理能夠促進光合速率上升,但高濃度(1 200 mg/kg)精喹禾靈處理后,光合速率受到抑制。藥后第17 天,精喹禾靈處理后萱草光合速率高于對照組,400、800、1 200mg/kg分別比對照高出184.02%、172.50%、124.17%。雙因素方差分析表明,藥后不同時間萱草光合速率之間存在顯著差異(p<0.01)。藥后6、10 d 光合速率顯著高于藥后13、17 d(見圖1)。藥后第6 d,萱草光合速率最高,CO2達9.941 7 mg·cm-2·h-1,分別比藥后10、13、17 d 高2.07%、287.48%及136.32%。
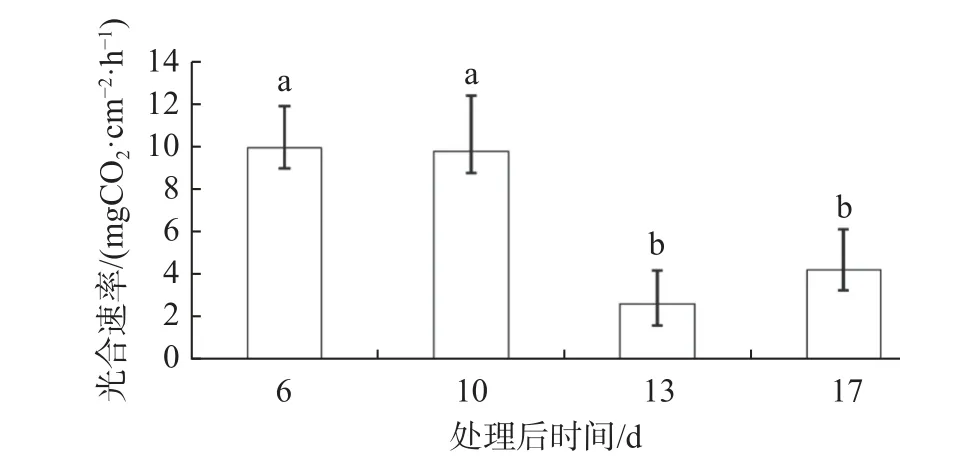
圖1 精奎禾靈對萱草光合速率影響的時間效應Fig. 1 Time-effect of quizalofop-p-ethyl on the photosynthetic rate of Hemerocallis

表1 精喹禾靈對萱草光合速率影響Tab.1 Effects of quizalofop-p-ethyl on the photosynthetic rate of Hemerocallis
2.2 精喹禾靈對萱草葉綠素含量影響研究
藥后11 d,同對照相比,精喹禾靈400 mg/kg處理后,萱草葉綠素總含量顯著下降28.99%。其余時間下,無論是葉綠素a、b,還是總葉綠素含量,處理與對照之間不存在顯著差異。雙因素方差分析表明,藥后不同時間葉綠素a、b 及總葉綠素含量之間均存在顯著差異(葉綠素a 含量:p<0.05;b 含量:p<0.01;總葉綠素含量:p<0.01)(見表2);不同濃度處理下,葉綠素a、b 及總葉綠素含量之間不均存在顯著差異(葉綠素a 含量:p>0.05;葉綠素b 含量:p>0.05;總葉綠素含量:p>0.05);在葉綠素總含量影響上處理與時間互作效應顯著(p<0.01)。雙因素方差分析同時表明葉綠素a、葉綠素b 及總葉綠素含量均表現出隨處理后時間延長而下降的變化趨勢,表現出明顯的時間效應(見圖2~4)。
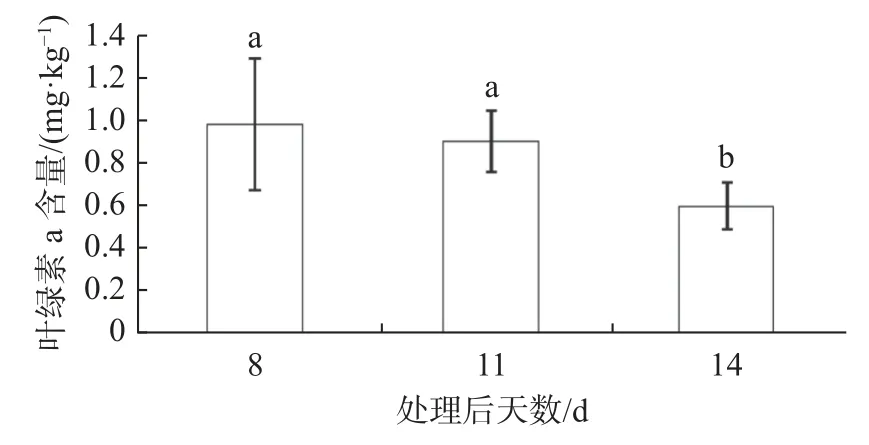
圖2 精奎禾靈葉綠素a 含量影響的時間效應Fig. 2 Time-effect of quizalofop-p-ethyl on the chlorophyll a content of Hemerocallis
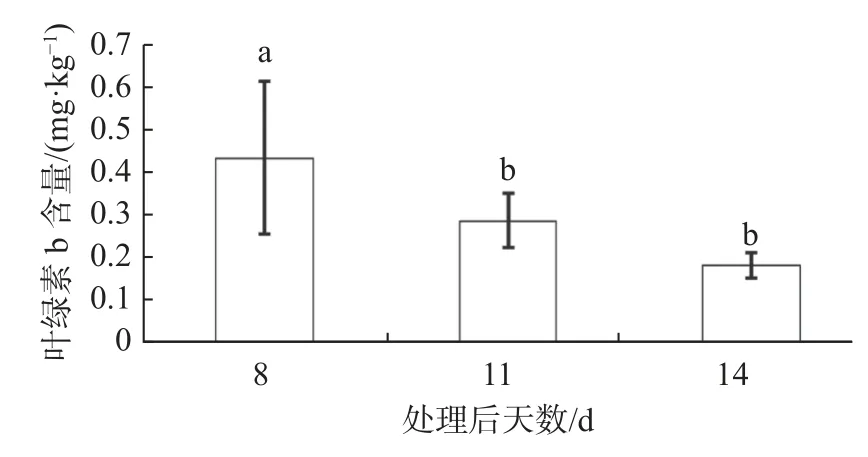
圖3 精奎禾靈葉綠素b 含量影響的時間效應Fig. 3 Time-effect of quizalofop-p-ethyl on the chlorophyll b content of Hemerocallis
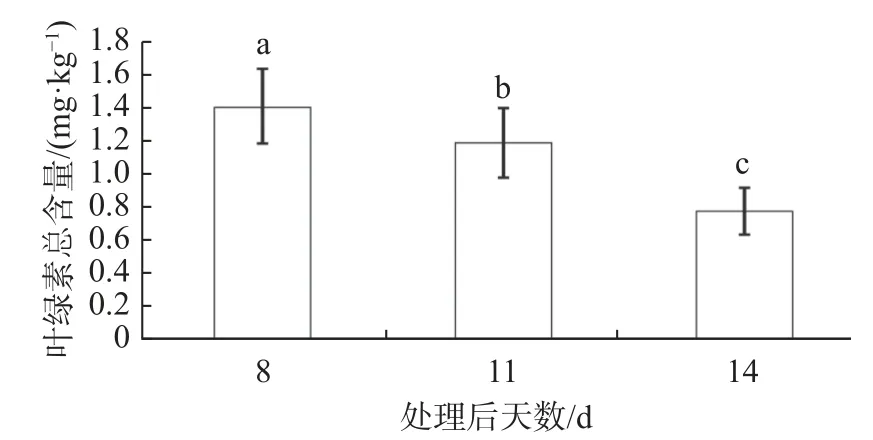
圖4 精奎禾靈葉綠素總含量影響的時間效應Fig. 4 Time-effect of quizalofop-p-ethyl on the total chlorophyll content of Hemerocallis
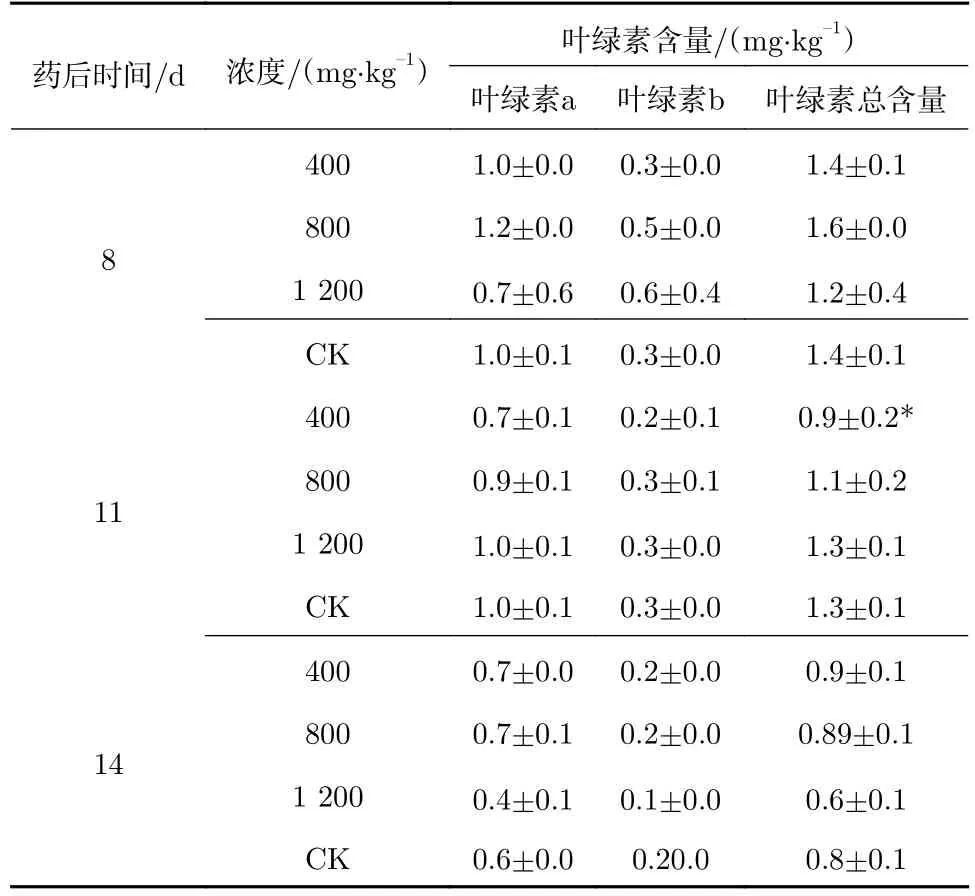
表2 精喹禾靈對萱草葉綠素含量的影響Tab.2 Effect of quizalofop-p-ethyl on the chlorophyll content of Hemerocallis
2.3 精喹禾靈對萱草根活力影響研究
表3 是精喹禾靈對萱草根活力影響研究結果,由表3 可知,藥后同一時間下,同對照相比,精喹禾靈處理對萱草根活力不產生顯著影響。雙因素方差分析表明,藥后不同時間萱草根活力之間存在顯著差異(p<0.01),且隨時間變化表現出先上升后下降的變化趨勢,在藥后第10 d 根活力顯著高于藥后第6、13 d,分別高出136.67%及77.11%(見圖5)。萱草根活力在精喹禾靈不同濃度處理之間不存在顯著差異(p>0.05)。時間與處理的互作將就對根活力影響顯著(p<0.05)。
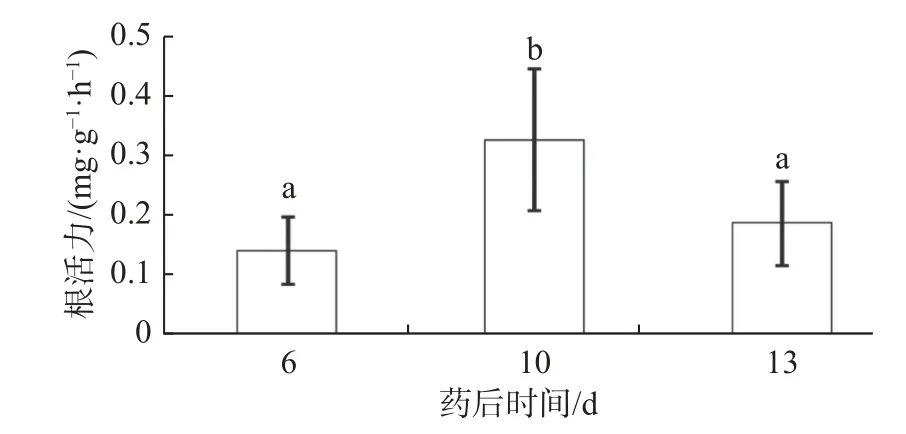
圖5 精奎禾靈對萱草根活力影響的時間效應Fig. 5 Time-effect of quizalofop-p-ethyl on the root vitality of Hemerocallis

表3 精喹禾靈對萱草根活力影響Tab.3 Effect of quizalofop-p-ethyl on the root activity of Hemerocallis
3 結語
植物光合作用是生態系統能量與物質來源的重要渠道,光合速率及葉綠素含量與植物光合作用強弱相關,反映了植物制造有機物質及轉化太陽能的效能,其不僅受到光、二氧化碳及水含量的影響,還與農藥、肥料及溫度等條件的影響[9-11]。根是植物吸收無機礦質營養及水分的重要器官,其活力大小表明根吸收能力的強弱,直接反映植物地上部的營養狀況與植物的產量水平。研究表明重金屬、農藥及鹽脅迫能對植物根活力產生明顯影響[12-14]。余月書等[11]研究報道了百菌清等殺菌劑使用后短期內能夠顯著降低萱草的光合速率,并引起葉綠素含量的顯著變化。同時,一定濃度的百菌清與吡蚜酮處理能夠顯著促進綠蘿根活力上升[14]。
本試驗研究表明,精喹禾靈處理對萱草光合速率、葉綠素含量及根活力不產生顯著影響。但是,高濃度精喹禾靈使用后對萱草光合速率及根活力抑制比較強(見表1~3),低濃度抑制作用較弱。對葉綠素含量影響方面,同樣是高濃度精喹禾靈抑制作用較強。因此,萱草生產上田間使用精喹禾靈除草時,建議選擇低濃度精喹禾靈防除雜草。同時,試驗結果表明,萱草光合速率、葉綠素含量及根活力在精喹禾靈處理后表現出明顯的時間效應。但是,光合速率、葉綠素及根活力三者時間效應并不表現出同步的變化趨勢,這可能與農藥隨時間延長在萱草葉片與根累積量有關。
植物光合速率、葉綠素含量及根活力不僅與水、二氧化碳、溫度等因素有關,還與體內的礦質營養、酶系統活力及氣孔導度等方面相關。農田生態系統中引入農藥的目的在于控制農田有害生物。但是,研究報道農藥還能對植物體內酶系統造成破壞及影響植物對礦質元素的吸收,而礦質元素與植物光合作用、葉綠素含量、蛋白質合成及酶系統等相關[15-17]。本研究中精喹禾靈對萱草光合速率等影響是由于精喹禾靈對萱草體內清除氧自由基的過氧化物酶系統產生破壞作用引起氧自由基積累而影響根活力,及其在萱草體內積累引起葉綠素合成探到阻礙,進而引起光合速率的變化,還是由于精喹禾靈對葉綠體破壞引起光吸收變化而引起光合速率變化有待進一步深入研究。

