腐植酸在水處理過程中的定量分析及其與消毒副產物的關系
王 碩 劉梓晶 王依晴 黃向陽*
1 長江大學城市建設學院 荊州 434000
2 北京市熱力工程設計有限責任公司 北京 100164
腐植酸在土壤和湖泊等自然界中大量存在。腐植酸具有絡合性、溶解性、酸性等化學性質,進入水體,可能會促進水中的銅、鉛等重金屬離子溶解,毒性在水中累積,導致植物和動物的死亡。因腐植酸具有羰基、羥基、羧基等難降解基團,在工業水處理中降解較為困難,因此腐植酸在水處理過程中的含量變化引起公眾關注[1]。腐植酸占水體中溶解性有機質(DOM)含量的70%以上,因受環境、天氣、來源、生成條件等因素影響,其結構較為復雜且多變,目前沒有相關結構的定性結論[2]。工業領域的快速發展促使外源有機污染物質的進入,導致了水體中腐植酸含量的增加及其結構的變化[3]。水中腐植酸在氯化消毒時易與游離氯生成鹵代烴等消毒副產物(DBPs),長期飲用者易患泌尿系統癌癥及腸道癌等疾病[4];同時,由于水中腐植酸在混凝過程中的水解作用及其羧基、羥基與金屬離子的絡合反應,降低了水處理工藝中混凝劑的效果,也會抑制人體對鈣、鎂等金屬離子的吸收[5]。因此,定量分析腐植酸在水處理流程中的含量變化是很有必要的。通過腐植酸結構特性的研究找出消毒副產物與其前驅物的關系,將有助于水處理工藝優化,可為飲用水源健康風險評價和環境生態風險評價,從而設定生活用水與環境水體中腐植酸指標的限定值提供技術支撐。
1 實驗材料與方法
1.1 試劑與儀器
實驗樣品:3 種腐植酸標準物質為腐植酸(HA,3S101H、地表水,國際腐殖質學會)、黃腐酸(FA,2S101F、地表水,國際腐殖質學會)、天然有機質(NOM,2R101N、地表水,國際腐殖質學會,主要成分為腐植酸)[6]。實驗試劑:聚合氯化鋁(商用混凝劑,太倉某水廠)、磷酸緩沖劑(AR 分析純,國藥集團化學試劑有限公司)、次氯酸鈉溶液(CP 分析純,國藥集團化學試劑有限公司)、過硫酸鈉(AR 分析純,國藥集團化學試劑有限公司)。實驗設備:過砂濾裝置、玻璃聚四氟砂板層析柱、MY3000-2N 型便攜式混凝器、Five Easy Plus 型pH 計、TOC-LCPN 型總有機碳(TOC)分析儀、FLS1000 型穩態瞬態熒光光譜儀、UH4150型紫外可見分光光度計、GC-2030 型氣相色譜儀、7890B/7200B 型氣相色譜/串聯四級桿-飛行時間質譜儀等。
1.2 實驗方法
用常規水處理流程“混凝—沉淀—過濾—消毒”流程對3 種腐植酸標準物質進行模擬。
(1)實驗水樣配制。
自來水提前放置12 h 以去除里面的余氯,將3 種腐植酸標準物質配制成質量濃度為10 mg/L 的實驗水樣,將溶液pH 值調節為7.5。
(2)混凝—沉淀實驗。
混凝實驗使用便攜式混凝器,加入聚合氯化鋁(PAC)進行混凝。在恒溫20 ℃的條件下,向1 L實驗水樣中投入12 mg/L PAC,混凝程序分為三步(表1),快速攪拌使混凝劑快速、均勻地分布在水中,慢速攪拌使絮凝體進一步變大,以實現固液分離。取樣時,在距液面2 cm 處抽取上清液,進行腐植酸標準物質、三鹵甲烷(THMs)和鹵乙酸(HAAs)含量的測定。
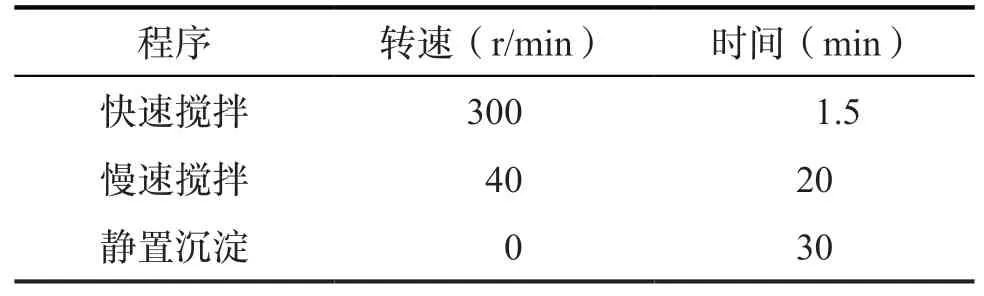
表1 混凝程序Tab.1 Coagulation procedure
(3)過濾實驗。
本次實驗采用小型過砂濾裝置,為避免石英砂攜帶的其他雜質的干擾,將石英砂洗滌至水體無色透明,并用超純水清洗至pH 值為中性,將4 ~10 目(2 ~5 mm)、8 ~16 目(1 ~2 mm) 和16 ~30 目(0.55 ~1 mm)3 種粒徑大小的石英砂依次填入至玻璃聚四氟砂板層析柱(表2)。移取混凝沉淀后的上清液泵入至石英濾料玻璃聚四氟砂板層析柱中,設置濾速為5 ~12 m/L。取樣時,將過濾后的溶液放入棕色瓶1 中,進行腐植酸標準物質、THMs 和HAAs 含量的測定。

表2 石英砂填充層析柱濾料比例Tab.2 Filter ratio of quartz sand filled chromatography column
(4)消毒實驗。
從棕色瓶1 中取500 mL 的過濾液于棕色瓶2中,加入10 mL 的磷酸緩沖劑,反應期間保持中性(pH=7);充分混合后加入35.71 μL 次氯酸鈉溶液,將棕色瓶2 瓶口封嚴,放入生化培養箱中。在20 ℃的溫度下保存24 h,避免光線照射。分別對0、1、8、24 h 共計4 個反應時間點進行采樣,將提取水樣放到含有適量過硫酸鈉的褐色玻璃樣品瓶中,進行腐植酸標準物質、THMs 和HAAs 含量的測定。
1.3 分析與表征
采用FLS1000 型穩態瞬態熒光光譜儀進行測定,檢測FI 值,激發波長為300 ~500 nm,Δλ取18 nm,進行同步掃描,測定混凝階段各腐植酸標準物質特征熒光峰的變化情況。TOC 的檢測采用TOC-LCPN 型總有機碳分析儀(島津日本有限公司)。紫外可見吸收光譜采用UH4150 型紫外可見分光光度計檢測,用超純水作為空白對照,掃描范圍設為200 ~500 nm,測定實驗水樣中腐植酸標準物質紫外參數:特征紫外吸光度(SUVA)、E4/E6值和UV254值。使用GC-2030 型氣相色譜儀,測定水處理流程中消毒副產物THMs 的濃度變化。HAAs 的測定使用7890B/7200B 型氣相色譜/串聯四級桿-飛行時間質譜儀(表3)。
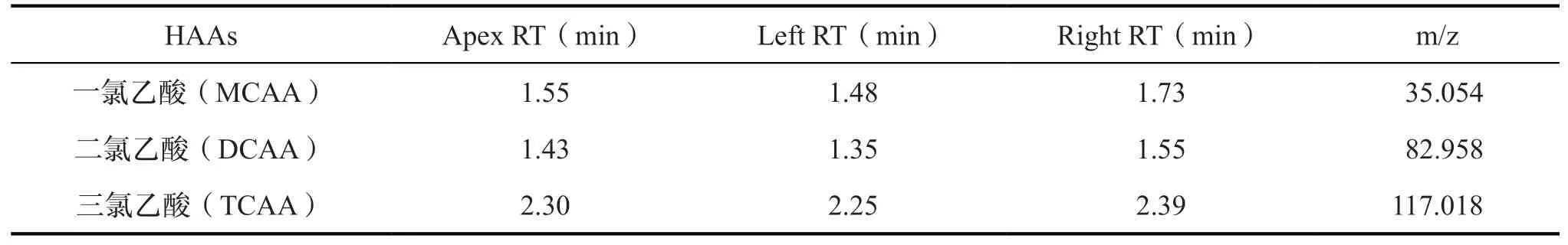
表3 鹵乙酸(MCAA、DCAA、TCAA)特征峰信息Tab.3 The information of haloacetic acid (MCAA, DCAA, TCAA) characteristic peak
2 結果與討論
2.1 水處理工藝流程中腐植酸的定量分析
2.1.1 不同腐植酸標準物質在水處理流程中的含量變化
對量程為12 mg/L 的不同濃度梯度的腐植酸標準物質進行熒光強度測定,HA、FA、NOM 各熒光峰處熒光強度F 與質量濃度C 的線性回歸方程分別為F=22898.21×C+8799.36,R2=0.994(HA);F=73485.46×C+18536.78,R2=0.996(FA);F=35075.06×C+8406.22,R2=0.998(NOM)。 采用上述3 種腐植酸標準物質的回歸方程對水處理流程模擬實驗中各采樣點進行腐植酸標準物質質量濃度的測定,以TOC 為定量參考值,腐植酸標準物質的質量濃度變化和TOC 質量濃度變化見圖1。

圖1 腐植酸標準物質的質量濃度變化和TOC 濃度變化圖Fig.1 The variation of mass concentration and TOC of humic acid standard materials
由圖1 可知,混凝階段后,PAC 對3 種腐植酸標準物質的混凝去除效果明顯,采用熒光分析法定量腐植酸標準物質的質量濃度去除率均大于TOC 表征的質量濃度去除率,說明腐植酸標準物質中的熒光基團在混凝階段的參與程度高于腐植酸標準物質中的碳。表4 為混凝階段各腐植酸標準物質的去除率。去除率指處理前和處理后腐植酸標準物質的質量濃度比值,是由圖1 中斜率體現出來的。由表可知,PAC 對腐植酸標準物質的去除效果為FA >HA >NOM,其質量濃度和TOC 呈現相同的去除效果,說明FA(2S101F)具有更多的活性基團,對聚合氯化鋁中Al3+的絡合能力高于HA(3S101H)和NOM(2R101N)。水樣經過過濾后,各腐植酸標準物質水樣的TOC均出現了輕微升高,該現象可能是由于濾池中石英砂濾層引入了其他有機物的污染。而TOC 濃度變化不明顯,說明消毒階段主要由熒光基團參與了反應。由于腐植酸標準物質苯環上的羥基和氨基作為反應中的供電基團,促進了苯環受到氯的親電進攻,加速了腐植酸中熒光基團的反應消耗和消毒副產物的生成。因此,對于低腐植酸標準物質含量的水體,適合采用熒光分析法追蹤腐植酸在整個消毒過程中的含量變化。
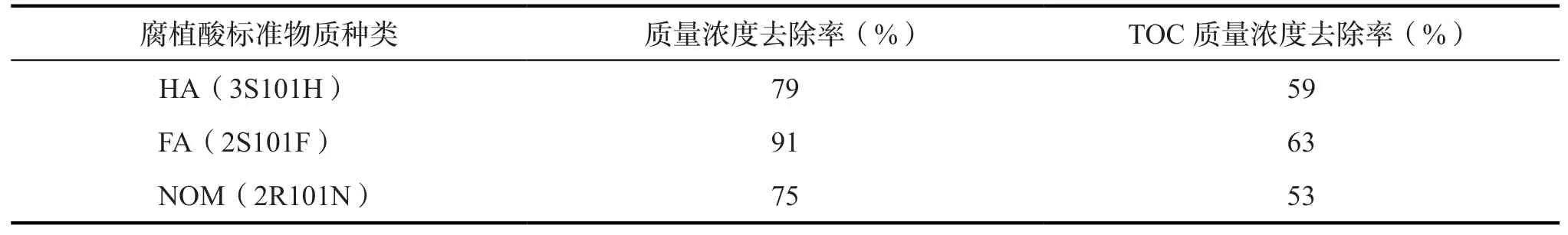
表4 混凝階段腐植酸標準物質的去除率Tab.4 Removal rate of humic acid standard materials in coagulation stage
2.1.2 不同腐植酸標準物質的熒光定量結果與TOC濃度的相關性
表5分別列出了水處理流程中不同腐植酸標準物質的質量濃度和TOC 的線性關系。圖1 是腐植酸標準物質的質量濃度變化和TOC 濃度變化圖。由此可知,以熒光基團標定的腐植酸標準物質質量濃度和TOC 呈現線性相關性,最高相關性為0.999,說明可以使用熒光定量分析法替代傳統TOC 定量分析法,對水處理流程中的腐植酸定量追蹤及分析。
同時,以上述分析過程作為參考,依據混凝、消毒各工藝階段反應機理,發現相比于TOC 定量,以熒光基團標定的質量濃度更適用于在水處理流程中腐植酸的定量分析。

表5 水處理流程中腐植酸標準物質的質量濃度和TOC 的線性關系Tab.5 Linear relationship between mass concentration and TOC of humic acid standard materials in water treatment process
2.2 腐植酸對水處理工藝流程中消毒副產物含量的影響
在整個水處理工藝流程中,通過檢測3 種腐植酸標準物質在處理流程中對消毒副產物含量的影響,對實驗水樣、混凝沉淀出水、過濾出水、消毒出水中THMs、HAAs 的含量進行了分析。
2.2.1 不同腐植酸標準物質對消毒副產物生成量的貢獻
圖2為水處理流程中THMs 的濃度變化。3 組實驗中的THMs(本實驗僅含三氯甲烷)含量變化趨勢一致。混凝沉淀后,含3 種腐植酸標準物質水樣中THMs 濃度均出現減小現象,混凝階段中NOM(2R101N)的THMs 去除率最高,HA(3S101H)的THMs 去除率高于FA(2S101F)中THMs 的去除率。過濾后,含3 種腐植酸標準物質水樣中THMs 濃度均繼續減小,這主要是由于THMs 揮發性較強,水樣在砂濾池中的水力停留時間導致THMS 持續揮發。加入次氯酸鈉的瞬間,即余氯消毒0 min 節點時,含3 種腐植酸標準物質水樣中THMs 迅速生成。在消毒24 h 時,含NOM(2R101N)、HA(3S101H)、FA(2S101F)水樣中的THMs 生成率分別為107%、82%、19%。含NOM(2R101N)水樣的THMs 生成率最大,生成速率最快;HA(3S101H)次之;而FA(2S101F)對THMs 生成的貢獻最小,并且在消毒1 h 后,其水樣THMs 的生成速率逐漸減小。故不同腐植酸標準物質對THMs 生成的貢獻為:NOM >HA >FA。
在整個水處理流程中,含3 種腐植酸標準物質水樣均只檢測到DCAA 和TCAA 2 種HAAs 類消毒副產物,MCAA 等其他鹵乙酸均未達到檢出限(圖3)。
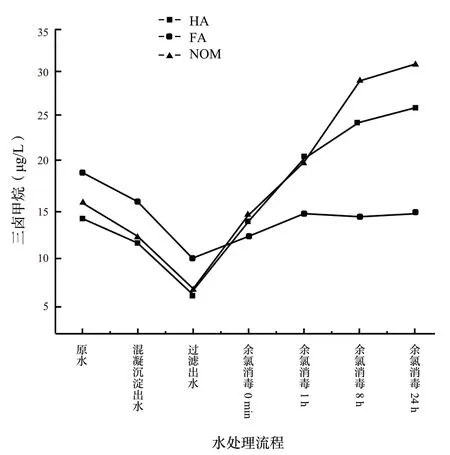
圖2 水處理流程中THMS 消毒副產物的濃度變化Fig.2 The evolution of THMS concentration in water treatment process
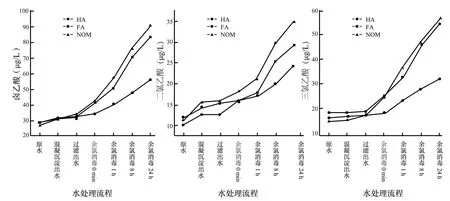
圖3 水處理流程中HAAS 類消毒副產物的濃度變化Fig.3 The evolution of HAAS concentration in water treatment process
由圖3 可知,DCAA、TCAA 和HAAs(兩者之和)的變化趨勢較為相似,鹵乙酸類消毒副產物的含量在實驗水樣、混凝沉淀出水和過濾出水中無明顯變化。這主要是由于HAAs 為難揮發性消毒副產物,在混凝和過濾中無明顯揮發。進入消毒工藝后,含3 種腐植酸標準物質水樣的鹵乙酸類消副產物生成率均呈現明顯的上升趨勢;并且含NOM(2R101N)水樣的鹵乙酸類消毒副產物生成速率最快,生成率最大,其HAAs、DCAA、TCAA 的生成率分別為114%、91%、131%;HA(3S101H)次之;含FA(2S101F)水樣的鹵乙酸類消副生成率最小。因此,不同腐植酸標準物質對鹵乙酸生成的貢獻為:NOM >HA >FA。
水處理流程中總消毒副產物(DBPs)含量的變化見圖4。由圖可知,過濾出水中,各腐植酸標準物質的DBPs 大約為40 μg/L。加入次氯酸鈉后,經過24 h 反應產生大量氯代消毒副產物于70 ~120 μg/L 之間,說明氯代消毒副產物的主要生成因素為次氯酸鈉。通過比較不同腐植酸標準物質對DBPs 的貢獻,發現依舊為NOM >HA >FA。
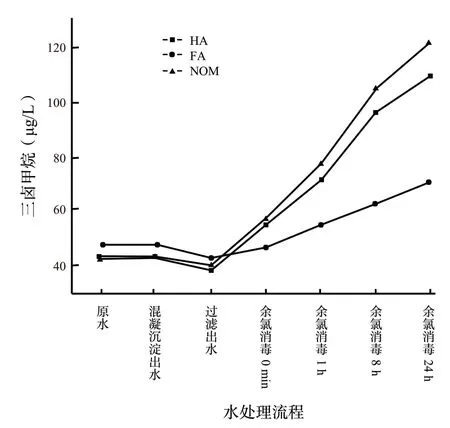
圖4 水處理流程中DBPs 的濃度變化Fig.4 The evolution of DBPs concentration in water treatment process
2.2.2 不同腐植酸標準物質與消毒副產物的轉化關系
水處理流程中消毒副產物的濃度變化情況見圖5。由圖可知,在消毒24 h 后,含HA(3S101H)水樣中HAAs 的生成量高于THMs 生成量的144%,含NOM(2R101N)水樣中HAAs 的生成量高于THMs 生成量的164%,而含FA(2S101F)水樣中HAAs 的生成量高于THMs 生成量的402%。可知FA(2S101F)可能為HAAs 的主要前驅體,與已有研究結果一致[7]。3 種腐植酸標準物質消毒24 h 后,HAAs 中TCAA 的生成量均遠高于DCAA,這一現象可能與較高的投氯量有關,當投氯量較高時,腐植酸標準物質會與次氯酸鈉先生成R-CO-Cl2,中間產物R-CO-Cl2再與活性氯生成R-CO-Cl3[8],因此TCAA 的生成量高于DCAA。有研究表明,中間產物的R 基團決定了消毒副產物的生成種類,如果R 為羥基時,R-CO-Cl2將主要生成DCAA,R-CO-Cl3將直接生成TCAA;如果R 為甲基,R-CO-Cl3是THMs 和HAAs(TCAA、DCAA)的共同中間產物[9,10]。消毒24 h 后,3 種腐植酸標準物質均生成了DCAA、TCAA、THMs 3 種消毒副產物,而含HA(3S101H)與含NOM(2R101N)水樣中DCAA 和THMs 的生成率較為相近,含FA(2S101F)水樣中DCAA 的生成量高于THMs 生成量的92.75%,說明在該投氯量下,HA(3S101H)和NOM(2R101N)的主要氯代中間產物為CH3-CO-Cl3,而FA(2S101F)的主要氯代中間產物有HO-CO-Cl2和CH3-CO-Cl3。
為分析消毒過程中腐植酸標準物質與消毒副產物的轉化關系,將各消毒副產物濃度和腐植酸標準物質以熒光基團標定的質量濃度進行線性關系分析,回歸方程中的斜率表示反應速率(表6)。發現各腐植酸標準物質(HA、FA、NOM)以熒光基團標定的質量濃度均與消毒副產物濃度(THMs、HAAs)具有良好的線性關系,說明使用以熒光基團標定的質量濃度追蹤腐植酸標準物質在消毒反應過程中的含量變化是適合的,同時也反映了芳香性熒光基團參與了消毒反應。由各回歸方程的斜率可知,對于不同腐植酸標準物質的消毒反應速率,均存在生成HAAs 的反應速率大于THMs 的生成反應速率,生成TCAA 的反應速率大于DCAA 的生成反應速率。對于DBPs 的反應生成來說,NOM 的反應速率最大,FA 的反應速率最小。
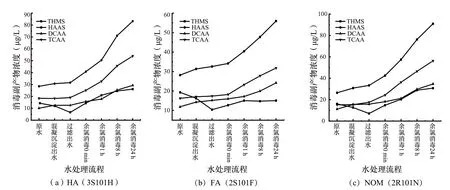
圖5 水處理流程中消毒副產物變化比對Fig.5 Comparison of disinfection by-products in water treatment process
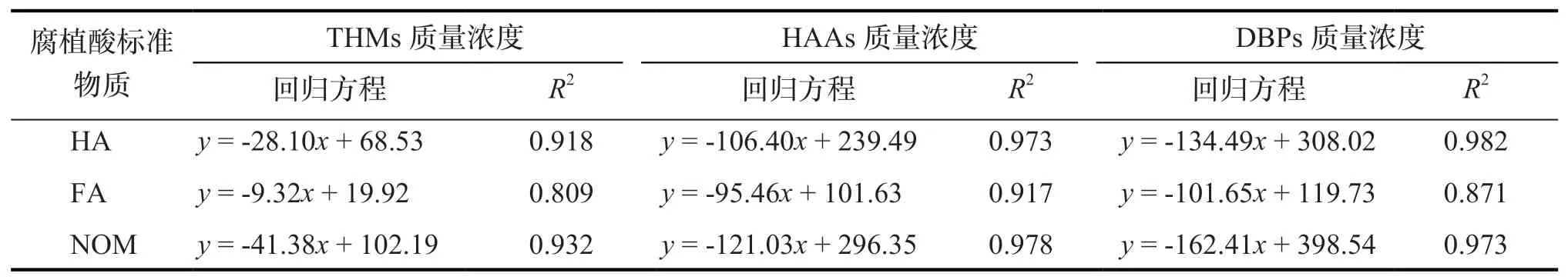
表6 消毒過程中THMs、HAAs、DBPs、DCAA、TCAA 的生成量和腐植酸標準物質質量濃度的關系Tab.6 Correlation between THMs, HAAs, DBPs, DCAA, TCAA production and mass concentration of humic aicd standard materials in disinfection
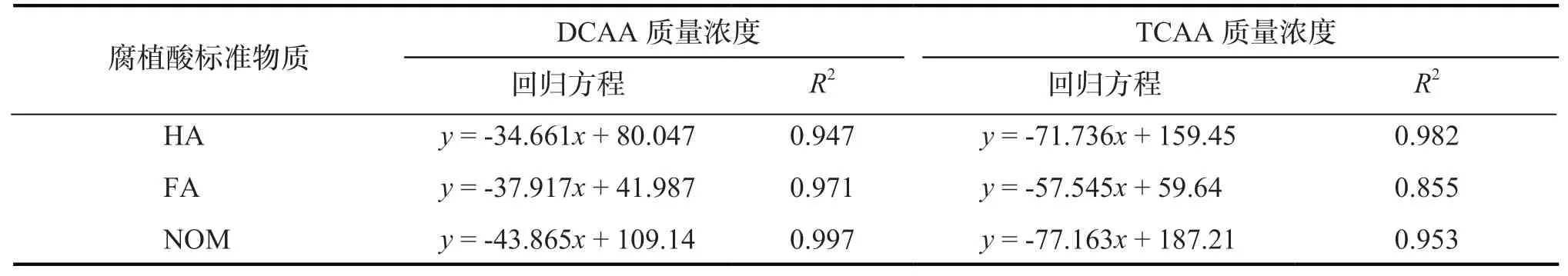
表6 續
2.3 腐植酸的形態和結構對水處理工藝的影響
2.3.1 紫外可見光吸收光譜
(1)不同腐植酸標準物質的結構特性差異。
通過觀察實驗水樣中3 種腐植酸標準物質的紫外可見光吸收光譜,對腐植酸標準物質的發色團有機質的形態和結構進行分析。結果見圖6 和表7。
圖6顯示,實驗水樣中3 種腐植酸標準物質的紫外吸收效應明顯,均呈現為較為平緩的曲線,最高點的吸光度大小不同,說明3 種腐植酸標準物質中不飽和雙鍵和芳香基團所占比例不同;并且圖中FA(2S101F)在270 nm 波長處存在的肩縫相較于NOM(2R101N)和HA(3S101H)更加明顯,說明FA(2S101F)中含有較高占比的羧基等含氧基團。再次驗證了UV254、SUVA、E4/E6值的分析結果。
由表7 可知,實驗水樣中3 種腐植酸標準物質的SUVA 值:HA >FA >NOM,NOM(2R101N)存在較少的疏水性基團,HA(3S101H)中有較多的親水性基團。比較3 種腐植酸標準物質的E4/E6值,FA(2S101F)的E4/E6值大于HA(3S101H)與NOM(2R101N),說明其為小分子量腐植酸標準物質,含有較多的氧、羧基和較少的碳[11]。由UV254值可知,3 種腐植酸標準物質芳香度大小依次為HA、FA、NOM,說明HA(3S101H)較FA(2S101F)和NOM(2R101N)有較多的脂肪結構。結合上文可知芳香度與THMs 的生成呈正比。但NOM(2R101N)的THMs 的生成值大于HA(3S101H)與FA(2S101F),而其UV254值低于其余2 種腐植酸標準物質,說明NOM(2R101N)中除芳香性結構外,還存在其他結構可以生成THMs。已有研究表明,胺和鹵代脂肪烴、芳香烴和含C-O 鍵的脂肪烴也可以導致THMs 的生成[12,13]。
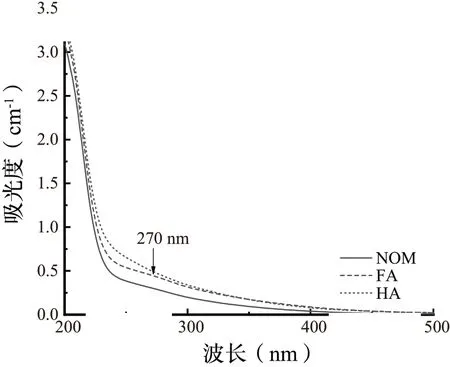
圖6 實驗水樣中3 種腐植酸標準物質的紫外可見吸收光譜Fig.6 Uv-vis spectra of three humic acid standard materials in raw water

表7 實驗水樣中腐植酸標準物質紫外參數Tab.7 Ultraviolet parameter of humic acid standard materials in raw water
(2)不同腐植酸標準物質在水處理工藝流程中的結構轉變。
圖7為3 種腐植酸標準物質在不同水處理流程的紫外可見吸收光譜圖。
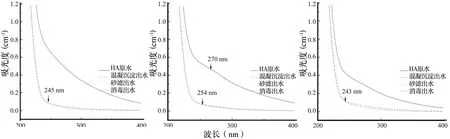
圖7 3 種腐植酸標準物質在不同水處理流程下的紫外可見吸收光譜Fig.7 Uv-vis spectra of three humic acid standard materials in different water treatment stages
由圖7 可知,普通砂濾池對腐植酸標準物質沒有明顯的去除效果;相比于過濾出水,消毒出水的吸光度存在微小程度的降低,這可能是由于腐植酸標準物質中的不飽和鍵和部分芳香基團與活性氯反應生成了消毒副產物,降低了腐植酸標準物質對于紫外光的吸收。由于腐植酸結構中共軛程度的增加或芳香環上電子供體的存在,易導致最大吸收波長和發色團的摩爾吸收系數的增大,使其光譜變寬[14]。因此,腐植酸中的基團對紫外光存在吸收限制,使紫外吸收譜帶為平滑的曲線,無明顯的吸收波峰,導致無法判斷基團的具體參與情況,后使用同步熒光光譜對各腐植酸水樣中的基團變化進行分析。
(3)不同腐植酸標準物質的熒光定量結果與UV254的相關性。
為驗證熒光定量方法在工程中的實用性,對工藝流程中各采樣點的腐植酸標準物質質量濃度、TOC、UV254進行檢測,研究其相關性。從表8發現以熒光基團標定的腐植酸標準物質質量濃度和UV254呈現較強的相關性,各相關系數均大于0.9,最高相關性為0.997;腐植酸標準物質的TOC與UV254也具有較好的相關性,相關系數均大于0.99。在以往研究中,也常使用TOC[15]或UV254[16]跟蹤有機質在工藝中的含量變化,但無法實現腐植酸的精準定量。
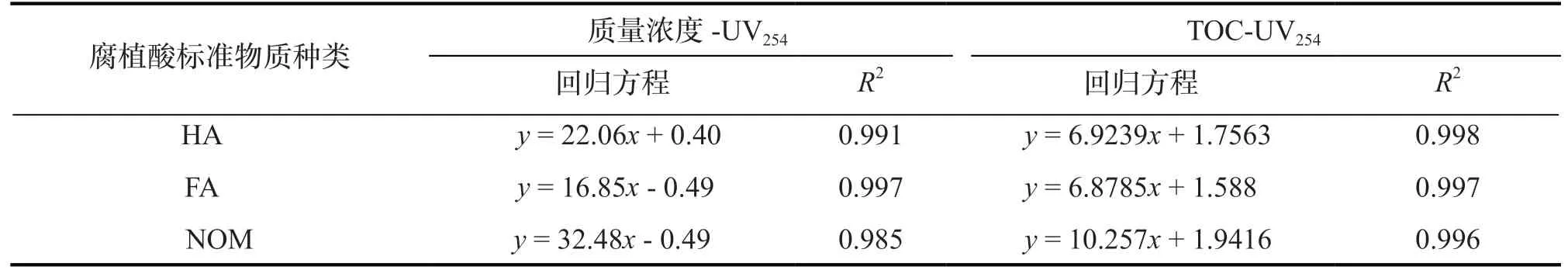
表8 腐植酸標準物質在水處理流程中其質量濃度、TOC 與UV254 的相關性Tab.8 Correlation of mass concentration, TOC and UV254 of humic acid standard materials in water treatment process
2.3.2 同步熒光光譜
同步熒光光譜常用于對自然水體中溶解性有機質進行定性定量分析,對3 種腐植酸標準物質在整個水處理工藝流程取樣測定同步熒光光譜,用以分析不同腐植酸標準物質的區別以及在工藝流程中的變化,控制實驗檢測條件一致進行比對分析,將3 組檢測的Δλ 均設為18 nm,圖8 ~圖10 為3種腐植酸標準物質在整個水處理流程中的同步熒光光譜掃描結果。
(1)不同腐植酸標準物質的結構比對分析。
圖8~圖10 為HA(3S101H)、FA(2S101F)、NOM(2R101N)在水處理流程中的同步熒光光譜變化情況。由圖可知,不同腐植酸標準物質的同步熒光出峰情況,HA(3S101H)實驗水樣在355、397、465 nm 處存在明顯的熒光峰,且397 nm 處熒光峰強度最大。同樣研究發現,在340、370 nm或380、480 nm 附近出現的熒光峰可能是由腐植酸存在引起的[17]。而FA(2S101F),僅具有位于360 nm 和480 nm 的2 個特征熒光峰,且360 nm處的熒光峰熒光強度最大,為較寬的平臺形狀,這可能是由于FA(2S101F)中的2 個或多個熒光基團在Δλ=18 nm 掃描時產生了重疊。引起FA(2S101F)在480 nm 處的熒光基團與HA(3S101H)中465 nm 處的熒光基團可能為同一種基團,但FA(2S101F)該基團的熒光強度遠大于HA(3S101H)該基團的熒光強度,說明FA(2S101F)該熒光基團含量遠高于HA(3S101H)的該基團含量。NOM(2R101N)在355、387 nm 處存在明顯的熒光峰,且355 nm 處的熒光信號最強。NOM(2R101N)中引起355 nm 和387 nm 處出現熒光峰的基團可能與HA(3S101H)中355 nm 和397 nm處的熒光基團相同,但是NOM(2R101N)中兩基團呈現的熒光強度均大于HA(3S101H)中的兩基團熒光強度,說明兩基團在NOM(2R101N)中的含量高于HA(3S101H)中的含量。
綜上所述,由3 種腐植酸標準物質的同步熒光掃描結果比對發現,HA(3S101H)中含有與NOM(2R101N)和FA(2S101F)相同的熒光基團,但相同基團的含量占比也是不同的。并且由3 種腐植酸標準物質整體熒光譜帶的熒光強度比對發現,FA(2S101F)的整體熒光強度>NOM(2R101N)的整體熒光強度>HA(3S101H)的整體熒光強度,說明FA(2S101F)含有更多的活性熒光基團。
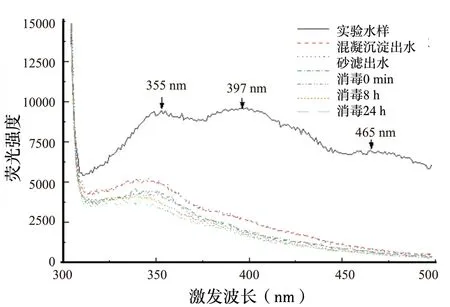
圖8 水處理流程中HA 的同步熒光光譜(Δλ=18 nm)Fig.8 Synchronous fluorescence spectra of HA in water treatment process
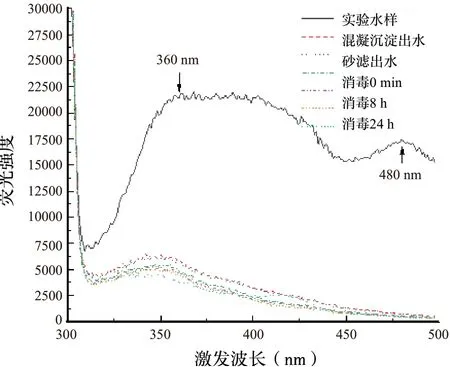
圖9 水處理流程中FA 的同步熒光光譜(Δλ=18 nm)Fig.9 Synchronous fluorescence spectra of FA in water treatment process
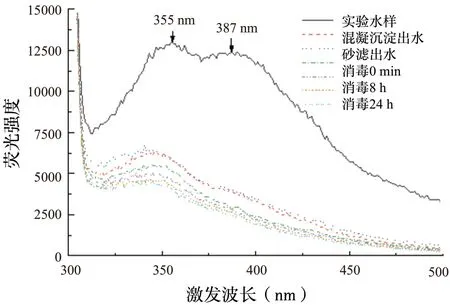
圖10 水處理流程中NOM 的同步熒光光譜(Δλ=18 nm)Fig.10 Synchronous fluorescence spectra of NOM in water treatment process
(2)水處理流程中不同腐植酸標準物質的結構變化分析。
由圖8 ~圖10 可知,3 種腐植酸標準物質的同步熒光光譜在水處理流程中的變化趨勢相似。均出現以下現象:相比于實驗水樣進水,混凝沉淀出水中腐植酸標準物質的各熒光峰強度明顯降低,460nm 和480 nm 處的特征熒光峰消失,說明該波長處的熒光基團較高程度地參與了混凝反應;相比于混凝沉淀出水,過濾出水的熒光譜帶與混凝沉淀出水的重疊,說明物理砂濾對腐植酸標準物質的熒光基團沒有影響;相比于過濾出水,隨著消毒反應時間的延長,各熒光基團的特征熒光峰強度逐漸降低,說明活性氯破環了腐植酸標準物質中類似羰基和酚羥基的含氧熒光基團,降低了各基團的熒光信號。
雖然各腐植酸標準物質的同步熒光光譜在水處理流程中的變化相似,但在熒光譜帶變化最大的混凝階段,各腐植酸標準物質中熒光基團的具體變化情況略有不同。如表9 所示,HA(3S101H)實驗水樣原在355 nm 和397 nm 的特征熒光峰,混凝后藍移至346 nm 和389 nm,461 nm 處熒光峰消失;FA(2S101F)實驗水樣原在360 nm 處的熒光峰藍移至346 nm,480 nm 處熒光峰消失;NOM(2R101N)實驗水樣原在355 nm 和387 nm 處的熒光峰藍移至346 nm 和384 nm。這主要是由于混凝過程中腐植酸標準物質的共軛芳香π 電子體系減少,導致取代基的空間結構發生了變化,使熒光峰的波長向短波方向移動。并且各腐植酸標準物質中熒光基團在混凝反應中與金屬離子的絡合程度不同,由表中熒光基團參與度發現,與HA(3S101H)和NOM(2R101N)中各熒光基團的參與度相比,FA(2S101F)在360 nm 處的熒光基團參與反應程度最大,數值為70.72%;其次為HA(3S101H)在397 nm 處的熒光基團,參與程度為69.15%;最小為NOM(2R101N)在387 nm 處熒光基團參與度,數值為66.20%。結合混凝階段PAC 對腐植酸標準物質去除率FA >HA >NOM,說明混凝效果與腐植酸標準物質各熒光基團參與程度呈正比關系。由于熒光指數FI 值與芳香性為負相關關系[18],對3種腐植酸標準物質混凝前后的熒光強度(FI 值)進行檢測得知,HA、FA、NOM 實驗水樣的FI 值分別為0.978、0.977、1.014,混凝后FI 值為1.252、1.324、1.245,發現3 種腐植酸標準物質混凝后FI值都呈現了一定程度的增長,說明腐植酸標準物質的芳香結構參與了反應,并且FI 值增長程度為:FA >HA >NOM,這與混凝去除率大小順序一致,再次驗證了基團參與反應程度和混凝效果息息相關。
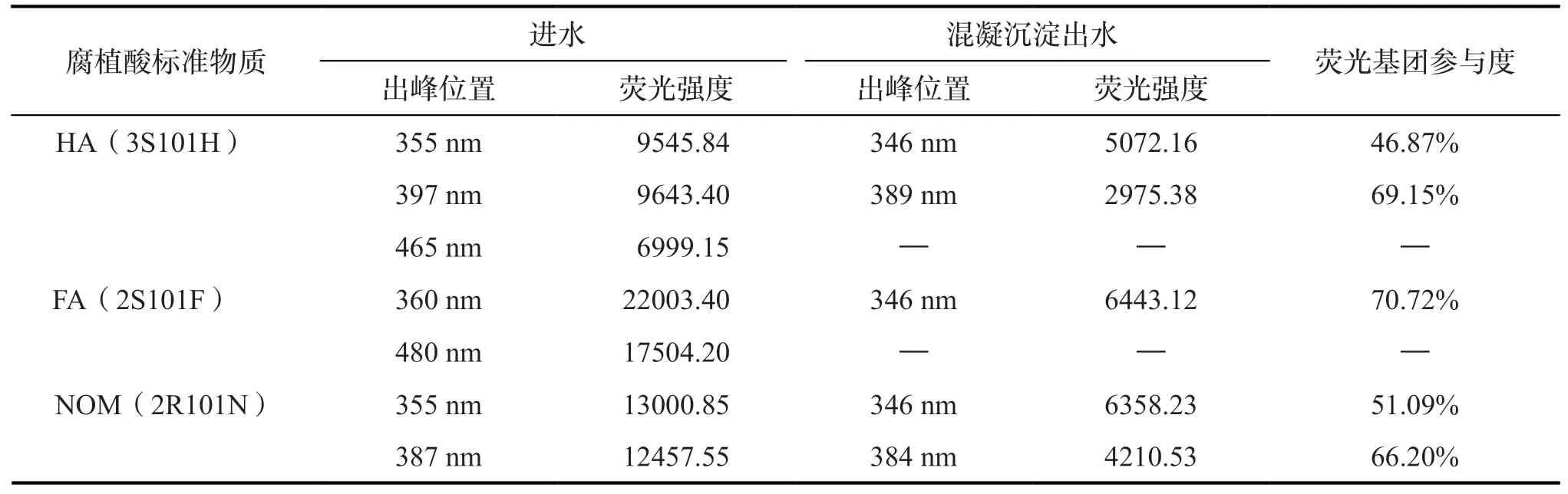
表9 混凝階段各腐植酸標準物質特征熒光峰的變化情況Tab.9 Changes of characteristic fluorescence peaks of humic acid standard materials in coagulation stage
3 結論與展望
(1)采用熒光定量技術對來自同流域中的3種腐植酸標準物質在水處理流程中進行定量分析,發現3 種腐植酸標準物質在水處理流程中的質量濃度與其TOC 和UV254均呈現較高的相關性,說明采用熒光基團標定的腐植酸標準物質質量濃度在實現精準定量的同時也可以用于各種水體的腐植酸的定量分析。
(2)通過3 種腐植酸標準物質生成的消毒副產物對比分析,發現HA(3S101H)和NOM(2R101N)的主要氯代中間產物為CH3-CO-Cl3,FA(2S101F)的主要氯代中間產物有HO-CO-Cl2和CH3-CO-Cl3。腐植酸標準物質在消毒過程中其熒光定量的質量濃度與消毒副產物生成量具有較好的相關性,表明熒光基團參與了消毒反應。
(3)由紫外參數的分析可知,腐植酸標準物質的結構特性差異影響了其在不同水處理流程的處理效果,尤其是混凝和消毒工藝流程。由同步熒光光譜比對發現,HA(3S101H)中含有與NOM(2R101N)和FA(2S101F)相同的熒光基團,但不同腐植酸標準物質中相似基團的含量占比不同。不同腐植酸標準物質中各熒光基團在混凝階段的參與程度也不相同,基團參與反應程度和混凝效果呈正比。
本文通過研究腐植酸標準物質HA(3S101H)、FA(2S101F)和NOM(2R101N)與產生的消毒副產物HAAs、THMs 之間的關系,為今后研究腐植酸在水處理流程中的變化提供了思路,對飲用水中存在的腐植酸的隱患提供了安全保障,為生活飲用水及環境水體中腐植酸的檢測提供技術支持。

