人參皂苷Rg3通過抑制mTOR通路介導的磷酸戊糖途徑對肺癌細胞的放射增敏作用
黃琳 李彬 胡作為

摘要:目的 探討人參皂苷Rg3通過抑制哺乳動物雷帕霉素靶蛋白(mTOR)通路介導的磷酸戊糖途徑(PPP),對肺癌細胞放射敏感性的影響。方法 以0、10、20、40、60、80 mg/L的人參皂苷Rg3處理肺癌細胞A549;MTT法檢測細胞增殖情況;將細胞分為對照組(正常培養,不照射)、放射組(X射線照射處理)、人參皂苷Rg3組(60 mg/L人參皂苷Rg3,不照射)、聯合組(X射線照射+60 mg/L人參皂苷Rg3)、激活劑組(X射線照射+60 mg/L人參皂苷Rg3+100 nmol/L mTOR通路激活劑MHY1485);均為加入相對應藥物培養48 h后放射組、聯合組和激活劑組采用8 Gy X射線照射。平板克隆實驗檢測各組細胞克隆形成率;酶聯免疫吸附試驗(ELISA)測定各組細胞葡萄糖-6-磷酸脫氫酶(G6PD)、還原型煙酰胺腺嘌呤二核苷酸磷酸(NADPH)水平;DCFH-DA熒光探針法檢測細胞內活性氧(ROS)水平;流式細胞儀檢測細胞凋亡;γ-H2AX免疫熒光染色分析DNA損傷修復情況;Western blot檢測細胞中mTOR、p-mTOR、增殖細胞核抗原(PCNA)、Bcl-2相關X蛋白(Bax)、胱天蛋白酶3(caspase-3)、γ-H2AX蛋白的表達。結果 人參皂苷Rg3以劑量依賴性的方式抑制A549細胞的增殖(P<0.05);與對照組比較,放射組、人參皂苷Rg3組細胞克隆形成率、G6PD、ROS、NADPH水平下降,p-mTOR/mTOR、PCNA蛋白表達水平降低,細胞凋亡率、γ-H2AX焦點數、Bax、caspase-3、γ-H2AX蛋白表達水平升高(P<0.05);與放射組、人參皂苷Rg3組比較,聯合組細胞克隆形成率、G6PD、ROS、NADPH水平下降,p-mTOR/mTOR、PCNA蛋白表達水平降低,細胞凋亡率、γ-H2AX焦點數、Bax、caspase-3、γ-H2AX蛋白表達升高(P<0.05);與聯合組比較,激活劑組細胞克隆形成率、G6PD、ROS、NADPH水平升高,p-mTOR/mTOR、PCNA蛋白表達水平升高,細胞凋亡率、γ-H2AX焦點數、Bax、caspase-3、γ-H2AX蛋白表達水平降低(P<0.05)。結論 人參皂苷Rg3發揮抑制肺癌作用可能是通過抑制mTOR介導的PPP實現的。
關鍵詞:人參皂苷Rg3;肺腫瘤;輻射耐受性;輻射增敏藥;磷酸戊糖途徑;哺乳動物雷帕霉素靶蛋白
中圖分類號:R285,R734.2 文獻標志碼:A DOI:10.11958/20222018
The radiosensitizing effect of ginsenoside Rg3 on lung cancer cells by inhibiting mTOR pathway-mediated pentose phosphate pathway
HUANG Lin, LI Bin, HU Zuowei
Department of Oncology, Wuhan NO.1 Hospital, Wuhan 430000, China
Corresponding Author E-mail: 827823053@qq.com
Abstract: Objective To investigate the influence of ginsenoside Rg3 on the radiosensitivity of lung cancer cells by inhibiting the pentose phosphate pathway (PPP) mediated by mammalian target of rapamycin (mTOR) pathway. Methods A549 lung cancer cells were treated with 0, 10, 20, 40, 60, 80 mg/L ginsenoside Rg3. The proliferation of A549 cells was detected by MTT method. Cells were divided into the control group (normal culture, no irradiation), the radiation group (X-ray irradiation), the ginsenoside Rg3 group (60 mg/L ginsenoside Rg3, no irradiation), the combination group (X-ray irradiation +60 mg/L ginsenoside Rg3) and the activator group (X-ray irradiation +60 mg/L ginsenoside Rg3+100 nmol/L mTOR pathway activator MHY1485). All of groups were irradiated by 8 GyX ray after 48 h of culture with corresponding drugs. Plate cloning experiment was applied to detect the formation rate of cell clones in each group. Enzyme-linked immunosorbent assay (ELISA) was applied to determine levels of glucose-6-phosphate dehydrogenase (G6PD) and reduced nicotinamide adenine dinucleotide phosphate (NADPH) in cell supernatant of each group. DCFH-DA fluorescent probe method was applied to detect the level of intracellular reactive oxygen species (ROS). Cell apoptosis was detected by flow cytometry. γ-H2AX immunofluorescence staining was applied to analyze DNA damage repair. Western blot assay was applied to detect expression levels of mTOR, p-mTOR, proliferating cell nuclear antigen (PCNA), Bcl-2-associated X protein (Bax), caspase-3 and γ-H2AX protein in cells. Results Ginsenoside Rg3 inhibited the proliferation of A549 cells in a dose-dependent manner (P<0.05). Compared with the control group, the cell clone formation rate, G6PD, ROS, NADPH levels, p-mTOR/mTOR and PCNA protein expressions were significantly decreased in the radiation group and the ginsenoside Rg3 group, and the cell apoptosis rate, γ-H2AX foci number, Bax, caspase-3, γ-H2AX protein expressions were significantly increased (P<0.05). Compared with the radiation group and the ginsenoside Rg3 group, the cell clone formation rate, G6PD, ROS, NADPH levels, p-mTOR/mTOR, and PCNA protein expressions were significantly decreased in the combination group, the cell apoptosis rate, γ-H2AX foci number, Bax, caspase-3, γ-H2AX protein expressions were significantly increased (P<0.05). Compared with the combination group, the cell clone formation rate, G6PD, ROS, NADPH levels, p-mTOR/mTOR and PCNA protein expressions were significantly increased in the activator group, and the cell apoptosis rate, γ-H2AX foci number, Bax, caspase-3, γ-H2AX protein expressions were significantly decreased (P<0.05). Conclusion The inhibitory effect of ginsenoside Rg3 on lung cancer cells may be realized through inhibition of PPP mediated by mTOR.
Key words: Ginsenoside Rg3; lung neoplasms; radiation tolerance; radiation-sensitizing agents; pentose phosphate pathway; mammalian target of rapamycin
肺癌是全球最常見的惡性疾病之一,近年來,其發病率和死亡率迅速上升[1]。肺癌分為小細胞肺癌和非小細胞肺癌(NSCLC),其中以NSCLC較為多見[2]。放療是肺癌的主要治療方法之一,手術切除加放療可延長患者無病生存期和總生存期[3]。放療效果會受各方面影響,如何在不增加不良反應的前提下進一步增強放射治療效果,提高患者的生活質量是國內外研究熱點[4-5]。研究發現,人參皂苷Rg3是一種潛在的治療NSCLC的天然藥物[6-7]。人參皂苷Rg3能減弱放化療不良反應,增強肺癌細胞對放射的敏感性[8-9]。此外,抑制哺乳動物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)通路介導的糖酵解作用可增強NSCLC細胞的放療敏感性[10]。Tsouko等[11]發現,mTOR介導的磷酸戊糖途徑(pentose phosphate pathway,PPP)在前列腺癌細胞的生長中發揮促進作用。下調mTOR通路可抑制PPP和脂肪生成,從而降低黑色素瘤對維穆拉非尼的耐藥性[12]。但人參皂苷Rg3能否通過抑制mTOR通路介導的PPP影響肺癌細胞對放射的敏感性尚不明確。本研究旨在探討人參皂苷Rg3通過抑制mTOR通路介導的PPP,對肺癌細胞放射增敏的影響。
1 材料與方法
1.1 主要試劑及儀器
人肺癌細胞A549購于上海匹拓生物科技有限公司。人參皂苷Rg3、mTOR通路激活劑MHY1485購于北京伊塔生物科技有限公司;MTT試劑購于美國Sigma公司;兔源一抗Bcl-2相關X蛋白(Bax)、胱天蛋白酶3(caspase-3)、增殖細胞核抗原(PCNA)及辣根過氧化物酶標記的羊抗兔二抗均購于英國Abcam公司;兔源一抗磷酸化γ-H2AX組蛋白H2AX、mTOR、p-mTOR均購于Proteintech中國公司;葡萄糖-6-磷酸脫氫酶(glucose-6-phosphate de-hydrogenase,G6PD)、酶聯免疫吸附試驗(ELISA)試劑盒、還原型煙酰胺腺嘌呤二核苷酸磷酸(nicotinamide adenine dinucleotide phosphate,NADPH)ELISA試劑盒購于上海富雨生物科技有限公司;DCFH-DA活性氧(ROS)熒光探針購于北京索萊寶科技有限公司;蛋白提取試劑盒購自亞科因(武漢)生物公司;DNA損傷檢測試劑盒(γ-H2AX免疫熒光法)購于廣州威佳科技有限公司;多功能全自動酶標儀購于南京德鐵實驗設備有限公司;離心機購于艾本德中國有限公司;電泳儀購于美國Bio-Rad公司;流式細胞儀購于美國BD公司;srt100放療劑量儀購于北京康科達有限公司。
1.2 細胞培養
將A549細胞置于DMEM的培養基中,在恒溫培養箱中常規培養,培養條件為37 ℃、5%CO2。定期觀察,及時更換新的培養基,當細胞融合度達到85%以上時,用0.25%胰蛋白酶消化傳代,收集對數生長期的細胞進行實驗。
1.3 MTT法檢測細胞增殖情況
將對數生長期A549細胞以1×104個/孔,接種到96孔板中,放入5%CO2、37 ℃細胞培養箱中孵育,設6個復孔,培養24 h后吸去原培養液,加入含0、10、20、40、60、80 mg/L人參皂苷Rg3[13]的培養液48 h后,加入MTT溶液20 μL/孔,再培養4 h后,加入二甲基亞砜150 μL/孔,在搖床上充分振蕩后,在酶標儀上于490 nm波長處檢測各孔的吸光度(A490)值,細胞增殖抑制率(%)=[(A對照-A實驗)/(A對照-A空白)]×100%。
1.4 平板克隆實驗檢測各組細胞克隆形成能力
將對數生長期A549細胞接種在直徑60 mm細胞培養板中,將A549細胞分為對照組(正常培養,不照射)、放射組(X射線照射)、人參皂苷Rg3組(60 mg/L人參皂苷Rg3,不照射)、聯合組(X射線照射+60 mg/L人參皂苷Rg3)、激活劑組(X射線照射+60 mg/L人參皂苷Rg3+100 nmol/L MHY1485[14])。培養24 h,待細胞貼壁后加入相對應藥物培養48 h后,放射組、聯合組及激活劑組給予8 Gy X射線照射,照射后立即更換培養液,繼續培養14 d,甲醇固定細胞10 min,吉姆薩液染色30 min,水洗,干燥,計數克隆細胞數。計算細胞克隆形成率=克隆細胞數/接種細胞數×100%。
1.5 細胞G6PD、ROS、NADPH水平測定
將各組A549細胞懸液制成勻漿后按照G6PD、NADPH ELISA試劑盒檢測說明書,檢測細胞內G6PD、NADPH水平,用DCFH-DA探針通過流式細胞術檢測細胞ROS的水平。
1.6 流式細胞儀檢測細胞凋亡
將各組A549細胞以預冷的PBS洗滌2次,添加100 μL結合緩沖液懸浮各組A549細胞,再分別添加Annexin V-FITC和PI染液5 μL,充分混勻,于室溫下避光染色15 min,離心棄上清液,加入0.5 mL PBS重懸細胞,使用流式細胞儀檢測細胞凋亡情況。
1.7 γ-H2AX免疫熒光染色分析DNA損傷修復情況
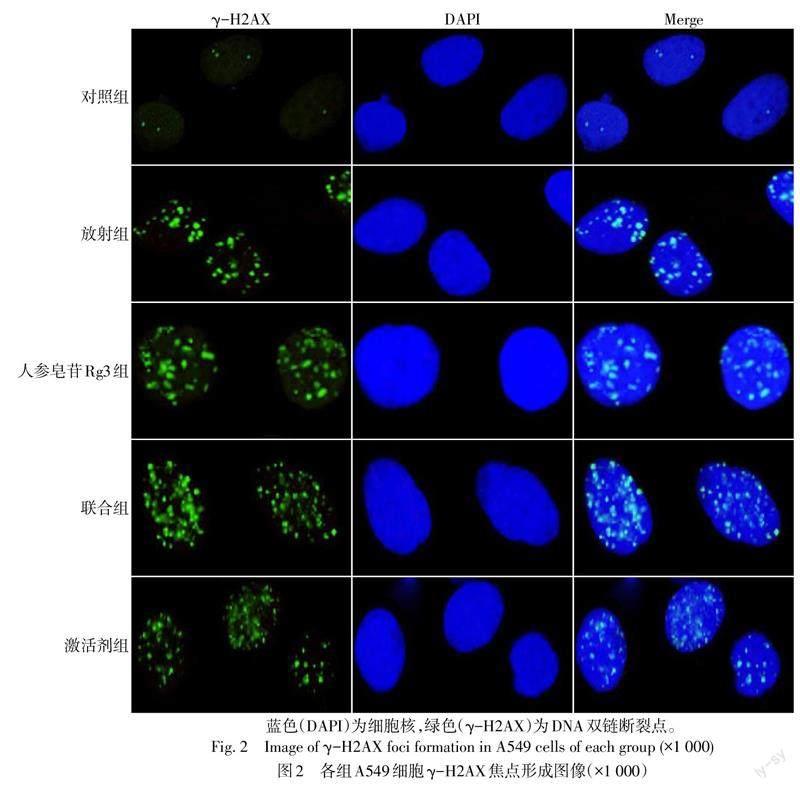
將對數生長期A549細胞爬片接種至培養皿中,培養24 h后,待細胞貼壁后按1.4描述的方法對各組進行相應處理,再培養48 h,用4 Gy X射線照射各組細胞,照射結束記為0 h,照射后立即更換培養液,3 h后收集細胞進行固定和免疫熒光染色。用含DAPI的抗熒光淬滅封片液進行封片,利用熒光顯微鏡觀察并拍照,計算每個細胞γ-H2AX平均焦點數。
1.8 Western blot檢測細胞中mTOR、p-mTOR、PCNA、Bax、caspase-3、γ-H2AX蛋白表達
提取各組A549細胞的總蛋白,定量后進行聚丙烯酰胺凝膠電泳。轉膜后室溫條件下封閉2 h,最后再分別加入mTOR(1∶1 000)、p-mTOR(1∶1 000)、PCNA(1∶2 000)、Bax(1∶2 000)、caspase-3(1∶2 000)、γ-H2AX(1∶1 000)一抗在4 ℃條件下孵育過夜,加入二抗(1∶4 000)在室溫條件下孵育90 min,使用GAPDH作為內源性對照。最后分析各個蛋白條帶的灰度值,計算各蛋白的相對表達水平。
1.9 統計學方法
采用Graphpad Prism 7.0軟件進行數據分析。計量資料以x±s表示。多組間比較采用單因素方差分析,組間多重比較采用SNK-q檢驗。P<0.05為差異有統計學意義。
2 結果
2.1 人參皂苷Rg3對細胞的增殖的影響
經0、10、20、40、60、80 mg/L人參皂苷Rg3處理的A549細胞增殖抑制率(%)分別為0、10.21±2.16、14.89±2.48、28.57±3.48、42.58±4.21和58.64±4.38,10、20、40、60、80 mg/L人參皂苷Rg3處理的A549細胞增殖抑制率相比0 mg/L人參皂苷Rg3處理下,以劑量依賴性的方式升高(n=6,F=288.244,P<0.05),人參皂苷Rg3對A549細胞的IC50為69.18 mg/L,本研究選取60 mg/L人參皂苷Rg3進行后續實驗。
2.2 各組細胞克隆形成率變化
對照組、放射組、人參皂苷Rg3組、聯合組、激活劑組細胞克隆形成率(%)分別為98.23±4.82、76.54±3.74、54.31±3.58、37.82±3.43和58.61±3.66,差異有統計學意義(n=6,F=212.563,P<0.05)。與對照組比較,放射組、人參皂苷Rg3組細胞克隆形成率降低(P<0.05);與放射組、人參皂苷Rg3組比較,聯合組細胞克隆形成率降低(P<0.05);與聯合組比較,激活劑組細胞克隆形成率升高(P<0.05)。
2.3 各組細胞凋亡水平變化
對照組、放射組、人參皂苷Rg3組、聯合組和激活劑組細胞凋亡率(%)分別為10.36±2.14、18.48±3.10、23.25±2.68、45.58±3.45和24.65±3.21,差異有統計學意義(n=6,F=117.396,P<0.05)。與對照組相比較,放射組、人參皂苷Rg3組細胞凋亡率升高(P<0.05);與放射組、人參皂苷Rg3組比較,聯合組細胞凋亡率升高(P<0.05),與聯合組比較,激活劑組細胞凋亡率降低(P<0.05),見圖1。
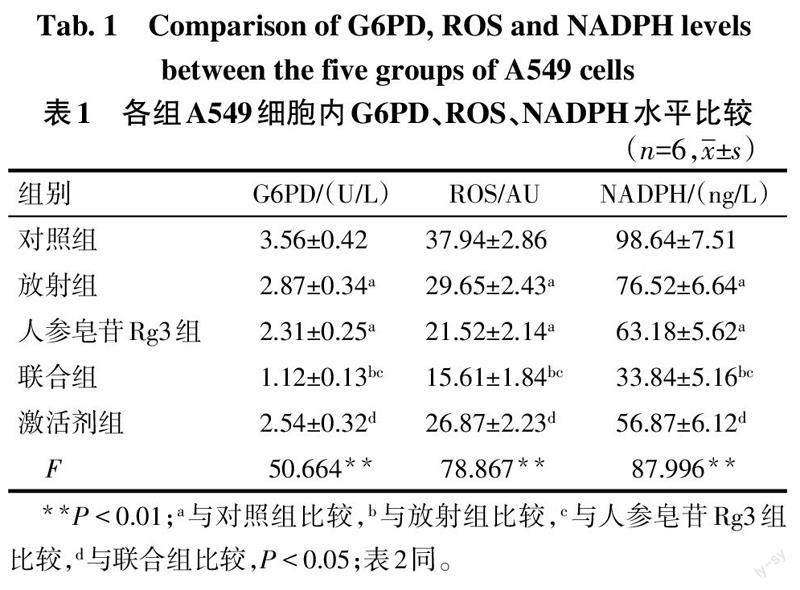
2.4 各組細胞內G6PD、ROS、NADPH水平比較
與對照組比較,放射組、人參皂苷Rg3組G6PD、ROS、NADPH水平降低(P<0.05);與放射組、人參皂苷Rg3組比較,聯合組G6PD、ROS、NADPH水平降低(P<0.05);與聯合組比較,激活劑組G6PD、ROS、NADPH水平升高(P<0.05)。見表1。
2.5 各組細胞中γ-H2AX焦點數比較
對照組、放射組、人參皂苷Rg3組、聯合組和激活劑組γ-H2AX焦點數(個/視野)分別為3.14±0.70、22.15±2.17、27.68±2.54、43.32±3.46和25.71±2.68,差異有統計學意義(n=6,F=201.470,P<0.05)。與對照組比較,放射組、人參皂苷Rg3組細胞內γ-H2AX焦點數增加(P<0.05);與放射組、人參皂苷Rg3組比較,聯合組細胞內γ-H2AX焦點數增加(P<0.05);與聯合組比較,激活劑組細胞內γ-H2AX焦點數減少(P<0.05),見圖2。
2.6 各組細胞mTOR、p-mTOR、PCNA、Bax、caspase-3、γ-H2AX蛋白表達水平比較
與對照組比較,放射組、人參皂苷Rg3組p-mTOR/mTOR、PCNA蛋白表達水平降低,Bax、caspase-3、γ-H2AX蛋白表達水平升高(P<0.05);與放射組、人參皂苷Rg3組比較,聯合組p-mTOR/mTOR、PCNA蛋白表達水平降低,Bax、caspase-3、γ-H2AX蛋白表達水平升高(P<0.05);與聯合組比較,激活劑組p-mTOR/mTOR、PCNA蛋白表達水平升高,Bax、caspase-3、γ-H2AX蛋白表達水平降低(P<0.05)。見圖3、表2。
3 討論
肺癌已成為人類癌癥死亡的主要原因之一,嚴重威脅著患者的生活質量和生命安全[15]。尋找安全有效的治療肺癌藥物具有重要意義。人參皂苷Rg3是人參中的主要活性成分,具有廣泛藥理作用,如抗疲勞、抗氧化、降血糖、增強免疫功能等[7]。此外,人參皂苷Rg3在腫瘤的預防和治療中發揮重要的作用,不僅可以抑制乳腺癌[16]、消化系統腫瘤[17]、肺癌等癌癥的發生發展,還可提高肺癌對放療的敏感性[8-9,18]。γ-H2AX蛋白是DNA損傷標志物,其產生的數量與DNA雙鏈斷裂呈正相關[19]。PCNA蛋白可以反映細胞增殖狀態,其表達水平越高,表明細胞增殖越快。caspase-3是細胞凋亡過程中的剪切酶,Bax是細胞中的凋亡蛋白,在細胞發生凋亡時,Bax、caspase-3蛋白表達量水平顯著升高[20-21]。本研究發現,人參皂苷Rg3通過抑制A549細胞的增殖,降低PCNA蛋白表達和細胞克隆形成率,提高Bax、caspase-3、γ-H2AX蛋白表達和細胞凋亡率,增加γ-H2AX焦點數,從而發揮抑制肺癌作用,聯合X射線照射效果更強。
G6PD是PPP的限速酶,PPP產生的NADPH作為供氫體參與脂肪酸、氧化還原等代謝過程。G6PD在正常細胞的表達及活性被嚴格控制,而在腫瘤細胞其活性被異常激活,G6PD穩定敲低可以抑制癌細胞的遷移[22]。PPP通過提供DNA損傷修復原料及NADPH,在DNA損傷修復過程中起重要作用[23]。研究發現,清燥救肺湯(主要成分枇杷葉、麥冬、黨參片等)通過抑制G6PD和NADPH氧化酶表達、減少ROS含量,抑制PPP,從而發揮抑制肺癌的作用[24]。本研究中人參皂苷Rg3與X射線照射抑制DNA損傷修復可能是通過降低G6PD、NADPH及ROS水平來實現的。另有研究表明,抑制mTOR介導的PPP在抑制腫瘤生長,克服耐藥性方面發揮重要作用[11-12]。Marquard等[25]研究發現,激活的mTOR信號通路可能通過增強DNA修復機制,與放療敏感性和細胞抑制藥物的耐藥性有關,而使用mTOR的抑制劑后,可顯著抑制細胞和小鼠模型中的腫瘤細胞增殖,增強放射敏感性。本研究發現,使用mTOR激活劑不但可以減弱人參皂苷Rg3聯合X射線照射對A549細胞增殖及DNA損傷修復的抑制作用,而且還能減弱對細胞凋亡的促進及放射敏感性的增強作用,提示人參皂苷Rg3發揮抑制肺癌的作用可能是通過抑制mTOR介導的PPP實現的。
綜上所述,人參皂苷Rg3可能通過抑制mTOR介導的PPP,抑制A549細胞增殖、促進細胞凋亡、加速細胞DNA損傷,進而增強A549細胞對放療的敏感性。但本研究僅在細胞水平上進行驗證,后續將在體內進行進一步探索。
參考文獻
[1] BADE B C,DELA CRUZ C S. Lung Cancer 2020:epidemiology,etiology,and prevention[J]. Clin Chest Med,2020,41(1):1-24. doi:10.1016/j.ccm.2019.10.001.
[2] HOWLADER N,FORJAZ G,MOORADIAN M J,et al. The effect of advances in lung-cancer treatment on population mortality[J]. N Engl J Med,2020,383(7):640-649. doi:10.1056/NEJMoa1916623.
[3] HUI Z,MEN Y,HU C,et al. Effect of postoperative radiotherapy for patients with pIIIA-N2 non-small cell lung cancer after complete resection and adjuvant chemotherapy:the phase 3 PORT-C randomized clinical trial[J]. JAMA Oncol,2021,7(8):1178-1185. doi:10.1001/jamaoncol.2021.1910.
[4] JIE X,FONG W P,ZHOU R,et al. USP9X-mediated KDM4C deubiquitination promotes lung cancer radioresistance by epigenetically inducing TGF-β2 transcription[J]. Cell Death Differ,2021,28(7):2095-2111. doi:10.1038/s41418-021-00740-z.
[5] LIU Y,CROWE W N,WANG L,et al. An inhalable nanoparticulate STING agonist synergizes with radiotherapy to confer long-term control of lung metastases[J]. Nat Commun,2019,10(1):5108. doi:10.1038/s41467-019-13094-5.
[6] 王愛華,劉維,金玥,等. 人參皂苷Rg3:一種潛在的治療非小細胞肺癌的天然藥物[J]. 中華中醫藥學刊,2022,40(2):156-159,272. WANG A H,LIU W,JIN Y,et al. Ginsenoside Rg3:a potential natural drug in treatment of non-small cell lung cancer[J]. Chinesearchives of traditional chinese medicine,2022,40(2):156-159,272. doi:10.13193/j.issn.1673-7717.2022.02.03.
[7] 喬雪涵,岳麗玲,朱文斌. 人參皂苷Rg3的抗腫瘤作用研究現狀[J]. 中國臨床藥理學雜志,2021,37(10):272-1276. QIAO X H,YUE L L,ZHU W B. Research progress of ginsenoside Rg3 in anticancer effects[J]. Chin J Clin Pharmacol,2021,37(10):272-1276. doi:10.13699/j.cnki.1001-6821.2021.10.032.
[8] 黃琳,李彬,胡作為. 人參皂苷Rg3通過調控PXN-AS1促進肺癌放射增敏的機制探討[J]. 中西醫結合研究,2022,14(4):239-242,252. HUANG L,LI B,HU Z W. Mechanism of ginsenoside Rg3 promoting radiosensitization in lung cancer by regulating PXN-AS1[J]. Research of Integrated Traditional Chinese and Western MedicineAug,2022,14(4):239-242,252. doi:10.3969/j.issn.1674-4616.2022.04.006.
[9] YANG M,SHEN C,ZHU S J,et al. Chinese patent medicine Aidi injection for cancer care:an overview of systematic reviews and meta-analyses[J]. J Ethnopharmacol,2022,282:114656. doi:10.1016/j.jep.2021.114656.
[10] 張樸花,徐志廣. 苦參堿通過抑制mTOR通路介導的糖酵解作用增強非小細胞肺癌細胞的放療敏感性[J]. 中藥材,2020,43(10):2559-2564. ZHANG P H,XU Z G. Matrine enhances the radiosensitivity of non-small cell lung cancer cells by inhibiting mTOR pathway-mediated glycolysis[J]. Journal of Chinese Medicinal Materials,2020,43(10):2559-2564. doi:10.13863/j.issn1001-4454.2020.10.040.
[11] TSOUKO E,KHAN A S,WHITE M A,et al. Regulation of the pentose phosphate pathway by an androgen receptor-mTOR-mediated mechanism and its role in prostate cancer cell growth[J]. Oncogenesis,2014,3(5):e103. doi:10.1038/oncsis.2014.18.
[12] WANG L,OTKUR W,WANG A,et al. Norcantharidin overcomes vemurafenib resistance in melanoma by inhibiting pentose phosphate pathway and lipogenesis via downregulating the mTOR pathway[J]. Front Pharmacol,2022,13:906043. doi:10.3389/fphar.2022.906043.
[13] 孟子琪,張睿,吳旭微,等. 人參皂苷Rg3靶向Wnt/β-連環蛋白信號通路調控胃癌順鉑耐藥性[J]. 中國醫學科學院學報,2022,44(3):366-376. MENG Z Q,ZHANG R,WU X W,et al. Ginsenoside Rg3 regulates cisplatin resistance in gastrsc cancer by Wnt/β-catenin signaling pathway[J]. Acta Academiae Medicinae Sinicae,2022,44(3):366-376. doi:10.3881/j.issn.1000-503X.14775
[14] 姚劉旭,滕文彬,黃素琴,等. mTOR/P70S6K/HIF-1α信號通路在脂多糖誘導Caco-2細胞屏障損傷中的作用及機制[J]. 中國病理生理雜志,2022,38(1):122-129. YAO L X,TENG W B,HUANG S Q,et al. Role of mTOR/P70S6K/HIF-1α signaling pathway in Caco-2 cell barrier injury induced by lipopolysaccharide[J]. Chinese Journal of Pathophysiology,2022,38(1):122-129. doi:10.3969/j.issn.1000-4718.2022.01.016.
[15] TOUMAZIS I,BASTANI M,HAN S S,et al. Risk-based lung cancer screening:a systematic review[J]. Lung Cancer,2020,147:154-186. doi:10.1016/j.lungcan.2020.07.007.
[16] NAKHJAVANI M,HARDINGHAM J E,PALETHORPE H M,et al. Ginsenoside Rg3:potential molecular targets and therapeutic indication in metastatic breast cancer[J]. Medicines(Basel),2019,6(1):17-36. doi:10.3390/medicines6010017.
[17] PAN L,ZHANG T,SUN H,et al. Ginsenoside Rg3(Shenyi Capsule) combined with chemotherapy for digestive system cancer in China:a meta-analysis and systematic review[J]. Evid Based Complement Alternat Med,2019,2019:2417418. doi:10.1155/2019/2417418.
[18] LIANG Y,ZHANG T,JING S,et al. 20(S)-Ginsenoside Rg3 inhibits lung cancer cell proliferation by targeting EGFR-mediated Ras/Raf/MEK/ERK pathway[J]. Am J Chin Med,2021,49(3):753-765. doi:10.1142/S0192415X2150035X.
[19] PLAPPERT-HELBIG U,LIBERTINI S,FRIEAUFF W,et al. Gamma-H2AX immunofluorescence for the detection of tissue-specific genotoxicity in vivo[J]. Environ Mol Mutagen,2019,60(1):4-16. doi:10.1002/em.22238.
[20] GONZáLEZ-MAGA?A A,BLANCO F J. Human PCNA structure,function and interactions[J]. Biomolecules,2020,10(4):570-588. doi:10.3390/biom10040570.
[21] WANG Z,CHEN X,LIU N,et al. A nuclear long non-coding RNA LINC00618 accelerates ferroptosis in a manner dependent upon apoptosis[J]. Mol Ther,2021,29(1):263-274. doi:10.1016/j.ymthe.2020.09.024.
[22] 白宏剛,張巧,況應敏,等. 葡萄糖-6-磷酸脫氫酶穩定敲低對腎透明細胞癌細胞遷移的抑制作用[J]. 醫學研究生學報,2018,31(7):697-702. BAI H G,ZHANG Q,KUANG Y M,et al. Stable G6PD knockdown inhibits the migration of renal cell carcinoma cells[J].J Med Postgra,2018,31(7):697-702. doi:10.16571/j.cnki.1008-8199.2018.07.006.
[23] 郭翠,唐然,江世杰,等. 耐輻射異常球菌磷酸戊糖途徑對DNA損傷修復的影響[J]. 核農學報,2016,30(2):252-258. GUO C,TANG R,JIANG S J,et al. Effects of pentose phosphate pathway on DNA damage repair in deinococcus radiodurans[J]. Journal of Nuclear Agricultural Sciences,2016,30(2):252-258. doi:10.11869/j.issn.100-8551.2016.02.0252.
[24] 陳江濤,余功,謝斌. 清燥救肺湯對肺癌磷酸戊糖能量代謝途徑的關鍵酶G6PD活性及其調控因子的影響[J]. 中國實驗方劑學雜志,2020,26(4):59-63. CHEN J T,XU G,XIE B. Effect of Qingzao Jiufei Tang on enzymatic activity and regulatory factor of key enzyme G6PD in pentose phosphate energy metabolism pathway in lung cancer[J]. Chinese Journal of Experimental Traditional Medical Formulae,2020,26(4):59-63. doi:10.13422/j.cnki.syfjx.20200426.
[25] MARQUARD F E,J?CKER M. PI3K/AKT/mTOR signaling as a molecular target in head and neck cancer[J]. Biochem Pharmacol,2020,172:113729. doi:10.1016/j.bcp.2019.113729.
(2022-12-08收稿 2023-02-10修回)
(本文編輯 李志蕓)

