過磷酸鈣反應(yīng)原理再剖析
顏 鑫
(湖南化工職業(yè)技術(shù)學(xué)院化學(xué)工程學(xué)院 湖南株洲 412004)
化工生產(chǎn)中有些化學(xué)反應(yīng)是一步完成的,有些分為兩步、三步甚至多步才能完成,這些分步反應(yīng)常有一個(gè)顯著的特點(diǎn),就是兩步或多步反應(yīng)相加應(yīng)等于總反應(yīng)。普通過磷酸鈣(簡稱過磷酸鈣,亦稱普鈣)是一種最常用的水溶性速效磷肥,主要成分是水合磷酸二氫鈣[Ca(H2PO4)2·H2O,又稱磷酸一鈣]和CaSO4,其生產(chǎn)原理由兩步組成[1-2]。第一步由H2SO4分解磷礦粉[主要成分是氟磷酸鈣Ca5(PO4)3F]產(chǎn)生H3PO4、CaSO4和HF,第二步由產(chǎn)生的H3PO4與剩余的磷礦粉反應(yīng)生成Ca(H2PO4)2·H2O和HF,化學(xué)反應(yīng)過程如下:
第一步:Ca5(PO4)3F+5H2SO4→5CaSO4+3H3PO4+HF↑
(1)
第二步:Ca5(PO4)3F+7H3PO4+5H2O→5Ca(H2PO4)2·H2O+HF↑
(2)
總反應(yīng):2Ca5(PO4)3F+7H2SO4+3H2O→7CaSO4+3Ca(H2PO4)2·H2O+2HF↑
(3)
副反應(yīng):Ca5(PO4)3F+2H3PO4+10H2O→5CaHPO4·2H2O+HF↑
(4)
3Ca5(PO4)3F+H3PO4+10H2O→
5Ca3(PO4)2·2H2O+3HF↑
(5)
第一步反應(yīng)中的CaSO4為CaSO4·1/2H2O,第二步反應(yīng)結(jié)束后才轉(zhuǎn)化為無水CaSO4,為了簡化反應(yīng)過程,直接用無水CaSO4代替。在實(shí)際生產(chǎn)中,這兩步反應(yīng)是過磷酸鈣生產(chǎn)過程的兩個(gè)不同階段,也是在不同反應(yīng)器中進(jìn)行的。第一步反應(yīng)主要在混合器中進(jìn)行,是快速放熱反應(yīng),反應(yīng)時(shí)間僅為1~6 min,所需時(shí)間取決于磷礦粉的種類及粒徑、H2SO4的濃度及溫度、混合器類型等;磷礦粉主要為粉碎至D90通過0.15 mm(100目)篩的磷灰石或磷塊巖粉末,混合器通常采用立式。第二步反應(yīng)在化成室和熟化倉庫中進(jìn)行,化成室又分為回轉(zhuǎn)化成室、皮帶化成室、鏈板化成室等,化成時(shí)間需要20~60 min,倉庫熟化時(shí)間需要7~30 d,才能使磷礦粉的總分解率達(dá)到94%~96%,所需時(shí)間取決于磷礦粉的種類及粒徑、H2SO4的濃度及溫度、化成器類型等。總反應(yīng)即H2SO4與磷礦粉反應(yīng)生成過磷酸鈣、CaSO4和HF。但是在《無機(jī)化工生產(chǎn)技術(shù)》教學(xué)過程中發(fā)現(xiàn),第一步反應(yīng)和第二步反應(yīng)相加并不等于總反應(yīng)。即使不考慮CaSO4和Ca(H2PO4)2分子式中結(jié)晶水的存在和轉(zhuǎn)化,上述兩個(gè)分步反應(yīng)式之和仍不等于總反應(yīng)式。
關(guān)于過磷酸鈣生產(chǎn)的化學(xué)原理在相關(guān)教材中已有大量闡述[1-2],本文在此只補(bǔ)充剖析兩個(gè)分步反應(yīng)與總反應(yīng)的關(guān)系、兩步反應(yīng)所分解的磷礦粉數(shù)量,并探討對過磷酸鈣實(shí)際生產(chǎn)的指導(dǎo)意義。
1 兩個(gè)分步反應(yīng)之和不等于總反應(yīng)的原因
1.1 磷酸分解的磷礦石物質(zhì)的量實(shí)際上不到硫酸物質(zhì)的量的1/3
第一步反應(yīng)屬于快速反應(yīng),反應(yīng)物H2SO4是二元強(qiáng)酸,且在反應(yīng)過程中得到了充分和完全的利用。第二步反應(yīng)中的H3PO4雖然是三元中強(qiáng)酸,但由于產(chǎn)物為Ca(H2PO4)2·H2O,是過磷酸鈣的主要成分,實(shí)際上磷酸相當(dāng)于一元酸參與反應(yīng),且反應(yīng)過程中未得到完全和充分的利用。
為簡化起見,暫不考慮磷礦粉中鈣鹽、鎂鹽和倍半氧化物等雜質(zhì)在第一步、第二步反應(yīng)中對H2SO4和H3PO4的消耗,僅以雜質(zhì)含量較少的過磷酸鈣優(yōu)等品為例進(jìn)行分析。由于第一步反應(yīng)中產(chǎn)生了HF,造成了酸的揮發(fā)流失,流失的HF與H3PO4的物質(zhì)的量之比為1∶9。因此,不僅理論上第一步反應(yīng)所消耗的H2SO4的物質(zhì)的量要多于所產(chǎn)生的H3PO4的物質(zhì)的量,而且是所產(chǎn)生的H3PO4(按一元酸計(jì))實(shí)際物質(zhì)的量的3倍以上,即理論上參與第二步反應(yīng)的磷礦粉的量還不到第一步反應(yīng)的1/3。實(shí)際上H2SO4分解的磷礦粉的量應(yīng)大于總量的2/3,H3PO4分解的磷礦粉的量小于總量的1/3。
1.2 兩個(gè)分步反應(yīng)需要乘以相應(yīng)系數(shù)再相加才等于總反應(yīng)
由國家標(biāo)準(zhǔn)《過磷酸鈣》(GB/T 20413—2017)可知,優(yōu)等品的有效磷(以P2O5計(jì))的質(zhì)量分?jǐn)?shù)≥18.0%,水溶性磷(以P2O5計(jì))的質(zhì)量分?jǐn)?shù)≥13.0%,游離H3PO4(以P2O5計(jì))的質(zhì)量分?jǐn)?shù)≤5.5%。假如典型的過磷酸鈣優(yōu)等品中有效磷、水溶性磷、游離H3PO4的質(zhì)量分?jǐn)?shù)分別按19%、14%、5%進(jìn)行計(jì)算,水溶性磷包括H3PO4和Ca(H2PO4)2·H2O,水溶性磷和游離H3PO4的含量之差即為Ca(H2PO4)2·H2O的含量(質(zhì)量分?jǐn)?shù)為9%);有效磷中另有枸溶性磷(以P2O5計(jì),質(zhì)量分?jǐn)?shù)5%),枸溶性磷主要成分為CaHPO4·2H2O(磷酸氫鈣)和Ca3(PO4)2·2H2O(磷酸三鈣),見反應(yīng)(4)和(5)。國家標(biāo)準(zhǔn)中各成分的質(zhì)量分?jǐn)?shù)和典型組成見表1。第一步反應(yīng)產(chǎn)生的H3PO4中只有9/19即47.4%的磷酸轉(zhuǎn)化為Ca(H2PO4)2·H2O,另外仍有5/19即26.3%的H3PO4轉(zhuǎn)化為枸溶性磷,其余作為游離酸存在于產(chǎn)品中。

表1 典型的過磷酸鈣優(yōu)等品組成(均以P2O5計(jì)) %
事實(shí)上,由于H2SO4用量通常為理論用量的103%~105%,是充分且完全利用的;H3PO4由于酸性較弱,反應(yīng)后期的磷礦粉粒徑較大、反應(yīng)活性較差,總有一定量的H3PO4和磷礦粉同時(shí)殘留于過磷酸鈣產(chǎn)品中,沒有得到充分分解和完全利用,因此H2SO4分解磷礦粉的量占磷礦粉總量超過2/3,而H3PO4分解的磷礦粉占比小于1/3。
基于上述分析,如果將第一步反應(yīng)乘以7/5,第二步反應(yīng)乘以3/5,然后再相加,兩步反應(yīng)的磷酸相互抵消,分步反應(yīng)式相加等于總反應(yīng)式。這說明在過磷酸鈣生產(chǎn)中,兩個(gè)分步反應(yīng)理論上不是1∶1的關(guān)系,而是7∶3的關(guān)系。因此,對于分步反應(yīng),有時(shí)直接相加不等于總反應(yīng)式,而要根據(jù)實(shí)際反應(yīng),乘以合適的系數(shù)后再相加才等于總反應(yīng)式。
2 兩步反應(yīng)分解的磷礦粉比例的推測
假設(shè)反應(yīng)(1)中H2SO4的理論物質(zhì)的量為10,則H3PO4的理論物質(zhì)的量為9。由于H3PO4只按一元酸參與反應(yīng),實(shí)際表觀物質(zhì)的量只有3,可見H2SO4的物質(zhì)的量是H3PO4的物質(zhì)的量的3.33倍。理論上H2SO4及其產(chǎn)生的H3PO4能夠使磷礦粉完全分解,則磷礦粉的總物質(zhì)的量應(yīng)為H2SO4和H3PO4的物質(zhì)的量之和13。當(dāng)H2SO4的實(shí)際用量是理論用量的105%時(shí),H2SO4的實(shí)際物質(zhì)的量為10.5,產(chǎn)生的H3PO4實(shí)際物質(zhì)的量為3.15,但磷礦粉的總物質(zhì)的量并未增加,仍然是13。當(dāng)過磷酸鈣產(chǎn)品中游離H3PO4的質(zhì)量分?jǐn)?shù)為5%左右時(shí),則可以推測出H2SO4實(shí)際分解磷礦粉的比例、H3PO4理論上和實(shí)際分別分解磷礦粉的比例、產(chǎn)品中殘留的磷礦粉比例等,數(shù)據(jù)見表2。
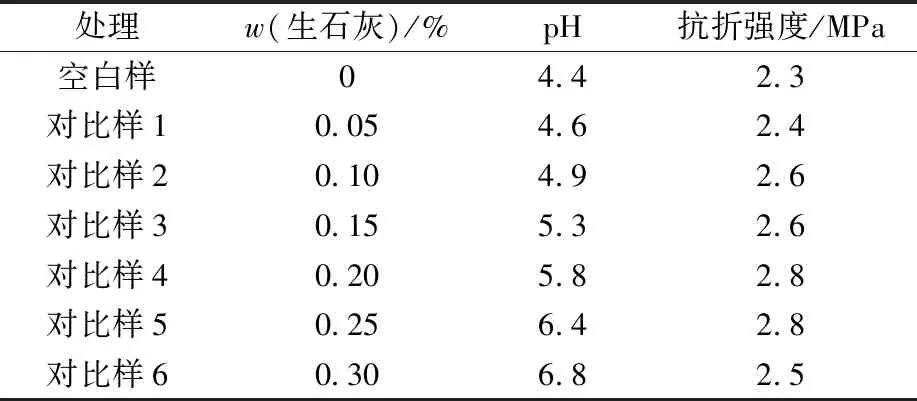
表2 不同生石灰加入量的試驗(yàn)結(jié)果

表2 過磷酸鈣優(yōu)等品生產(chǎn)參數(shù)的合理估算
推測過程:
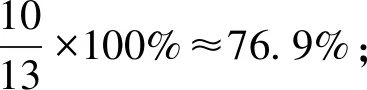
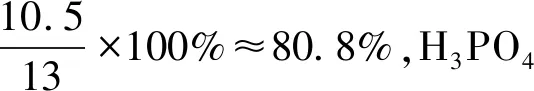
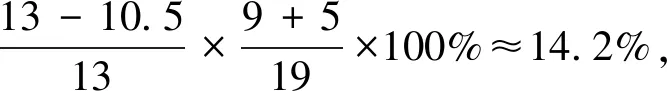
(4)計(jì)算H3PO4殘留物質(zhì)的量應(yīng)該為H3PO4實(shí)際物質(zhì)的量×游離H3PO4在枸溶性磷中所占比例26.3%,3.15×26.3%≈0.83。
表2中的推測數(shù)據(jù),如殘留的磷礦粉比例等與實(shí)際生產(chǎn)中的數(shù)據(jù)是非常接近的,說明推測的理論依據(jù)是可靠的。
3 對過磷酸鈣實(shí)際生產(chǎn)的指導(dǎo)意義
專著和教材上的內(nèi)容:第一步反應(yīng)理論上分解的磷礦粉占70%,第二步反應(yīng)理論上分解的磷礦粉占30%[1-2];由于實(shí)際H2SO4用量為理論用量的103%~105%,實(shí)際上第一步反應(yīng)分解的磷礦粉為72%~74%[1-2]。
由表2的數(shù)據(jù)可知,理論上第一步反應(yīng)H2SO4分解的磷礦粉約占76.9%,第二步反應(yīng)H3PO4分解的磷礦粉約占23.1%。在實(shí)際生產(chǎn)中,如果H2SO4用量按理論用量的105%進(jìn)行計(jì)算,則反應(yīng)第一階段約有80.8%的磷礦粉參與H2SO4的分解反應(yīng),剩下約19.2%的磷礦粉參與H3PO4的分解反應(yīng),但實(shí)際上H3PO4分解的磷礦粉僅為14.2%。
H2SO4用量超出理論用量越多,第一步反應(yīng)占比越大,過磷酸鈣產(chǎn)品中過量的H3PO4就越多,殘留的磷礦粉就越少。H2SO4過量的具體數(shù)值取決于磷礦粉的種類、反應(yīng)活性,也與H2SO4濃度和溫度等條件相關(guān)。一般來說,過量H2SO4的應(yīng)用并不會(huì)導(dǎo)致過磷酸鈣產(chǎn)品中有游離H2SO4的存在,因?yàn)镠2SO4的物質(zhì)的量相對磷礦粉的物質(zhì)的量始終都是不足的,而且游離H2SO4并不能與Ca(H2PO4)2共存,因?yàn)樯傻腃a(H2PO4)2也將與H2SO4反應(yīng)生成CaSO4和H3PO4,化學(xué)方程式如下:
Ca(H2PO4)2+H2SO4→CaSO4+2H3PO4
(6)
可見,適當(dāng)過量的H2SO4只是導(dǎo)致過磷酸鈣產(chǎn)品中少量H3PO4的殘留,并不影響產(chǎn)品的品質(zhì)和應(yīng)用。但仍然要嚴(yán)格控制H2SO4用量和比例,過剩系數(shù)一般不能超過1.05,以免游離H3PO4含量超過5%,造成游離H3PO4含量超過殘余磷礦粉含量,導(dǎo)致整個(gè)體系呈酸性。
4 結(jié)語
(1)過磷酸鈣生產(chǎn)反應(yīng)原理中,兩個(gè)分步反應(yīng)直接相加并不等于總反應(yīng),其本質(zhì)是第一步反應(yīng)所有H2SO4的物質(zhì)的量明顯大于第二步反應(yīng)H3PO4的物質(zhì)的量,H2SO4的物質(zhì)的量理論上是H3PO4的物質(zhì)的量的3.33倍。將第一步反應(yīng)式乘以系數(shù)7/5,第二步反應(yīng)式乘以系數(shù)3/5,才能抵消兩步反應(yīng)中的H3PO4,然后再相加,就等于總反應(yīng)式。這說明兩步反應(yīng)理論上不是1∶1的關(guān)系,而是7∶3的關(guān)系。
(2)理論上第一步反應(yīng)中H2SO4分解的磷礦粉應(yīng)占76.9%而不是70%,第二步反應(yīng)中H3PO4分解的磷礦粉理論上應(yīng)為23.1%而不是30%。
(3)實(shí)際生產(chǎn)中,由于H2SO4用量通常超過理論用量的5%,且H2SO4反應(yīng)完全,因此,過磷酸鈣優(yōu)等品中第一步反應(yīng)分解的磷酸粉應(yīng)為80.8%。由于H3PO4酸性較弱,反應(yīng)不充分,產(chǎn)品中殘留5%左右的游離H3PO4和5.1%的磷礦粉,殘留的游離H3PO4和磷礦粉的含量基本上是一致的,因此第二步反應(yīng)分解的磷礦粉為14.2%左右。
(4)本文依據(jù)過磷酸鈣的生產(chǎn)原理和理論,對實(shí)際生產(chǎn)中H2SO4用量的上限為理論用量的105%,造成游離H3PO4含量超過殘留磷礦粉含量以及整個(gè)體系呈酸性的情況進(jìn)行了切合實(shí)際的剖析,對正確估算游離H3PO4含量和殘留磷礦粉數(shù)量等具有一定的指導(dǎo)意義。

