生物炭對間歇曝氣濕地N2O排放途徑的影響
王清華,熊海峰,鄧朝仁,何璽,黃磊,4,陳玉成,4
1.西南大學 三峽庫區生態環境教育部重點實驗室,重慶 400715;2.西南大學 資源環境學院,重慶 400715;3.四川省水利科學研究院,成都 610072;4.農村清潔工程重慶市工程研究中心,重慶 400715
人工濕地因凈化性能良好、運營成本低和生態友好等優點,被廣泛用于受污水體治理[1].然而,人工濕地在去除污染物的同時,會產生大量N2O溫室氣體,降低其環境和生態效益[2].人工濕地釋放N2O與濕地填料、進水濃度等多種因素有關[3].近年來,生物炭由于比表面積大、芳香化程度高等特點[4],被廣泛應用于人工濕地以改善濕地內部環境條件[5],強化污染物的去除和調控濕地N2O的排放[6].研究表明,在人工濕地中添加生物炭可以為微生物提供良好的定植環境,改善微生物群落結構和多樣性[7],提高amoA,hao,nirS和nosZ等硝化-反硝化相關酶的活性[8-9],降低N2O排放量.
盡管已有研究探明了生物炭對實現人工濕地N2O減排的重要作用,但N2O減排途徑尚不清晰.目前,區分N2O產生途徑的研究方法主要有抑制劑法和同位素示蹤法等.抑制劑法能有效阻斷氮轉化過程中某單一酶活性,量化N2O排放途徑[10].Castro-Gonzalez等[11]采用抑制劑法評估了濕地旱/雨季硝化作用在脫氮作用過程中的占比;Starr等[12]發現天然濕地真菌反硝化速率比人工濕地高出30%.近年來,15N同位素標記法因環境適宜性和對微生物影響小等優點,被用于識別N2O來源和跟蹤氮素轉化[13].Wang等[14]采用同位素示蹤技術發現濕地中80%的氮通過硝化-反硝化進行循環;Tortosa等[15]的同位素示蹤結果表明,濕地反硝化產生的N2O與人類活動和降雨量相關.將抑制劑法和穩定同位素法聯用不僅可以甄別硝化和反硝化過程對N2O排放的貢獻,還能量化硝化過程中不同環節N2O的釋放量.本研究通過構建室內間歇曝氣生物炭濕地系統,采用化學抑制劑耦合同位素特征值法,研究間歇曝氣人工濕地N2O的產排途徑,解析生物炭投加對濕地N2O排放的影響,以期為生物炭調控濕地N2O排放提供理論依據.
1 材料方法
1.1 系統的構建與運行
濕地裝置采用聚乙烯圓筒容器(圖1),填料以1~2 cm碎石為主,以未添加生物炭的濕地系統作對照(命名為CW),按30%體積投加比構建生物炭濕地系統(命名為BW).生物炭制備方法及物理性質參考團隊前期Huang等[16]的研究.生物炭投加前經2~3次水洗并去除表面污垢和雜質后,選取粒徑約1~2 cm的生物炭投加至濕地內部.系統中央設置直徑為5 cm的PVC穿孔管用于虹吸排水、取樣及各參數測定.為保證濕地植物生長,在裝置外側設置水浴加熱保溫系統,以控制濕地溫度在(26±1) ℃.常規試驗設置2組反應器,抑制劑與同位素試驗另設置6組反應器,所有系統分別設置2個平行,共計16個濕地反應器.
濕地植物馴化、污泥馴化和人工配水方法參考Liang等[8]的研究.反應器均采用間歇進水,有效進水量10 L,水力停留時間24 h.曝氣方式為間歇曝氣,進氣量為0.4 L/min,采用電子流量計(AST10-DX,阿斯特,北京)控制,進水完成時刻記為“0”時刻,曝氣段和非曝氣段均為3 h,交替循環.
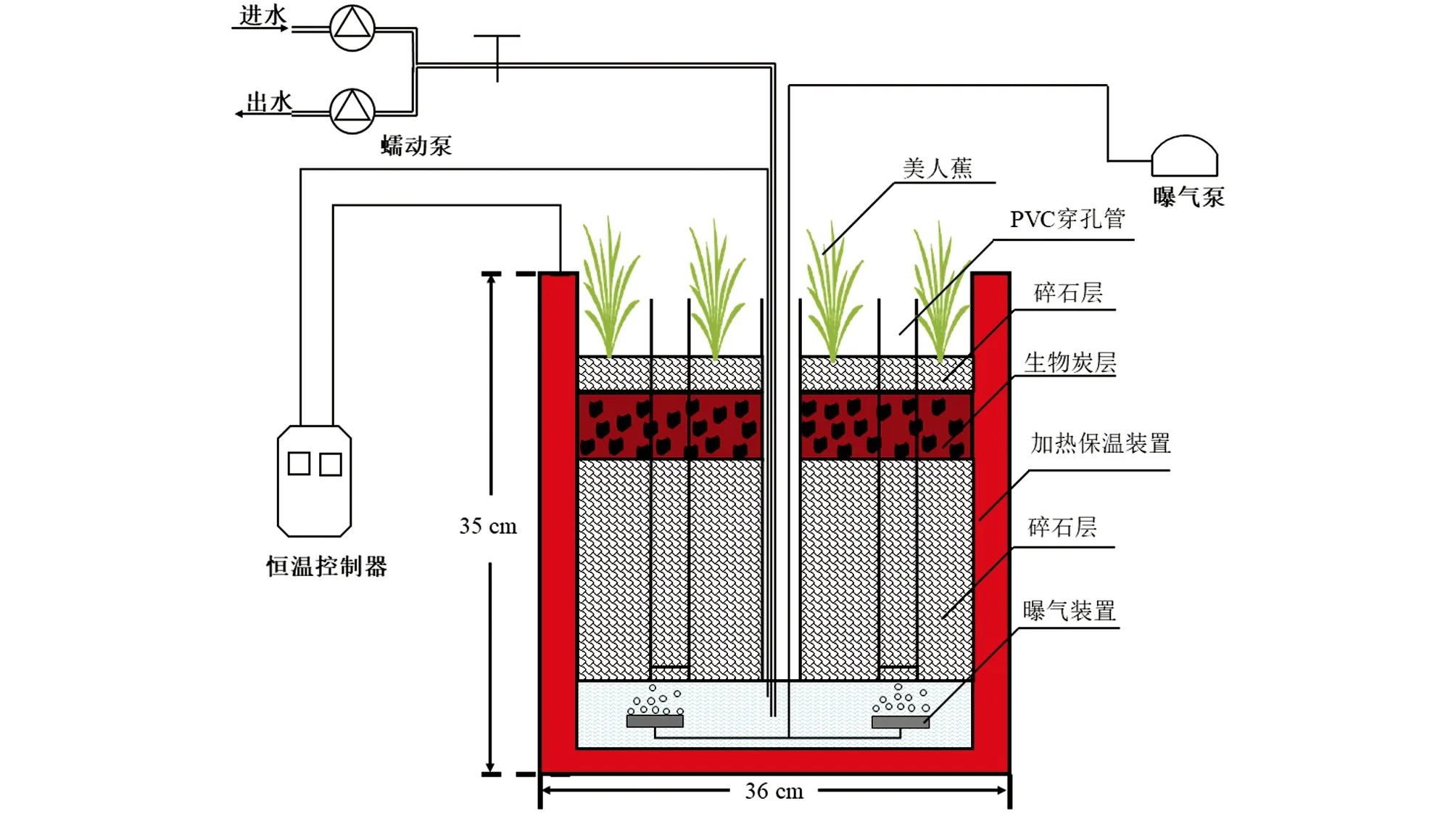
圖1 試驗裝置示意圖
1.2 水質的測定方法
1.3 N2O的采集與測定
N2O的采集方法根據已有研究基礎建立,具體方法參考文獻[18].N2O質量濃度采用氣相色譜儀(Agilent 7890A,美國)測定,氣相色譜設置參數詳見文獻[8].N2O釋放速率和累計釋放量計算方法參考文獻[19].
1.4 不同途徑N2O貢獻率
1.4.1 硝化和反硝化過程N2O產排貢獻
分別設置無抑制劑添加、添加0.1 g/L氯酸鈉、同時添加0.1 g/L氯酸鈉與0.01 g/L丙烯基硫脲3個處理組[20],分別命名為M1,M2和M3,待裝置穩定運行后進行試驗.硝化過程和反硝化過程的N2O產排貢獻采用如下公式計算:
(1)
(2)
(3)
(4)
(5)
式中:CN2O為N2O釋放量,而NF和DD分別為硝化作用和反硝化作用.
1.4.2 NH2OH氧化和AOB反硝化途徑N2O釋放量
為進一步量化硝化途徑中NH2OH氧化和AOB反硝化N2O產排,在裝置穩定運行后采集氣樣送樣至中國農業科學院進行同位素特征值(δ15Nbulk,δ18O)測定.同位素值采用同位素質譜儀(IRMS,賽默飛,德國)配合痕量氣體濃縮系統(Delta V Plus-Precon,賽默飛,德國)測定,δ15Nbulk和δ18O的精度都在0.5‰以下.NH2OH氧化和AOB反硝化途徑對總N2O產量的相對貢獻采用如下公式計算[21]:
FNN=(1-FND)=(SPsample-SPND)/(SPNN-SPND)
(6)
式中:FNN為NH2OH氧化過程產生N2O所占比例(%);FND為AOB反硝化過程產生N2O所占比例(%);SP值為分子內15N的位點偏好值(‰),其中SPNN對應NH2OH氧化過程,SPND對應AOB反硝化過程.SPNN和SPND分別取(33±4)‰和(-1±5.5)‰[21].
1.5 數據分析
試驗數據通過Origin 9.1整理作圖,并由SPSS 24.0進行數據分析.所有試驗數據均采用平均值加減標準差表示.對象之間的差異性分析采用One-way ANOVA(水平包括顯著p<0.05和極顯著p<0.01).
2 結果與討論
2.1 濕地運行效果
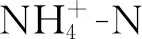
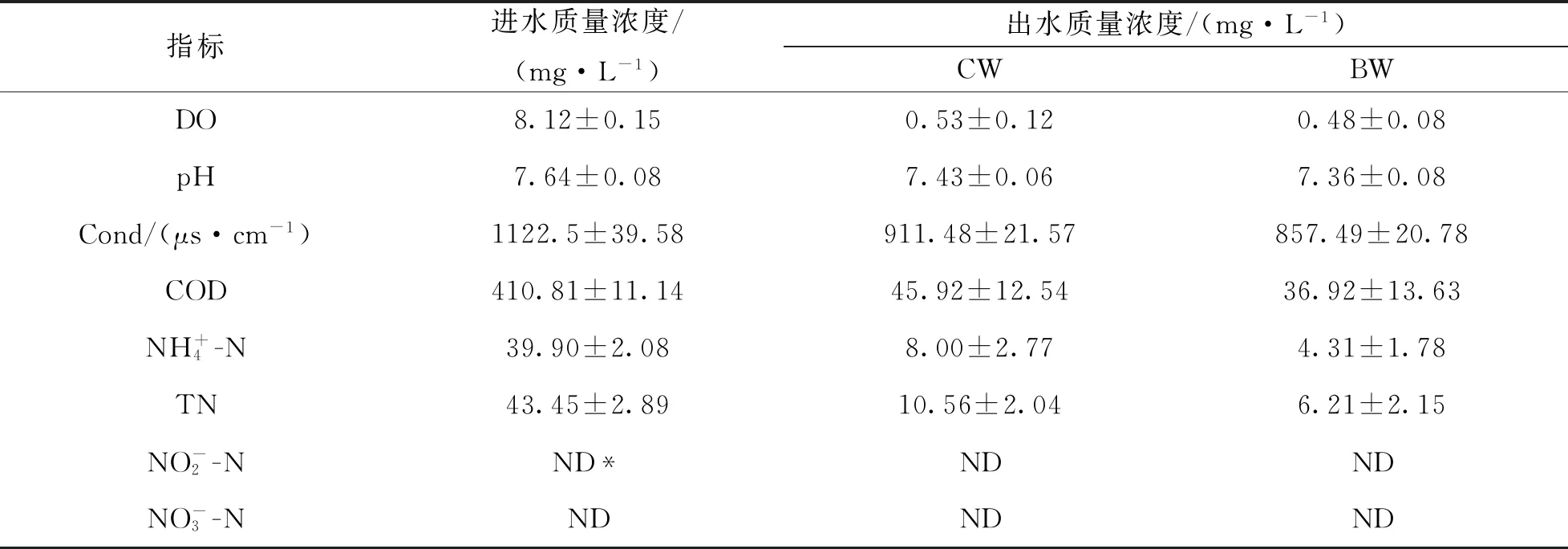
表1 濕地系統進水和出水水質特征
2.2 N2O釋放量及其與污染物的關系
濕地系統N2O累積釋放量均在曝氣段呈上升趨勢(圖2).進水3 h后,CW與BW的N2O釋放量出現明顯差異.總體來看,生物炭投加顯著降低了N2O排放;整個反應周期內(24 h),CW的N2O累積釋放量為18.91 mg/m2,而BW的N2O累積釋放量為12.60 mg/m2,較CW減少了33.37%.通常認為,微氧環境條件造成的不完全硝化和反硝化是人工濕地系統N2O釋放的主要原因.添加生物炭改善了濕地內部DO環境,硝化作用更加徹底,減少了N2O的排放[25].
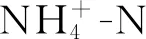
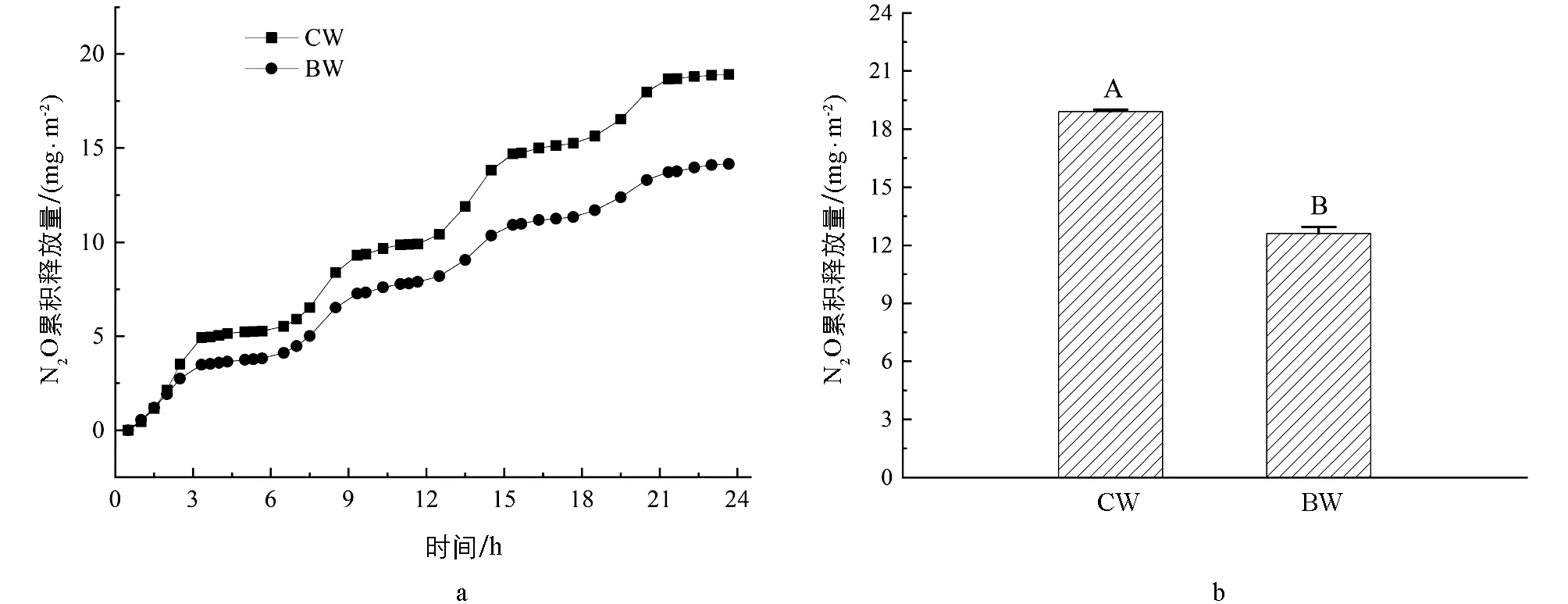
字母A和B代表具有顯著性差異.圖2 典型周期內N2O釋放量隨時間變化(a)和累積釋放量(b)

圖3 典型周期內CW(a)和BW(b)中和N2O通量的動態變化
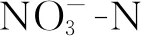
2.3 生物炭濕地中N2O減排途徑
2.3.1 硝化和反硝化過程
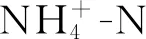
通過對比兩組濕地系統典型周期內硝化和反硝化作用N2O釋放量可以發現(圖5),在反應前期,N2O釋放主要以硝化作用為主;在反應中期,N2O產生途徑則逐漸以反硝化作用為主;在反應后期,反硝化作用表現出弱匯.反應初期濕地DO和有機物充足,硝化作用占主導地位,隨著有機物不斷消耗,異養反硝化作用不完全,導致N2O釋放[30].反應后期處于非曝氣階段,部分N2O以溶解態存在,并通過反硝化作用轉化成N2,表現出N2O弱匯.
對比CW和BW,在曝氣段和非曝段硝化作用的N2O釋放量分別為0.33~1.83 mg/m2和0.05~0.87 mg/m2,反硝化作用的N2O釋放量分別為-0.22~2.68 mg/m2和-0.36~1.17 mg/m2.生物炭作為一種疏松多孔的富碳材料,不僅能改善濕地內部環境條件,還能為后期異養反硝化作用提供碳源,促進N2O轉化為N2而被消耗[31],因此生物炭能在整個周期內有效降低硝化和反硝化過程的N2O排放量.
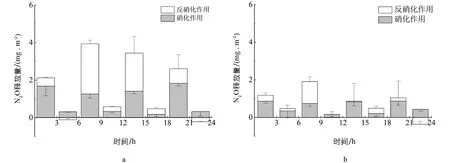
圖5 濕地系統典型周期內CW(a)和BW(b)不同途徑N2O釋放量
2.3.2 NH2OH氧化和AOB反硝化途徑
為進一步明確生物炭對硝化過程中N2O減排途徑的作用,采用SP值法作為反映指標,區分N2O的產生途徑[32-33].圖6為CW和BW中N2O的同位素特征值(δ18O,δ15Nbulk和SP).除19.5 h外,CW的δ18O值δ略高于BW,但無顯著差異(p>0.05).隨著反應的進行,15Nbulk不斷升高;15Nbulk值與δ18O的變化趨勢類似,總體來看CW的15Nbulk值高于BW.值得注意的是,生物炭濕地的SP值為2.251‰~26.273‰,顯著高于對照濕地(0.505‰~21.080‰),且曝氣段SP值顯著高于非曝氣段,說明兩組濕地N2O排放特征存在區別,曝氣段與非曝氣段的N2O產生機制也可能不同.
一般將δ18O和δ15Nbulk,δ18O和δαN之間斜率(k1和k2)大于1作為判別N2O還原對SP影響的依據[34-35].擬合得到CW和BW的k1和k2均小于1,說明N2O還原對SP值影響不顯著.因此,采用SP值法可以較好地區分濕地硝化過程中NH2OH氧化和AOB反硝化途徑.
根據SP值計算N2O的產生途徑可以發現(圖7),在曝氣段,兩種濕地系統NH2OH氧化途徑與AOB反硝化途徑N2O累積釋放量相當,NH2OH氧化和AOB反硝化對N2O的產生均有重要作用;在非曝氣段,N2O釋放主要以AOB反硝化途徑為主,主要是因為低DO質量濃度限制了NH2OH氧化.BW中NH2OH氧化和AOB反硝化的N2O累積釋放量分別為2.21,2.22 mg/m2,較CW分別減少了29.40%,47.12%.
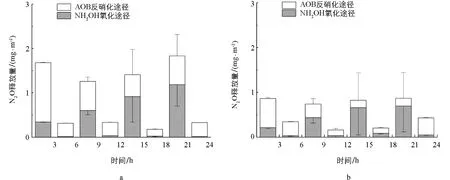
圖7 CW(a)與BW(b)中NH2OH氧化和AOB反硝化產生N2O的累積釋放量變化
3 結論
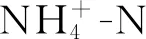
2) N2O釋放主要集中在曝氣階段,在整個周期投加生物炭顯著降低了濕地N2O的釋放速率;與對照濕地相比,生物炭濕地N2O排放量減少了33.37%.
3) 投加生物炭能為后期脫氮過程提供碳源,有效降低硝化和反硝化過程中N2O的排放量,減排率分別為39.51%和67.06%,對硝化和反硝化外的其他途徑無顯著影響.
4) 在間歇曝氣人工濕地中,生物炭可以通過影響曝氣段NH2OH氧化和AOB反硝化,實現硝化過程N2O減排,減排率分別為29.40%和47.12%.

