多模態超聲預測乳腺癌腋窩淋巴結轉移的價值
成靜,李文肖,吳芳,曹春莉,侯吉學,李軍
根據2020年癌癥數據統計分析顯示[1],乳腺癌已經成為女性癌癥死亡的主要原因,早診斷、早治療是提高乳腺癌5年生存率的關鍵。乳腺癌主要通過淋巴結擴散轉移,腋窩淋巴結的狀態是決定臨床手術方式的關鍵因素及患者預后因素之一[2],乳腺癌患者發生腋窩淋巴結轉移時,需行腋窩淋巴結清掃術,然而腋窩淋巴結清掃術術后會給患者帶來一定的后遺癥,如術側上肢活動受限,水腫等,極大地影響了患者的生活質量。乳腺癌的腋窩淋巴結轉移是多步驟、多種機制參與調節的復雜過程,與其本身的生物學特征存在著一定的關系[3]。乳腺癌原發病灶的多模態超聲成像特征在一定程度上可以反映乳腺癌的生物學特征。本研究通過分析乳腺癌原發病灶的常規超聲(conventional ultrasound,CUS)、聲觸診組織量化成像技術(virtual touch tissue imaging and quantification,VTIQ)、聲輻射力成像(virtual touch tissue imaging,VTI)及超聲造影(contrast-enhanced ultrasound,CEUS)特征參數與腋窩淋巴結轉移之間的關系,并評價CUS聯合三種新技術預測乳腺癌腋窩淋巴結轉移的價值,旨在術前準確、有效評估乳腺癌患者腋窩淋巴結狀態,為臨床選擇合適的治療方案及減少術后并發癥提供理論依據。
材料與方法
1.研究對象
回顧性收集2018年1月-2021年12月在石河子大學第一附屬醫院診斷為乳腺癌并行手術的患者,共91例患者94個病灶,均為女性,年齡26~74歲,平均年齡(51.74±8.38)歲。所有患者術前均行CUS、VTIQ、VTI、CEUS檢查,術后具有完善的病理結果。納入標準:①均具有完整的CUS、VTIQ、VTI、CEUS檢查的影像圖像及視頻資料;②均接受乳腺癌切除術及淋巴結清掃術。排除標準:①未獲得明確的病理結果;②既往有乳腺相關的放化療病史的患者;③妊娠期或哺乳期患者。本研究經醫院醫學倫理委員會批準(編號:KJ2020-059-01),均已簽署知情同意書。
2.檢查儀器與對比劑
采用Siemens S3000超聲診斷儀,選用9L4高頻探頭,探頭頻率4~9 MHZ,配備有VTI、VTIQ軟件和對比脈沖序列造影成像技術。對比劑選用聲諾維(SonoVue)。電腦端安裝有ImageJ光密度分析軟件。囑患者平臥位或側臥位,充分暴露雙乳及腋窩,進行CUS、VTI、VTIQ、CEUS檢查。
常規超聲檢查中,多切面多角度掃查雙側乳腺及腋窩,確定病灶后,記錄在二維灰階模式下病灶的最大徑線、后方回聲、鈣化等超聲征象,彩色多普勒模式下病灶的Alder血流分級。
然后在二維灰階模式下,將探頭輕置于病灶的最大徑切面皮膚處,固定探頭且不施壓,切換VTI模式,在機械指數為1.6條件下,連續獲取3幅VTI圖像,將穩定的3幅VTI圖像導入裝有ImageJ軟件的電腦中進行分析,得出VTI病灶平均光密度值(VTI平均)、VTI病灶邊緣平均光密度值(VTI邊緣)、VTI腺體平均光密度值(VTI腺體),進一步計算VTI病灶平均光密度值(VTI平均)與VTI腺體平均光密度值(VTI腺體)的比值(VTI平均/腺體),得出結果并記錄。
在二維灰階模式下確定病灶的最大徑切面,輕置探頭于皮膚表面,固定探頭且不施壓,切換VTIQ模式,調整感興趣區(ROI),使其可能覆蓋病灶最大區域,包括病灶邊緣、周邊腺體區域。囑患者保持平靜狀態,按下“Update”鍵,待質量模式下呈現出均勻綠色(表示彈性成像穩定)時切換成速度模式,獲取剪切波速度(shear wave velocity,SWV)平均值(SWVmean)、剪切波速度最大值(SWVmax)、剪切波速度最小值(SWVmin),得出最大值與最小值比值(SWVmax/min)。所有數據均測定5次,最后選擇平均值。
在二維灰階模式下確定病灶的最大徑切面,輕置探頭于皮膚表面,固定探頭且不施壓,進入超聲造影模式,機械指數為0.08,囑患者保持平靜呼吸,經肘靜脈注射對比劑2.4 mL,緊接著沖注生理鹽水5 mL,同時啟動計時按鈕和存儲按鈕。觀察造影時間均不少于2 min。對CEUS視頻進行分析,分別記錄增強強度、增強順序、充盈缺損等CEUS特征。
以上檢查均由兩名7年以上診斷經驗的超聲醫師進行圖片及視頻資料的分析,如遇到意見不一致時,則加入一名高級職稱醫師進行討論,最終達成一致結果。
4.統計學方法
采用SPSS 26.0統計軟件對數據進行分析,計量資料符合正態分布以均數±標準差表示,采用t檢驗,不符合正態分布以M(Q1,Q3)表示,采用非參數Wilcoxon檢驗;計數資料采用例(%)表示。組間比較常用單因素分析,多因素分析采用二元Logistic回歸分析。以病理結果為金標準,采用Kappa檢驗分析Logistic預測模型的一致性。當Kappa值>0.75時,表示一致性極好,當Kappa值>0.40~0.75時,表示中高度一致,當Kappa值≤0.40時,表示一致性較差,P<0.05為差異具有統計學意義。
結 果
1.病理結果
91例患者94個病灶中,其中浸潤性導管癌65個,導管原位癌9個,浸潤性導管癌伴其他癌(原位癌、粘液癌、髓樣癌)16個,髓樣癌1個,粘液癌2個,小葉癌1個。
2.多模態超聲預測乳腺癌腋窩淋巴結轉移的單因素分析
在CUS特征參數中,彈性評分(χ2=7.188,P=0.027)、最大徑(χ2=6.682,P=0.010)、后方回聲衰減(χ2=3.910,P=0.048)、Adler血流分級(χ2=12.097,P=0.001)差異有統計學意義(表1)。
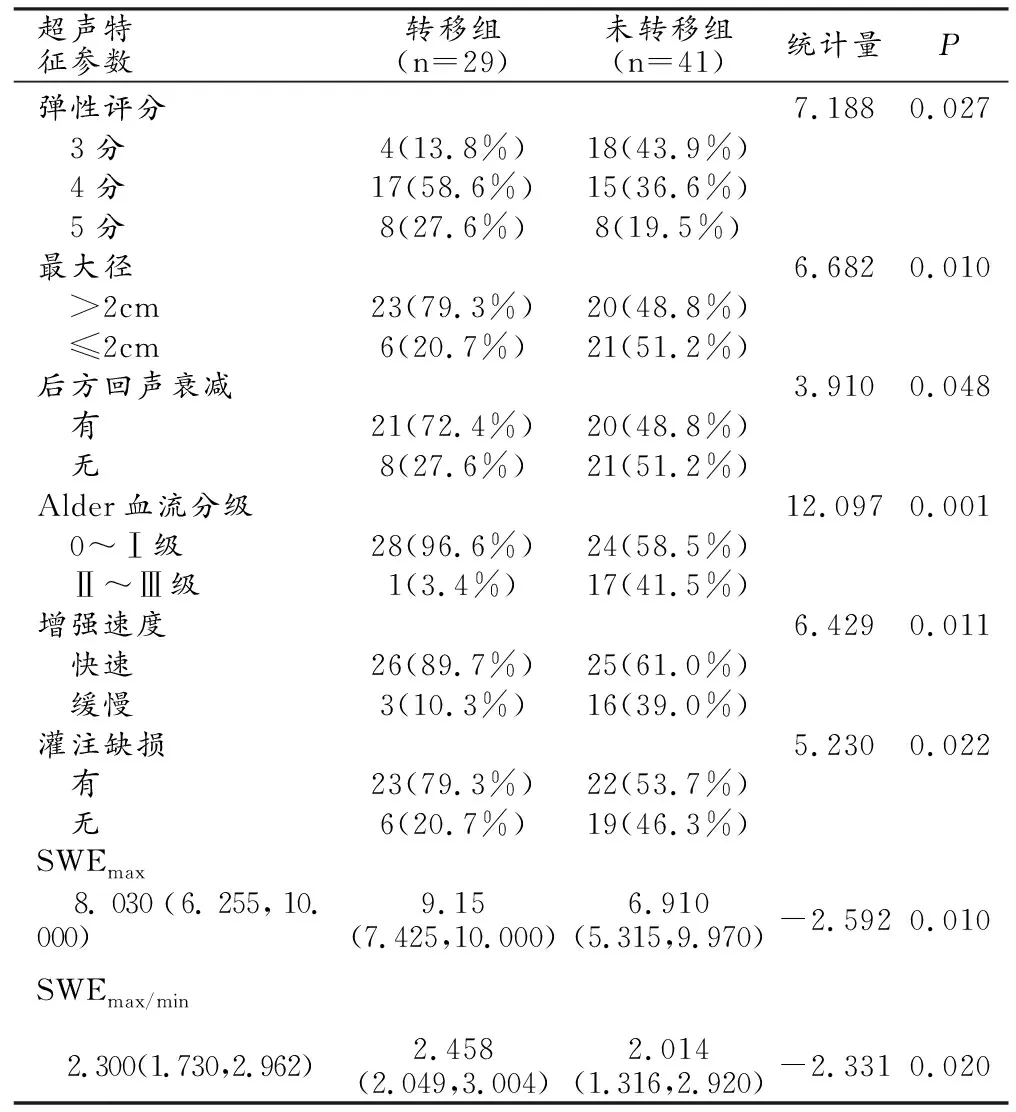
表1 單因素分析多模態超聲預測乳腺癌腋窩淋巴結轉移的超聲特征參數
在VTIQ特征參數中,SWVmax(Z=-2.592,P=0.010)、SWVmax/min(Z=-2.331,P=0.020)差異具有統計學意義。在VTI中,VTI平均(Z=-0.817,P=0.414)、VTI邊緣(Z=-0.590,P=0.555)、VTI平均/腺體(Z=-0.745,P=0.456)差異均無統計學意義。在CEUS特征參數中,增強速度(χ2=6.429,P=0.011)、灌注缺損(χ2=5.230,P=0.022)差異具有統計學意義。
3.多模態超聲預測乳腺癌腋窩淋巴結轉移的多因素分析
將以上單因素篩選出有意義的超聲特征參數進行多因素分析,結果顯示Alder血流分級、增強速度、SWVmax差異具有統計學意義,受試者操作特征(receiver operating characteristic,ROC)曲線下面積(area under curve,AUC)分別為0.690(95%CI:0.568~0.795)、0.643(95%CI:0.520~0.754)、0.681(95%CI:0.559~0.788),見表2。聯合以上三個超聲特征參數建立預測模型方程Y=-6.903+2.100×Alder血流分級+1.790×增強速度+0.423×SWVmax,該預測模型AUC為0.814(95%CI:0.703~0.897),敏感度為82.76%,特異度為78.05%。一致性檢驗(Kappa=0.625,P=0.002,表3),表明該預測模型結果與病理結果檢驗中高度一致(表2,圖1、2)。
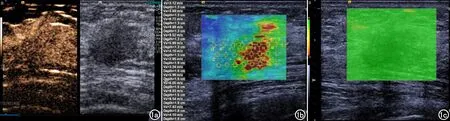
圖1 女,51歲,右側乳腺浸潤性導管癌伴腋窩淋巴結轉移。a)超聲造影表現為早于周圍乳腺組織呈快速高增強,增強后邊界清晰,邊緣不規整,增強后范圍增大;b)SWVmax=9.88 m/s,SWVmin=4.05 m/s VTIQ檢查;c)質量模式圖呈均勻綠色。
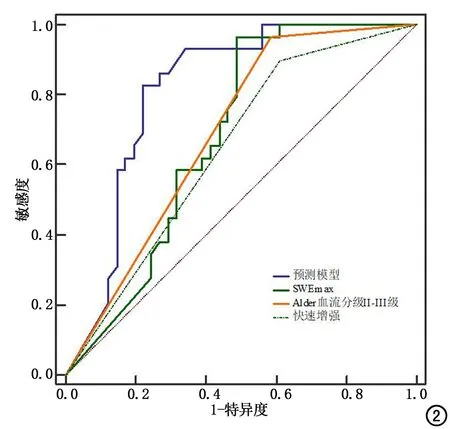
圖2 多模態超聲特征參數及預測模型ROC曲線。
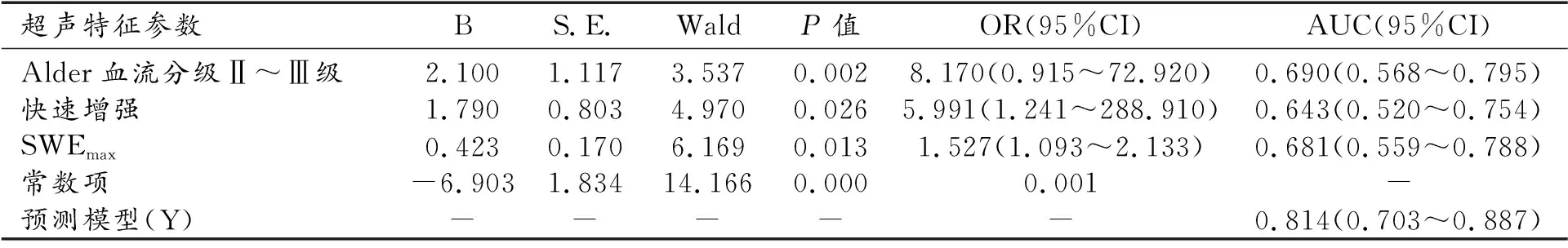
表2 多因素分析多模態超聲預測乳腺癌腋窩淋巴結轉移的超聲特征參數

表3 預測模型與病理學結果一致性檢驗
討 論
腋窩淋巴結是否發生轉移對于乳腺癌患者的預后評估至關重要,臨床實踐中乳腺癌的手術范圍主要通過腋窩淋巴結活檢以及冰凍切片檢查進行評估[2]。如若腋窩淋巴結的活檢結果表明發生轉移,則需要進行腋窩淋巴結清掃術。然而術中冰凍活檢切片需要專業的病理科醫師來評估,使得手術的操作時間及治療成本增加。因此術前對乳腺癌淋巴結轉移的情況進行預測,可以為臨床醫師選擇手術方式及選擇更加合理的治療方案提供依據。本研究通過分析乳腺癌原發病灶的多模態超聲(CUS、VTIQ、VTI及CEUS)特征參數與腋窩淋巴結轉移之間的相關性,篩選出有意義的超聲特征,并建立乳腺癌患者腋窩淋巴結的預測模型,為乳腺癌患者術前腋窩淋巴結狀態的準確評估提供參考。
本研究中表明乳腺癌原發病灶的Alder血流分級Ⅱ~Ⅲ級是腋窩淋巴結轉移的獨立危險因素。既往研究表明[4,5]發生腋窩淋巴結轉移的乳腺癌原發病灶血流較豐富,與本研究結果一致。乳腺癌具有復雜多形性表現的一種腫瘤,具有較高的血管依懶性。腫瘤細胞通過分泌大量的血管內皮生長因子,誘導腫瘤周邊組織形成大量血管網,進而使腫瘤細胞更易發生轉移。因此當乳腺癌原發灶的血流越豐富,其Adler血流分級更高,發生轉移的風險就越高。
VTIQ作為第三代ARFI技術,可以從速度模式圖中直觀的獲取組織硬度的定量信息,同時可以多次測量SWV,獲取腫瘤組織不同部位、不同深度的硬度信息,從而更準確的反映病灶的硬度。此外,它還具備質量模式圖,可以高質量的獲取彈性圖像并進行測值,使獲取的結果更加準確。本研究分別測取了腫塊組織內部最硬、最軟以及周邊腺體的SWV,研究結果表明腫塊最硬的SWV與腋窩淋巴結轉移具有統計學意義。腫瘤組織的SWV的最大值越高,腫瘤促進內部及周邊結締組織增生且形成新生血管,向腋窩淋巴結轉移的可能就越大,同時伴隨著腫瘤間質水腫越嚴重,使得腫瘤組織的硬度值增加[6,7]。
VTI技術是一種定性評價腫瘤組織軟硬程度的方法,Image J是一種光密度分析軟件,通過聯合運用VTI與Image J可以定量評估病灶的軟硬度。本研究通過定性及定量分析乳腺腫塊的VTI超聲圖像,結果表明VTI平均光密度值、邊緣光密度值、平均光密度值與周邊腺體光密度值的比值以及有無“馬賽克”征均無統計學意義。VTI圖像的“馬賽克”對于乳腺腫塊的定性診斷具有一定的價值[8],但對于腋窩淋巴結轉移沒有相關性,原因可能在于VTI圖像只對病灶組織的軟硬度進行灰階成像,組織整體較硬時其內部會出現“馬賽克”征,但對于腫瘤組織內部的液性區域及鈣化區域等,其往往不能很好表現出來。既往研究表明[9-11]定量后的VTI值可以校正乳腺影像報告和數據系統(breast imaging reporting and data system,BI-RADS)分類,提高乳腺腫塊的診斷價值,而對于能否可以預測乳腺癌腋窩淋巴結轉移目前國內尚未見報道,本研究初步探討了VTI定性及定量特征與乳腺癌腋窩淋巴結轉移的關系,但由于病例數有限,今后將進一步擴大樣本量進行深入研究。
本研究超聲造影定性參數中快速增強是乳腺癌腋窩淋巴結轉移的危險因素,且呈正相關(Z=0.318,P=0.007),表明增強速度越快,就越易發生腋窩淋巴結轉移。既往研究[12]表明超聲造影能夠清楚顯示彩色多普勒技術無法顯示的腫瘤組織內的微細血管分布及走向,可以獲得腫瘤組織中的微循環狀況及血流灌注信息。乳腺癌腫塊在促血管因子作用下往往形成較多的纖細血管及新生組織[13],并向周邊不斷侵犯,在超聲造影模式下,會快速顯示腫塊的灌注情況。然而當淋巴結轉移時,癌腫的血流信號豐富,增強造影時其增強速度會加快。有學者認為[14]增強造影時造影劑增強的速度越快,表明腫塊內部血流豐富且阻力指數值也較高,本研究中缺乏阻力指數值的量化,在后期研究中將逐步完善。
本研究的局限性:本研究為單中心研究,會存在不可避免的選擇偏倚,未來將進行多中心研究證實本研究所得出的結論。其次,本研究中病例數相對不足,后期研究中間進一步擴充樣本量進行深入研究。
綜述所述,當乳腺癌患者原發病灶的Alder血流分級為Ⅱ~Ⅲ級,剪切波速度最大值最快、增強速度為快速增強時,容易發生腋窩淋巴結轉移,基于這三種危險因素建立的預測模型對乳腺癌患者腋窩淋巴結轉移具有較高的預測價值,可為臨床診療與預后提供診斷依據。

