解郁止痛方對偏頭痛—抑郁共病模型大鼠行為學(xué)及腦組織中Iba1/RhoA蛋白表達(dá)的影響*
申莉鐸,張慧,邵笑笑,蔣若琛,簡芋鑫
(1.陜西中醫(yī)藥大學(xué),咸陽 712046;2.陜西中醫(yī)藥大學(xué)附屬醫(yī)院,咸陽 712000)
偏頭痛是一種常見的以單側(cè)或雙側(cè)搏動性中度或重度為主的原發(fā)性頭痛,在現(xiàn)代社會中廣泛存在[1-2],嚴(yán)重影響了人類的生活質(zhì)量,對人類的健康造成了極大影響。有數(shù)據(jù)表明,在當(dāng)今社會,越來越多的人飽受偏頭痛的折磨,偏頭痛的患病率也逐步上升,其在全世界年患病率高達(dá)18%,在中國患病比例為9.3%[3-4]。此外,偏頭痛不僅對人體傷害巨大,還可與多種疾病共病,進(jìn)一步給人體生理、心理帶來極大創(chuàng)傷。抑郁是偏頭痛病程中一種常見的并發(fā)疾病[5],與其他正常人群相比,偏頭痛患病人群抑郁的發(fā)病率風(fēng)險(xiǎn)增加(OR=5.8),同時(shí),抑郁患病人群并發(fā)偏頭痛的風(fēng)險(xiǎn)也呈增加趨勢(OR=3.4),由此可見,偏頭痛與抑郁共病具有雙向性,兩者常相伴存在,互相影響[6],對人類的生活質(zhì)量產(chǎn)生嚴(yán)重的影響,進(jìn)一步對社會生產(chǎn)力造成影響。因此,偏頭痛-抑郁共病的預(yù)防與治療尤為重要,現(xiàn)代臨床對于偏頭痛-抑郁共病暫無明確、有效、規(guī)范的認(rèn)識,關(guān)于其發(fā)病機(jī)制的研究也較貧乏,臨床多以西醫(yī)治療為主,西藥多副作用大,且癥狀改善不明顯。中醫(yī)治療疾病具有個(gè)體差異,且多藥聯(lián)合可多靶點(diǎn)發(fā)揮作用,并可減輕西藥帶來的不良作用,有效防治偏頭痛-抑郁共病對個(gè)人及社會的危害,提高社會生產(chǎn)力。有研究表明,偏頭痛與抑郁兩者之間常相伴存在可能與其受相同的腦組織調(diào)控有關(guān),偏頭痛-抑郁患者腦組織海馬及杏仁核等均發(fā)生了明顯改變[7-8]。疼痛與抑郁有共同的傳導(dǎo)通路,中樞神經(jīng)系統(tǒng)痛覺信息傳導(dǎo)通路中神經(jīng)元敏化可產(chǎn)生皮膚異常性疼痛伴隨強(qiáng)烈的負(fù)性情緒。小膠質(zhì)細(xì)胞是中樞神經(jīng)系統(tǒng)中固有的免疫效應(yīng)細(xì)胞,在維持腦內(nèi)穩(wěn)態(tài)和神經(jīng)炎癥反應(yīng)中發(fā)揮重要作用。電離鈣結(jié)合適應(yīng)分子1(Iba1)是小膠質(zhì)細(xì)胞分子標(biāo)記物,激活后表達(dá)增加[9],神經(jīng)再生抑制因子Ras 同源物基因A(RhoA)與下游Rho 蛋白激酶(ROCK)的相互作用可阻止中樞神經(jīng)再生,加重神經(jīng)元受損[10]。解郁止痛方在治療偏頭痛—抑郁共病疾患方面有著顯著療效,但其作用機(jī)制尚不明確。相關(guān)研究表明,偏頭痛—抑郁共病大鼠模型中大鼠腦組織杏仁核內(nèi)Iba1 及RhoA蛋白含量均顯著升高[11],本實(shí)驗(yàn)主要研究偏頭痛—抑郁共病大鼠模型行為學(xué)改變及腦組織杏仁核內(nèi)Iba1/RhoA 蛋白的含量,探究偏頭痛—抑郁共病大鼠的發(fā)病機(jī)制及解郁止痛方治療偏頭痛—抑郁共病疾患的分子機(jī)制,以期為臨床偏頭痛—抑郁共病疾患的防治提供可靠依據(jù)。
1 材料與方法
1.1 實(shí)驗(yàn)動物 健康雄性SD 大鼠54 只,體質(zhì)量(200±20)g,由成都達(dá)碩實(shí)驗(yàn)動物有限公司提供。合格證書號:SCXK(川)2022-002。實(shí)驗(yàn)前于陜西中醫(yī)藥大學(xué)動物實(shí)驗(yàn)中心適應(yīng)性喂養(yǎng)1 周,實(shí)驗(yàn)中心動物房于8:00-20:00 光照、20:00-8:00 黑暗,實(shí)驗(yàn)室溫度(23±1)℃,濕度(50±5)%,喂養(yǎng)期間自由飲食,飲自來水,食標(biāo)準(zhǔn)顆粒飼料。
1.2 藥物和試劑 解郁止痛方(由川芎12 g,柴胡10 g,合歡皮10 g,全蝎6 g,黃芪10 g 組方),由陜西中醫(yī)藥大學(xué)校醫(yī)院制劑中心提供;硝酸甘油注射液,規(guī)格1 mL∶5 mg,山東華信制藥有限公司;國藥準(zhǔn)字:H37021469;尼莫地平片,規(guī)格:20 mg/片,廣東華南藥業(yè)集團(tuán)有限公司,國藥準(zhǔn)字:H44025019。
Iba1 抗體,兔克隆抗體,貨號:GTX100042,genetex;RhoA 抗體,鼠克隆抗體,貨號:66733-1-lg,proteintech;β -actin 抗體,兔克隆抗體,貨號:AC026,abclonal;生物素化山羊抗鼠IgG(H+L),貨號:ab6789,英國abcam 艾博抗(上海)貿(mào)易有限公司;生物素化山羊抗兔IgG (H+L),貨號:s0001,affinity;1.0 mol/L Tris-HCl(pH=8.8)電泳緩沖液、PBS磷酸鹽緩沖液、RIPA 裂解液(強(qiáng)),貨號:G2002-100 mL,servicebio;BCA 蛋白濃度測定試劑盒,貨號:P0009,beyotime;PAGE 凝膠快速制備試劑盒,貨號:PG112,上海雅酶生物科技有限公司;甘氨酸,貨號:G5010-500 g,servicebio;Tris-base,貨號:1115GR500,Biofroxx;SDS,貨號:1275GR500,Biofroxx;氯化鈉,天津市致遠(yuǎn)化學(xué)試劑有限公司。
1.3 主要儀器 電子天平(上海民橋公司);2390系列電子VonFrey 測痛儀(美國ITLife Science 公司);JY-SCZ4+型垂直電泳槽、JY200C 型電泳儀(北京君意東方電泳設(shè)備有限公司);TY-80A 型水平脫色搖床(江蘇科析儀器有限公司);5200 型化學(xué)發(fā)光凝膠成像儀(上海天能科技有限公司);MK3 型全功能酶標(biāo)儀(美國ThermoFisher 儀器有限公司);DW-86L386 型超低溫冰箱(海爾集團(tuán));H2050R 高速低溫離心機(jī)(湘儀集團(tuán));優(yōu)普超純水制造系統(tǒng)(成都超純科技有限公司);KZ-Ⅲ-F 型高速低溫組織研磨儀(武漢賽維爾生物科技有限公司);HI1210 型水浴鍋(德國Leica 公司)。
1.4 實(shí)驗(yàn)方法 健康SD 實(shí)驗(yàn)大鼠適應(yīng)性喂養(yǎng)1 周,1 周后將54 只大鼠隨機(jī)分為6 組(空白組、模型組、西藥組、中藥解郁止痛方低、中、高劑量組),每組9 只。實(shí)驗(yàn)開始第1 天,除空白組外,其余5 組復(fù)制偏頭痛模型,按照偏頭痛間斷性發(fā)作特點(diǎn),于實(shí)驗(yàn)開始第1、7、14、21 天分別在大鼠頸背部皮下注射硝酸甘油注射液(硝酸甘油注射液用生理鹽水稀釋為10 mg/kg),偏頭痛造模成功的標(biāo)志為:大鼠頸背部注射硝酸甘油注射液20 min 后,大鼠耳朵發(fā)紅,前肢搔頭動作和攀籠次數(shù)增多[12]。偏頭痛模型復(fù)制成功7 天內(nèi),每天對除空白組外其余5 組大鼠進(jìn)行一種隨機(jī)不重復(fù)慢性不可預(yù)知性刺激誘導(dǎo)偏頭痛-抑郁共病大鼠模型[13]。1)晃籠:200 Hz 10 min。2)夾尾:將大鼠分籠放置,使用夾取力度相同且適中的鼠尾夾,在距大鼠尾巴根部1 cm 處夾緊,時(shí)間4 min。3)濕籠:在籠子里撒100 mL 水,至墊料全部濕透,持續(xù)24 h。4)冰水游泳:將4 ℃冷水加入水深15 cm的水桶,放入大鼠8 min 后取出,其間保證大鼠的足尖可以碰到水桶的底部但不能越出水桶。5)電擊足底:電壓38 V 每次1 s 間隔2 s 刺激1次持續(xù)2 min。6)斜籠:將動物籠傾斜45°放置,持續(xù)24 h。7)禁食、禁水:禁食、禁水24 h。通過觀察大鼠搔頭及攀籠次數(shù)、礦場實(shí)驗(yàn)、糖水消耗實(shí)驗(yàn)、強(qiáng)迫游泳實(shí)驗(yàn)、新奇抑食實(shí)驗(yàn)等行為學(xué)檢測評分判斷偏頭痛-抑郁共病大鼠造模是否成功[13]。實(shí)驗(yàn)開始造模同時(shí)予以藥物灌胃干預(yù),空白組以純水灌胃,模型組以0.9% NaCl溶液灌胃,西藥組以尼莫地平尼混懸液6 mg/kg灌胃,中藥低、中、高劑量組分別予以解郁止痛方(0.25 g/100 g、0.5 g/100 g、1.0 g/100 g)灌胃,每日1 次,共21 d。
1.5 檢測指標(biāo)與方法
1.5.1 行為學(xué)評分 于實(shí)驗(yàn)造模前第0 天、造模治療中第10 天、造模治療后第21 天分別測量實(shí)驗(yàn)各組大鼠以下行為學(xué)。
1.5.1.1 體質(zhì)量 分別測量各組大鼠體質(zhì)量并記錄。
1.5.1.2 曠場試驗(yàn) 準(zhǔn)備長、寬各100 cm,高50 cm的敞口紙箱,并將其內(nèi)壁四面均勻涂黑,內(nèi)底等分為25 個(gè)正方形。將大鼠沿一側(cè)內(nèi)壁放置于紙箱中,適應(yīng)2 min 后觀察4 min 內(nèi)其爬過的方塊數(shù)量(四肢同時(shí)經(jīng)過)及直立次數(shù)(雙側(cè)前肢離開地面或爬于側(cè)壁)評分[14]。各組大鼠依次檢測,檢測過程中盡量保持安靜以確保實(shí)驗(yàn)準(zhǔn)確性,并用視頻記錄檢測結(jié)果,每次檢測前保證紙箱干凈無排泄物。分析各組大鼠曠場水平及垂直運(yùn)動評分之間的差異。
1.5.1.3 糖水消耗實(shí)驗(yàn) 實(shí)驗(yàn)前準(zhǔn)備兩只500 mL水瓶,一只瓶身標(biāo)注糖水,另一只標(biāo)注純水。每次評估前24 h 對大鼠實(shí)行糖水?dāng)z入適應(yīng)性訓(xùn)練,即每籠同時(shí)放2 個(gè)瓶內(nèi)均裝有1%蔗糖水500 mL 的水瓶。24 h 后,一只瓶內(nèi)仍裝1%蔗糖水500 mL、另一只瓶內(nèi)裝純水500 mL。24 h 后,取走水瓶,分別記錄每只大鼠的總液體攝入量、糖水?dāng)z入量、純水?dāng)z入量。計(jì)算其糖水偏好百分率(糖水偏好百分率=糖水?dāng)z入量/總液體攝入量×100%)[14]。比較各組大鼠糖水偏好差異。
1.5.1.4 強(qiáng)迫游泳實(shí)驗(yàn) 檢測前準(zhǔn)備一長方形塑料桶(桶長100 cm 寬50 cm 高50 cm),桶內(nèi)放置高40 cm 23~25 ℃的水。將同組大鼠依次放入水中,強(qiáng)迫其游泳8 min,大鼠被動漂浮在水中,將其在水中停止掙扎3 s 以上規(guī)定為不動狀態(tài),記錄大鼠不動時(shí)間[14],分析各組之間的差異。
1.5.1.5 新奇抑食實(shí)驗(yàn) 實(shí)驗(yàn)前大鼠禁食1 d,不禁水,準(zhǔn)備1 個(gè)50 cm×40 cm 的箱子,在箱子中央放置數(shù)枚大小相似的食標(biāo)準(zhǔn)顆粒飼料,每次從箱子的同一個(gè)角放入大鼠,記錄大鼠第一次咬食的時(shí)間[15]。分析各組大鼠新奇抑食-潛伏時(shí)間之間的差異。
1.5.2 機(jī)械痛閾的測定 實(shí)驗(yàn)開始第1、7、14、21 天復(fù)制偏頭痛模型前測量各組實(shí)驗(yàn)大鼠的機(jī)械痛閾值。機(jī)械痛閾的測定:將各組大鼠依次放置于底部具有網(wǎng)狀金屬孔格的透明測試籠中,適應(yīng)5 min,待大鼠趨于安靜后用Vonfrey 纖維絲緩慢輕柔地刺激大鼠左后肢足底中部,持續(xù)幾秒,觀察大鼠縮足反應(yīng),記錄引起爪子回縮的最小閾值,機(jī)械痛閾值均每只測量3 次,每次測量應(yīng)間隔5 min,取其均值[15]。
1.5.3 Western blot 檢測各組大鼠模型腦組織杏仁核中Iba1 及RhoA 蛋白的含量 實(shí)驗(yàn)第21 天造模治療結(jié)束后,腹腔注射麻藥麻醉大鼠,腹主動脈采血約4 mL,室溫凝固20 min,離心機(jī)3 000 g 離心20 min,ep 管收集離心后血清進(jìn)行分裝,置于-80 ℃冰箱保存。取血后大鼠用0.9%Nacl 心臟灌注以置換出全身血液,隨后進(jìn)行斷頭取腦,取出的腦組織在-20 ℃冰箱加以凝固后依照大鼠腦解剖圖譜將杏仁核取出并稱質(zhì)量,放于2 mL 離心管中液氮速凍后轉(zhuǎn)-80 ℃冰箱保存。于WB 檢測時(shí)將樣本取出放入2 mL 研磨管中,向每管加入3 mm 鋼珠及RIPA 裂解液(按照質(zhì)量比樣本:裂解液=1∶10),置于高速低溫組織研磨儀內(nèi)(溫度-20 ℃,研磨4 次,每次60 s);取出放4 ℃冰箱30 min 進(jìn)行裂解,30 min 后取出放入離心機(jī)(4 ℃、12 000 g 離心、10 min);離心完后取上清液,通過BCA 蛋白定量試劑盒進(jìn)行分析、蛋白變性、上樣、電泳、轉(zhuǎn)膜、封閉、孵育抗體、顯影定影等步驟以檢測大鼠腦組織杏仁核中Iba1 及RhoA蛋白的水平。
1.6 統(tǒng)計(jì)學(xué)處理 實(shí)驗(yàn)數(shù)據(jù)均采用SPSS 22.0 軟件進(jìn)行統(tǒng)計(jì)學(xué)分析。計(jì)量數(shù)據(jù)均符合正態(tài)分布,將其按均數(shù)±標(biāo)準(zhǔn)差(±s)表示,組間比較采用One-Way ANOVA 單因素方差分析,P<0.05 則有統(tǒng)計(jì)學(xué)意義,差異顯著。
2 結(jié)果
2.1 大鼠體質(zhì)量比較 在造模治療前(第0 天)各組大鼠體質(zhì)量均差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。在造模治療第10 天、21 天,與空白組相比,模型組大鼠體質(zhì)量明顯下降(P<0.01);與模型組相比,中藥低劑量組大鼠體質(zhì)量增加(P<0.05),西藥組、中藥中劑量及高劑量組大鼠體質(zhì)量顯著升高(P<0.01)。見表1。
表1 大鼠體質(zhì)量比較(±s) g

表1 大鼠體質(zhì)量比較(±s) g
注:與空白組比較,#P<0.05,##P<0.01;與模型組比較,*P<0.05,**P<0.01。
組別 數(shù)量(n) 第0 天 第10 天 第21 天空白組 7 234.84±18.23 263.84±19.18 277.25±22.77模型組 7 239.40±10.17 221.56± 9.98## 229.16±17.16##西藥組 7 227.67±12.64 242.75±13.88** 251.17±14.02**中藥低劑量組 7 234.13± 8.91 229.11±10.79* 233.27±15.09*中藥中劑量組 7 239.52± 9.88 250.11±13.95** 254.94±18.94**中藥高劑量組 7 235.21±10.38 256.04±16.86** 268.43±22.43**
2.2 大鼠曠場實(shí)驗(yàn)評分比較 造模治療前(第0 天),各組大鼠曠場實(shí)驗(yàn)的水平及垂直運(yùn)動評分均無統(tǒng)計(jì)學(xué)的差異(P>0.05)。造模治療第10 天、21 天,與空白組相比,模型組大鼠水平及垂直運(yùn)動評分均下降(P<0.01);與模型組相比,西藥組及中藥各劑量組大鼠水平及垂直運(yùn)動評分均顯著升高(P<0.01)。見表2,表3。
表2 大鼠礦場實(shí)驗(yàn)水平運(yùn)動評分比較(±s) 次

表2 大鼠礦場實(shí)驗(yàn)水平運(yùn)動評分比較(±s) 次
注:與空白組比較,#P<0.05,##P<0.01;與模型組比較,*P<0.05,**P<0.01。
組別 n 第0 天 第10 天 第21 天空白組 7 74.92±10.35 70.75±10.82 71.33±12.07模型組 7 77.50± 8.15 18.26± 3.54## 26.83± 6.19##西藥組 7 71.25± 9.11 50.92±10.93** 53.00± 7.02**中藥低劑量組 7 72.67±12.14 39.05± 7.79** 42.73± 9.15**中藥中劑量組 7 70.66± 9.70 46.36±10.91** 48.50± 8.41**中藥高劑量組 7 72.92±11.14 63.62± 8.37** 65.18±10.35**
表3 大鼠礦場實(shí)驗(yàn)垂直運(yùn)動評分比較(±s) 次

表3 大鼠礦場實(shí)驗(yàn)垂直運(yùn)動評分比較(±s) 次
注:與空白組比較,#P<0.05,##P<0.01;與模型組比較,*P<0.05,**P<0.01。
組別 n 第0 天 第10 天 第21 天空白組 7 16.33±4.55 18.42±3.82 19.00±3.21模型組 7 18.92±3.33 3.58±3.10## 5.67±2.80##西藥組 7 17.00±4.31 10.18±2.35** 12.50±3.40**中藥低劑量組 7 18.41±4.69 9.43±2.93** 11.44±3.65**中藥中劑量組 7 18.13±3.81 10.36±3.05** 12.67±2.99**中藥高劑量組 7 17.92±3.38 12.78±3.36** 13.41±3.05**
2.3 大鼠糖水偏好百分率比較 造模治療前(第0 天)各組大鼠的糖水偏好百分率均無統(tǒng)計(jì)學(xué)差異(P>0.05)。造模治療第10 天,與空白組相比,模型組大鼠糖水偏好百分率降低(P<0.01);與模型組相比,西藥組及中藥各劑量組大鼠糖水偏好百分率均顯著升高(P<0.01)。造模治療第21 天,與空白組相比,模型組大鼠糖水偏好百分率降低(P<0.01);與模型組相比,中藥低劑量組大鼠糖水偏好百分率升高(P<0.05),西藥組、中藥中劑量及高劑量組大鼠糖水偏好百分率均顯著升高(P<0.01)。見表4。
表4 大鼠糖水偏好百分率比較(±s) %

表4 大鼠糖水偏好百分率比較(±s) %
注:與空白組比較,#P<0.05,##P<0.01;與模型組比較,*P<0.05,**P<0.01。
組別 n 第0 天 第10 天 第21 天空白組 7 80.79±5.11 82.21± 5.28 82.03±5.30模型組 7 79.90±4.37 48.10± 5.03## 50.91±4.43##西藥組 7 77.82±4.89 66.62± 6.21** 73.22±5.26**中藥低劑量組 7 78.70±4.93 67.51± 7.13** 70.14±7.45*中藥中劑量組 7 78.10±6.15 69.35±11.10** 75.00±9.20**中藥高劑量組 7 77.92±6.32 71.20± 7.24** 74.09±6.11**
2.4 大鼠強(qiáng)迫游泳實(shí)驗(yàn)比較 造模治療前(第0 天)各組大鼠的強(qiáng)迫游泳實(shí)驗(yàn)均差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。造模治療第10 天,與空白組相比,模型組大鼠游泳不動時(shí)間延長(P<0.01);與模型組相比,西藥組及中藥各劑量組大鼠游泳不動時(shí)間均顯著縮短(P<0.01)。造模治療第21 天,與空白組相比,模型組大鼠游泳不動時(shí)間延長(P<0.01);與模型組相比,中藥低劑量組大鼠游泳不動時(shí)間縮短(P<0.05),西藥組、中藥中劑量及高劑量組大鼠游泳不動時(shí)間均顯著縮短(P<0.01)。見表5。
表5 大鼠游泳不動時(shí)間比較(±s) s

表5 大鼠游泳不動時(shí)間比較(±s) s
注:與空白組比較,#P<0.05,##P<0.01;與模型組比較,*P<0.05,**P<0.01。
組別 n 第0 天 第10 天 第21 天空白組 7 77.75±10.21 76.90±13.08 74.31±12.78模型組 7 76.10±13.63 113.12±12.56## 110.23±17.31##西藥組 7 79.41±11.12 96.23±11.21** 94.92±13.20**中藥低劑量組 7 70.55±15.00 102.91± 9.87** 99.24±11.49*中藥中劑量組 7 72.30±12.64 98.45±18.07** 96.33±18.01**中藥高劑量組 7 74.34±14.48 96.17±12.49** 92.12± 9.93**
2.5 大鼠新奇抑制攝食-潛伏時(shí)間比較 造模治療前(第0 天)各組大鼠的潛伏時(shí)間均差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。造模治療第10 天,與空白組相比,模型組大鼠新奇抑食-潛伏時(shí)間延長(P<0.01);與模型組相比,西藥組及中藥各劑量組大鼠新奇抑食-潛伏時(shí)間均顯著縮短(P<0.01)。造模治療第21 天,與空白組相比,模型組大鼠新奇抑食-潛伏時(shí)間延長(P<0.01);與模型組相比,中藥低劑量組大鼠新奇抑食-潛伏時(shí)間縮短(P<0.05),西藥組、中藥中劑量及高劑量組大鼠新奇抑食-潛伏時(shí)間均明顯縮短(P<0.01)。見表6。
表6 大鼠抑制攝食-潛伏時(shí)間比較(±s) s

表6 大鼠抑制攝食-潛伏時(shí)間比較(±s) s
注:與空白組比較,#P<0.05,##P<0.01;與模型組比較,*P<0.05,**P<0.01。
組別 n 第0 天 第10 天 第21 天空白組 7 36.83±11.63 37.23±13.08 39.11±12.88模型組 7 31.16± 7.24 49.01±12.56## 47.20± 7.35##西藥組 7 35.42± 9.36 38.49±15.11** 37.09± 8.26**中藥低劑量組 7 37.19± 8.06 39.64±11.88** 38.34±13.23*中藥中劑量組 7 34.99±14.91 35.42±14.26** 34.75±15.01**中藥高劑量組 7 32.77±12.40 33.66± 8.63** 31.27± 9.80**
2.6 大鼠機(jī)械痛閾值比較 造模治療第1 天,各組大鼠的機(jī)械痛閾值比較均差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。造模治療第7 天,與空白組相比,模型組大鼠機(jī)械痛閾值明顯降低(P<0.01);與模型組比較,西藥組及中藥各劑量組大鼠機(jī)械痛閾值明顯升高(P<0.01)。造模治療第14 天,與空白組相比,模型組大鼠機(jī)械痛閾值顯著降低(P<0.01);與模型組比較,西藥及中藥高劑量組大鼠機(jī)械痛閾值升高(P<0.05),中藥低、中劑量組大鼠機(jī)械痛閾值明顯升高(P<0.01)。造模治療第21 天,與空白組相比,模型組大鼠機(jī)械痛閾值明顯下降(P<0.01);與模型組比較,西藥及中藥低劑量組大鼠機(jī)械痛閾值升高(P<0.05),中藥中、高劑量組大鼠機(jī)械痛閾值顯著升高(P<0.01)。見表7。
表7 大鼠機(jī)械痛閾值比較(±s) g

表7 大鼠機(jī)械痛閾值比較(±s) g
注:與空白組比較,#P<0.05,##P<0.01;與模型組比較,*P<0.05,**P<0.01。
組別 n 第1 天 第7 天 第14 天 第21 天空白組 7 43.75±5.32 42.65±2.53 41.17±4.72 41.98±3.99模型組 7 40.12±5.11 21.03±3.34## 22.75±3.64## 19.22±3.13##西藥組 7 38.22±6.15 37.44±4.11** 33.21±5.44* 31.15±4.32*中藥低劑量組 7 42.68±4.29 36.10±5.73** 35.14±6.19** 33.74±4.85*中藥中劑量組 7 39.97±6.42 38.50±6.31** 37.84±7.21** 35.95±6.37**中藥高劑量組 7 41.32±4.03 37.21±5.45** 33.50±5.03* 31.91±4.36**
2.7 大鼠杏仁核組織Iba1 及RhoA 蛋白表達(dá)結(jié)果 造模治療結(jié)束后,檢測大鼠杏仁核組織Iba1 蛋白的表達(dá)水平,與空白組相比,模型組大鼠杏仁核組織中的Iba1 升高,但差異無統(tǒng)計(jì)學(xué)意義(P>0.05);與模型組相比,西藥組及中藥各劑量組大鼠杏仁核組織中的Iba1 蛋白表達(dá)呈下降趨勢,但差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。檢測大鼠杏仁核組織RhoA蛋白表達(dá)水平,與空白組相比,模型組大鼠杏仁核中的RhoA 蛋白表達(dá)顯著升高(P<0.01);與模型組相比,中藥低劑量組大鼠杏仁核組織中的RhoA 蛋白表達(dá)無明顯差異(P>0.05),中藥中劑量組大鼠杏仁核組織中的RhoA 蛋白表達(dá)降低(P<0.05),西藥組及中藥高劑量組大鼠杏仁核組織中的RhoA 蛋白表達(dá)顯著降低(P<0.01)。見表8,圖1。

圖1 大鼠杏仁核組織中Iba1 及RhoA 蛋白的表達(dá)水平
表8 大鼠杏仁核中Iba1 及RhoA 蛋白表達(dá)比較(±s)
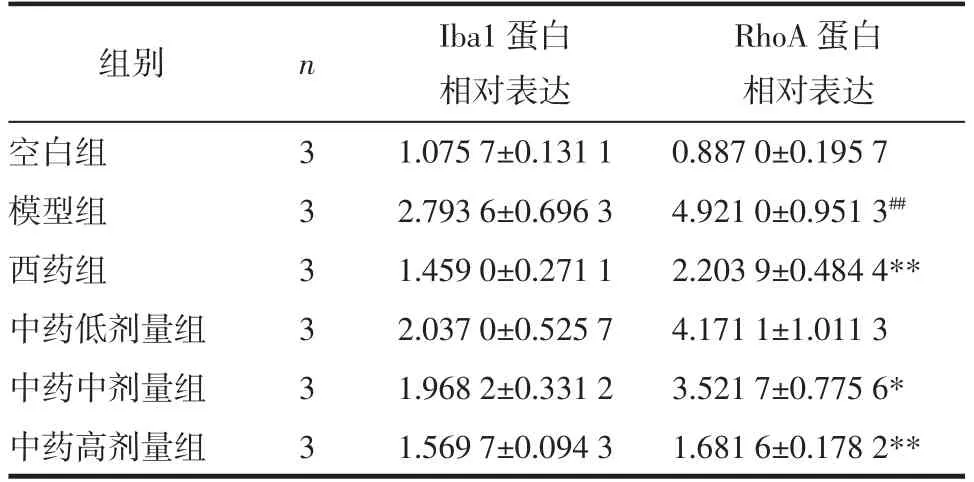
表8 大鼠杏仁核中Iba1 及RhoA 蛋白表達(dá)比較(±s)
注:與空白組比較,#P<0.05,##P<0.01;與模型組比較,*P<0.05,**P<0.01。
RhoA 蛋白相對表達(dá)空白組 3 1.075 7±0.131 1 0.887 0±0.195 7模型組 3 2.793 6±0.696 3 4.921 0±0.951 3##西藥組 3 1.459 0±0.271 1 2.203 9±0.484 4**中藥低劑量組 3 2.037 0±0.525 7 4.171 1±1.011 3中藥中劑量組 3 1.968 2±0.331 2 3.521 7±0.775 6*中藥高劑量組 3 1.569 7±0.094 3 1.681 6±0.178 2**組別 n Iba1 蛋白相對表達(dá)
3 討論
偏頭痛是臨床上常見的致殘性疾病之一。隨著現(xiàn)代社會壓力的增加,偏頭痛的患病人數(shù)逐年增加并趨于年輕化,偏頭痛反復(fù)頻繁發(fā)作且嚴(yán)重時(shí)使人喪失生活能力[16]。久而久之,患者產(chǎn)生負(fù)面情緒,影響患者的身心健康,致使很大一部分患者產(chǎn)生抑郁,進(jìn)而導(dǎo)致偏頭痛與抑郁共病疾患,使其喪失勞動生產(chǎn)力,減少了社會生產(chǎn)率,對社會經(jīng)濟(jì)造成極大影響。因此,應(yīng)盡早對偏頭痛-抑郁共病進(jìn)行普及與預(yù)防,重視中醫(yī)藥治療。
中醫(yī)認(rèn)為肝主疏泄、主藏血。肝臟疏泄功能失調(diào),影響人體氣機(jī),使情志產(chǎn)生變化。肝疏泄失調(diào),氣行不順,致使體內(nèi)肝氣瘀滯,使人出現(xiàn)情緒低落、喜嘆氣、胸脅兩肋脹痛等癥狀;情志不舒,氣郁于內(nèi),進(jìn)而化火,肝火上炎出現(xiàn)面紅耳赤、耳鳴、頭脹頭痛等。肝藏血功能受損,肝血不足,可出現(xiàn)頭暈?zāi)垦!⑿臒┮鈦y等;肝氣血不足,周身氣血運(yùn)行不暢,日久損傷正氣,出現(xiàn)濕氣、痰濁、內(nèi)熱、淤血等病理產(chǎn)物[17],發(fā)為頭痛抑郁共病。解郁止痛方是治療偏頭痛—抑郁共病效果顯著的驗(yàn)方。該方以川芎、柴胡共同組成君藥,川芎辛溫升散功用活血行氣、祛風(fēng)止痛,《醫(yī)學(xué)啟源》有“頭痛需用川芎”之說,酒制川芎,可增強(qiáng)其止痛之功。現(xiàn)代醫(yī)學(xué)研究表明;川芎中含有的阿魏酸鈉及川芎嗪可明顯抑制偏頭痛活性[18]。此外,川芎嗪還有抗炎、防止細(xì)胞老化及營養(yǎng)神經(jīng)等功能[19-21]。柴胡可疏肝解郁,疏散退熱,其性升散,古有“柴胡劫肝陰”之說;現(xiàn)代藥理學(xué)研究表明:柴胡含有的皂苷、多糖、黃酮等具有抗炎、抗抑郁及保護(hù)心、肝、腎臟器的作用[22-24]。兩者共用疏肝調(diào)肝止痛功用更甚。合歡皮為臣,歸心、肝、肺經(jīng),功用解郁安神活血,提取物合歡皮總皂苷可鎮(zhèn)靜寧心安神,對于郁癥引起的心神不寧、失眠多夢效果甚佳。黃芪可益氣生津養(yǎng)血,含有的黃芪多糖等對機(jī)體免疫、造血功能及心腦血管系統(tǒng)等均具有良好的保護(hù)作用,偏頭痛—抑郁病癥纏綿難愈,久病易耗傷元?dú)猓侗静菥V目》言黃芪“耄,長也,黃耄色黃,為補(bǔ)藥之長”,故黃芪可扶正氣以驅(qū)邪。全蝎歸肝經(jīng),功用息風(fēng)鎮(zhèn)痙、通絡(luò)止痛,可應(yīng)用于風(fēng)濕頑痹及偏正頭痛,其含有的三甲胺、甜菜堿及牛磺酸等可鎮(zhèn)靜安神、抗驚厥、抗血栓及鎮(zhèn)痛等。全方中諸藥和用共奏疏肝活血、理氣補(bǔ)氣之功。
偏頭痛所表現(xiàn)出來的疼痛是發(fā)作性的鈍痛,其嚴(yán)重程度可能與患者負(fù)面情緒密切相關(guān)[25]。研究表明,疼痛和抑郁疾患均與杏仁核之間有不可分割的關(guān)系,杏仁核不僅可參與疼痛及抑郁的生理過程,還能調(diào)控情緒并記錄與儲存所發(fā)生的情感事件[26]。因此,它參與對疼痛刺激的編碼和調(diào)節(jié),從而在痛與鎮(zhèn)痛中均起重要作用。
現(xiàn)代醫(yī)學(xué)對于偏頭痛-抑郁共病疾患的病理機(jī)制尚不完全清楚。有研究發(fā)現(xiàn),偏頭痛的發(fā)病機(jī)制與小膠質(zhì)細(xì)胞活化有很大關(guān)系。小膠質(zhì)細(xì)胞占據(jù)神經(jīng)膠質(zhì)細(xì)胞的5%-20%,小膠質(zhì)細(xì)胞被激活后,會產(chǎn)生大量的神經(jīng)遞質(zhì)(腦源性神經(jīng)營養(yǎng)因子、腫瘤壞死因子、白細(xì)胞介素等)提高神經(jīng)興奮作用,神經(jīng)興奮性增強(qiáng)導(dǎo)致痛覺過敏進(jìn)而產(chǎn)生偏頭痛[27]。Iba1被認(rèn)為是小膠質(zhì)細(xì)胞激活的標(biāo)志,它是結(jié)合特殊信號傳遞的信號分子,是一種特異性的鈣結(jié)合蛋白,可捆綁肌動蛋白活性、參與小膠質(zhì)細(xì)胞的重塑并在激活的小膠質(zhì)細(xì)胞中調(diào)控細(xì)胞的遷移、膜褶皺及吞噬。RhoA 是一種小分子G 蛋白,在活性(GTP 結(jié)合)和非活性(GDP 結(jié)合)形式之間循環(huán)。GTP-RhoA 通過與下游Rho 蛋白激酶ROCK 的相互作用參與調(diào)控細(xì)胞功能。Rho 蛋白激酶ROCK 抑制劑可改變小膠質(zhì)細(xì)胞極化、增強(qiáng)小膠質(zhì)細(xì)胞吞噬能力,降低神經(jīng)病理學(xué)疼痛的發(fā)生,表明ROCK 介導(dǎo)偏頭痛的病理作用,但對于RhoA 參與偏頭痛的發(fā)生無明確研究。因此本實(shí)驗(yàn)通過硝酸甘油注射液及不同刺激誘導(dǎo)偏頭痛—抑郁共病大鼠模型,予以中醫(yī)藥的治療來研究偏頭痛—抑郁共病大鼠行為學(xué)及腦組織杏仁核內(nèi)Iba1 及RhoA 蛋白含量的變化。
本實(shí)驗(yàn)研究結(jié)果顯示:解郁止痛方能明顯改善偏頭痛—抑郁共病模型大鼠體質(zhì)量、曠場實(shí)驗(yàn)水平和垂直運(yùn)動評分、糖水偏好程度,降低強(qiáng)迫游泳不動時(shí)間及新奇抑食—潛伏時(shí)間,減少偏頭痛發(fā)作時(shí)的撓頭、攀籠次數(shù),降低機(jī)械痛閾值。偏頭痛—抑郁共病模型組大鼠腦組織杏仁核內(nèi)Iba1 及RhoA 蛋白表達(dá)水平明顯升高,表明兩者共病可能由發(fā)生中樞敏化激活小膠質(zhì)細(xì)胞介導(dǎo)Iba1/RhoA/ROCK 信號通路引發(fā),而解郁止痛方能夠有效降低本實(shí)驗(yàn)?zāi)P痛笫竽X組織杏仁核內(nèi)Iba1 及RhoA 的蛋白表達(dá)水平,推測解郁止痛方可能通過抑制Iba1/RhoA/ROCK 信號通路激活,減少中樞敏化,從而抑制小膠質(zhì)細(xì)胞活化,減少炎癥反應(yīng),從而減少偏頭痛-抑郁共病的發(fā)生。

