多模態(tài)MRI技術(shù)鑒別肺癌病理類型的研究進(jìn)展
張紅玉(綜述), 錢(qián)麗霞(審校)
全球肺癌的發(fā)病率和病死率均較高。據(jù)全球癌癥統(tǒng)計(jì)報(bào)告2020年的數(shù)據(jù)統(tǒng)計(jì),全球肺癌新發(fā)病例約220萬(wàn)例,發(fā)病率居第二位(11.4%)[1];2018年,我國(guó)肺癌新發(fā)病例數(shù)和死亡數(shù)均列于首位[2]。肺癌是一種復(fù)雜的疾病,其治療效果取決于患者的特征、腫瘤的組織學(xué)類型,以及評(píng)估的生物標(biāo)志物,不同病理類型的肺癌治療方案不同。因此,準(zhǔn)確地判斷肺癌的病理類型對(duì)患者的治療及預(yù)后至關(guān)重要。
目前,臨床用于鑒別肺癌病理類型的方式有很多種,例如:組織病理學(xué)活檢、計(jì)算機(jī)斷層掃描(computed tomography,CT)、正電子發(fā)射斷層掃描(positron emission tomography,PET)及磁共振成像(magnetic resonance imaging,MRI)等,各種檢查方式各有利弊。組織病理學(xué)檢查是肺癌診斷和病理分型的金標(biāo)準(zhǔn),廣泛應(yīng)用于臨床,但也存在部分禁忌證,例如依從性差或心肺功能不好的患者易發(fā)生術(shù)前并發(fā)癥或間質(zhì)性肺病。CT或PET/CT是胸部最常用的檢查方法,在肺癌病理類型的鑒別方面也有一定價(jià)值,例如多種雙源CT灌注參數(shù)聯(lián)合對(duì)非小細(xì)胞肺癌(non-small cell lung cancer, NSCLC)患者的病理類型具有較高鑒別價(jià)值,能譜CT多參數(shù)成像也能夠?yàn)榉伟┎±眍愋偷蔫b別診斷提供幫助,但CT的軟組織對(duì)比度差且輻射劑量高。MRI則可提供良好的軟組織對(duì)比度。研究[3]發(fā)現(xiàn),MRI增強(qiáng)掃描及彌散加權(quán)成像(diffusion-weighted imaging, DWI)可出色地鑒別兩者,同時(shí)MRI通過(guò)多序列成像提高了區(qū)分肺癌實(shí)性或壞死囊性區(qū)域的敏感性和準(zhǔn)確度,從而提供更多有關(guān)病變成分的信息,且無(wú)電離輻射。SANCHEZ等[4]依據(jù)CT的檢查結(jié)果將結(jié)節(jié)分類后行MRI檢查,結(jié)果顯示,肺部MRI有足夠的性能檢測(cè)實(shí)性和亞實(shí)性肺結(jié)節(jié)(>4 mm),可替代CT檢查。這說(shuō)明通過(guò)更強(qiáng)的梯度、更高的場(chǎng)均勻性、更短的回波時(shí)間和并行成像重建,可以實(shí)現(xiàn)MRI技術(shù)的發(fā)展(圖1)。此外,從磁共振動(dòng)態(tài)對(duì)比增強(qiáng)(magnetic resonance dynamic contrast enhancement, DCE-MRI)導(dǎo)出的常數(shù)和從體素內(nèi)非相干運(yùn)動(dòng)(intravoxel incoherent motion, IVIM)DWI模型導(dǎo)出的表觀擴(kuò)散系數(shù)(apparent diffusion coefficient, ADC)均顯示,功能MRI技術(shù)是一種區(qū)分肺癌與孤立性肺結(jié)節(jié)的潛在方法[5],但目前該技術(shù)尚未在臨床上廣泛使用。近年來(lái),MRI被越來(lái)越廣泛地應(yīng)用于肺癌的研究中。本研究主要對(duì)多模態(tài)MRI技術(shù)鑒別肺癌病理類型的研究進(jìn)展進(jìn)行綜述,主要包括酰胺質(zhì)子轉(zhuǎn)移(amide proton transfer, APT)成像、IVIM、DWI、彌散峰度成像(diffusion kurtosis imaging,DKI)、DCE-MRI、磁共振波譜成像(magnetic resonance spectroscopy,MRS)等技術(shù),報(bào)道如下。

A:計(jì)算機(jī)斷層掃描;B:超短回波時(shí)間;C:半傅立葉單次激發(fā)Turbo自旋回波;D:容積內(nèi)插屏氣檢查。
1 傳統(tǒng)檢查方法篩查肺癌及鑒別病理類型的價(jià)值
CT是檢測(cè)肺結(jié)節(jié)的常用方式,但輻射負(fù)荷高。目前,MRI作為CT潛在的無(wú)輻射的替代方法,廣泛應(yīng)用于臨床。YU等[6]通過(guò)比較各種MRI序列與CT的肺結(jié)節(jié)檢出率,得出r-Vibe可準(zhǔn)確檢測(cè)出94% 的肺結(jié)節(jié),其中直徑≥6 mm的肺結(jié)節(jié)的檢出率為100%,顯示出MRI檢測(cè)肺結(jié)節(jié)的可行性。然而,一項(xiàng)薈萃分析[7]顯示,MRI并不能取代CT診斷肺結(jié)節(jié),CT和MRI在診斷肺結(jié)節(jié)方面均具有較高的準(zhǔn)確性,但CT在敏感性、特異性、陽(yáng)性似然比、陰性似然比和曲線下面積方面均優(yōu)于MRI。此外,OHNO等[8]通過(guò)比較薄層MRI和低劑量薄層CT檢測(cè)肺結(jié)節(jié)和評(píng)估結(jié)節(jié)類型的準(zhǔn)確率,發(fā)現(xiàn)兩者的差別無(wú)統(tǒng)計(jì)學(xué)意義。不同病理類型的肺癌在MRI上的表現(xiàn)各有特點(diǎn),T2WI的信號(hào)形態(tài)改變尤為明顯,這有助于不同病理類型肺癌的鑒別[9]。但傳統(tǒng)MRI的肺部成像受到低質(zhì)子密度、快速信號(hào)衰減和呼吸運(yùn)動(dòng)偽影的限制,篩查早期肺結(jié)節(jié)及鑒別肺癌病理類型的準(zhǔn)確率還有待提高。因此,需要依靠MRI技術(shù)的發(fā)展,利用各種功能性MRI技術(shù)的不同優(yōu)勢(shì)來(lái)克服這些局限性,更有價(jià)值地補(bǔ)充傳統(tǒng)MRI技術(shù)對(duì)于肺癌病理類型鑒別的意義。
2 APT成像篩查肺癌及鑒別病理類型的價(jià)值
2.1 原理 瘤灶代謝的變化反映了腫瘤的特征。非侵入性成像方法通過(guò)監(jiān)測(cè)體內(nèi)代謝物的變化或表征腫瘤微環(huán)境,在闡明腫瘤生物學(xué)方面發(fā)揮著重要作用。在MRI模式中,化學(xué)交換飽和技術(shù)(chemical exchange saturation transfer,CEST)已成為一種新技術(shù),能夠選擇性飽和代謝物結(jié)合的質(zhì)子,這種飽和通過(guò)化學(xué)交換進(jìn)一步影響自由水的信號(hào)強(qiáng)度。因此,通過(guò)檢測(cè)水的信號(hào),可間接反映肽、葡萄糖、酰胺質(zhì)子及黏多糖等低濃度代謝物及微環(huán)境的特征,可為腫瘤代謝和酸中毒的體內(nèi)成像提供高空間分辨率和高靈敏度[10]。APT是CEST成像的一個(gè)子集,具體指游離組織水(體水)的質(zhì)子與內(nèi)源移動(dòng)的蛋白質(zhì)和肽的酰胺基團(tuán)(—NH)之間的化學(xué)交換。該技術(shù)無(wú)需常規(guī)造影劑或放射性示蹤劑即可獲得有關(guān)代謝活動(dòng)和組織微環(huán)境的額外信息。
2.2 應(yīng)用 OHNO等[11]前瞻性評(píng)估APT加權(quán)CEST MRI表征胸部病變的能力,研究結(jié)果表明,惡性腫瘤磁化轉(zhuǎn)移率的不對(duì)稱性顯著高于良性病變、腺癌顯著高于鱗癌。APT加權(quán)CEST MRI成像可以顯示惡性和良性胸部病變、肺癌和其他胸部惡性腫瘤、肺癌和惡性淋巴瘤以及腺癌和鱗癌之間的顯著差異。因此,在3.0T MRI系統(tǒng)上使用CEST成像,有望鑒別和表征胸部結(jié)節(jié)或腫塊。APT成像對(duì)于表征肺癌亞型潛在有用。TOGAO等[12]在小鼠肺癌原位模型的基礎(chǔ)上進(jìn)行研究,證明了肺腫瘤體內(nèi)氨基質(zhì)子轉(zhuǎn)移成像的可行性,該方法可定量區(qū)分2種不同類型的肺腫瘤,且APT效應(yīng)與腫瘤細(xì)胞的增殖能力呈正相關(guān)。APT成像有可能提供一種無(wú)創(chuàng)的區(qū)分肺癌類型或分級(jí)的表征測(cè)試,最終可能減少肺癌有創(chuàng)穿刺活檢或切除的需要,利于早日開(kāi)啟治療,改善肺癌患者的預(yù)后。還有學(xué)者[13]通過(guò)比較APT和IVIM與PET成像區(qū)分良性和惡性孤立性肺部病變及其亞型的能力,發(fā)現(xiàn)APT比PET成像能更有效地區(qū)分肺鱗癌和腺癌,可成為表征肺部病變的一種成像方式。OHNO等[14]收集了82例肺結(jié)節(jié)患者,比較APT、DWI和FDG-PET/CT成像區(qū)分惡性和良性肺結(jié)節(jié)的能力,結(jié)果發(fā)現(xiàn),雖然ADC的敏感性顯著高于非對(duì)稱磁化轉(zhuǎn)移率(magnetization transfer ratio asymmetry,MTRasym)和最大標(biāo)準(zhǔn)攝取值(maximum value of standard uptake value,SUVmax),但后兩者的特異性顯著高于ADC。MTRasym與SUVmax聯(lián)合使用的靈敏度顯著高于兩者單獨(dú)使用。此外,MTRasym(3.5×10-6)和SUVmax聯(lián)合檢測(cè)的特異性和準(zhǔn)確性顯著高于ADC,APT成像與DWI和FDG-PET/CT一樣可用于區(qū)分惡性和良性肺結(jié)節(jié)。
3 IVIM 篩查肺癌及鑒別病理類型的價(jià)值
3.1 原理 生物體的微觀運(yùn)動(dòng)包括水分子的擴(kuò)散和血液的微循環(huán)。IVIM是一種雙指數(shù)模型,它將生物組織分為2個(gè)組成部分:一個(gè)緩慢移動(dòng)的組成部分,其中水分子基于布朗運(yùn)動(dòng)擴(kuò)散;一個(gè)快速移動(dòng)的組成部分,其中水分子由于血液循環(huán)而移動(dòng)。IVIM的3個(gè)定量參數(shù)分別是純擴(kuò)散系數(shù)(D)、偽擴(kuò)散系數(shù)(D*)和灌注分?jǐn)?shù)(f)。D代表純的水分子擴(kuò)散運(yùn)動(dòng)(緩慢的擴(kuò)散運(yùn)動(dòng));D*為血液循環(huán)產(chǎn)生的假擴(kuò)散系數(shù),代表灌注相關(guān)的擴(kuò)散運(yùn)動(dòng)(快速的擴(kuò)散運(yùn)動(dòng));f是感興趣區(qū)域內(nèi)毛細(xì)血管網(wǎng)中存在的血液循環(huán)灌注效應(yīng)擴(kuò)散在整體擴(kuò)散效應(yīng)中的體積分?jǐn)?shù),代表血流量。
3.2 應(yīng)用 目前,IVIM技術(shù)已應(yīng)用到活體肝臟、乳腺、腎臟、前列腺、胰腺和頭頸等部位的多種疾病的灌注測(cè)量中,展示了IVIM技術(shù)的潛力。ZHENG等[15]通過(guò)評(píng)估IVIM定量參數(shù)在預(yù)測(cè)術(shù)前肺癌組織中Ki-67表達(dá)水平中的價(jià)值,以及IVIM和DKI定量值在小細(xì)胞肺癌(small cell lung cancer, SCLC)和NSCLC之間是否存在差異,得出IVIM導(dǎo)出的真實(shí)D值與肺癌組織中Ki-67的表達(dá)呈負(fù)相關(guān),首次證明了IVIM的D值在區(qū)分SCLC和NSCLC方面的準(zhǔn)確性,同時(shí)發(fā)現(xiàn)在3個(gè)定量參數(shù)中,D值在區(qū)分Ki-67高和低表達(dá)狀態(tài)方面具有最高的診斷性能,這為預(yù)測(cè)Ki-67表達(dá)和區(qū)分不同肺癌類型提供了一種非侵入性的方法,未來(lái)可以用IVIM定量參數(shù)來(lái)評(píng)估腫瘤的增殖能力。陳明梅等[16]通過(guò)分析IVIM定量參數(shù)在不同類型肺癌中的意義,發(fā)現(xiàn)SCLC患者的D和D*值低于腺癌和鱗癌患者,而腺癌與鱗癌間的定量參數(shù)差別無(wú)統(tǒng)計(jì)學(xué)意義,且D值鑒別診斷肺癌病理類型的價(jià)值更高、各定量參數(shù)結(jié)合起來(lái)的診斷效能最佳。黨珊等[17]通過(guò)探究 98例肺癌患者中IVIM 3個(gè)定量參數(shù)鑒別SCLC與NSCLC的價(jià)值,表明D值對(duì)于鑒別兩者有意義,而D*值和f值對(duì)鑒別無(wú)意義。然而,另有學(xué)者[18]發(fā)現(xiàn),腺癌的f值高于鱗癌和SCLC,而鱗癌與SCLC間差別無(wú)統(tǒng)計(jì)學(xué)意義。
4 DWI篩查肺癌及鑒別病理類型的價(jià)值
4.1 原理 DWI描述了生物組織中水分子的微觀布朗運(yùn)動(dòng),反映了水分子彌散限制的變化,以表征組織的微觀結(jié)構(gòu),從而鑒別不同病理類型的腫瘤。擴(kuò)散限制的變化可以使用ADC來(lái)量化。ADC是體內(nèi)量化毛細(xì)血管灌注和自旋核與擴(kuò)散分子合并的組合效應(yīng)的最佳成像參數(shù)。Ki-67蛋白是一種與腫瘤增殖相關(guān)的核抗原,與肺癌的發(fā)生、轉(zhuǎn)移和預(yù)后密切相關(guān)。Ki-67的高表達(dá)與腫瘤細(xì)胞高增殖狀態(tài)有關(guān),增加的腫瘤細(xì)胞密度限制了水分子擴(kuò)散,并相應(yīng)降低ADC值[19]。
4.2 應(yīng)用 LI等[20]通過(guò)探討原始T1-mapping和DWI對(duì)肺癌病理類型和分化程度的鑒別價(jià)值及其與Ki-67蛋白表達(dá)的相關(guān)性,得出SCLC與鱗癌、腺癌ADC值的差別均有統(tǒng)計(jì)學(xué)意義,鱗癌與腺癌ADC值的差別無(wú)統(tǒng)計(jì)學(xué)意義,ADC值與Ki-67指數(shù)之間存在負(fù)相關(guān),且本次研究首次將DWI與T1-mapping 相結(jié)合,證實(shí)了兩者聯(lián)合可無(wú)創(chuàng)鑒定肺癌的病理類型和分化程度,并可提高分化程度的診斷功效。REN等[21]通過(guò)比較Ki-67指數(shù)在腺癌、鱗癌和SCLC中的不同表達(dá)水平,發(fā)現(xiàn)ADC值與Ki-67 指數(shù)間存在中度負(fù)相關(guān)(相關(guān)系數(shù)介于0.3~0.7),而在區(qū)分肺癌病理類型方面,兩者并無(wú)相關(guān)性,且腺癌的ADC值高于其他類型肺癌。USUDA等[22]通過(guò)分析DWI的ADC與肺癌病理之間的關(guān)系,發(fā)現(xiàn)黏液腺癌的ADC值明顯高于其他細(xì)胞類型的腺癌,且有壞死的肺癌的ADC值明顯低于無(wú)壞死的肺癌,肺癌的ADC值隨細(xì)胞分化程度的降低而降低。其他學(xué)者[23]也發(fā)現(xiàn),NSCLC患者的ADC值明顯高于SCLC患者,腺癌的ADC值明顯高于鱗癌。原因可能是SCLC細(xì)胞的數(shù)量多且核大,幾乎沒(méi)有細(xì)胞質(zhì),從而限制了水分子的擴(kuò)散,降低了ADC值。DWI可以比CT提供更多的信息,包括腫瘤內(nèi)脈管系統(tǒng)、淋巴結(jié)受累和積液等(圖2)。ZHANG等[24]分析了孤立性肺部病變(solitary pulmonary lesions,SPL)中ADC值與多個(gè)組織病理學(xué)參數(shù)之間的相關(guān)性,發(fā)現(xiàn)惡性SPL中細(xì)胞密度和黏液與ADC值獨(dú)立相關(guān),但核質(zhì)比、壞死分?jǐn)?shù)和分化程度均與ADC值無(wú)關(guān);同時(shí),良性腫瘤的ADC值與組織病理學(xué)參數(shù)無(wú)明顯相關(guān)性。因此,ADC值可以準(zhǔn)確鑒別良性和惡性肺腫瘤。

1例62歲左上葉肺腺癌女性患者。ROI:感興趣區(qū)。A:CT圖像;B:T2加權(quán)圖像;C:放置ROI的DWI ADC圖(ROI中的平均ADC值為1.01×10-3 mm2/s);D:用于分析的組織病理切片中的1個(gè)視野。
5 DKI篩查肺癌及鑒別病理類型的價(jià)值
5.1 原理 DKI是DWI的擴(kuò)展[25],其特點(diǎn)是描述非高斯分布水分子擴(kuò)散的模型,可以更加準(zhǔn)確地反映癌灶的微觀結(jié)構(gòu)特征。DKI模型的2個(gè)定量參數(shù)分別是反映感興趣區(qū)域組織微結(jié)構(gòu)復(fù)雜性的平均擴(kuò)散峰度值(mean kurtosis,MK)和反映水分子擴(kuò)散水平及阻力的平均擴(kuò)散率(mean diffusivity,MD)。
MK為DKI技術(shù)最關(guān)鍵的參數(shù),定義為擴(kuò)散峰度在所有方向的平均值。MD與ADC類似,均反映了水分子在單位時(shí)間內(nèi)擴(kuò)散運(yùn)動(dòng)的范圍,并且與細(xì)胞密度數(shù)量即細(xì)胞內(nèi)的基質(zhì)緊密相關(guān)。
5.2 應(yīng)用 目前,在肺部病變的評(píng)估領(lǐng)域,只有少數(shù)研究探討了DKI在區(qū)分肺癌病理學(xué)類型方面的價(jià)值。謝磊等[26]通過(guò)探討DKI模型成像技術(shù)在鑒別肺癌病理學(xué)類型中的價(jià)值,得出SCLC與腺癌及鱗癌MD值的差別均有統(tǒng)計(jì)學(xué)意義,而腺癌與鱗癌MD值的差別無(wú)統(tǒng)計(jì)學(xué)意義;SCLC、腺癌和鱗癌的MK值兩兩比較,差別均無(wú)統(tǒng)計(jì)學(xué)意義,且肺癌的分化程度與DKI的定量參數(shù)有關(guān),即與MD值呈正相關(guān),與MK值呈負(fù)相關(guān)。然而,部分研究卻得出相反的結(jié)論,例如FENG等[27]通過(guò)研究DKI參數(shù)在NSCLC分型中的應(yīng)用,發(fā)現(xiàn)腺癌的MK值顯著高于鱗癌,2組的MD值差別無(wú)統(tǒng)計(jì)學(xué)意義。本研究進(jìn)一步探討了ADC和MD在評(píng)價(jià)NSCLC分期中的價(jià)值,結(jié)果顯示,ADC和MD與NSCLC分期無(wú)明顯關(guān)聯(lián)。這可能是由于NSCLC分期是根據(jù)原發(fā)灶大小、浸潤(rùn)深度、鄰近組織受累范圍、有無(wú)淋巴結(jié)轉(zhuǎn)移等多種因素綜合判斷的,而ADC和MD主要反映細(xì)胞密度。因此僅根據(jù)ADC和MD值不能準(zhǔn)確預(yù)測(cè)腫瘤分期。
6 DCE-MRI篩查肺癌及鑒別病理類型的價(jià)值
6.1 原理 DCE-MRI通過(guò)高壓注射器向靜脈團(tuán)中注入對(duì)比劑后,連續(xù)不斷地在病變區(qū)域內(nèi)掃描檢查。由于對(duì)比劑的外滲及肺部不同性質(zhì)的病變對(duì)代謝的影響差異,不同病灶的信號(hào)強(qiáng)度變化不同,從而可用于檢測(cè)和反映肺癌的血供規(guī)律,對(duì)肺部的腫塊性質(zhì)進(jìn)行定性和定量評(píng)估[5,28]。在擴(kuò)展的Tofts數(shù)學(xué)模型的基礎(chǔ)上進(jìn)行分析,得到3個(gè)定量參數(shù):從血漿到血管外細(xì)胞間隙(extravascular extracellular space,EES)的體積轉(zhuǎn)移常數(shù)(Ktrans),主要受血流灌注及組織滲透率的影響;從EES到血漿的速率常數(shù)(Kep),是反映造影劑從血管外和細(xì)胞外空間轉(zhuǎn)移回血液的速率的反向速率常數(shù);作為每單位體積組織的EES的體積(Ve),反映血供情況、組織細(xì)胞結(jié)構(gòu)特點(diǎn),且與預(yù)后相關(guān)[29]。
6.2 應(yīng)用 王大勇等[30]發(fā)現(xiàn),DCE-MRI定量參數(shù)有助于鑒別肺癌的不同病理類型,可有效指導(dǎo)肺癌的臨床診治,肺腺癌的定量參數(shù)Ktrans、Kep及Ve值均顯著高于鱗癌及SCLC。庫(kù)雷志等[31]也發(fā)現(xiàn),不同病理類型肺癌的3個(gè)定量參數(shù)有差異,鱗癌與SCLC的Ktrans、Kep及Ve值均小于腺癌(圖3)。血流動(dòng)力學(xué)的半定量參數(shù)也可用來(lái)展示肺部癌性病灶及微循環(huán)灌注的改變。孟思等[32]發(fā)現(xiàn),肺癌患者血流動(dòng)力學(xué)的半定量參數(shù)與肺癌的病理類型緊密相關(guān),腺癌患者的達(dá)峰時(shí)間和流入速率均顯著高于鱗癌和SCLC。此外,由于肺癌、肺部炎性及良性腫塊患者之間信號(hào)強(qiáng)度-時(shí)間(SI-T)曲線的重疊與交叉,良性病灶與急性炎癥患者病變區(qū)通常會(huì)產(chǎn)生肉芽腫,并伴有不同分化程度,且不同病理類型的肺癌患者SI-T曲線也存在一定差異,因此,不能單純依靠SI-T曲線對(duì)肺部病變進(jìn)行鑒別診斷。另有學(xué)者[33]發(fā)現(xiàn),DCE-MRI定量灌注直方圖可作為一種無(wú)創(chuàng)且可復(fù)制的方法,間接評(píng)價(jià)肺癌PI3K/Akt/mTOR信號(hào)通路基因的激活情況,為MRI在分子水平上評(píng)價(jià)腫瘤的異質(zhì)性提供了新方法。

A:1例55歲左肺下葉鱗癌女性患者。箭頭所指?jìng)尾蕡D示ROI內(nèi)動(dòng)態(tài)增強(qiáng)定量參數(shù)Ktrans、Kep、Ve值分別為0.297 min-1、1.633 min-1、0.185;B:1例55歲左肺上葉小細(xì)胞肺癌男性患者。箭頭所指?jìng)尾蕡D上測(cè)的動(dòng)態(tài)增強(qiáng)定量參數(shù)Ktrans、Kep、Ve值分別為 0.077 min-1、0.592 min-1、0.130。
7 MRS篩查肺癌及鑒別病理類型的價(jià)值
7.1 原理 MRS為目前唯一能無(wú)創(chuàng)性觀察活體組織代謝及生化變化的技術(shù)[34],主要利用原子核化學(xué)位移現(xiàn)象進(jìn)行成像。不同化合物的相同原子核以及相同化合物的不同原子核之間,由于所處的化學(xué)環(huán)境不同,其周圍磁場(chǎng)可有輕微變化,共振頻率也會(huì)有差異,這種情況就是化學(xué)位移現(xiàn)象。MRS的原理就是通過(guò)共振頻率的微小差異區(qū)分不同化學(xué)位移,從而鑒別感興趣區(qū)域內(nèi)組織不同化學(xué)物質(zhì)的類型及含量。MRS是振幅與頻率的函數(shù),橫軸表示化學(xué)位移(頻率差別),單位為百萬(wàn)分之一(10-6),縱軸表示信號(hào)強(qiáng)度。由于心臟搏動(dòng)和呼吸運(yùn)動(dòng)導(dǎo)致勻場(chǎng)的受限及定位困難,體外1H-MRS 在肺組織的應(yīng)用較為困難,且圖像中乳酸峰與脂質(zhì)信號(hào)常重疊,因此,MRS較少用于肺癌的檢測(cè)。但FUJIMOTO等[35]用1H-MRS 檢測(cè)了1例右上葉肺腺癌的乳酸和膽堿,顯示出肺癌較正常組織有較高的乳酸和膽堿信號(hào)。
7.2 應(yīng)用 血清代謝譜可能在臨床無(wú)癥狀階段檢測(cè)出肺癌,因此,建立血清代謝譜可為臨床提供巨大意義。JORDAN等[36]通過(guò)同時(shí)測(cè)量肺腺癌和鱗癌患者的組織和血清代謝譜,基于病理學(xué)結(jié)果使用可測(cè)量代謝物的主成分和典型分析,建立評(píng)價(jià)癌癥類型的組織代謝組學(xué)特征及代謝譜,認(rèn)為血清MRI光譜學(xué)可以區(qū)分肺癌的病理類型(圖4)。ROCHA等[37]通過(guò)高分辨率魔角旋轉(zhuǎn)MRI光譜分析肺癌病灶,指出腺癌與磷脂和蛋白質(zhì)的分解代謝相關(guān),而鱗癌與較強(qiáng)的糖酵解和谷氨酰胺的分解代謝相關(guān)。其他腫瘤代謝特征,如肌酸和谷胱甘肽在鱗癌中特別突出,牛磺酸和尿苷核苷酸在腺癌中增加較為明顯,均顯示出輔助鑒別肺腫瘤亞型的巨大潛力。還有研究[38]對(duì)常規(guī)臨床實(shí)踐期間獲得的10例腺癌、10例鱗癌和10例非惡性疾病患者的淋巴結(jié)穿刺液進(jìn)行代謝組學(xué)分析,生成代謝譜,證明了基于淋巴結(jié)抽吸物的代謝特征及淋巴結(jié)抽吸物代謝物分析鑒別肺癌病理類型的可行性和相關(guān)性,并揭示新的治療靶點(diǎn),補(bǔ)充和完善肺癌診斷的有效途徑。
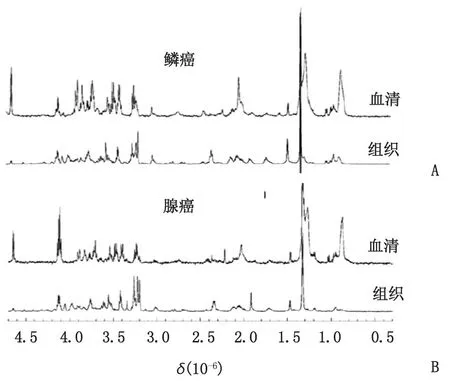
HRMAS:高分辨率魔角旋轉(zhuǎn)。δ:化學(xué)位移。A:鱗癌患者完整組織和配對(duì)血清的HRMAS MRI譜;B:腺癌患者完整組織和配對(duì)血清的HRMAS MRI譜。
綜上所述,雖然多模態(tài)MRI仍存在許多局限性,例如脂肪干擾、呼吸運(yùn)動(dòng)偽影及B0/B1不均勻性等,但該技術(shù)將在肺癌的診療中發(fā)揮應(yīng)有的作用。組織病理學(xué)檢查雖然是診斷肺癌和判斷病理分型的金標(biāo)準(zhǔn),但也存在一些禁忌證。無(wú)論是CT還是PET-CT都無(wú)法避免電離輻射,同時(shí)也不能直觀反映腫瘤組織的分子生物學(xué)特征。MRI作為一種無(wú)創(chuàng)、安全且具有高分辨率的檢查技術(shù),與CT或PET-CT相比,具有無(wú)電離輻射的優(yōu)點(diǎn),不僅對(duì)解剖學(xué)成像,而且對(duì)生理和化學(xué)特性成像具有無(wú)限的可能性。利用其功能成像,可無(wú)創(chuàng)地了解病變的組織學(xué)特征,有助于區(qū)分肺癌的病理類型和腫瘤的分化程度,并且可通過(guò)分析相關(guān)定量參數(shù)與增殖指數(shù)Ki-67的相關(guān)性,發(fā)掘功能性MRI評(píng)估肺癌患者疾病進(jìn)展的潛力,有望成為輔助肺癌診治的有效手段。

