高生物利用度姜黃素對(duì)腫瘤壞死因子-α致人臍靜脈內(nèi)皮細(xì)胞炎癥損傷模型的保護(hù)作用
何飛燕,陳 歡,邱志霞,金子恒,齊淑貞,黃 芳
(1.中國(guó)藥科大學(xué)中藥學(xué)院,江蘇 南京 211198;2.河南中大恒源生物科技股份有限公司,河南 漯河 462600;3.中國(guó)醫(yī)學(xué)科學(xué)院皮膚病研究所,江蘇 南京 210042)
動(dòng)脈粥樣硬化(atherosclerosis,AS)是以脂質(zhì)代謝障礙為基礎(chǔ)的血管疾病,病變常累及大、中動(dòng)脈,同時(shí)伴有平滑肌細(xì)胞和纖維基質(zhì)增生[1]。AS是目前引起心血管疾病的主要原因之一[2]。炎癥在AS發(fā)生發(fā)展的各個(gè)階段都具有重要作用,因此AS通常也被認(rèn)為是一種慢性炎癥性疾病[3]。內(nèi)皮細(xì)胞是維持血管內(nèi)穩(wěn)態(tài)和低氧化應(yīng)激的重要調(diào)節(jié)器。其可以通過(guò)分泌各種因子響應(yīng)物理化學(xué)信號(hào),進(jìn)而調(diào)節(jié)血管張力、細(xì)胞黏附、血栓生成、平滑肌細(xì)胞增殖和血管壁炎癥等[4]。持續(xù)的炎癥刺激可以誘導(dǎo)內(nèi)皮細(xì)胞持續(xù)激活,發(fā)生內(nèi)皮細(xì)胞功能障礙,在AS等心血管疾病的進(jìn)程中發(fā)揮重要作用[5]。
姜黃素(Curcumin)是從姜黃屬(CurcumaL.)中藥材中提取獲得的多酚類活性成分。研究[6-8]證實(shí)其具有抗炎、抗氧化、免疫調(diào)節(jié)等多種作用,表現(xiàn)出很強(qiáng)的內(nèi)在活性。然而,傳統(tǒng)姜黃素水溶性低,腸道吸收相對(duì)較差,體內(nèi)代謝途徑廣泛,經(jīng)膽囊排泄迅速,口服的系統(tǒng)生物利用度較低[9-10],嚴(yán)重影響姜黃素的臨床應(yīng)用。

1 材料
1.1 實(shí)驗(yàn)動(dòng)物 12只清潔級(jí)SD大鼠,6~8周齡,體質(zhì)量180~220 g,雌雄各半,購(gòu)于湖南斯萊克景達(dá)實(shí)驗(yàn)動(dòng)物有限公司。生產(chǎn)許可證號(hào)為SCXK(湘)2019-0004,實(shí)驗(yàn)動(dòng)物質(zhì)量合格證號(hào)為430727200101169841。動(dòng)物飼養(yǎng)于西南大學(xué)藥學(xué)院實(shí)驗(yàn)動(dòng)物中心,相對(duì)濕度50%~70%,室溫23~25 ℃,自然晝夜光線照明。
1.2 細(xì)胞株 HUVECs:江蘇凱基生物技術(shù)股份有限公司。
1.4 儀器 多功能熒光酶標(biāo)儀:美國(guó)Thermo Fisher Scientific公司;化學(xué)發(fā)光成像儀:上海天能科技有限公司;實(shí)時(shí)熒光定量PCR儀:美國(guó)Bio-Rad公司;液質(zhì)聯(lián)用系統(tǒng)UPLC(I-Class)-MS(XEXO TQD):美國(guó)Waters公司;AB 135-S天平:梅特勒·托利多儀器有限公司。
2 方法
2.2.1 標(biāo)準(zhǔn)溶液的配制 對(duì)照品溶液的配制:精密稱取姜黃素對(duì)照品1.09 mg,甲醇定容至10 mL,得濃度為10.9 μg/mL的貯備液。內(nèi)標(biāo)溶液的配制:精密稱取鹽酸小檗堿對(duì)照品1.60 mg,甲醇定容至10 mL,得濃度為160 μg/mL的貯備液,再用甲醇稀釋,配制濃度為960 ng/mL的內(nèi)標(biāo)對(duì)照品溶液。
2.2.2 樣品的預(yù)處理方法 取空白血漿100 μL,加入鹽酸小檗堿內(nèi)標(biāo)溶液10 μL,混勻,加乙酸乙酯0.3 mL,渦旋混合2 min,4 000 r/min離心10 min,分離上清液;下層沉淀重復(fù)上述操作,合并2次的上清液,40 ℃真空干燥。殘?jiān)?00 μL甲醇復(fù)溶,渦旋混勻2 min,經(jīng)0.22 μm微孔濾膜過(guò)濾,待測(cè)。
2.2.3 UPLC-MS/MS分析條件 色譜條件:Waters ACQUITY UPLC BEH(2.1 mm×50 mm,1.8 μm)色譜柱;流動(dòng)相為0.1%甲酸水溶液(A相)及0.1%甲酸乙腈溶液(B相),流速0.4 mL/min;柱溫35 ℃;進(jìn)樣量1 μL。梯度洗脫(0~0.5 min,95% A;0.5~1.5 min,95%~2% A;1.5~3.5 min,2% A;3.5~4 min,2%~95% A,4~6 min,95%A)。質(zhì)譜條件:ESI離子源;正離子模式;離子源溫度400 ℃;脫氣流速700 L/h;錐孔體積流量流速50 L/h;毛細(xì)管電壓3.0 kV。
2.3 HUVECs培養(yǎng) HUVECs采用含10%血清的RPMI-1640培養(yǎng)基培養(yǎng),于37 ℃、5% CO2培養(yǎng)箱中孵育。倒置顯微鏡觀察,細(xì)胞生長(zhǎng)至約80%時(shí)傳代。

2.5 TNF-α誘導(dǎo)HUVECs炎癥模型 HUVECs炎癥模型的建立參照文獻(xiàn)[11-12]。將生長(zhǎng)良好的HUVECs接種于96孔板中,細(xì)胞貼壁后棄去培養(yǎng)液,加入含TNF-α(30 ng/mL)的無(wú)血清培養(yǎng)基培養(yǎng)24 h,誘導(dǎo)HUVECs炎癥模型。


2.8 實(shí)時(shí)定量PCR檢測(cè)關(guān)鍵炎癥因子環(huán)氧合酶-2(cyclooxygense-2,COX-2)、MCP-1 mRNA表達(dá)水平 HUVECs給藥及模型復(fù)制方法同“2.6”項(xiàng)。模型復(fù)制24 h后收集細(xì)胞以提取RNA。以20 μL逆轉(zhuǎn)錄反應(yīng)體系進(jìn)行逆轉(zhuǎn)錄后進(jìn)行實(shí)時(shí)熒光定量PCR。反應(yīng)條件:95 ℃預(yù)變性5 min;95 ℃變性10 s;55~60 ℃退火20 s;72 ℃延伸20 s。引物序列見表1。實(shí)驗(yàn)平行重復(fù)3次。

表1 目標(biāo)基因的引物序列
2.9 Western blot法檢測(cè)NF-κB通路關(guān)鍵蛋白的表達(dá)水平 將生長(zhǎng)良好的HUVECs以每孔2×105個(gè)接種于6孔板,按照“2.6”項(xiàng)的分組對(duì)細(xì)胞進(jìn)行給藥預(yù)保護(hù)及TNF-α作用24 h,模型復(fù)制完成后于冰上提取蛋白。BCA試劑盒進(jìn)行蛋白定量,SDS-PAGE進(jìn)行電泳分離并電轉(zhuǎn)到PVDF膜,5% BSA封閉1 h,4 ℃孵育p65、p-p65、IκB、p-IκB一抗過(guò)夜,次日于室溫孵育對(duì)應(yīng)二抗1 h,洗膜后加入ECL發(fā)光液顯影成像。實(shí)驗(yàn)重復(fù)3次。

3 結(jié)果

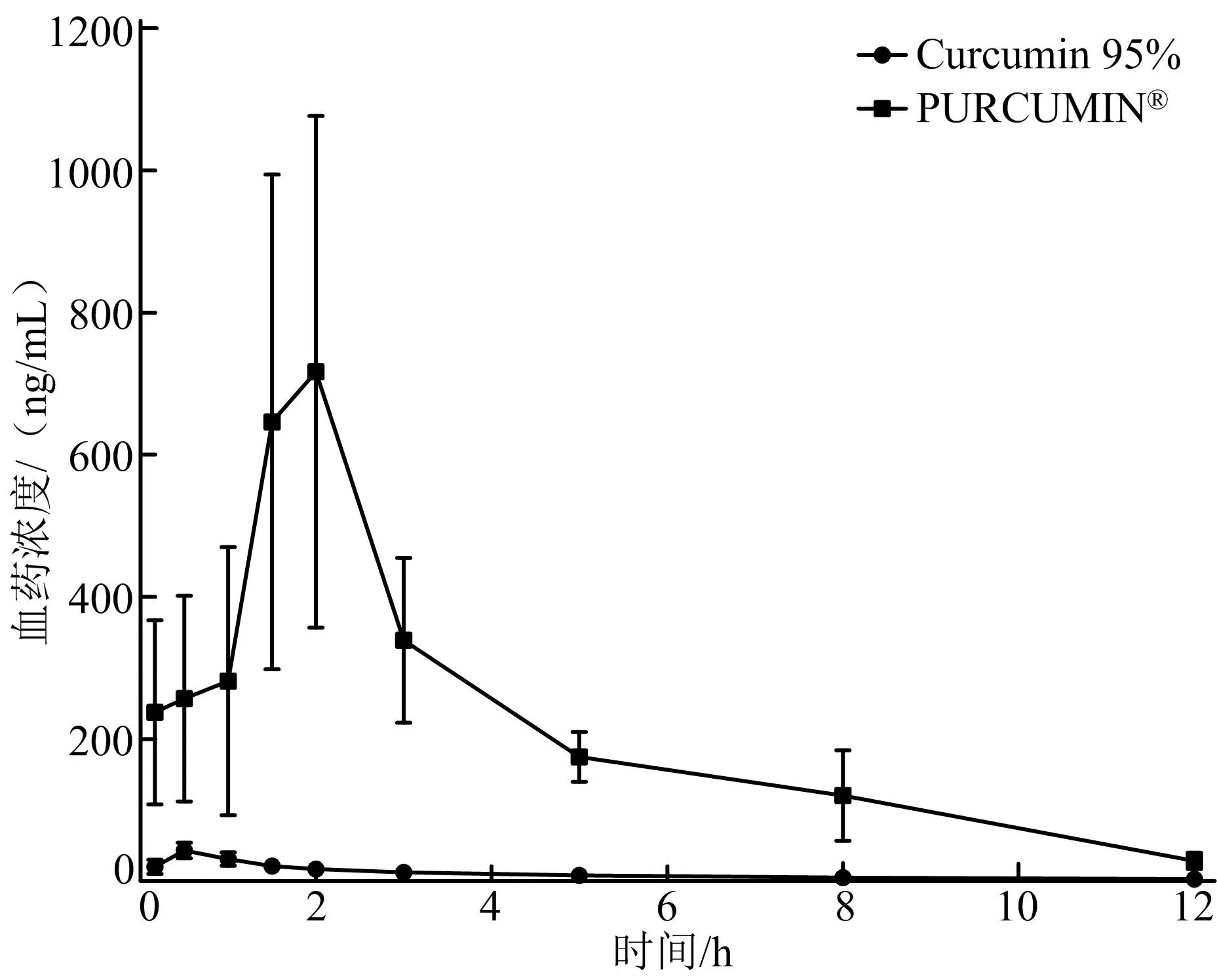
圖1 兩種姜黃素制劑在大鼠體內(nèi)的血藥

表2 兩種姜黃素制劑在大鼠體內(nèi)的主要藥物動(dòng)力學(xué)參數(shù)比較

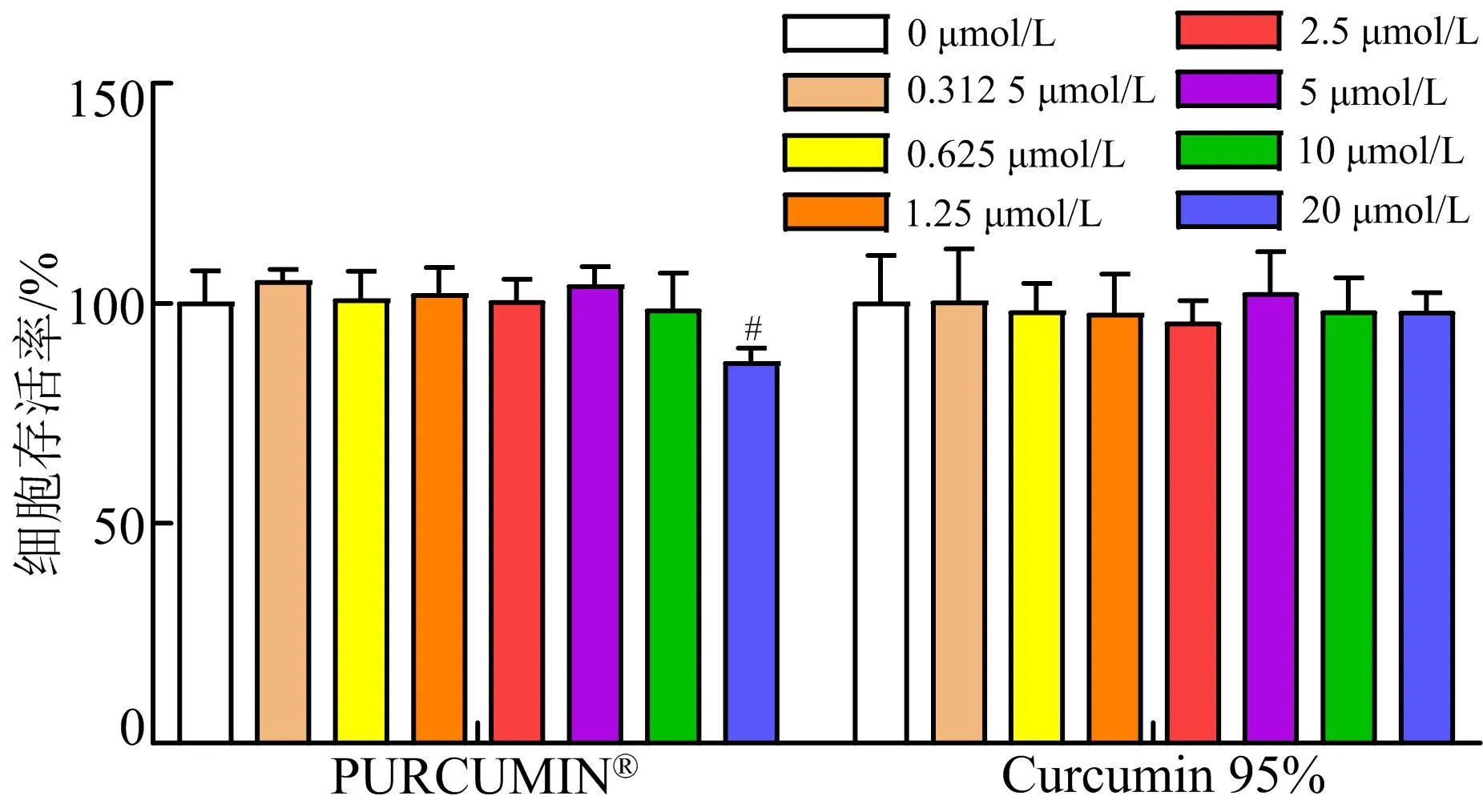
注:與0 μmol/L比較,#P<0.05
3.3 相同給藥時(shí)間、不同給藥濃度兩種姜黃素制劑的抗炎作用比較
3.3.1 8組HUVECs內(nèi)NO水平比較 與空白組比較,模型組NO水平顯著升高(P<0.05);與模型組比較,各濃度姜黃素組NO水平顯著降低(P<0.05)。結(jié)果表明,姜黃素干預(yù)可顯著降低TNF-α誘導(dǎo)的細(xì)胞內(nèi)NO水平,減輕內(nèi)皮細(xì)胞損傷。見圖3。

注:A.空白組;B.模型組;C.0.5 μmol/L PURCUMIN組;D.1 μmol/L PURCUMIN組;E.5 μmol/L PURCUMIN組;F.10 μmol/L PURCUMIN組;G.5 μmol/L Curcumin 95%組;H.10 μmol/L Curcumin 95%組;與空白組比較,#P<0.05;與模型組比較,*P<0.05


注:A.空白組;B.模型組;C.0.5 μmol/L PURCUMIN組;D.1 μmol/L PURCUMIN組;E.5 μmol/L PURCUMIN組;F.10 μmol/L PURCUMIN組;G.5 μmol/L Curcumin 95%組;H.10 μmol/L Curcumin 95%組;與空白組比較,#P<0.05;與模型組比較,*P<0.05


注:A.空白組;B.模型組;C.0.5 μmol/L PURCUMIN組;D.1 μmol/L PURCUMIN組;E.5 μmol/L PURCUMIN組;F.10 μmol/L PURCUMIN組;G.5 μmol/L Curcumin 95%組;H.10 μmol/L Curcumin 95%組;與空白組比較,#P<0.05;與模型組比較,*P<0.05


注:A.空白組;B.模型組;C.0.5 μmol/L PURCUMIN組;D.1 μmol/L PURCUMIN組;E.5 μmol/L PURCUMIN組;F.10 μmol/L PURCUMIN組;G.5 μmol/L Curcumin 95%組;H.10 μmol/L Curcumin 95%組;與空白組比較,#P<0.05;與模型組比較,*P<0.05
3.4 相同給藥濃度、不同給藥時(shí)間兩種姜黃素制劑的抗炎作用比較


注:A.空白組;B.模型組;C.10 μmol/L PURCUMIN組;D.10 μmol/L Curcumin 95%組;與空白組比較,#P<0.05;與模型組比較,*P<0.05


注:A.空白組;B.模型組;C.10 μmol/L PURCUMIN組;D.10 μmol/L Curcumin 95%組;與空白組比較,#P<0.05;與模型組比較,*P<0.05
4 討論



值得注意的是,在相同給藥時(shí)間、不同給藥濃度的抗炎作用實(shí)驗(yàn)中,兩種姜黃素制劑的濃度設(shè)計(jì)并不完全對(duì)應(yīng),這一方面是由于在摸索給藥濃度的預(yù)實(shí)驗(yàn)中,低濃度(0.5、1 μmol/L)的Curcumin 95%抗炎作用的差異無(wú)統(tǒng)計(jì)學(xué)意義;另一方面,從正式實(shí)驗(yàn)的定量結(jié)果中可以看到,Curcumin 95%(5 μmol/L)給藥后除顯著降低IL-6水平之外,對(duì)其他炎癥因子及關(guān)鍵炎癥基因的抑制作用并不顯著,對(duì)NF-κB通路中關(guān)鍵蛋白表達(dá)也不存在顯著的調(diào)節(jié)作用,即5 μmol/L Curcumin 95%體外抗炎作用仍然較差。基于上述背景,筆者認(rèn)為沒有必要設(shè)置低濃度(0.5、1 μmol/L)的Curcumin 95%組別,并在最終的實(shí)驗(yàn)中取消了這兩個(gè)組別。

