植物黃酮防治多囊卵巢綜合征研究進展*
達(dá)晶,趙珊珊,匡洪影
1.黑龍江中醫(yī)藥大學(xué),黑龍江 哈爾濱 150000; 2.黑龍江中醫(yī)藥大學(xué)附屬第一醫(yī)院,黑龍江 哈爾濱 150000
多囊卵巢綜合征(polycystic ovary syndrome,PCOS)是育齡期婦女常見的生殖內(nèi)分泌疾病,以月經(jīng)異常、高雄激素表現(xiàn)、卵巢多囊樣改變?yōu)橹饕R床表現(xiàn),同時也是2型糖尿病、心腦血管疾病和子宮內(nèi)膜癌等臨床常見疾病發(fā)病的高危因素[1-3]。調(diào)查顯示,全球約有15%的女性受累[4-5],其中18~44歲的女性為主要患病人群[6]。中醫(yī)并無“多囊卵巢綜合征”的病名,可將其歸屬于“閉經(jīng)”“不孕”和“崩漏”等范疇[7-8]。肝、脾、腎三臟功能失調(diào),痰瘀互結(jié),被認(rèn)為是PCOS的主要發(fā)病機制,補腎、疏肝、健脾,祛濕化痰,活血化瘀為其主要的治療原則[9-10]。中醫(yī)藥因其獨特的優(yōu)勢在治療PCOS方面取得了一定的療效。黃酮類化合物是常見蔬菜、水果和中藥等植物的主要成分,因此又被稱為植物黃酮[11]。現(xiàn)代藥理學(xué)研究表明,植物黃酮因其高活性氧自由基以及有效抑制膠束系統(tǒng)中脂質(zhì)過氧化的作用,被認(rèn)為與抗炎、抗衰老、抗真菌,尤其是抗癌活性有關(guān)[12]。本綜述對目前植物黃酮在治療PCOS中取得的成果做以闡述,以期為更好地開發(fā)用于治療 PCOS 的中藥提供一定的思路。
1 植物黃酮概述
1930年,研究者從橙子中分離出來一種新物質(zhì),在當(dāng)時被視為一種新的維生素,而且被命名為維生素P,后期經(jīng)過研究證實此物質(zhì)即黃酮類化合物[13-14]。黃酮類化合物又稱植物黃酮,是一種多酚類化合物(Polyphenolic Compounds),通常是指兩個苯環(huán)通過中央三碳鏈相互連結(jié)而成的一系列C6-C3-C6結(jié)構(gòu)的化合物[15],其基礎(chǔ)結(jié)構(gòu)骨架如圖1[16]。
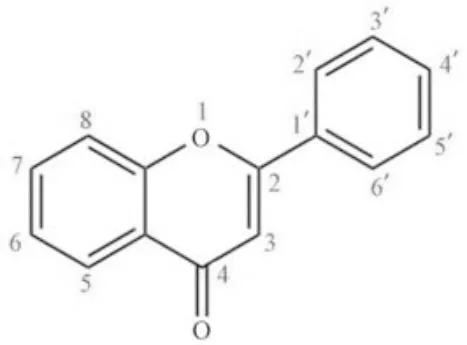
圖1 植物黃酮基本骨架結(jié)構(gòu)
根據(jù)不同的化學(xué)結(jié)構(gòu)可將植物黃酮分為黃酮醇、黃烷酮、異黃酮、雙黃酮、黃烷醇和花青素等12個亞型,這些亞型又以不同組分劃分不同的結(jié)構(gòu),如查爾酮、芹菜素、木犀草素、槲皮素、柚皮素、兒茶素等[17-18]。目前發(fā)現(xiàn)的植物黃酮大致有15 000多種,以糖苷酮、糖苷和甲基化衍生物的形式存在,基本結(jié)構(gòu)是糖苷元[19-20]。目前植物黃酮因其不良反應(yīng)較小、價格低廉的優(yōu)點,被廣泛用于治療各種臨床常見疾病,并且取得了一定的療效[21-22]。
2 PCOS發(fā)病機制
PCOS作為臨床常見的內(nèi)分泌疾病,發(fā)病機制眾多,目前尚未被完全闡明,多認(rèn)為與胰島素抵抗、炎癥、氧化應(yīng)激、高雄激素血癥等因素相關(guān)。約50%~70%的PCOS患者伴有胰島素抵抗,且胰島素抵抗在PCOS肥胖患者中比例更高[23-25]。胰島素抵抗一方面使血清胰島素水平升高異常,進而增加黃體生成素(luteinizing hormone,LH)的分泌,減少性激素結(jié)合球蛋白(sex hormone-binding globulin,SHBG)合成,增加睪酮水平,加重PCOS進程;另一方面,促使卵巢增加雄激素的分泌,卵泡發(fā)育異常,導(dǎo)致PCOS稀發(fā)排卵或無排卵形成[24-26]。
慢性低度炎癥作為PCOS的關(guān)鍵發(fā)病因素之一,主要表現(xiàn)為巨噬細(xì)胞分泌的炎癥因子如腫瘤壞死因子-α(tumor necrosis factor-α,TNF-α)、白細(xì)胞介素-6(interleukin-6,IL-6)等水平的異常升高,致使雄激素水平上升,卵巢發(fā)生多囊樣改變。此外,炎癥因子也可能與PCOS相關(guān)并發(fā)癥關(guān)系密切[27-28]。
氧化應(yīng)激是機體氧化與抗氧化作用失衡的一種狀態(tài),可與炎癥相互作用,影響PCOS的發(fā)生發(fā)展[29-31]。研究發(fā)現(xiàn),肥胖型PCOS氧化應(yīng)激水平最高,氧化應(yīng)激與肥胖相互作用,惡性循環(huán),使卵泡損傷,排卵功能異常[32-33]。
高雄激素血癥已被認(rèn)為是PCOS的核心病理特征之一,在我國PCOS患者中,約76%存在高雄激素血癥[34]。Wang等[35]認(rèn)為,高雄激素血癥能刺激PCOS患者早期卵泡過度激活,出現(xiàn)大量竇性、囊性卵泡,影響卵巢功能。此外,雄激素增高還會使脂肪生成增加,并對脂肪分解產(chǎn)生一定的抑制作用,從而加重PCOS肥胖的發(fā)生,肥胖又能引起內(nèi)分泌紊亂,加劇月經(jīng)周期異常、糖脂代謝紊亂,增加遠(yuǎn)期并發(fā)癥風(fēng)險[26,36]。
3 植物黃酮調(diào)控PCOS
3.1 杜仲總黃酮杜仲是杜仲科植物杜仲的干燥樹皮,《中華本草》記載其具有補肝腎、強筋骨、安胎之功效,現(xiàn)代藥理學(xué)研究發(fā)現(xiàn)木脂素類、環(huán)烯醚萜類、苯丙素類、黃酮類等為其主要有效成分[37-38]。近年來,杜仲總黃酮在防治PCOS方面取得了不錯的成果。實驗研究發(fā)現(xiàn),杜仲總黃酮能降低來曲唑聯(lián)合高脂飲食誘導(dǎo)的多囊卵巢綜合征胰島素抵抗(PCOS-IR)模型大鼠的體質(zhì)量、Lee′s指數(shù)和卵巢面積、體積,減輕血清睪酮、血清瘦素(leptin,Lep)、胰島素(insulin,INS)、胰島素抵抗指數(shù)(homeostasis model assessment of insulin resistance,HOMA-IR)和空腹血糖(fasting blood glucose,FBG)(全血)水平,升高雌二醇(estrogen,E2)、SHBG水平和胰島素敏感指數(shù),改善大鼠卵巢和胰腺組織的病理學(xué)變化。親吻素(kisspeptin,Kiss1)在下丘腦的不同區(qū)域表達(dá),杜仲總黃酮能調(diào)節(jié)Kiss1、胰島素樣生長因子-1(insulin-like growth factor-1,IGF-1)、雄性激素受體(androgen receptor,AR)和瘦素受體1(leptin receptor1,LEPR)在下丘腦弓形核、垂體和卵巢中的表達(dá),上調(diào)卵巢PI3Kp85α、p-PI3Kp85α、p-AKT和GLUT4的表達(dá)。因此,杜仲總黃酮可以通過作用于下丘腦-垂體-卵巢軸發(fā)揮作用,防治PCOS[39]。研究者采用來曲唑灌胃構(gòu)建PCOS大鼠模型,以杜仲總黃酮(200 mg·kg-1)干預(yù)模型大鼠,3周以后取材,結(jié)果顯示,和模型組相比,給予杜仲總黃酮之后,大鼠卵巢體積減小,表面色澤變紅,黃體少量增加,囊狀擴張卵泡減少,抗謬?yán)展芗に?anti-müllerian hormone,AMH)、LH、T含量明顯降低,FSH含量明顯升高,且卵巢組織顆粒細(xì)胞自噬率顯著降低[40]。
3.2 小茴香總黃酮小茴香為藥食同源之品,具有溫補肝腎、行氣止痛之功效[41]。研究發(fā)現(xiàn),小茴香中的揮發(fā)油與黃酮類是其調(diào)節(jié)性激素分泌和調(diào)脂降糖的主要物質(zhì)基礎(chǔ)[42]。目前,小茴香總黃酮尚少用于PCOS的實驗研究,有研究者采用高脂膳食聯(lián)合來曲唑構(gòu)建PCOS-IR模型,給予高、中、低劑量小茴香總黃酮(240 mg·kg-1、120 mg·kg-1、60 mg·kg-1),干預(yù)3周后發(fā)現(xiàn):高、低劑量能縮小模型大鼠卵巢面積和體積,升高血清E2、SHBG水平;高、中劑量能降低模型大鼠血清T和AMH水平,升高25-羥基維生素D3水平,高劑量組可不同程度地降低三酰甘油(triglyceride,TG)、膽固醇(total cholesterol,TC)、低密度脂蛋白膽固醇(low density lipoprotein cholesterol,LDL-C)、TG/HDL-C、TC/HDL-C和三酰甘油-葡萄糖指數(shù)(triglyceride-glucose index,Tyg-Index),升高高密度脂蛋白膽固醇(high density lipoprotein cholesterol,HDL-C)水平;中劑量組可不同程度地降低TG、LDL-C、TG/HDL-C、TC/HDL-C和TyG-index,升高HDL-C水平;低劑量組可不同程度地降低LDL-C和TG/HDL-C水平[43],表明小茴香總黃酮可有效調(diào)節(jié) PCOS-IR大鼠性激素失衡、脂代謝紊亂和胰島素抵抗。
3.3 青天葵總黃酮植物黃酮是青天葵的主要成分,具有良好的抗炎、鎮(zhèn)痛、增強免疫力、解熱、止咳等作用[44-45]。青天葵中的主要藥效物質(zhì)為植物黃酮,具有抗腫瘤、抗菌、抗病毒的功效,且含量較高。以脫氫表雄酮(dehydroepiandrosterone,DHEA)構(gòu)建PCOS-IR大鼠模型,采用高、中、低劑量(200 mg·kg-1、100 mg·kg-1、50 mg·kg-1)的青天葵總黃酮干預(yù)4周,結(jié)果顯示PCOS-IR大鼠以劑量依賴性方式恢復(fù)動情周期,可顯著增加血清FSH水平,同時使血清LH、T和INS水平急劇降低,抑制Janus激酶2(Janus kinas 2,JAK2)和信號轉(zhuǎn)導(dǎo)與轉(zhuǎn)錄激活因子3(signal transducer and activator of tran-scriptions3,STAT3)磷酸化,從而降低炎癥因子IL-6的表達(dá)[12]。
3.4 木犀草素木犀草素是存在于辣椒、野菊花、金銀花、紫蘇等多種蔬菜和草藥中的類黃酮,是治療高血壓、癌癥及過敏癥的傳統(tǒng)中藥,具有抗氧化、抗微生物、抗炎、化學(xué)預(yù)防、化療、保護心臟、抗糖尿病、神經(jīng)保護和抗過敏等作用[46-47]。針對來曲唑和高脂飲食誘導(dǎo)的PCOS大鼠,以不同劑量的木犀草素(25 mg·kg-1,50 mg·kg-1,100 mg·kg-1)腹腔注射進行干預(yù),結(jié)果顯示木犀草素能夠使大鼠的動情周期正常化,以劑量依賴性改善卵巢形態(tài),減輕大鼠卵巢的多囊性結(jié)構(gòu),減少卵母細(xì)胞和黃體的丟失,使血清FSH、LH、E2、T水平恢復(fù)正常,并且降低FBG、FINS濃度,顯著上調(diào)骨骼肌組織中PI3K p85α和 p-AKT蛋白表達(dá)水平,顯著增加血清超氧化物歧化酶(super oxide dismutase,SOD)、谷胱甘肽過氧化物酶(glutathione peroxidase,GPx)、過氧化氫酶(catalase,CAT)和谷胱甘肽(erythrocyte reduced glutathione,GSH)等抗氧化劑的活性[48]。因此,木犀草素可通過激活磷脂酰肌醇3-激酶(phosphoinositide 3-kinase,PI3K)/蛋白激酶B(protein kinase B,AKT) 信號通路抑制胰島素抵抗,并增強抗氧化反應(yīng)。
3.5 槲皮素槲皮素是一種植物黃酮,存在于100多種中草藥中,包括山楂和紅花,具有降糖、降脂、抗氧化損傷等作用[49]。研究建立以高脂飲食和來曲唑誘導(dǎo)的PCOS-IR大鼠模型,造模成功后提取卵巢顆粒細(xì)胞,并用槲皮素低、高劑量(0.5 mg·L-1、1 mg·L-1)干預(yù),結(jié)果顯示槲皮素能夠增強細(xì)胞活性,降低E2、LH、T含量,顯著降低活性氧(reactive oxygen species,ROS)活性,顯著降低晚期糖基化終末產(chǎn)物(advanced glycation end products,AGEs)和晚期糖基化終末產(chǎn)物受體(receptors for advanced glycation end products,RAGE)蛋白表達(dá)水平,顯著升高磷酸化細(xì)胞外信號調(diào)節(jié)激酶(phosphorylated ERK,p-ERK)和磷酸化p38有絲分裂原蛋白激酶(p38 phospho-mitogen-activated protein kinase,p-p38MAPK)蛋白表達(dá)水平[50]。
在PCOS中,自由基生成超過機體自身的抗氧化能力,ROS堆積使細(xì)胞、組織等功能異常,體內(nèi)氧化與抗氧化失衡[51]。研究者采用槲皮素干預(yù)DHEA構(gòu)造的PCOS模型,發(fā)現(xiàn)大鼠SOD濃度升高,一氧化氮、丙二醛濃度降低[52],說明槲皮素能較好地改善PCOS大鼠異常的氧化應(yīng)激狀態(tài)。
研究者用槲皮素溶液(100 mg·kg-1)干預(yù)DHEA誘導(dǎo)的PCOS-IR大鼠模型,發(fā)現(xiàn)大鼠動情周期和體質(zhì)量有一定程度的恢復(fù),血胰島素、白細(xì)胞介素-1b(interleukin-1b,IL-1b)、IL-6和 TNF-α 水平被顯著抑制,因此,槲皮素可能是通過改善炎癥微環(huán)境發(fā)揮作用的[53]。
3.6 柚皮素有研究以柚皮素(100 mg·kg-1)改善DHEA誘導(dǎo)的PCOS大鼠模型,結(jié)果發(fā)現(xiàn)大鼠血清TC、TG、FPG、FINS、HOMA-IR、LH、T水平降低,FSH、E2水平升高,p-PI3K/PI3K、p-AKT/AKT、p-IRS-1/IRS-1蛋白表達(dá)升高,下游p-GSK-3β/GSK-3β、葡萄糖轉(zhuǎn)運蛋白因子4(glucose transporter 4,GLUT-4)蛋白表達(dá)升高[54]。因此,柚皮素可以通過激活PI3K/AKT通路防治PCOS,并改善糖脂代謝異常、胰島素抵抗和生殖系統(tǒng)激素紊亂。
3.7 葛根素葛根素是中藥葛根的主要提取物,研究發(fā)現(xiàn)其能有效緩解肥胖型PCOS患者的病理狀態(tài)[55]。研究發(fā)現(xiàn),給予以DHEA構(gòu)建的PCOS大鼠模型腹腔注射葛根素注射液(100 mg·kg-1)治療后,FSH水平升高,LH、T水平均降低,FBG、2 h PBG、FINS水平及胰島素抵抗均低于模型組,血清IL-6、TNF-α和CRP水平均降低,大鼠卵巢組織Toll樣受體4(Toll-like receptor 4,TLR4)、核因子-κB(nuclear factor κb,NF-κB)、氧化低密度脂蛋白(oxidized low density lipoprotein,ox-LDL)表達(dá)均降低[56]。因此,葛根素可以通過調(diào)控機體生殖激素緩解胰島素抵抗,加快恢復(fù)卵巢功能,從而明確PCOS的治療效果。
3.8 菟絲子總黃酮研究顯示,PCOS是一種低炎癥疾病,諸多炎癥因子、氧化應(yīng)激參與該病的發(fā)展過程[57-58]。菟絲子是臨床上常用的補腎中藥,能夠調(diào)節(jié)生殖系統(tǒng)功能,常與各種中藥配伍治療常見婦科疾病[59-60]。藥理實驗發(fā)現(xiàn),酚酸和黃酮類是其主要成分,黃酮類因其抗炎、抗氧化應(yīng)激作用在PCOS的防治上具有較好的療效[61]。
有實驗對采用菟絲子總黃酮干預(yù)DHEA聯(lián)合人絨毛膜促性腺激素(human chorionic gonadotropin,HCG)誘導(dǎo)的PCOS大鼠進行研究,發(fā)現(xiàn)菟絲子總黃酮低、中、高劑量組(200 mg·kg-1,100 mg·kg-1,50 mg·kg-1)均能夠降低大鼠卵巢指數(shù)和子宮指數(shù),顯著下降血清P、PRL和INS水平及LH/FSH比值,降低卵巢中TNF-α、胰島素樣生長因子-1(insulin-like growth factor-1,IGF-1)蛋白水平,改善子宮內(nèi)膜炎癥[62],目前已被廣泛用于PCOS的治療,并取得了較好的療效。

表1 植物黃酮防治PCOS的機制
3.9 山楂葉類黃酮從山楂葉中分離出的山楂葉類黃酮(HLF)具有廣泛的藥用特性,如緩解非酒精性肝病、改善急性心肌缺血/再灌注、抗氧化和抗炎等[63]。以HLF(200 mg·kg-1·d-1)干預(yù)皮下注射DHEA(60 mg·kg-1·d-1)構(gòu)建的PCOS大鼠模型,干預(yù)3周后,顯示其能夠抑制PCOS大鼠的體質(zhì)量增加,HLF的共同給藥顯著降低了卵泡囊腫的發(fā)生率,降低血清LH、FSH、E2、P和T水平,抑制TNF-α、IL-6表達(dá)[64]。
3.10 淫羊藿總黃酮淫羊藿有補腎陽、強筋骨、祛風(fēng)濕的功效[65-66]。藥理學(xué)研究發(fā)現(xiàn),淫羊藿總黃酮作為淫羊藿中起雌激素樣作用的主要部分,能夠有效防治生殖系統(tǒng)疾病[67-68]。對SD大鼠以來曲唑灌胃21 d,建立PCOS模型,給予低、中、高劑量組(50 mg·kg-1、100 mg·kg-1、200 mg·kg-1)淫羊藿總黃酮干預(yù)3周后,發(fā)現(xiàn)淫羊藿總黃酮能夠顯著降低卵巢重量、卵巢指數(shù),降低大鼠血清T、LH水平,升高E2,降低LH/FSH比值,且高劑量組較低劑量組效果更為明顯[69]。
4 小結(jié)與展望
植物黃酮種類多,價格低,毒性微,在多種臨床疾病的治療中效果顯著,故研究其對PCOS的治療作用有助于拓展PCOS的用藥范圍。PCOS作為臨床常見的生殖內(nèi)分泌紊亂疾病之一,以對癥治療為主,如降低雄激素水平、緩解糖脂代謝和改善生育障礙等,但治療效果欠佳,不良反應(yīng)發(fā)生率高。近年來研究證實,中醫(yī)藥治療PCOS療效顯著,不良反應(yīng)少。植物黃酮能夠調(diào)節(jié)激素水平,如降低T、LH水平,升高E2等;改善炎癥狀態(tài),如抑制TNF-α、IL-6 表達(dá);緩解糖脂代謝,如減輕INS和FBG水平,從而治療PCOS。因此,從更深層次研究植物黃酮有效成分并開發(fā)安全有效的新藥在防治PCOS中前景廣闊。
現(xiàn)有研究仍存在一些不足之處:PCOS發(fā)病機制復(fù)雜,相互交織,目前只對植物黃酮治療PCOS的多種機制進行概述,缺少對單一機制的深入挖掘,研究缺乏客觀性。本文重點研究了單個植物黃酮有效成分治療PCOS的進展,可參考中藥藥對思路,對多對植物黃酮有效成分進行研究,以期獲得最佳療效。目前,多數(shù)相關(guān)研究都停留在動物實驗階段,臨床研究匱乏,未來需要開展更加嚴(yán)謹(jǐn)、高質(zhì)量的研究以指導(dǎo)臨床。

