離線自適應技術在鼻咽癌放射治療中的劑量學分析*
石先偉 何英 唐組閣 王麗 袁志 任杰 別俊 潘榮強
(川北醫學院第二臨床醫學院·南充市中心醫院腫瘤中心,四川 南充 637000)
鼻咽癌是我國常見的惡性腫瘤之一,鼻咽解剖位置深居頭顱中間,周圍有許多重要器官、血管和神經組織,如眼,脊髓,神經和腦干等,外科手術很難將腫瘤和淋巴引流區大范圍地切除,同時鼻咽癌病理類型以未分化型非角化癌多見,對射線有較高的敏感性,放射治療是目前鼻咽癌主要的治療手段[1]。由于鼻咽腫瘤解剖位置復雜,周圍危及器官多,如何保證鼻咽癌放射治療的精確與安全是國內外學者研究的熱點[2-3]。自適應放射治療(Adaptive radiotherapy,ART)是在病人整個治療過程中,通過CT掃描等方式,對病人治療中各種變化如靶區位置、器官的運動等進行系統地監測,并用監測到的反饋信息及時對放療計劃進行修改,以改進治療,避免靶區欠量或危及器官超量,從而保證病人治療的準確性與安全性[4-5]。理想自適應方式是在線對每一次治療都行劑量追蹤并調整計劃,但這種方式工作量很大,需大量的人力和時間,特別是對于較復雜的鼻咽癌,靶區勾畫和計劃自動優化都需要較長時間,目前國內外學者研究的熱點仍是離線的自適應[6],即在當次治療中獲取影像資料進行線下分析研究,接受到反饋結果,對下次治療或者以后分次的治療進行干預,確保放射治療質量安全。該研究利用離線自適應技術應用于鼻咽癌放射治療中的劑量學分析,探討再計劃的必要性以及其帶來的劑量學改善[7]。
1 資料與方法
1.1 一般資料 選取2021年10月—2022年10月在我院行根治性放療的鼻咽癌患者10例。納入標準:①病理證實為鼻咽癌。②年齡18~70歲。③無遠處轉移。④第8版AJCC/UICC分期:T分期T2及以上,N分期N1及以上。⑤KPS評分≥70分。排除標準:①既往接受過鼻咽部放療或手術治療。②無法耐受放療副反應。10例患者中位年齡56歲,其中男性6例,女性4例,均行同步推量放療[8],原發灶區給予高劑量照射(2.12~2.40 Gy/次)的同時,亞臨床灶或其周圍擴大區給予較低劑量的照射(1.70~2.10 Gy/次)。
1.2 圖像采集 10例患者的圖像包括初始計劃CT圖像,并在治療過程中每周行一次CT掃描(6~7幅CT圖像),計劃CT和每周CT均在聯影Uct510機器掃描,掃描電壓為120 KV,FOV為600 mm,掃描層厚為3 mm。
1.3 計劃設計 利用Monaco 5.4.03進行VMAT計劃設計[9-10],一周治療5次,共33次治療。將10例患者的所有CT圖像導入治療計劃系統,由同一個熟練的放療科臨床醫生勾畫靶區和危及器官[1],其中GTVnx是增強計劃CT所顯示患者鼻咽部的原發腫瘤及其侵犯范圍(Gross tumor volume,GTV),GTVnd為頸部轉移淋巴結的腫瘤,CTV1為包括GTVnx + 5~10 mm +整個鼻咽腔粘膜及粘膜下5 mm,CTVnd包括GTVnd + 5 mm及需要預防照射的頸部淋巴結分區,CTV2涵蓋CTV1,同時根據腫瘤的具體位置和侵入的范圍合適增加預防照射的范圍,PTV將以上相應靶區外擴3 mm;正常組織的勾畫包括脊髓、腦干、腮腺、視神經、視交叉、晶體、眼球、下頜骨、顳頜關節,垂體等[11]。靶區以及危及器官的限制條件是:PGTVnx和PGTVnd的處方劑量為70~74 Gy,PCTV1為60 Gy,PCTV2和PCTVnd為54~56 Gy,脊髓不超過40 Gy,腦干不超過54 Gy,腮腺D50小于30 Gy等[12]。
2 結果
2.1 靶區和危及器官體積及分次劑量變化
2.1.1 靶區體積和分次劑量平均變化 在治療過程中,10例患者GTVnx和GTVnd的平均體積都在縮小,在治療末最后掃描CT上可以觀察到,10例患者的GTVnx平均縮小13.17%;GTVnd平均縮小13.95%,由于沒有參照的MRI圖像,所以靶區進行修改時相對比較保守,實際靶區的變化可能更大一些。而GTVnx和GTVnd的D95在治療過程中變化不大,實際受照劑量波動均在±3%以內。說明在實際治療過程中,靶區體積雖然會有所變化或者變化程度較大,但是其所受照劑量或者臨床要求劑量基本不會變化。因為靶區縮小是向心性的,也就是靶區縮小也是向高劑量區移動,所以在治療過程中靶區一直處于高劑量區,不會出現靶區欠量情況。見圖1。
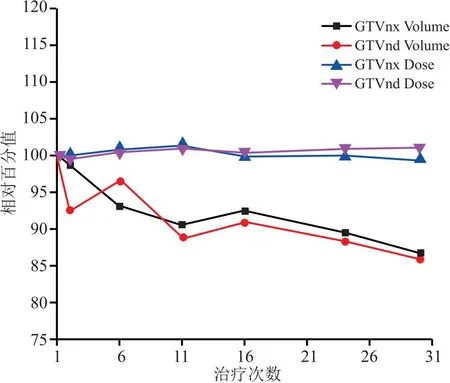
圖1 靶區隨治療次數體積與分次劑量平均變化圖
2.1.2 腮腺體積和分次劑量(D50)平均變化 在治療過程中腮腺的體積和劑量都會發生較大的變化。在治療末最后掃描CT上可以觀察到,左腮腺體積平均縮小17.05%,右腮腺體積平均縮小24.53%。10例患者實際腮腺平均D50劑量均比計劃劑量高,左腮腺D50劑量平均增加10.66%;右腮腺D50劑量平均增加12%。總體上隨治療次數增加,腮腺體積有逐漸縮小的趨勢,同時所受到的實際分次劑量有逐漸增加的趨勢。見圖2。
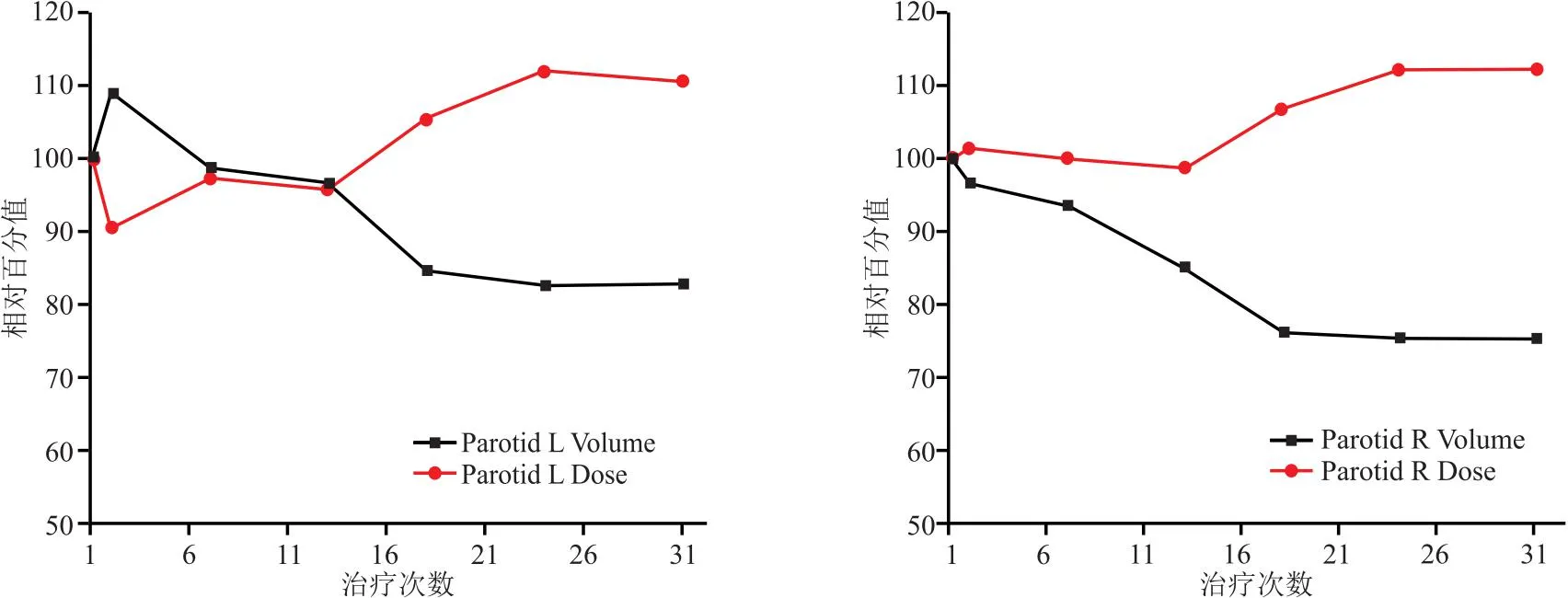
圖2 左右腮腺隨治療次數體積與分次劑量平均變化圖
2.1.3 腦干和脊髓體積及分次劑量(Dmax)平均變化 在整個治療過程中,脊髓和腦干的體積及受照劑量均未發生較大的變化。腦干的體積在治療過程中波動范圍為±5%,所受到的劑量也在±7%以內。脊髓的體積在治療過程中波動范圍也在±3%以內,脊髓劑量波動也在±5%以內。說明在治療過程中腦干和脊髓體積及劑量基本未發生比較明顯的變化,兩者所受到的劑量也均在臨床可接受范圍之內。見圖3。
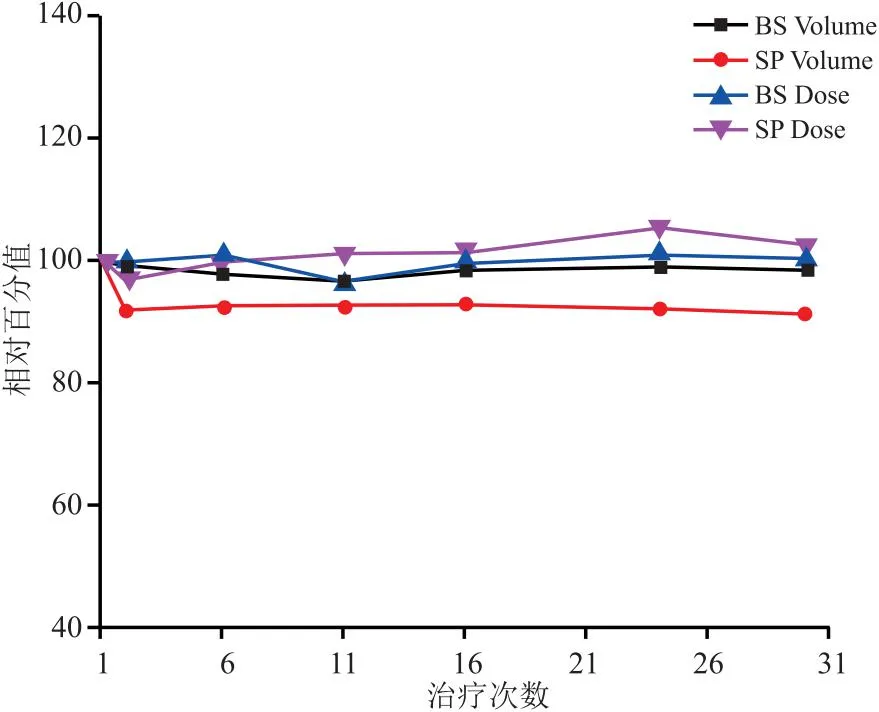
圖3 腦干和脊髓隨治療次數體積與分次劑量平均變化圖
2.2 靶區和危及器官累積劑量的變化
2.2.1 靶區GTVnx和GTVnd累積劑量(D95)的平均變化 在整個治療過程中,靶區內GTVnx和GTVnd由CT變形累加得到的實際受照劑量與原始計劃預期照射劑量基本相當,10例患者GTVnx和GTVnd的實際平均受照劑量差別均在0.03%以內,保證了在治療期間內,靶區內不會發生欠缺劑量或者漏照問題。見圖4。
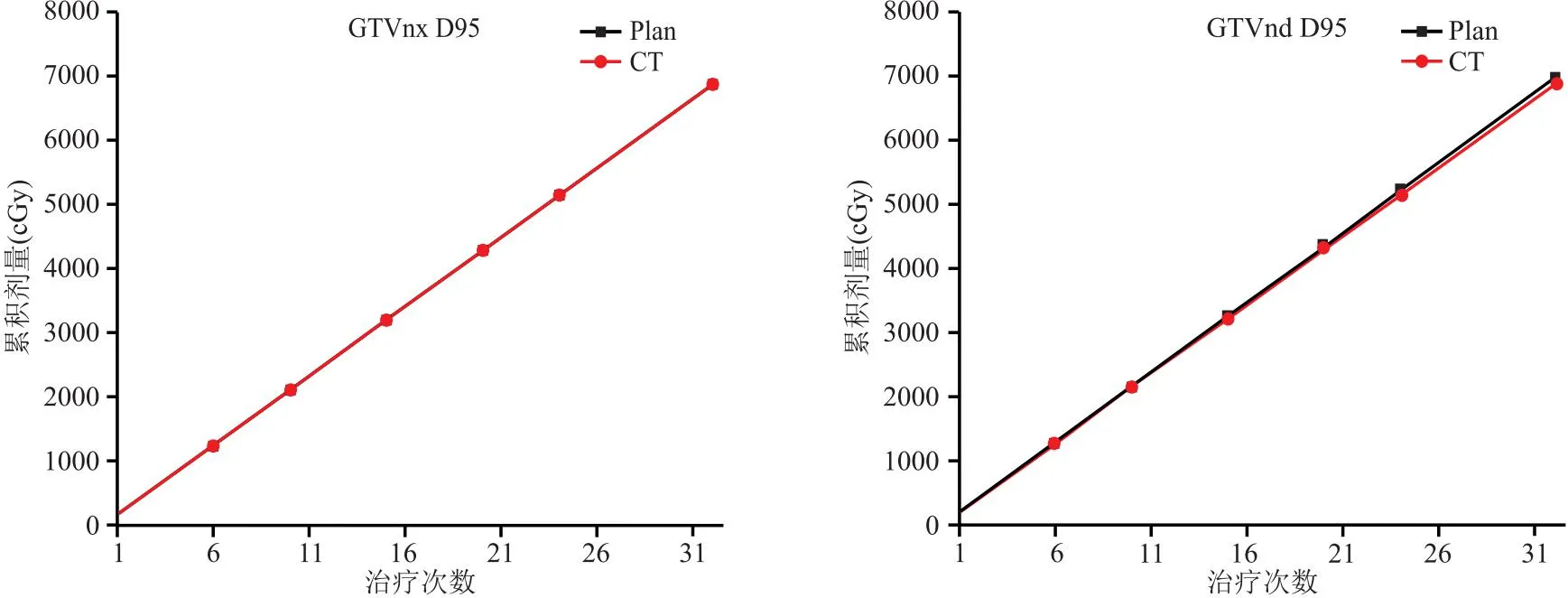
圖4 GTVnx和GTVnd累積劑量平均變化圖
2.2.2 左右腮腺累積劑量(D50)的平均變化 在治療末,左右腮腺所實際受到的累積劑量,均大于原始計劃累積劑量。10例患者左腮腺(PL)D50最后實際受到的劑量平均增加至原始計劃劑量的109.6%;右腮腺(PR)D50平均增加至原始計劃劑量的105.1%。10例患者中,有些患者的腮腺實際受照劑量已經超出了腮腺D50<3000 cGy的閾值劑量。由圖中也可看出,在第三周至第四周腮腺實際劑量相較計劃劑量開始有所變化,在治療過程中受到了高于預期劑量的照射。見圖5。
2.2.3 腦干和脊髓累積劑量(Dmax)平均變化 脊髓和腦干在實際治療中所受到的最大劑量Dmax與初始計劃相比并無太大變化,變化均在2%以內,而且即使變化也均在合理范圍內(腦干PRV<5400 cGy,脊髓PRV<4500 cGy)。說明實際治療中腦干和脊髓所受到的劑量與預期計劃劑量相當,基本未有超量現象。見圖6。
2.3 自適應計劃后靶區和危及器官劑量的變化 根據所得到的CT變形累加劑量和原始計劃劑量的對比圖,發現在治療的三到五周(15至22次)腮腺劑量變化較大。張勇乾等[13]通過觀察15例接受調強放射治療的鼻咽癌患者,建議在放療的第5周前重新定位做計劃,以減輕放療過程中的靶區及危及器官結構變化帶來的影響。因此,在本研究中10例患者也均選擇在第20次治療結束后進行自適應計劃設計,將20次治療分次附近掃描的CT圖像作為二次計劃圖像,各項優化參數以及優化條件保持與原計劃相同進行優化,在得到比較滿意的結果后,將20次原計劃劑量和后續新計劃劑量變形累加起來。并將原始計劃劑量、自適應計劃后的總體累加劑量進行對比分析。
2.3.1 二次計劃后GTVnx和GTVnd劑量平均變化 10例患者GTVnx和GTVnd的平均D95、D98、D2可以發現,原始計劃預期劑量和經過二次計劃后的兩階段累加劑量差別也不大,劑量偏差均在±2%以內。其余原始計劃、二次計劃后的靶區均勻性指數HI也都很接近,均能很好的滿足臨床要求。說明在整個治療過程中,靶區所受到的劑量和原始計劃預期劑量相符,經過二次計劃后也不會影響到靶區的劑量分布。見表1。

表1 靶區自適應計劃后劑量與原計劃劑量比較
2.3.2 二次計劃后危及器官劑量平均變化 患者腦干和脊髓經自適應計劃后所得到的劑量與原始計劃劑量相比均有減少,但差別不大,自適應計劃前后均未有超量發生。腮腺經二次計劃后,與原始計劃相比,D50和Dmean均明顯降低,其中D50平均降低10.12%和7.73%,Dmean平均降低6.76%和6.36%。見表2。
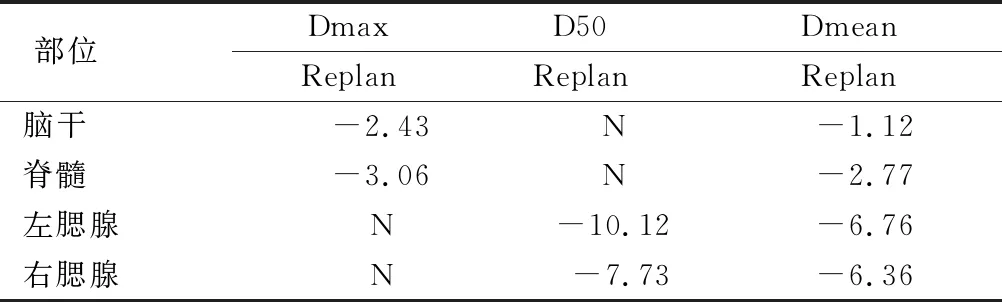
表2 危及器官自適應計劃后劑量與原計劃劑量比較(%)
3 討論
要保證鼻咽癌放療安全精確,分次放療中靶區和危及器官解剖結構和空間位置的穩定是一個重要因素,但是在臨床中發現,除了系統和擺位誤差外,放射治療過程中鼻咽原發病灶或頸部轉移淋巴結縮小、部分重要器官體積和位置發生改變、患者外形輪廓有明顯改變或患者體質量減輕,有可能會造成靶區及周圍器官所受到的劑量偏離原始計劃,影響預期放療效果[14]。
本研究應用每周CT來探討鼻咽癌放療過程中靶區和危及器官體積和劑量的變化。在研究中發現,隨著治療的進行,10例患者的靶區和腮腺的體積均呈現出了不同程度的萎縮,治療結束后GTVnx、GTVnd體積平均縮小了13.17%、13.95%,左腮腺、右腮腺體積平均縮小17.05%、24.53%。杜鐳等[15]研究了5例接受螺旋斷層治療(Tomotherapy)的局部晚期鼻咽癌患者,發現左腮腺在治療結束平均縮小了42%,右腮腺平均縮小了33%。蔣振東等[16]在CBCT圖像上觀察到,鼻咽癌調強放療中腮腺、外輪廓體積逐步縮小。Lu等[17]選擇了43例鼻咽癌患者在第20次治療時進行二次CT掃描,發現與原始CT相比,GTVnx、GTVnd體積平均縮小了30.1%、41.6%,左腮腺、右腮腺平均縮小33.4%、33.5%。Cheng等[18]選擇了19例鼻咽癌患者,在靶區接收到30 Gy和50 Gy時分別進行CT和MRI掃描,發現GTVnx體積分別縮小了9.1%和13.1%,GTVnd體積分別縮小了16.2%和28.7%,患側腮腺分別縮小了5.3、8.4 cm3,對側腮腺分別縮小了0.7、3.4 cm3。與國內外研究結果對比可知,國內研究中的患者腫瘤消退速度普遍沒有國外得出的結論快,腮腺的體積變化反而較大,這是否是因為人種體質的不同造成的,還有待進一步研究。
通過每周CT進行劑量累加后發現,雖然靶區GTVnx和GTVnd的體積一直在縮小,但劑量D95與計劃劑量相當,最大波動也在0.03%以內,觀察發現靶區整體往中心(即高劑量區)移動,所以靶區體積的變化不會影響到靶區的受量,在治療過程中基本不會發生靶區漏照或者欠量現象。而患者的左腮腺、右腮腺的D50平均增加了9.6%、5.1%。腦干和脊髓的Dmax與原始計劃劑量相當。姚鑫森等[19]通過形變配準分析18例鼻咽癌患者放療中腫瘤靶區和危及器官劑量變化,發現放療過程中靶區所受劑量基本無變化,與本研究結果一致。王微等[20]在鼻咽癌患者治療的第15次和第25次采集重復CT圖像,分析放療前半程和后半程靶區和危及器官的體積劑量變化,發現脊髓劑量在放療過程中基本無變化,腦干劑量略有升高。腮腺劑量增加會使其產生的副作用加重[21],腮腺功能下降會導致口干、齲齒、口腔潰瘍、影響患者吞咽、言語、味覺以及睡眠等方面。
本研究系統分析了靶區和危及器官累積劑量的變化后,10例患者均在第20次治療左右進行二次自適應計劃,然后與原始計劃劑量進行對比,靶區、腦干和脊髓劑量并無太大變化,均能很好的達到臨床預期,二次計劃能稍微提高靶區的均勻性。而腮腺經二次計劃后D50和Dmean均明顯降低。盧潔等[22]利用MimVista軟件對第25次掃描CT進行形變配準并重新計劃后,發現左腮腺Dmean平均降低2.0%,右腮腺Dmean平均降低1.1%。Schwartz等[23]通過對22例頭頸部腫瘤患者進行ART研究得出,在患者治療過程中,與單獨IGRT比較,根據影像資料得到的反饋信息調整一次計劃,可使對側和同側腮腺所受劑量平均減少 2.8% 和3.9% ,而進行了兩次計劃調整以后平均減少3.8%和9.0%。Nishi等[24]通過對鼻咽癌患者進行二次計劃,腮腺Dmean平均能降低5 Gy左右,這些結果都有一致性。
本研究只實施了一次自適應計劃,對于靶區或危及器官體積變化梯次比較大的患者,可進行多次自適應計劃以達到更好的臨床目標,但是也要同時考慮患者本身和醫務工作者的經濟和勞力狀況。此外,本研究在討論中提出的國內外鼻咽癌患者放療過程中的腫瘤消退速度有很大的差異,其具體原因有待進一步研究。
4 結論
晚期鼻咽癌患者放療過程中靶區和危及器官的位置和體積均會發生變化,靶區和腮腺體積變化較大,腦干和脊髓體積基本無變化,腮腺會受到超過預期劑量的照射,在治療后期有必要修改治療計劃,提高患者的生活質量。

