鈷配合物催化CO2氫化為甲醇的“氫質子和氫負離子”同時轉移機理
閆秀麗 趙雪喬 石博 郝勇靜

摘要:全球二氧化碳(CO2)過度排放,由此引發的溫室效應日益嚴峻.將CO2選擇性加氫為甲醇,可以將豐富、安全的碳源轉化為有價值的化學品和燃料.文中采用密度泛函理論對半三明治結構鈷配合物催化CO2加氫制甲醇的反應機理及新型催化劑的設計進行計算研究.計算結果表明,形成甲二醇分子時金屬Co上的氫負離子和吡啶配體中的氫質子同時轉移至甲酸分子上的過程是該反應的決速步,總反應能壘為122.2 kJ·mol-1(2→TS8,11).此外,通過不同的取代基取代酰胺氮原子和吡啶配體上的氫原子,設計了6種鈷配合物,計算預測了它們催化CO2加氫到甲醇的活性.在所有新提出的鈷配合物中,1a,1b,1c有潛力在溫和條件下高效催化CO2加氫到甲醇,它們的總自由能壘分別為107.5,109.2和111.7 kJ·mol-1.
關鍵詞:二氧化碳;催化加氫;密度泛函理論;反應機理;催化劑設計
中圖分類號:O 643.36;TQ 223.121 文獻標志碼:A 文章編號:1001-988Ⅹ(2024)02-0058-07
Simultaneous transfer mechanism of“a hydroxyl proton and hydride”for the hydrogenation of CO2to methanol catalyzed by cobalt complexes
YAN Xiu-li ZHAO Xue-qiao ,SHI Bo3,HAO Yong-jing1
Abstract:The greenhouse effect caused by excessive global carbon dioxide(CO2) emissions is becoming more and more serious.Selective hydrogenation of CO2 to methanol can convert abundant and safe carbon sources into valuable chemicals and fuels.A computational study using density functional theory is conducted to investigate the reaction mechanism of CO2 hydrogenation to methanol catalyzed by a half-sandwich cobalt complex,as well as the design of new catalysts.The calculated results show that the formation of methanediol via the simultaneous transfer of a hydroxyl proton in the pyridine ligand and the hydride on the metal Co to the formic acid is the rate-determining step with a total barrier of 122.2 kJ·mol-1(2→TS8,11).Furthermore,six cobalt complexes are designed by replacing the hydrogen atom on the amide nitrogen atom and pyridine ligand with different substituents.Among all newly proposed cobalt complexes,1a,1b,and 1c are the promising catalyst candidates for hydrogenation of CO2 to methanol with low total free energy barriers of 107.5,109.2,and 111.7 kJ·mol-1,respectively.
Key words:carbon dioxide;catalytic hydrogenation;density functional theory;reaction mechanism;catalyst design
根據英國BP石油公司統計的2022年世界能源消耗結果,全球對于煤炭、石油、天然氣等的能源消耗總量依舊不斷增加,化石燃料仍為目前能源的主要來源[1].過度使用化石能源也引起了嚴重的環境問題,如二氧化碳(CO2)過度排放導致全球氣候變化和溫室效應[2].據統計,在1960~2023年,大氣中CO2的濃度已由工業化前的2.8×10-4上升至4.19×10-4,如果全球能源需求繼續增長并且主要通過化石燃料來滿足,那么到本世紀末,大氣中的CO2濃度預計將超過9.0×10-4,這可能帶來更加強烈的氣候變化.在這種背景下,氫(H2)作為一種清潔的替代能源引起了科學家們越來越多的關注,目前主要通過化石燃料的燃燒以及電解水制氫[3],但溫室氣體的排放和較高的生產成本使得發展經濟、可持續的氫能源仍處在瓶頸期.
CO2作為自然界中豐富、安全、廉價的C1資源,在循環利用的諸多方式中,可以實現高附加值化學品和燃料的合成,對于實現人類社會的可持續發展具有重要的意義和廣泛的應用前景.CO2加氫制甲醇反應(CO2+3H2→CH3OH+H2O)是實現CO2轉化利用的一種理想方式.這是因為甲醇既可以作為代用燃料,又具有較高的氫含量(12.6%)和方便運輸的優點[4-5].
近年來,科研工作者對催化CO2轉化的反應進行了大量研究[4,6-11].Schneidewind等[12]報道了一種均相非貴金屬Co配合物,其催化CO2直接加氫到甲醇的TON僅為78.Kar等[13]報道了Mn-PNP 配合物均相催化CO2加氫到甲醇,反應的最大TON僅為36.Schieweck等[11]報道了三齒磷配體螯合的Ru配合物,在乙醇溶劑中催化CO2直接加氫到甲醇的TON最高可達2100.Kanega等[14]報道了在溫和反應條件下(30 ℃,5 MPa(TON 2.0)和70 ℃,0.5 MPa(TON 3.0)),使用多核過渡金屬Ir配合物加氫制備甲醇的新方法.Kanega等[10]報道了一系列Ir配合物催化CO2加氫和甲酸脫氫的反應,其中含酰胺配體的銥配合物Cp*Ir(L12)(H2O)HSO4(L12=6-hydroxy-N-phenylpicolinamidate)在反應初始1 h內的TOF為198 h-1.盡管關于均相催化CO2加氫到甲醇的報道已經取得了一定的進展,但是大多數實驗報道的催化體系都存在貴金屬以及對空氣和水敏感的磷配體,且反應條件嚴苛,催化效率低下.因此,發展可催化CO2加氫到甲醇的低成本、高效率以及不含磷配體的過渡金屬催化劑依然是亟待解決的重要問題.
受Kanega等[14]報道的半三明治結構銥配合物相關催化反應機理的啟發,文中計算了非貴金屬鈷配合物[Cp*Co(L)OH2]+(1,L=2-hydroxy-N-picolinamidate)催化CO2加氫到甲醇的詳細反應機理.在明確反應機理的基礎上,構建了6種鈷配合物,計算了其催化CO2加氫到甲醇的反應中潛在的關鍵中間體和過渡態之間的相對吉布斯自由能,從而提出了可以高效催化該反應的非貴金屬催化劑結構.
1 研究方法
文中所有的 DFT 計算均使用M06 泛函[15],并在Gaussian 09程序包[16]中完成.為了提高計算效率,在保證計算精度的前提下,對所有C,H原子采用6-31G(d,p)基組[17],N,O原子采用6-31+G(d)[18]基組,Co原子采用包含相對論效應修正的Stuttgart系列贗勢基組ECP10MDF[19-20].所有構型優化都考慮了溶劑效應的影響,采用SMD溶劑模型[21](極性部分使用IEFPCM方法[22]進行計算).對體系中所有結構均進行溶劑校正,文中以水作為溶劑.質子在水溶劑中的自由能Gsol(H+)使用實驗值-1 112.5 kJ·mol-1[23].在T為298.15 K和1 atm大氣壓條件下進行熱力學能量修正.采用超精細積分格點(99,590)進行數值積分計算.同時,對所有優化后的幾何構型進行頻率計算,結果表明所有中間體均無虛頻,過渡態有且只有一個虛頻.所有過渡態均通過內稟反應坐標法(IRC)確認能夠連接正確的中間體.3D分子結構圖由JIMP2軟件[24]繪制.
2 結果與討論
2.1 CO2加氫到甲酸
圖1為1催化CO2加氫到甲酸的催化反應循環(Cycle 1).
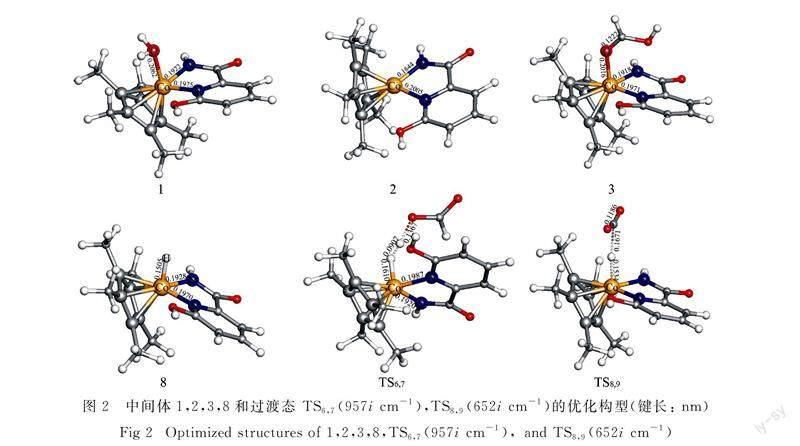
在反應的開始,催化劑1的中心金屬Co原子失去配位的H2O分子,經過10.5 kJ·mol-1的自由能下降過程,形成中間體2.隨后,H2分子占據中間體2的空位后形成自由能為10.5 kJ·mol-1的中間體5.之后中間體5中H2上的氫質子通過過渡態TS6,7(圖2,ΔG≠=97.1 kJ·mol-1)轉移到溶液中甲酸根陰離子的氧原子上形成甲酸.新形成的甲酸分子從中間體7中脫去后形成金屬氫化物8.接著,一個CO2分子與8反應,通過過渡態TS8,9(圖2,ΔG≠=99.2 kJ·mol-1)奪取中心金屬Co上的氫負離子到其不飽和的碳原子上,得到甲酸根陰離子.中間體9中的甲酸根陰離子從溶劑中得到一個氫質子,然后從10中以甲酸分子的形式離去.從自由能反應坐標圖可以看出(圖3),中間體2和過渡態TS8,9是CO2加氫到甲酸過程的決速態,能量跨度為109.7 kJ·mol-1(2→TS8,9).由于催化劑1并沒有參與該催化循環,因此可以被認為是該反應的預催化劑.除了H2,甲酸也可以占據中間體2 的空位,形成具有較強Co—O鍵(0.206 1 nm)的穩定中間體3.
2.2 甲酸加氫到甲醛和水
圖4為1催化甲酸加氫到甲醛和水的催化反應循環(Cycle 2).
甲酸加氫生成甲醛和水的反應由兩個催化循環構成:甲酸加氫生成甲二醇以及甲二醇分解生成甲醛和水.在該循環的開始與Cycle 1類似,都是形成中間體8.然后甲酸分子與8結合,通過過渡態TS8,11(圖5, ΔG≠=111.7 kJ·mol-1)同時奪取中心金屬Co上的氫負離子與吡啶配體中的氫質子到其不飽和碳原子和氧原子上形成中間
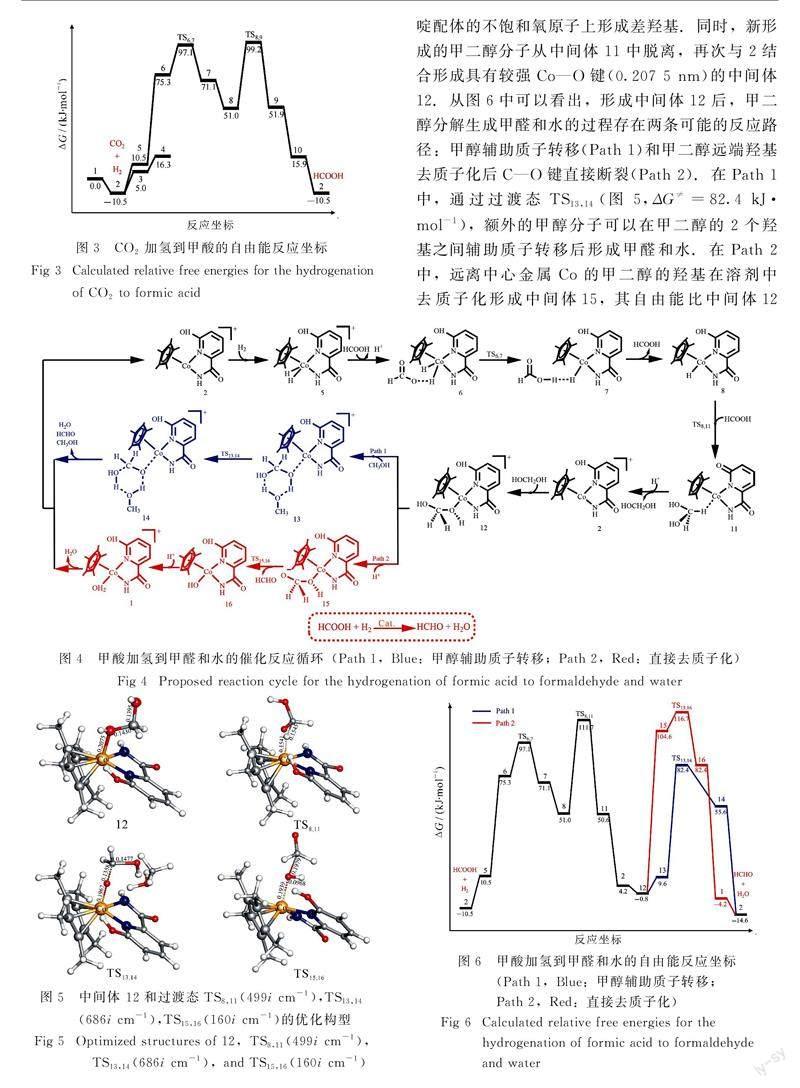
體11. 隨后, 溶劑向中間體11轉移一個質子到吡啶配體的不飽和氧原子上形成差羥基.同時,新形成的甲二醇分子從中間體11中脫離,再次與2結合形成具有較強Co—O鍵(0.207 5 nm)的中間體12.從圖6中可以看出,形成中間體12后,甲二醇分解生成甲醛和水的過程存在兩條可能的反應路徑:甲醇輔助質子轉移(Path 1)和甲二醇遠端羥基去質子化后C—O鍵直接斷裂(Path 2).在Path 1中,通過過渡態TS13,14(圖 5,ΔG≠=82.4 kJ·mol-1),額外的甲醇分子可以在甲二醇的2個羥基之間輔助質子轉移后形成甲醛和水.在Path 2中,遠離中心金屬Co的甲二醇的羥基在溶劑中質子化形成中間體15,其自由能比中間體12高105.4 kJ·mol-1.然后通過過渡態TS15,16(圖5, ΔG≠=116.7 kJ·mol-1),經過 C—O 鍵直接斷裂后生成產物甲醛分子,該過程的自由能僅比中間體15高12.1 kJ·mol-1.最后,中間體16中的羥基從溶劑中得到一個質子,以水分子的形式從1中脫離再次生成中間體2.比較圖4中的兩條反應路徑,從自由能反應坐標圖(圖6)可以看出,Path 1中甲醇輔助質子轉移(TS13,14)的自由能壘比Path 2中C—O鍵直接斷裂(TS15,16)要低34.3 kJ·mol-1.通過分析該循環的自由能反應坐標圖(圖6),中間體2和TS8,11是甲酸加氫到甲醛和水反應過程的決速態,能量跨度為122.2 kJ·mol-1(2→TS8,11).
2.3 甲醛加氫到甲醇
圖7為1催化甲醛加氫到甲醇的催化反應循環(Cycle 3).
與甲酸加氫反應類似,Cycle 3 的開始也是先通過過渡態TS6,7形成中間體 8.隨后甲醛分子可通過TS17,18(圖8, ΔG≠=73.2 kJ·mol-1)奪取金屬 Co上的氫負離子到其不飽和碳原子上,該過程跨越的自由能壘低于TS6,7(圖9).之后中間體18從溶劑中得到質子后以甲醇分子的形式脫去,再次生成中間體2,該過程自由能下降61.0 kJ·mol-1.甲醇分子也可以再次與2結合,形成穩定的中間體20.該中間體由于具有較強的Co—O 鍵(0.204 7 nm),因此其自由能比中間體2穩定72.3 kJ·mol-1.除了形成20,甲醛分子也可以占據中間體2的空位,形成自由能比分離的中間體2和甲醛高1.3 kJ·mol-1的中間體19.
通過比較上述3個催化循環的自由能反應坐標,整個催化循環的決速步為形成甲二醇分子時金屬Co上的氫負離子和吡啶配體中的氫質子同時轉移至甲酸分子上的步驟,總反應能壘為122.2 kJ·mol-1(2→TS8,11).
2.4 計算設計新型的催化劑
為了找到催化活性較高的潛在過渡金屬Co催化劑,使用不同取代基取代酰胺氮原子和吡啶配體上的氫原子,并設計了6種鈷配合物(圖10).圖10給出了新設計的鈷配合物催化CO2加氫反應中決速步驟之間的相對吉布斯自由能.可以看到,1e和1f具有相對較高的反應能壘,分別為126.8和128.9 kJ·mol-1,因此它們在水溶液中催化這類反應并不太容易.而催化劑1a,1b,1c具有相對較低的反應能壘,分別為107.5,109.2,111.7 kJ·mol-1,較低的能壘表明,在溫和的條件下可以有效地催化CO2加氫到甲醇.
為了深入了解催化活性和電子結構之間的關系,對1,8 和 TS8,11進行了自然鍵軌道(NBO)分析.從表1可知,1a-1f中金屬 Co 上的NPA電荷差距不大,但是 1a-1c中與 Co 相連的吡啶配體N原子的NPA電荷比1d-1f更負.對于金屬氫化物(8a-8f), 8a-8f中金屬 Co 上的NPA電荷差距不大,8a-8c中與Co相連的吡啶配體N原子的NPA電荷同樣比8d-8f更負,而H原子上的正電荷比8d-8f更少.因此,由于電荷分布的不同使得催化劑1a,1b,1c催化反應的自由能壘相對較低.
3 結論
對半三明治結構的鈷配合物催化CO2加氫反應進行了詳細的計算研究并提出了“氫質子和氫負離子”同時轉移的機理.整個催化循環的決速步為形成甲二醇反應中Co上的氫負離子和吡啶配體中的氫質子同時轉移至甲酸分子上的步驟,總反應能壘為122.2 kJ·mol-1(2→TS8,11).使用不同的取代基取代酰胺氮原子和吡啶配體上的氫原子,構建并預測了6種半三明治結構的鈷配合物.通過比較決速步的相對吉布斯自由能,研究了其催化CO2加氫反應的活性.計算結果表明,催化劑1a,1b,1c具有相對較低的反應能壘,分別為107.5,109.2, 111.7 kJ·mol-1.
這樣較低的能壘表明,在溫和的條件下可以有效地催化CO2加氫到甲醇.在此項工作中,通過對非貴金屬鈷配合物催化CO2加氫的反應機理研究和對不同取代基影響反應能壘的分析,為進一步設計可用于催化CO2加氫到甲醇的非貴金屬催化劑提供了思路.
參考文獻:
[1]POORMOHAMMADIAN S J,BAHADORAN F,VAKILI-NEZHAAD G R.Recent progress in homogeneous hydrogenation of carbon dioxide to methanol[J].Rev Chem Eng,2023,39(5):783.
[2]ONISHI N,HIMEDA Y.Homogeneous catalysts for CO2 hydrogenation to methanol and methanol dehydrogenation to hydrogen generation[J].Coord Chem Rev,2022,472:214767.
[3]SCHNEIDEWIND J,ARGELLO C M A,JUNGE H,et al.Two-photon,visible light water splitting at a molecular ruthenium complex[J].Energy Environ Sci,2021,14(8):4427.
[4]NAVARRO-JAN S,VIRGINIE M,BONIN J,et al.Highlights and challenges in the selective reduction of carbon dioxide to methanol[J].Nat Rev Chem,2021,5(8):564.
[5]NITOPI S,BERTHEUSSEN E,SCOTT S B,et al.Progress and perspectives of electrochemical CO2 reduction on copper in aqueous electrolyte[J].Chem Rev,2019,119(12):7610.
[6]DU X L,JIANG Z,SU D S,et al.Research progress on the indirect hydrogenation of carbon dioxide to methanol[J].Chem Sus Chem,2016,9(4):322.
[7]田海峰,廖建康,查飛,等.丙烷與二氧化碳耦合制丙烯的熱力學模擬研究[J].西北師范大學學報(自然科學版),2019,55(2):94.
[8]WESSELBAUM S,VOM S T,KLANKERMAYER J,et al.Hydrogenation of carbon dioxide to,methanol by using a homogeneous ruthenium-phosphine catalyst[J].Angew Chem Int Ed,2012,51(30):7499.
[9]BERNSKOETTER W H,HAZARI N.Reversible hydrogenation of carbon dioxide to formic acid and methanol:Lewis acid enhancement of base metal catalysts[J].Acc Chem Res,2017,50(4):1049.
[10]KANEGA R,ERTEM M Z,ONISHI N,et al.CO2 hydrogenation and formic acid dehydrogenation using ir catalysts with amide-based ligands[J].Organometallics,2020,39(9):1519.
[11]SCHIEWECK B G,JRLING-WILL P,KLANKERMAYER J.Structurally versatile ligand system for the ruthenium catalyzed one-pot hydrogenation of CO2 to methanol[J].ACS Catalysis,2020,10(6):3890.
[12]SCHNEIDEWIND J,ADAM R,BAUMANN W,et al.Low-temperature hydrogenation of carbon dioxide to methanol with a homogeneous cobalt catalyst[J].Angew Chem Int Ed,2017,56(7):1890.
[13]KAR S,GOEPPERT A,KOTHANDARAMAN J,et al.Manganese-catalyzed sequential hydrogenation of CO2 to methanol via formamide[J].ACS Catalysis,2017,7(9):6347.
[14]KANEGA R,ONISHI N,TANAKA S,et al.Catalytic hydrogenation of CO2 to methanol using multinuclear iridium complexes in a gas-solid phase reaction[J].J Am Chem Soc,2021,143(3):1570.
[15]ZHAO Y,TRUHLAR D G.The M06 suite of density functionals for main group thermochemistry,thermochemical kinetics,noncovalent interactions,excited states,and transition elements:two new functionals and systematic testing of four M06-class functionals and 12 other functionals[J].Theor Chem Acc,2008,120(1-3):215.
[16]FRISCH M J,TRUCKS G W,SCHLEGEL H B,et al.Gaussian 09,Revision E.01[Z].Wallingford CT:Gaussian,Inc.,2010.
[17]PERDEW J P,BURKE K,ERNZERHOF M.Generalized gradient approximation made simple[J].Phys Rev Lett,1996,77(18):3865.
[18]FRANCL M M,PIETRO W J,HEHRE W J,et al.Self-consistent molecular orbital methodsⅩⅫ.A polarization-type basis set for second-row elements[J].J Chem Phys,1982,77(7):3654.
[19]ANDRAE D,HUSSERMANN U,DOLG M,et al.Energy-adjusted Ab initio pseudopotentials for the second and third row transition elements[J].Theoretica Chimica Acta,1990,77(2):123.
[20]MARTIN J M L,SUNDERMANN A.Correlation consistent valence basis sets for use with the stuttgart-dresden-bonn relativistic effective core potentials:the atoms Ga-Kr and In-Xe[J].J Chem Phys,2001,114(8):3408.
[21]MARENICH A V,CRAMER C J and TRUHLAR D G.Universal solvation model based on solute electron density and on a continuum model of the solvent defined by the bulk dielectric constant and atomic surface tensions[J].J Phys Chem B,2009,113(18):6378.
[22]TOMASI J,MENNUCCI B,CAMMI R.Quantum mechanical continuum solvation models[J].Chem Rev,2005,105(8):2999.
[23]CAMAIONI D M,SCHWERDTFEGER C A.Comment on“accurate experimental values for the free energies of hydration of H+,OH-,and H3O+”[J].J Phys Chem A,2005,109(47):10795.
[24]MANSON J,WEBSTER C E,HALL M B.JIMP2,Version 0.091[Z].College Station,TX:Texas A&M University,2006.
(責任編輯 陸泉芳)
收稿日期:2023-09-28;修改稿收到日期:2023-12-23
基金項目:河北省自然科學基金資助項目(B2021402012; E2021402017)
作者簡介:閆秀麗 (1989—),女,河北邯鄲人,講師,博士.主要研究方向為理論有機催化反應.E-mail:yanxiuli@hebeu.edu.cn
*通信聯系人,女,副教授,博士.主要研究方向為催化化學.E-mail:haoyj@hebeu.edu.cn

