微波場中蛋白質-淀粉可食薄膜結構特性分子動力學研究進展
楊瑞炳,稅小林,梁 珊,毛偉杰,劉書成,2,魏 帥,2,*
(1.廣東海洋大學食品科技學院,廣東省水產品加工與安全重點實驗室,廣東省海洋生物制品工程實驗室,廣東省海洋食品工程技術研究中心,水產品深加工廣東普通高等學校重點實驗室,廣東 湛江 524088;2.大連工業大學海洋食品精深加工關鍵技術省部共建協同創新中心,遼寧 大連 116034)
蛋白質在自然狀態下以球狀或纖維狀存在,可生物降解,其物理和化學性質取決于氨基酸殘基的相對數量和在多肽鏈上的位置,適用于制造新型復合材料和混合材料[1]。根據化學結構的不同,蛋白質分為乳清蛋白(Ovalbumin,OVA)、鋅蛋白、大豆蛋白及卵清蛋白等,其所制作的薄膜廣泛應用在水果、蔬菜、堅果、肉類、預制甜點、奶酪片等[2]。OVA 屬于球狀蛋白,具有三級結構和球形,可因加熱、高壓、酶促反應、振蕩、pH值變化等而變性[3]。OVA 成膜特性較好,但純OVA制備的薄膜機械性能和阻隔性較差,需要絡合其他配體或進行物理、化學、酶法改性以提高其性能[4]。淀粉是一種可生物降解的聚合物,包括兩種初級聚合物(直鏈淀粉和支鏈淀粉)。淀粉膜的理化性質與其一級結構、二級結構、分子鏈相互排列、分子取向及累積的三級結構或晶體結構有關,在成膜過程中,淀粉鏈的取向有利于提高淀粉膜的機械強度和阻隔性能[5]。Wang 等[6]研究表明,較高的分子取向容易誘導重結晶和形成有序的晶體結構,可增強淀粉薄膜的功能特性。Shah等[7]研究發現,辛烯基琥珀酸是木薯淀粉分子鏈上的兩親基團,決定了木薯淀粉分子具有親水性和親脂性。單一的淀粉薄膜具有高親水性和吸濕性,但不具備高拉伸強度,在環境中易腐爛和變形,成膜時需搭配其他原料[8]。將生物聚合物進行混合后開發新的或具有特定功能的生物聚合物材料,是平衡或扭轉物料自身缺陷的有效途徑。如將松果木質素按照一定比例與蠶豆蛋白混合后制備的薄膜,其斷裂伸長率、熱穩定性、水汽阻隔性均顯著提高,木質素和蛋白質分子間的相互作用,有效降低了薄膜中的水分含量[9]。利用油酸(OA)與納米晶纖維素(NCC)相互作用制備的OA-NCC 復合薄膜,抗拉強度和斷裂伸長率顯著提高,薄膜內聚性得到加強[10]。OVA和小麥淀粉混合,可形成新的結晶區域,其能有效改善所制作產品的硬度、咀嚼性、回彈性、抗剪切性等質構特性,提升持水能力的同時降低體外消化率[11]。在蛋白質和淀粉構成的二元混合物中,生物聚合物之間的相容性決定了混合物的穩定性。若混合物之間不具備熱力學相容性,則可能發生相分離形成新的微觀結構,復合材料功能特性也將受到影響,表現在熱加工、化學作用或機械作用過程中,復合材料分子網絡破裂或基質的重組,材料中親水性或疏水性化合物從基質中遷移和釋放,進而造成復合材料功能特性改變[12]。
微波加熱食品具有便捷高效的特點,將食物置于微波電場時,在離子傳導機理中,正離子向電場方向移動,負離子向相反方向移動,場的方向改變致使離子來回移動,食物中含有的極性分子(如水)會產生偶極振動和旋轉,伴隨著劇烈的撞擊與摩擦,進而使食品升溫[13]。微波加熱直接作用于食品內部,且主要是微波場對食品物料中極性分子的作用,因此極性分子的自身介電特性及數量是影響食品中傳熱和傳質的重要影響因素。介電特性為靜電在電場中的節能和損耗性質,通常表示為介電常數(ε′)和介電損耗(ε″);食物介電特性的影響因素有很多,如成分(水和鹽含量)、密度、溫度、頻率和儲存時間[14]。
蛋白質和淀粉原料擁有不同的缺點與優點,但兩者配合形成的二元混合物卻可以在特定使用場景中彌補各自的缺點,蛋白質-淀粉薄膜就是很好的例子。將薄膜置于微波環境中,微波對薄膜的作用效果除去設備本身功率等因素后,主要與薄膜的含水量、極性基團數量、靜電作用力、范德華力、化學鍵能大小等相關[15]。然而這些研究超越了人肉眼直觀感受的范圍,無法用肉眼觀察。分子動力學(Molecular dynamics,MD)模擬經過不斷發展,在分析蛋白質構象變化及其動力學機理方面發揮了重要作用。MD技術依托牛頓力學理論,以物質的微觀結構系統反映宏觀特征,其在分子結構體系表征上的獨特優勢,為理解組分間構象變化和分子間作用力變化提供了關鍵信息[16]。食品領域中的MD 模擬(如蛋白質-淀粉薄膜材料)往往需涉及數以萬計分子量的大分子模擬,這阻礙了更高性能、更具特色的蛋白質-淀粉薄膜的開發與應用。因此,本綜述以蛋白質-淀粉薄膜研究為引,總結了MD 模擬技術在蛋白質-淀粉薄膜結構特性研究中的應用進展,重點以微波加熱為處理手段,以期為蛋白質-淀粉薄膜材料的開發提供參考。
1 MD模擬技術
1.1 經典MD技術的起源與發展
分子動力學的起源與發展歷程有三個重要階段:第一階段是Alder 和Wainwright 基于剛球勢提出的一種模擬方法,其核心理念是采用電子計算機求解多體運動的方程;第二階段是Rahman 利用Lennard-Jones 勢(又稱L-J 勢、6-12 勢、12-6 勢)函數法對液態氬性質的模擬,其解析式簡潔高效,尤其對惰性氣體分子間相互作用力的計算精確;第三階段是第一性原理分子動力學法(FPMD)的建立,在這個算法中,經典動力學的常數可在試驗中獲取或以函數進行擬合,最終繞開繁瑣的計算過程[16]。分子動力學模擬、量子模擬、大顆粒模擬有著本質的區別(如圖1A所示),在模擬過程中涉及許多復雜的分子勢能模型(圖1B)。基于剛球勢求解多體運動方程早期出現在各種非平衡現象所伴隨的弛豫現象研究,利用電子計算機精確求解數百個粒子的經典運動方程,其確定了系統中被處理粒子的周期性邊界條件,初始粒子出發于有序晶格內,運動方向隨機,但速度和大小統一[17]。Lennard-Jones 勢函數法則是基于兩粒子中心力相互作用的經典動力學計算方法。該方法需要依據現實條件假設相互作用勢被截斷到一定范圍外,體系中的粒子數量必須很小,同時需要施加系統邊界條件。最后,運動方程還必須作為一組差分方程來求解,這個方程涉及從一組速度和位置到下一組速度和位置間一定時間的增加量[18]。FPMD 法也叫“從頭算動力學”,可根據原子核和電子相互作用的原理及其基本運動規律,經過多個近似處理后直接求解薛定諤方程,進而得到材料幾乎所有的基態性質[19]。在FPMD 方法之后巨正則系綜蒙特卡羅法(Grand canonical monte carlo,GCMC)被提出,并在蛋白質、脂肪、碳水化合物等大規模分子系統中成功應用[20]。
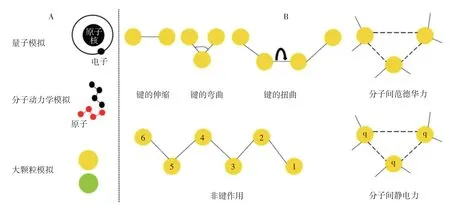
圖1 常見模擬方法(A)和MD模擬過程中常見的分子勢能模型(B)Fig.1 Common simulation methods(A)and molecular potential energy models in MD simulation(B)
1.2 現代分子動力學的發展
現代MD 技術核心依托牛頓運動方程以及相關作用勢進行演化,在現代計算機和超算技術及相關軟件技術的支持下迅速發展,模擬方向有:①大體系的局部精確模擬,用以實現不同水平的計算方法同時進行的方法,將對體系劃分為高層、中層和底層區分計算,在降低計算成本的同時得到可靠的幾何結構以及能量,可應用于生物分子、過渡金屬配合物和催化等領域[21];②對相空間中的特定狀態進行研究,演化出的方法是“增強采樣動力學”,其可用以解決常規采樣效率低且易陷入局部極小值問題,廣泛應用于蛋白質構象變化及計算相應的自由能變化研究[22];③克服經典動力學不能模擬成鍵或斷鍵反應,誕生了反應力場動力學,以解決經典力場模擬過程中化學鍵的固定問題,其時間尺度和空間尺度計算介于經典MD 力場計算與量子力學計算之間;④對MD 模擬過程中特定區域分子施加額外受力研究,并且促生了拉伸動力學,用于考察外力作用下目標分子解折疊或分子復合物解離過程中的構象動態變化。
1.3 MD模擬步驟
MD 模擬結合了物理學、化學及數學計算方法,通過牛頓第二定律演化得到相應運動方程,可以在物理定律(包括量子和經典力學理論)的影響下,模擬特定時間段內分子之間的相互作用,它被認為可以直接洞察聚合物基系統的分子相互作用和能量狀態[23]。MD模擬一般分4步,如圖2所示。其中又細分構型、力場和模擬軟件選擇、構建體系與能量最小化、平衡、結果分析。構型是模擬前提,試驗數據或量子化計算是構型主要來源,如X 射線衍射分析、核磁共振波譜法測定及已知分子結構的同源建模得到目標分子結構信息(鍵、角、扭轉角、Lennard-Jones 相互作用及靜電相互作用)[24]。構型完成后需要依據模擬體系特性選擇適宜的力場和模擬軟件,而軟件選擇通常是依據力場而定(表1)。

表1 MD模擬常用軟件及信息Table 1 Common software and information for MD simulation
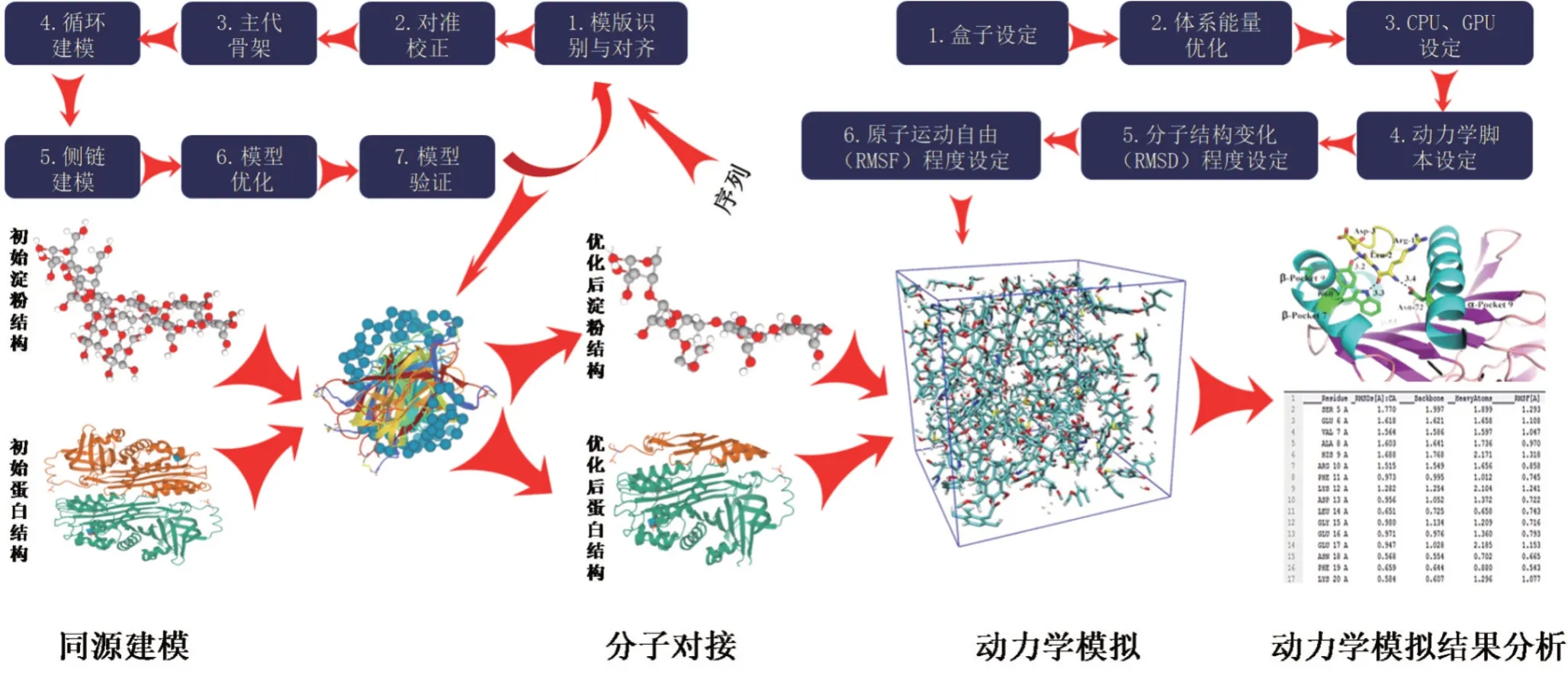
圖2 YASARA軟件MD模擬步驟示意圖Fig.2 Schematic diagram of YASARA software MD simulation steps
依照研究對象所處的環境(如氣相、溶液或跨膜環境)構建模擬體系,同時運用最陡下降法和共軛梯度法將體系能量最小化,以解決初步構型體系中產生的相鄰原子間隔過近問題。體系完成后的分子應當依據玻爾茲曼分布指定原子初始速度,并調整體系到任意方向的動能之和為零,此時MD體系溫度恒定,以保證體系無平動位移[34]。經平衡相的體系進行模擬時,體系中的分子和原子依照構型狀態進行吸引、排斥、碰撞運動,引入牛頓運動方程及預先給定的粒子間相互作用勢計算分子內部的勢能和動能轉換,得到粒子坐標、速度及能量(靜電能、范德華能、體系動能、勢能及總能量)隨時間變化的運動軌跡,待體系再次平衡后可產生抽樣樣本[35]。通過MD 模擬軟件分析從系綜平均中得到的可與試驗結果相比較的物理量[36],常用的分析方法包括:①平均能量及其漲落隨模擬時間的變化;②體系平均原子坐標及其漲落隨模擬時間的變化;③計算體系的結合自由能;④由幾何判據分析分子內及分子間的氫鍵結構及其氫鍵占有率;⑤蛋白質二級結構及其隨時間變化;⑥計算體系的動力學性質[37-38]。
2 微波場中蛋白質和淀粉的響應及MD 模擬應用
2.1 蛋白質在微波場中的響應及MD模擬應用
微波加熱(MH)被稱為第二火焰,在蛋白基食品加工中被廣泛應用,微波與物料組分間存在相互作用,但作用機理尚不清晰,尤其是蛋白質分子與微波間的相互影響關系難以確定。MH屬于體積加熱,傳統加熱為從表面到核心,兩者在傳熱方式及傳熱效率上存在巨大差異。MH存在熱效應和非熱效應,對蛋白質溶解性、起泡性、乳化性、凝膠性、消化特性等存在改性作用[39]。MH 可促進蛋白質降解,如木瓜蛋白酶樣品中蛋白質的水解,MH會引發蛋白質結構中亞基位移,改變蛋白質的結構特征[40]。MH 可以利用非熱效應促使牛β-乳球蛋白(β-Lg)結構的展開,三級結構損失高于傳統加熱,對β-Lg 中埋藏酰胺基團的熱展開和暴露具有顯著增強作用[41]。Yoshida 等[42]研究顯示,微波可令分子擾動或影響分子轉運。依據MH 的核心原理,微波場中的分子能受微波場影響,相關分子必定表現出極性。如蛋白質中的氨基酸基團屬于帶正電的極性基團,MH形成的磁場會使極性分子運動和轉動,引起分子摩擦導致物料升溫[43]。因此,MH 引發的熱效應會導致對溫度敏感的蛋白質發生結構變化、展開和聚集效應。在蛋白質對微波的響應研究中,低水合卵清蛋白中卵清蛋白的低頻響應表現出異常的介電行為,其中實數和虛部介電常數平行,并向低頻急劇增加,也被稱為低頻色散(LFD),這可能是質子通過蛋白質基質的準直流滲透,且蛋白質在大分子尺度上發生了質子跳躍[44]。Xie等[45]的研究結果支持蛋白質在MH中發生的大分子跳躍現象,同時指出,跳躍可能發生在可電離的兩條側鏈之間,且屬于短程電荷跳躍。在蛋白質對MH的響應中,蛋白質骨架的靈活性,結合水和表面水合水的重新定向極化也可對響應程度產生影響,其在某種程度上取決于蛋白質中水分含量及水合水與蛋白質間的特定相互作用[46]。MD模擬參與的蛋白研究中可以提供條件變化后蛋白質與相關底物在特定條件下反應一段時間(通常為皮秒(ps)或納秒(ns))后,體系中各組分原子分子的位置信息、靜電作用力、范德華力、鍵角鍵能等關鍵信息。Eremenko等[47]在人血清蛋白(HSA)、H2O、NaCl、葡萄糖組成的NaCl-HSA水溶液體系及葡萄糖-HSA 水溶液體系中成功運用MD模擬得到了試驗中難以觀察的鍵能、成鍵主要作用力、氫鍵、體系能量等信息。如圖3A所示,MD模擬展現了經過一定時長(80 000 ps)的動力學反應后,NaCl-HSA 水溶液體系和葡萄糖-HSA水溶液體系的氫鍵數、氫鍵壽命、體系分子或離子的相對空間位置及數量,同時驗證了兩種溶液體系介電特性變化的關系。Wang等[48]則運用MD模擬了肌球蛋白-庚醛體系(圖3B),并且分析了模擬體系中均方根偏差(RMSD)、均方根波動值(RMSF)、分子動力學/泊松-玻爾茲曼表面積(MM/PBSA)平均自由能、單個殘基對肌球蛋白-庚醛復合物結合自由能的貢獻;與試驗結果相互驗證后表明,疏水相互作用是醛類可逆結合的主要驅動力,有助于肌球蛋白-庚醛體系的穩定性。Wang等[48]的研究雖然不像Eremenko等[47]的研究涉及MH 條件或體現MH 特性,但卻從MD 模擬含蛋白質體系的方法入手,為研究者解釋了微觀物質及能量變化信息,這些RMSF、體系能量、自由能、氨基酸殘基等信息是傳統試驗數據無法獲取的。
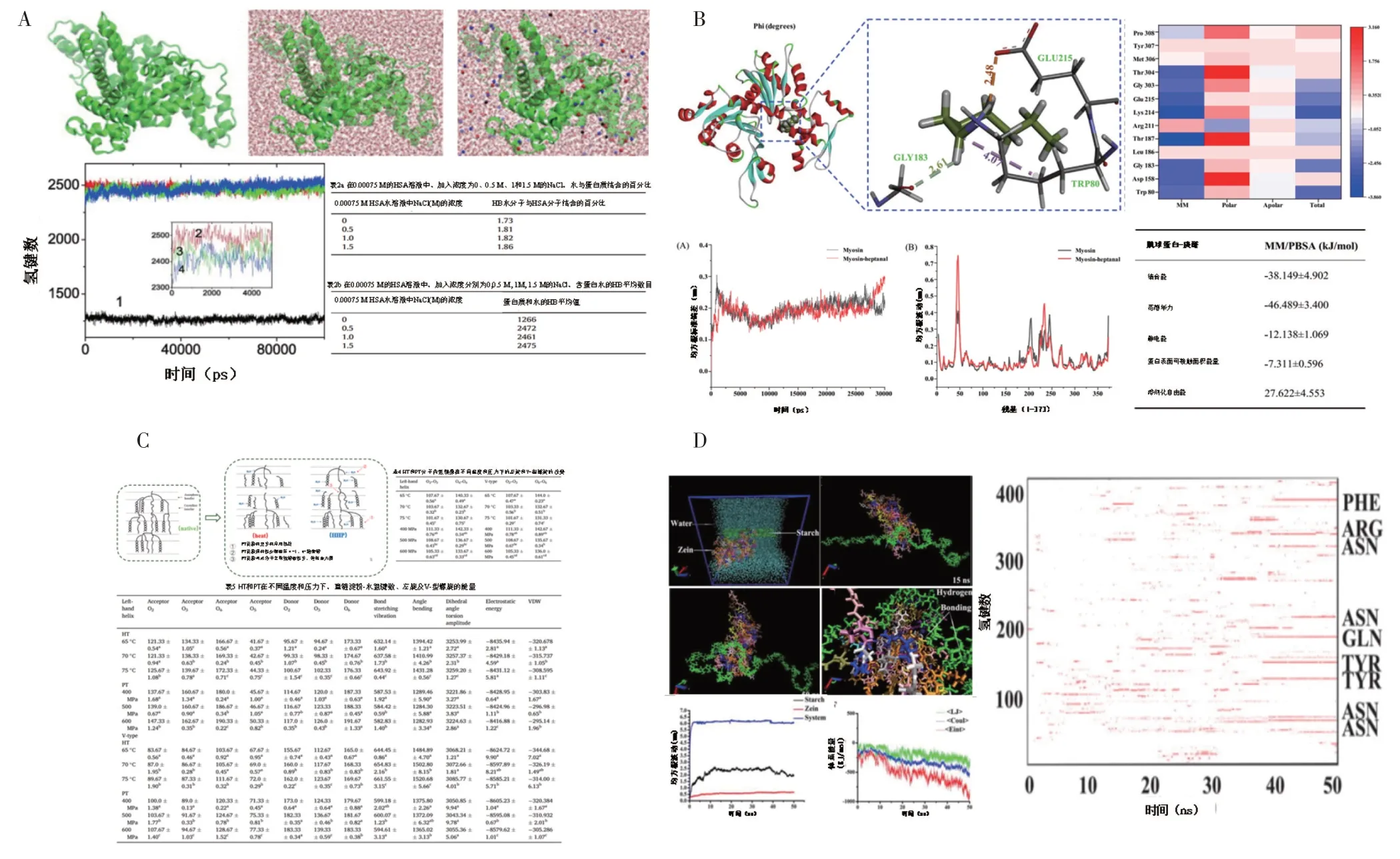
圖3 蛋白質、淀粉及蛋白質-淀粉體系MD模擬案例[47-48,51,55]Fig.3 The protein,starch and protein-starch system simulated using MD[47-48,51,55]
2.2 淀粉在微波場中的響應及MD模擬應用
微波可以直接或間接地誘發淀粉顆粒形態和內部結構的一系列變化,其與體系的介電特性和微波能量密度緊密相關。淀粉屬于高分子聚合物,在微波場環境中主要受到電子、原子、偶極和界面4 個極化分量中偶極極化的影響,MH不會引起官能團的產生與消失[49]。由于淀粉的長鏈分子結構和精致的空間結構,淀粉的極化現象并不明顯,使得淀粉的介電參數較低,但體系中混合水等極性分子后,淀粉基材料的介電特性會顯著變化[13]。淀粉材料的介電特性與其他特性的相關可用于預測體系中某成分的含量,如可溶性固形物含量的預測。Kubo 等[50]研究表明,可溶性固形物中糖的含量與其介電性能之間存在非線性關系。蔗糖、葡萄糖、果糖等糖溶液與其介電特性的關系也有相關報道:ε″隨溫度以二次方相加,而隨葡萄糖濃度線性降低,在較低溫度下,ε″隨濃度線性增加,達到一定濃度后降低,在高于40 ℃的溫度下,損耗因子在所研究的所有濃度范圍內隨濃度線性增加;而在水溶液中,單糖(D-果糖和D-木糖)和雙糖(D-麥芽糖-水合物)的混合物成分對ε″和弛豫時間影響顯著,同時通過分子間相互作用分析以及活化焓證實D-果糖的水溶液比D-木糖和D-麥芽糖的水溶液有更強的相互作用[13]。Liu 等[51]借助MD 技術對熱處理和壓力處理條件下的玉米淀粉分子結構進行了對比(圖3C)。MD 模擬提供的分子氫鍵和體系能量變化信息支持高靜水壓處理減少淀粉中固化水和提升水分子自由度的結論。通過可視化高靜水壓處理引發淀粉糊化過程中鍵合能量的變化數據,為淀粉研究提供了有益的參考。
2.3 蛋白質-淀粉薄膜在微波場中的響應及MD 模擬應用
將蛋白質和淀粉進行二元混合并通過相關條件制備成蛋白質-淀粉薄膜后,蛋白質-淀粉膜體系對微波場的響應不是蛋白質對MH 響應與淀粉對MH響應效果的疊加。在復雜的蛋白質與淀粉的締合或絡合過程中,鍵的生成和斷裂將蛋白質和淀粉的原子或分子進行了重新排列組合,在不考慮水等溶劑的影響下,微波場中蛋白質-淀粉薄膜的介電特性變化主要由薄膜中的偶極子密度和強度決定[52]。然而蛋白質-淀粉薄膜在完全無水時表現出極強的脆性且易碎裂,所以蛋白質-淀粉薄膜中需含有一定量的水。當薄膜中有水存在時,水本身具備較強的ε′和ε″,且可以促進蛋白質的溶解。此外,水的存在還會使薄膜材料中的極性基團(如淀粉中的-OH基團)或帶電粒子具有更強的流動性,進而增加單位空間內電荷載流子的數量和粒子間碰撞幾率,促進ε′和ε″值增大;蛋白質-淀粉薄膜的介電響應特征在考慮偶極子基礎上還需要考慮界面極化的影響[53-54]。
借助MD 模擬技術或許能將薄膜中的蛋白質和淀粉分子結構特征可視化,且通過牛頓運動方程、Lennard-Jones 勢函數及其他作用函數,薄膜中的偶極極化和界面極化機制也將得到更為直觀的解釋。Chen 等[55]在羥丙基淀粉-玉米醇溶蛋白雙層食用薄膜研究中成功應用了MD技術,如圖3D所示,其在模擬過程中發現初始時玉米醇溶蛋白只體現出聚集性的變化,螺旋狀的淀粉在水溶液中逐漸松弛并裂解,隨后淀粉和玉米醇溶蛋白發生了鍵合,在這個過程中氫鍵的作用促使淀粉和玉米醇溶蛋白的基團暴露于表面。Man 等[44]研究表明,在MH 中被顯著影響的淀粉基團是-OH,而蛋白質基團對應的可能是-NH2。因此,同樣可以借助MD 技術將蛋白質-淀粉薄膜的偶極極化和界面極化的信息進行可視化。
3 小結
蛋白質與淀粉具備形成結構更好的可食薄膜的潛力,近十年,二者的相關研究較多。可食膜對食品保鮮、抗機械損傷及提升食品加工性能非常重要,其研究涉及原子與分子層面動態變化的影響,為多學科交叉。食品在MH條件下,材料基的極性分子片段或極性大分子基團會受到微波的影響;然而原子及分子層面的微觀變化不僅速度極快,還無法被肉眼觀測到,嚴重阻礙了蛋白質-淀粉基薄膜材料的開發與應用。MD模擬將原子、分子可視化,且能提供氫鍵作用力、靜電作用力、范德華力、庫侖力及微觀化學鍵鍵能及其他信息,同時MD能清晰給出假設條件下的分子結構預測信息,為相關研究提供了新的技術途徑。

