2024年高考化學模擬試題A卷
高小艷 馮存良


一、選擇題:本題共7小題,每小題6分,共42分。在每小題給出的四個選項中,只有一項符合題目要求。
1.化學與生產、生活、科技及環境等密切相關。下列說法正確的是( )。
A.“天和”核心艙用到的鎂合金涂層中的自愈緩蝕劑2-巰基苯并噻唑(C7H5NS2),屬于有機高分子化合物
B.植物可以吸收利用空氣中的NOx 作為肥料,實現氮的固定
C.葡萄酒中通常添加有微量SO2,既可以殺菌,又可以防止營養成分被氧化
D.我國新一代長征七號運載火箭使用的是液氧煤油發動機,煤油主要由煤的干餾制得
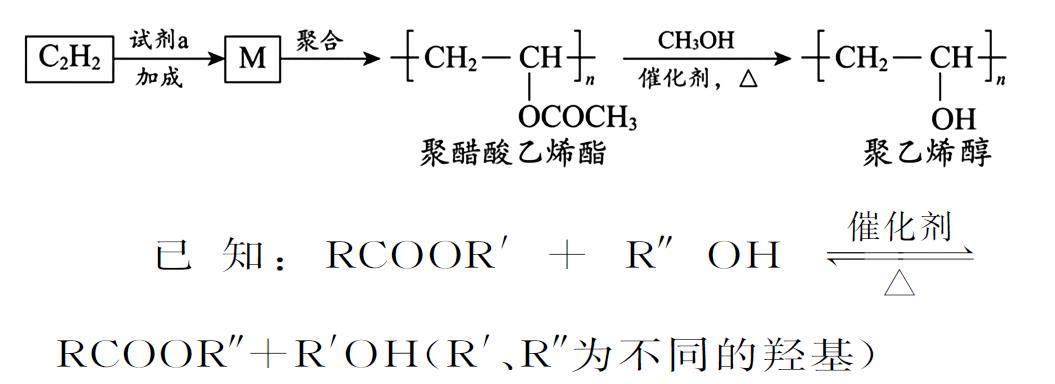
2.聚醋酸乙烯酯難溶于水,可用作白乳膠、塑料薄膜和涂料等,用它可得到聚乙烯醇,聚乙烯醇水溶液可用作醫用滴眼液。合成路線如下。
下列說法不正確的是( )。
A.試劑a是乙酸
B.通過增加甲醇用量可提高聚乙烯醇的產率
C.由M 轉化為聚醋酸乙烯酯的過程中發生了縮聚反應
D.由聚醋酸乙烯酯轉化為聚乙烯醇過程中還會生成乙酸甲酯
3.丁二酮肟常用于檢驗Ni2+ ,在稀氨水介質中,丁二酮肟與Ni2+ 反應可生成鮮紅色沉淀,其結構如下所示。下列說法不正確的是( )。
A.元素H、C、N、O、Ni電負性由大到小的順序為O>N>C>H>Ni
B.1 mol該沉淀含有σ鍵與π鍵的個數比為17∶2
C.基態Ni2+ 的價電子排布式為3d64s2
D.該沉淀中C的雜化方式為sp2、sp3
4.科學家近年發明了一種新型光電催化裝置,它能將葡萄糖和CO2 轉化為甲酸鹽,如圖1所示。光照時,光催化電極a產生電子(e- )和空穴(h+ ),圖中的雙極膜中間層中的H2O 會解離產生H+ 和OH- 。
下列說法錯誤的是( )。
①“沉渣”的主要成分除MnO2 外,還有_____。
②若加入過量的Na2S2O8,鈷元素會被氧化進入“沉渣”中,則溶液中殘留Co3+ 的濃度為_____mol·L-1。
(2)“沉鋅”時,在近中性條件下加入Na2CO3,可得堿式碳酸鋅[ZnCO3 ·2Zn(OH)2·H2O]固體,同時產生大量的氣體,試分析產生大量氣體的原因:_____。
(3)由堿式碳酸鋅生成氧化鋅的化學方程式為_____。
(4)沉鋅后的濾液經過一系列操作后得到的副產品為_____(填化學式)。
(5)ZnO 的晶胞結構如圖4,則鋅的配位數為_____;已知晶胞參數為a cm,該晶體的密度為_____g·cm-3(寫出計算式,阿伏加德羅常數的值為NA)。
9.(15分)科學探究要實事求是、嚴謹細致。某化學興趣小組設計實驗進行有關氯化物的探究,回答下列問題:
Ⅰ.制備FeCl2。裝置如圖5所示(夾持裝置省略),已知FeCl3 極易水解。
(1)儀器a的名稱是_____。
(2)裝置Ⅱ中制備FeCl2 的化學方程式為_____。
(3)該裝置存在的缺陷是:①_____;②缺少氫氣的尾氣處理裝置。
Ⅱ.利用惰性電極電解0.1 mol·L-1 FeCl2溶液,探究外界條件對電極反應(離子放電順序)的影響。
(4)實驗數據如表2所示。
①由實驗1、2現象可以得出結論:在溶液pH 相同時,增大電壓,_____優先于_____放電。
②由實驗1、4現象可以得出結論:_____。
Ⅲ.為了探究外界條件對氯化銨水解平衡的影響,某興趣小組設計了如表3所示實驗方案。
(5)該實驗限選藥品和儀器:恒溫水浴、pH 傳感器、燒杯、0.1 mol.L-1 硝酸銀溶液、蒸餾水和各種濃度的NH4Cl溶液。
①實驗中,“待測物理量”是_____。
②實驗目的A 是_____。
③上述表格中,b_____d(填“>”“<”或“=”)。
10.(14分)將CO2 轉化為更有價值的化工原料,正成為科學家們研究的一個重要領域。回答下列問題:
(1)已知:①2H2 (g)+ O2 (g)=2H2O(g) ΔH =- 484 kJ·mol-1
②2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) ΔH =-1 353 kJ·mol-1

