大概念視域下金屬與鹽溶液反應思維模型建構



摘要: 根據課程標準和教材,基于金屬與鹽溶液置換反應的本質提出“金屬為什么在性質上具有一定的相似性”的本原問題,認為其受“結構決定性質”的大概念所統攝。由金屬活動性順序衍生出的得失電子強弱順序以及電子得失過程構建的思維模型。結合中考試題分析,指出該思維模型能較好地揭示反應的本質,既可以作定性分析,還能進行半定量比較,幫助學生建立認識視角,形成思路和方法,促進大概念的認知進階。
關鍵詞: 金屬與鹽反應; 金屬活動性順序; 大概念教學; 思維模型; 化學教學研討
文章編號: 1005-6629(2024)07-0092-06 中圖分類號: G633.8 文獻標識碼: B
1 研究現狀及背景
金屬與鹽溶液反應是初中化學的重要內容,查閱資料發現,研究者多從不同角度探討解題策略和技巧,但一般僅涉及定性分析而沒有做定量比較,更沒有探討問題的化學本質,融入新課程理念的研究也比較少見。調查日常教學發現,大多數教師在應試壓力下以傳授具體解題方法為主,或就題論題沒有和前后教學內容或學段知識做結構化歸納梳理。可見目前的教學及評價仍停留在紙筆測試等應試層次,沒有上升到化學大觀念與高階科學思維。《義務教育化學課程標準(2022年版)》[1]提出大概念統領教學后,“金屬與鹽溶液反應”的教學和評價是否符合新課程理念?能否促進學生從具體知識學習轉到重視基本思路方法的形成?本文基于課程標準和教材,構建大概念視域下“金屬與鹽溶液反應”的思維模型,結合中考試題探討其學科本質和教學價值。
2 課程標準及教材分析
金屬與鹽溶液反應屬于課程標準中“物質的性質與應用”主題下“金屬與金屬礦物”主題的具體內容。課程標準相關描述有:通過實驗探究等活動認識常見金屬的主要化學性質及金屬活動性順序。了解廢棄金屬對環境的影響及金屬回收再利用的價值。了解物質的共性和差異性,認識一類物質性質的方法。從物質類別的視角,依據金屬活動性順序初步預測常見金屬的主要性質,解釋有關的實驗現象,進行證據推理,得出合理結論。能依據物質類別、金屬活動性順序等,預測、判斷與分析常見物質的性質及其轉化產物。可見金屬與鹽溶液的反應主要體現在金屬的化學性質及金屬活動性順序、判斷與分析轉化的產物等方面。
金屬與鹽溶液反應是義務教育人教版九年級《化學》(2012年版)下冊第八單元“金屬和金屬材料課”題2“金屬的化學性質”的內容,其標題是“金屬活動性順序”而不是“金屬與鹽溶液的反應”,說明該內容是學習了金屬與酸的反應以及置換反應后,為建立金屬活動性順序規律而進行的科學探究活動,弱化了以往傳統教學中以金屬化學性質知識邏輯為主的教學思路。在比較分析事實的基礎上,引導學生建構“金屬活動性”這一認識視角,并形成基于金屬活動性順序判斷金屬活動性的一般思路[2]。所以就標題的呈現上看,教材試圖從學科知識體系邏輯結構的完整性向促進學生認識視角的建立轉變,教育立場也從知識為本向素養為本發生轉變。
3 金屬活動性與大概念分析
金屬與鹽溶液反應是學生建構“金屬活動性”認識視角,建立金屬活動性順序,判斷金屬活動性的科學探究活動。理解好金屬活動性順序是建立金屬與鹽溶液反應模型的前提和條件。那么什么是金屬活動性,和活潑性有什么不同?通常情況下,物質的活潑性是指物質參加化學反應時表現的活潑程度[3]。金屬在氣態中失去電子的難易程度而表現的活潑性,通常就叫金屬的活潑性大小,如果是指金屬在水溶液中形成水合陽離子的趨勢,一般稱為金屬活動性[4]。金屬活動性順序是金屬在水溶液中的活潑性順序[5]。可見二者有區別又有聯系,適用條件和范圍并不相同,活潑性泛指各種物質,而活動性一般用來描述金屬在水溶液中的活潑性。金屬的活潑性與元素的原子結構有著密不可分的關系,原子失電子能力越強,金屬越活潑[6]。歷史上人們對“金屬活動性”的認識是不斷深化的,逐漸明晰金屬活動性反映的是金屬單質在水溶液里失電子形成水合離子傾向的大小,即反映金屬單質在水溶液里發生氧化反應的難易程度[7]。
鄭長龍指出,只有將大概念與認識視角有機結合,才能更為有效地解決化學問題[8]。課程標準中該學習主題大概念是“物質的多樣性”。凝練金屬與金屬礦物二級主題大概念是“同類物質在性質上具有一定的相似性”,以此統攝金屬的共性。金屬活動性順序既是金屬單質具有的一類共性又蘊含差異性,正是差異性導致(混合)金屬與(混合)鹽溶液反應變得復雜,反應順序、反應進程、產物成分隨反應條件的改變而改變。基于學科理解提出“金屬為什么在性質上具有一定的相似性”這一本原問題有助于誘發學生從微觀視角思考金屬與鹽溶液反應的本質,以及深度理解金屬活動性順序規律。因此該內容便串連起“物質的性質與應用”和“物質的組成與結構”兩大學習主題,將物質的宏觀性質和微觀結構建立起聯系,體現了跨學科主題的“結構決定性質”這一學科大概念。正如楊玉琴所述,課標的“一級大概念”一般是通過教材的多個單元“二級大概念”持續建構的,通過對不同物質的持續學習逐步建立起來的[9]。
“結構決定性質”大概念不僅是化學學科常見的學科觀點,而且還是跨學科、超學科的大概念,具有一定的哲學意義[10],貫穿整個化學課程。課程標準要求在教學中要注重學科主題大概念的抽提,引導學生建構大概念,發揮主題大概念對學生化學觀念形成和發展的獨特價值[11]。吳慶生認為根據教學內容存在的因果關系,采用能夠反映相互關系的表述作為大概念[12]。以此抽提“結構決定性質”大概念統攝的初中化學相關內容匯總見表1。
大概念學習是循序漸進的。吳星認為大概念并非是學習完本主題內容就能達到的最高水平,需要以前置單元學習為基礎、后置單元學習為補充,在整體課程中不斷學習加深理解[13]。由表1可知“結構決定性質”大概念的形成和建立不是一蹴而就的,是基于多種物質從原子結構、原子排列、微粒種類到分子結構不斷地完善的。
4 基于活動性和大概念建構思維模型
金屬與鹽溶液的反應是金屬活動性順序在工農業生產和科學研究的重要應用之一,是典型的置換反應,為何成為教學的重點與難點?究其原因可能是:金屬與鹽溶液反應體系物質多、反應多,物質關系影響反應進程、產物成分,且反應物、生成物均有固、液兩態,判斷某一階段濾渣、濾液成分時,需要綜合考慮反應順序與進程。現有文獻大多以圖形或表格羅列各種情況的物質組成,再根據現象一一比對。羅列既費時費力而且無法定量比較,本質上是運用數學思想的枚舉原理,枚舉的結果屬性易造成對產生原因的漠視,所以上述策略不能從根本上解決問題。建立科學思維模型除了必須理順反應順序、進程外,還需幫助學生形成化學觀念,發展科學思維。
基于此,建構思維模型既要考慮金屬因素,還要考慮鹽的因素。由表1知金屬活動性順序是“結構決定性質”大概念在金屬中的具體化,那么“結構決定性質”大概念在鹽溶液中的具體化是什么?我們知道,活動性強的金屬在溶液中易失去電子,活動性弱的金屬在溶液中難失去電子。因此金屬活動性順序便轉化為金屬單質在溶液里失電子能力的順序。反之,金屬離子得電子能力順序恰好和金屬單質失電子能力順序相反。“結構決定性質”大概念在鹽溶液中的具體化就是金屬離子得電子強弱順序。金屬與鹽溶液置換反應的本質是電子從失電子能力強的金屬單質轉移到得電子能力強的金屬離子。由此建立金屬與鹽溶液反應的認知思維模型(見圖1)。
該思維模型是由金屬失電子順序、離子得電子順序以及金屬和離子間得失電子過程構成的順時針環路。豎線位置高低表示反應先后順序,橫線箭頭長短表示電子得失強弱。反應過程中得失電子數守恒,元素種類不變,金屬轉化為離子成為溶質,離子轉化為金屬成為濾渣。濾渣、溶質產生的順序和離子、金屬得、失電子強弱的順序一致,故濾渣、溶質產生的先后順序見圖1。根據思維模型,最高位的金屬先失電子,最低位的離子先得電子,得失順序依強弱順序而改變。如反應至某一階段時,后產生的濾渣、溶質存在,則按順序易判斷之前的濾渣、溶質一定存在。若某反應恰好完全反應,則反應物一定消失、生成物一定存在;若不是恰好完全反應,需分別考慮金屬剩余或離子剩余,判斷剩余物能否滿足下個順時針環路,直到不能滿足環路反應結束為止。
5 運用模型解答金屬與鹽溶液反應舉例
5.1 利用模型解釋金屬與混合鹽溶液反應過程及物質組成
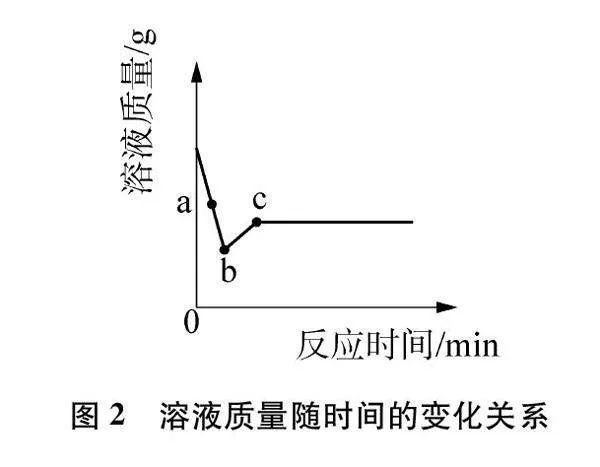
例1 競爭無處不在,微觀粒子之間的反應也是如此。將足量的Zn粉投入一定質量的AgNO3和Cu(NO3)2的混合溶液中發生反應,溶液的質量隨時間的變化關系見圖2。下列說法不正確的是( )
A. a點對應的溶液中含有三種金屬陽離子。
B. b點處的固體中含Ag和Zn。
C. 取少量b點處的溶液于試管中,滴加稀鹽酸會有沉淀出現。
D. 溶液先不變色,一段時間后由藍色逐漸變為無色。
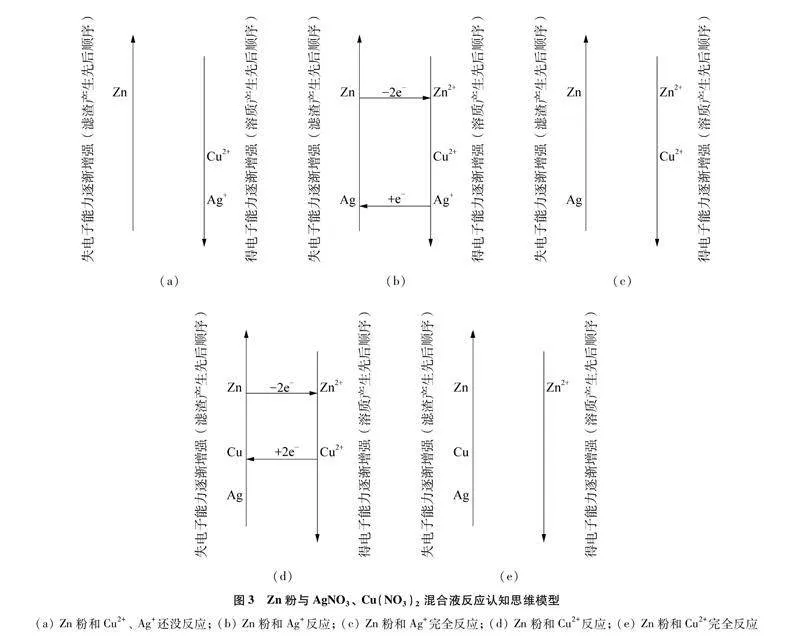
(1) 繪制思維模型,在相應位置標出Zn和Cu2+、 Ag+。見圖3(a)。
(2) 根據得失電子強弱標出電子得失情況,Zn失去2個電子形成Zn2+、 Ag+得到1個電子形成Ag,構成第一個順時針環路。見圖3(b)。書寫方程式Zn+2AgNO3Zn(NO3)2+2Ag。由于Zn粉足量,隨著反應進行至AgNO3完全反應,第一個置換反應結束,則Ag+不存在而Zn粉有剩余,生成的Zn2+、 Ag存在。見圖3(c)。
(3) 足量Zn粉和Cu2+構成第二個順時針環路。見圖3(d)。書寫方程式Zn+Cu(NO3)2Zn(NO3)2+Cu。隨著反應進行至Cu(NO3)2完全反應,第二個置換反應結束,則Cu2+不存在而Zn粉有剩余,生成的Zn2+、 Cu存在。見圖3(e)。
解答:由圖2中a點對應溶液質量減少知正在進行第一個置換反應,反應物生成物均存在,且Cu(NO3)2還沒參加反應。見圖3(b)。溶液中有三種陽離子,由溶質產生先后順序知其為Zn2+、 Cu2+、 Ag+。故A正確。折點b對應溶液質量最小,說明第一個置換反應結束第二個置換反應還沒開始。根據第一個順時針環路知,AgNO3完全反應則Ag+不存在,而Zn粉有剩余,生成的Zn2+、 Ag存在。見圖3(c)。b點處固體有Ag和Zn。故B正確。由于無Ag+,取少量b點處的溶液于試管中,滴加稀鹽酸沒有沉淀出現。故C不正確。隨著兩個置換反應依次結束,溶液中的Ag+、 Cu2+依次生成濾渣Ag、 Cu,溶液中只有Zn2+。見圖3(e)。由于Ag+、 Zn2+無色,Cu2+藍色,所以溶液先不變色,一段時間后由藍色逐漸變為無色。故D正確。實際運用思維模型時可在一張圖上進行,在相應物質上畫“√”表示存在,畫“×”表示不存在,更加直觀明了。
思維模型將復雜多變的置換反應細化成得失電子的環路模型,可清晰反映多步反應的先后順序、反應進程和產物成分。不同環路代表不同的置換反應,各步反應之間既有相同之處又有差異所在,既環環相扣又層層遞進。思維模型基于活動性和大概念指明解決問題的認識思路和實現路徑,幫助學生遷移知識,解決較復雜情境問題。
5.2 利用模型解釋金屬與鹽溶液不能反應的本質原因
例2 中國古代已掌握了銅冶煉和鑄造技術,現代銅冶煉廢氣、廢水需經過處理后排放。濕法煉銅產生酸性廢水,含有的CuSO4、 ZnSO4可用鐵炭混合物(鐵粉和活性炭的混合物)除去。其他條件不變,廢水pH對Cu2+、 Zn2+去除率的影響如圖4所示。
① pH<3時,鐵炭混合物表面有大量氣泡產生,產生該現象的化學方程式為____。
② 相同pH條件下,Cu2+的去除率遠高于Zn2+的原因可能是____。
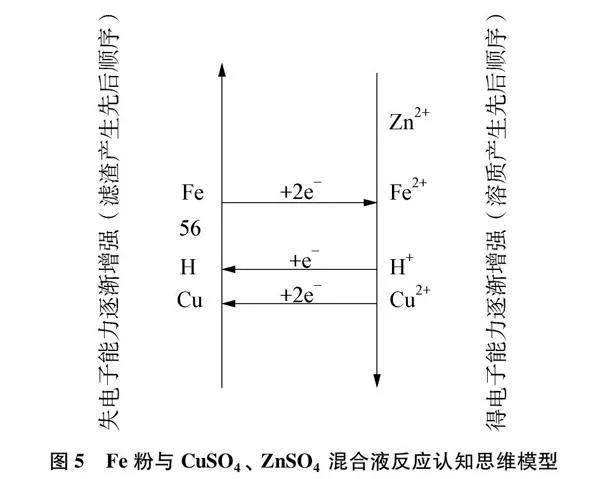
(1) 繪制思維模型,在相應位置標出Fe和Zn2+、 Cu2+。見圖5。
(2) pH<3時溶液呈酸性,在相應位置標出H+。金屬與酸反應先于金屬與鹽溶液。產生氣泡是Fe粉失電子形成Fe2+,H+得電子形成H再生成H2,化學方程式為Fe+H2SO4=FeSO4+H2↑。
(3) 相同pH條件下,即不考慮H+影響,Fe失電子形成Fe2+,而Cu2+得電子能力比Zn2+強,故Fe粉和Cu2+構成一個順時針環路而不能和Zn2+構成順時針環路,所以Fe粉不與ZnSO4反應。Cu2+的去除率遠高于Zn2+的原因可能是Fe能置換出Cu但不能置換出Zn,即宏觀上鐵的活動性比銅強而比鋅弱,微觀上Fe在溶液中失電子能力比Cu強而比Zn弱。
思維模型從金屬和離子得失電子能力入手,將宏觀物質和微觀粒子建立聯系。不僅能解釋發生置換反應的原因,還能從本質上解釋不能發生反應的原因。可引導學生辯證地看待置換反應實質,從死記硬背事實性知識到形成認識視角和分析反應過程。所以思維模型不是具體知識經驗總結,而是體現學科大概念“結構決定性質”的抽象概括,具有遷移性和本原性。
5.3 利用模型半定量解釋混合金屬與鹽溶液反應
例3 向硝酸銀溶液加入一定質量的鋅粉和銅粉的混合物,充分反應后過濾,得到濾渣和濾液。以下推斷正確的是( )
A. 若向濾渣中加入稀鹽酸有氣泡產生,則濾渣中一定有銀、銅、鋅。
B. 若濾液為無色,則濾渣中一定有鋅。
C. 若濾液為藍色,則濾液中一定有硝酸銀、硝酸銅和硝酸鋅。
D. 濾渣的質量可能比反應前鋅粉和銅粉混合物質量小。
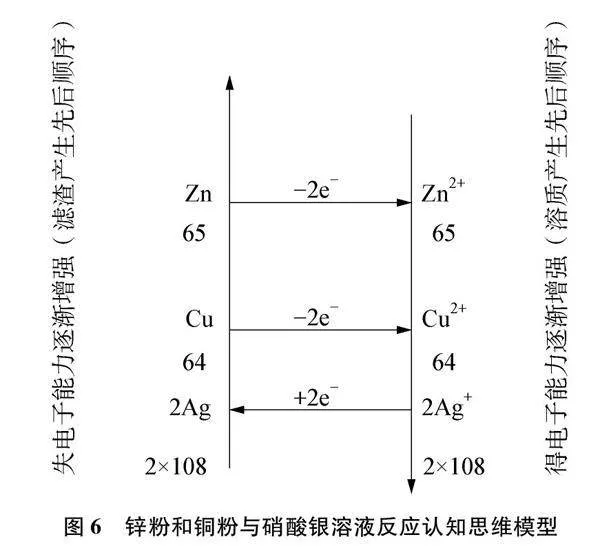
(1) 繪制思維模型,在相應位置標出Zn、 Cu和Ag+。見圖6。
(2) 根據得失電子強弱標出電子得失情況,Zn失去2個電子形成Zn2+、 2Ag+得到2個電子形成2Ag,構成一個順時針環路。書寫方程式Zn+2AgNO3Zn(NO3)2+2Ag。如果Ag+過量還會和Cu構成第二個順時針環路。書寫方程式Cu+2AgNO3 Cu(NO3)2+2Ag。標出Zn、 Cu和2Ag的相對原子質量。
解答:若向濾渣中加入稀鹽酸有氣泡產生,則濾渣中一定有活潑金屬鋅。說明只進行第一個置換反應且鋅粉有剩余。根據濾渣產生順序,還一定有銀、銅。故A正確。若濾液為無色,則溶質一定無Cu2+,說明還沒有發生第二個置換反應,根據溶質產生順序,溶質一定有Zn2+無Ag+。但第一個置換反應是否恰好完全反應卻無法判斷,即鋅粉可能有剩余,也可能恰好完全反應。故B不正確。若濾液為藍色,則溶質一定有Cu2+,說明第二個置換反應已經發生,根據溶質產生順序,溶質一定有Zn2+、 Cu2+。同樣第二個置換反應是否恰好完全反應也無法判斷,即銅粉可能有剩余,Ag+也可能有剩余,所以是否有硝酸銀無法判斷。故C不正確。根據得失電子數守恒,無論反應進程如何,都存在Zn或Cu置換2Ag的微觀過程,而Zn、 Cu相對原子質量65、 64都小于2Ag的相對原子質量216。即反應后濾渣的質量一定大于原鋅粉和銅粉混合物的質量。故D不正確。
思維模型將物質成分按濾渣、溶質分別依次呈現,直觀清晰,可以定性預測、判斷與分析不同階段的轉化產物,還能基于電子守恒半定量比較各成分的質量變化。凸顯思維可視AEWx9wFN+UUSC4fJ7BxRmA==化,幫助學生理順每一步反應,有助于學生從定性定量認識角度、深層次理解金屬和鹽溶液的反應,培養深刻、靈活、系統的思維品質。
6 結語
綜上所述,金屬與鹽溶液反應的思維模型是基于“金屬活動性”認識視角和“結構決定性質”大概念建立的,能較好地揭示置換反應的微觀本質,體現反應順序、反應進程和產物成分。其特點是將金屬活動性順序衍生為金屬和離子得失電子強弱順序,形式上從一維線型抽象規律轉化為二維平面環狀遞進圖形,內容上將濾渣、溶質的產生順序與得失電子的順序有機融合,認識方式上將宏觀和微觀建立對應聯系,進一步理順和豐富金屬活動性順序的內涵。幫助學生認識金屬參加置換反應失電子的共性,又能激發學生深度理解微觀粒子決定宏觀性質的化學觀念,發展比較、分類、推理、預測等科學思維。
參考文獻:
[1]中華人民共和國教育部制定. 義務教育化學課程標準(2022版)[S]. 北京: 北京師范大學出版社, 2022.
[2][8][11]鄭長龍. 核心素養導向的化學教學——義務教育化學教學改革的新方向[J]. 課程·教材·教法, 2022, 42, (9): 41~46.
[3][6]何盼, 錢勝, 高明哲等. 單質活潑性與鍵能的關系初探[J]. 化學教育, 2013, 34(12): 86~87, 91.
[4]金嗣安. 金屬的活潑性與活動性[J]. 安徽教育, 1982, (12): 46~32.
[5]魯梅. 金屬的電極電位、電離勢和活動順序[J]. 化學通報, 1978, (4): 46~48, 11.
[7]喬國才. 金屬活動性順序的變遷研究——從人教版《義務教育教科書·化學》(九年級下冊)修訂談起[J]. 中學化學教學參考, 2013, (4): 48~51.
[9]楊玉琴, 陸海燕, 呂榮冠. 學科大概念: 從課標到教材到教學的轉化——基于《義務教育化學課程標準(2022年版)》的分析[J]. 化學教學, 2022, (10): 3~9.
[10][12]吳慶生. 淺析化學大概念的凝練與建構[J]. 化學教學, 2021, (11): 37~40.
[13]吳星. 以大概念統領設計義務教育化學課程內容——《義務教育化學課程標準(2022年版)》解讀(二)[J]. 化學教學, 2022, (11): 3~8.
(無錫市教育科學“十三五”規劃2020年度立項課題“教育解釋學視閾下初中化學課程前期啟蒙行動研究”(課題編號:C/D/2020/05)的研究成果。)

