Cu0/Cu2+修飾Ti3C2Tx二維材料用于電催化還原二氧化碳


摘要以Ti3AlC2 和CuCl2·2H2O 為前驅體,成功制備了Cu0 納米顆粒修飾和Cu2+自插層的手風琴狀二維催化劑Cu0/Cu2+-Ti3C2Tx,用于電催化還原CO2。對材料的電化學性能進行了測試,結果表明,在CO2 飽和的0.5 mol/L KHCO3 電解液中,與原始的Ti3AlC2 相比, Cu2+/Cu0-Ti3C2Tx 催化劑電催化CO2 轉化為乙烯(C2H4)的起始電位從?0.65 V(vs RHE)降至?0.01 V(vs RHE),最大電流密度從0.19 mA/cm2 增至2.50 mA/cm2, Tafel 斜率從181 mV/dec 減至32 mV/dec,雙電層電容(Cdl)值從2.61 mF/cm2 增至55.06 mF/cm2,表現出更高的催化活性和更快的電子轉移速度(電荷轉移電阻(Rct)值僅為16.9 Ω),并且具有更大的電化學活性面積和極佳的穩定性。這為今后設計和制備CO2 的電催化還原反應(ECR)催化劑提供了一種有前景的方法。
關鍵詞銅;鈦碳化鋁;插層;電催化;二氧化碳;乙烯
近年來,化石燃料的大規模使用導致CO2 大量排放,造成了大氣污染、溫室效應和冰川融化等多種環境問題[1]。如何利用可再生能源將CO2 氣體還原為燃料和化工原料,以實現可持續碳循環,已成為當今的研究熱點[2],而CO2 電還原反應(CO2RR)作為一種高效的新型轉換方式[3],可將CO2 轉化為甲醇、甲烷和乙烯等。這些化合物可作為燃料或化學品原料,從而減少對化石燃料的依賴及CO2 的排放量,緩解上述環境問題。在CO2RR 過程中, CO2 分子首先被還原為CO, CO 再被進一步還原為一系列的有機化合物,可以通過選擇不同的反應條件和催化劑控制這些化合物的產率和選擇性[4]。隨著技術的不斷進步,許多催化劑相繼被開發出來。目前,金屬基電催化劑(如Au、Ag 和Cu 基電極)[5]、分子催化劑[6]和單原子催化劑[7]在CO2RR 過程中表現出很好的活性,可以催化CO2 生成CO、CH4、CH3OH、C2H4 和C2H5OH 等多種化合物[8-9]。但是, CO2RR 還存在很多缺陷,如惰性CO2 的激活能量大[10]、多電子轉移過程和競爭性析氫反應(HER)導致產物選擇性差[4]以及電極材料穩定性差[11]等,尚不能滿足工業化應用的要求。合理設計和開發穩定高效的電催化劑以克服這些缺陷是目前迫切需要解決的問題。
二維過渡金屬碳化物、氮化物和碳氮化物也稱Mxenes[12],由于具有可調節的結構和豐富的表面化學性質,已成為一種應用廣泛的潛在二維材料[13]。2007 年, Geim 等[14]發現,單層石墨烯相對于多層石墨烯而言,具有更大的比表面積和更多的活性位點。因此,對二維材料進行插層可使其具有更優越的性能。2014 年, Halim 等[15]使用氟化銨鹽作為插層劑合成了Ti3C2Tx(Mxene)。Bao 等[16]采用Li+插層的方法制備了孤立單原子位點Ti3C2Tx 材料,用于將CO2 高效還原為乙烯。該方法對乙烯的選擇性達到98%,與可逆氫電極相比,在?0.7 V 下,對乙烯的最大法拉第效率達到69.7%。隨后, Huang 研究組[17]報道了一種層狀碳化物(MAX 相)及其二維衍生物(Mxene)的插層方法,用金屬去除Mxenes 中的末端,然后將原子插入二維碳化物納米片,從而重建MAX 相和一系列金屬插入的二維碳化物。此外,還有研究者通過引入二甲基亞砜(DMSO)、異丙胺(C3H9N)、四甲基氫氧化銨(TBAOH)和氟化銨(NH4F)等有機試劑或鹽作為插層劑[18]。通過插層,可改變電子能帶結構[19],有效提高電導率,進而改變電荷波密度和各向異性[20];或者引發自發磁化和超導性等效應[21],降低材料的Rct 值[22]。
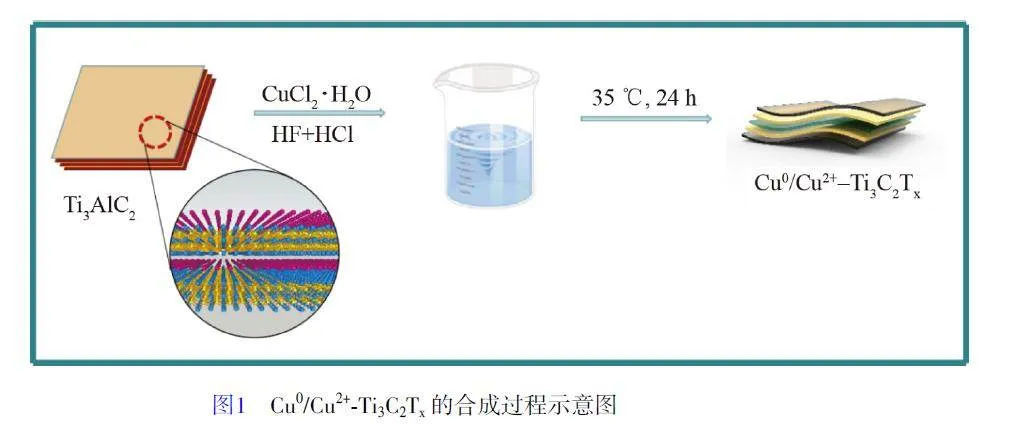
本研究采用一步合成法制備了Cu0/Cu2+-Ti3C2Tx 復合材料,圖1 為Cu0/Cu2+-Ti3C2Tx 材料合成過程示意圖。與使用Li+或其它插層劑相比,本研究以CuCl2·2H2O 為前驅體合成了Cu0/Cu2+-Ti3C2Tx 材料。此材料以Cu0 作為敏化劑/修飾劑, Cu2+作為插層劑,具有極低的過電位、更大的比表面積、更強的導電性以及更多的反應活性位點等優點,可用于電催化還原CO2 為乙烯。本合成方法未使用有機大分子插層劑,合成過程簡單且環保。
1 實驗部分
1 實驗部分
Admiral Squidstat Plus 1554 型電化學工作站和Agilent Technologies 7890A 型氣相色譜檢測器(美國Agilent 公司);SU-8020 場發射掃描電子顯微鏡(FE-SEM,德國Zeiss 公司,加速電壓為10 kV);JEM2100F 型透射電子顯微鏡(TEM,日本JEOL 公司,加速電壓為200 kV);DX-2700 型X 射線衍射儀(XRD,德國Bruker 公司, Cu-Kα輻射,波長為0.15418 nm, 加速電壓和加速電流分別為45 kV 和40 mA, 掃描范圍為2θ=20°~80°,掃描速率為2o/min);ESCALAB 250Xi 型X 射線光電子能譜儀(XPS,美國ThermoScientific 公司);DZF-6020 型真空干燥箱(上海精宏設備公司);S10-2 型恒溫磁力攪拌器(上海司樂儀器公司);H3-18K 臺式高速離心機(可成儀器設備有限公司)。
鈦碳化鋁(Ti3AlC2, 98%, 200 目(孔徑125 μm), 上海阿拉丁生化科技股份有限公司);HCl(37%)、HF(≥40%)和CuCl2·2H2O(分析純,上海阿拉丁生化科技股份有限公司)。實驗用水為超純去離子水(18.2 MΩ·cm)。
1.2 樣品的制備
依據文獻[16]的方法制備Cu0/Cu2+-Ti3C2Tx 催化劑。稱取0.425 g CuCl2·2H2O 于50 mL 燒杯中,準確加入50 mL 去離子水,超聲10 min, 配制成0.05 mol/L CuCl2 溶液,備用。在編號1、2、3、4的50 mL聚四氟乙烯燒杯中均加入6 mL去離子水、4 mL HCl、8 mL HF。稱取4份0.10 g Ti3AlC2 分別加入到燒杯中,用移液槍移取CuCl2 溶液1.2、1.4、1.5 和1.6 mL 分別加入到上述編號的燒杯中,對應的Cu 加入量分別為6×10?5、7×10?5、7.5×10?5 和8×10?5 mol,將4 個燒杯置于磁力攪拌器上于35 ℃恒溫攪拌24 h。反應結束后,棄去上清液,沉淀物用超純水洗滌離心,用酸堿指示劑檢測洗滌液pH值直至pH=7。收集沉淀物,置于真空干燥箱中,于80 ℃干燥6 h。上述制備好的樣品分別標記為Cu0/Cu2+-Ti3C2Tx-6、Cu0/Cu2+-Ti3C2Tx-7、Cu0/Cu2+-Ti3C2Tx-7.5 和Cu0/Cu2+-Ti3C2Tx-8。
1.3 工作電極的制備及電催化CO2性能測試
將4 mg Cu0/Cu2+-Ti3C2Tx-7.5 樣品分散于1 mL 無水乙醇-水(1∶4, V/V)中,加入80 μL Nafion 溶液,超聲處理30 min, 形成均勻的電極漿料。用微量進樣器量取5 μL 電極漿料,均勻地滴涂在玻碳電極(GCE,電極直徑為0.3 cm,天津艾達恒晟科技公司)表面,涂抹面積為0.07065 cm2。將涂抹后的GCE 先置于空氣中晾干定形30 min, 再置于干燥箱中80 ℃烘干2 h。
采用電化學工作站測試CO2RR 的性能。以鉑絲電極為對電極,飽和甘汞電極為參比電極,上述制備的修飾GCE 為工作電極。電解池選用典型的H 型電解池,將超純水洗過的質子交換膜(Nafion 117)放入兩電解室中,確保僅可通過H+。以0.5 mol/L KHCO3 溶液為電解液,并確保兩個電解室中的電解液液面保持水平。每次測試前,先用CO2 氣體鼓泡30 min,測試時CO2 氣體連續進入陰極室,用轉子流量計控制CO2 氣體的流速為15 cm3/min。采用氣相色譜測定氣相產物的含量。
2 結果與討論
2.1 形貌與結構
Cu0/Cu2+-Ti3C2Tx-6、Cu0/Cu2+-Ti3C2Tx-7、Cu0/Cu2+-Ti3C2Tx-7.5 和Cu0/Cu2+-Ti3C2Tx-8 的SEM 圖如圖2 所示。未經剝離和插層的原始Ti3AlC2 為封閉結構的立方塊碳化物(圖2A 插圖)。隨著銅加入量的增加,Ti3C2Tx 的層狀結構逐漸明顯,由多層片狀結構向更薄的單層片狀結構過渡,層與層之間緊密連接,表明Cu2+具有一定的插層作用。當銅加入量增大到8×10?5 mol 即合成材料Cu0/Cu2+-Ti3C2Tx-8 時,從圖2D 中可見在Ti3C2Tx 上有納米顆粒,這是由于HF 具有強還原性,將CuCl2 溶液中的Cu2+還原為Cu0。塊狀材料經過Cu2+插層后,具有類似手風琴狀的多層結構,使得材料具有更大的比表面積,這對Cu 納米顆粒的分散和CO2 電還原反應(ECR)過程中有效的質量傳輸具有十分重要的作用[23]。
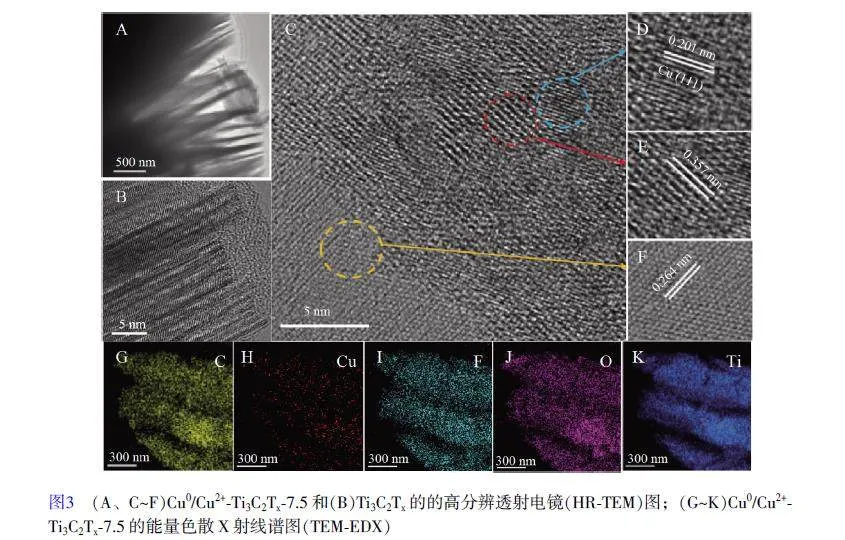
圖3 為合成的Cu0/Cu2+-Ti3C2Tx-7.5 的高分辨透射電鏡(HR-TEM)圖和能量色散X 射線譜圖(TEMEDX)。由圖3A 可以進一步確認Cu2+插層后的Cu0/Cu2+-Ti3C2Tx-7.5 材料具有手風琴狀的層狀結構,與SEM 的結果一致,再次證明Cu2+具有插層作用。圖3B 為Ti3C2Tx 的HR-TEM 圖像, Ti3C2Tx 的晶格清晰,說明材料的結晶度很高[ 24]。圖3C 為Cu/Ti3C2Tx-7.5 的HR-TEM 圖,圖3D~3F 分別為指定區域的HR-TEM 圖。由圖3D 清晰可見0.201 nm 的晶格條紋,對應于Cu 的(111)晶面;由圖3F 可見0.264 nm晶格條紋,對應于Ti3C2Tx 的(110)晶面;而圖3E 中的晶格條紋為0.357 nm, 相對于Ti3C2Tx 的(110)晶面的晶格條紋(0.264 nm)明顯增大,這是由于Cu2+的插層作用所致[25],與之前的結論一致。圖3G~3K 為Cu/Ti3C2Tx-7.5 的TEM-EDX,由圖中可見元素C、Cu、F、O 和Ti 均勻分布,再一次證實了復合材料Cu/Ti3C2Tx-7.5 的成功制備。
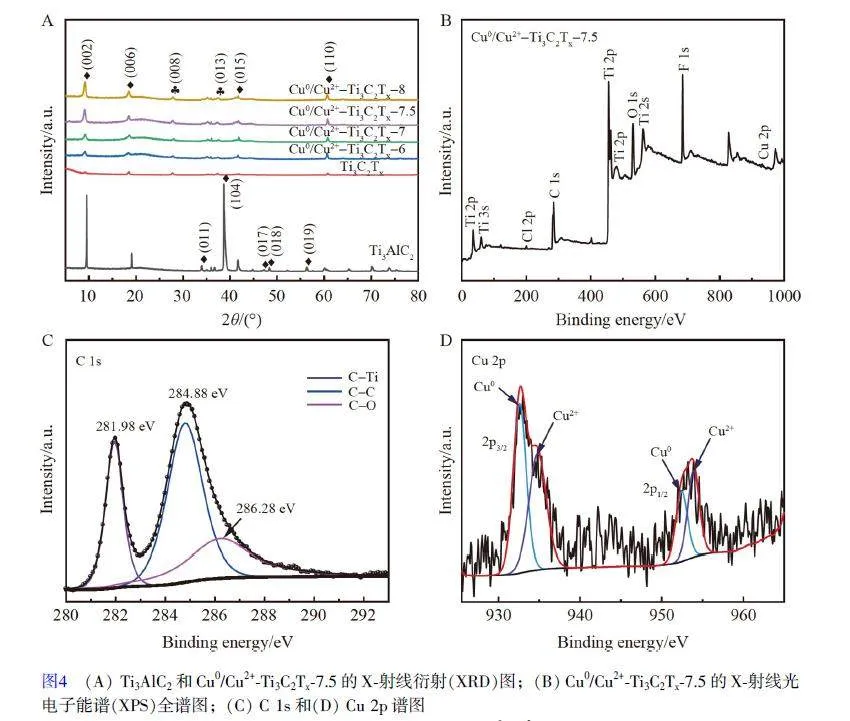
Ti3AlC2 和加入不同質量銅的Cu0/Cu2+-Ti3C2Tx 的XRD 譜圖如圖4A 所示,在2θ為9.6°、19.1°、38.7°和41.7°處的衍射峰分別對應Ti3AlC2 的(002)、(006)、(104)和(015)晶面[13]。在Cu0/Cu2+-Ti3C2Tx 的XRD譜圖中,存在Ti3AlC2 的(002)和(006)主要特征峰但有所減弱[26],而主峰(002)從9.6o移至8.9o,這是由于經HF 蝕刻后去除了Ti3AlC2 中的Al 以及Ti3C2Tx 中表面末端Tx 的引入(例如,—F,—O,—OH 等)[27]。Cu0/Cu2+-Ti3C2Tx 的XRD 譜圖中除了Ti3AlC2 的(002)、(006)、(015)和(110)峰以外,其它與Ti3AlC2 相關的峰都基本消失,而(008)和(013)是Ti3C2Tx 的特征峰。在Cu0/Cu2+-Ti3C2Tx-6、Cu0/Cu2+-Ti3C2Tx-7、Cu0/Cu2+-Ti3C2Tx-7.5 和Cu0/Cu2+-Ti3C2Tx 的XRD 譜圖中均未顯示銅的峰,這是由于銅的加入量過少。
為了進一步確定Cu0/Cu2+-Ti3C2Tx-7.5 的化學組成和元素的化學狀態,進一步通過XPS 分析Cu0/Cu2+-Ti3C2Tx-7.5 的表面化學成分。由圖4B 的全譜可知, Cu0/Cu2+-Ti3C2Tx-7.5 中含有Ti、Cl、C、O、F 和Cu元素,其中, Cl 和F 元素是由于加入HCl 和HF 所引入。Cu0/Cu2+-Ti3C2Tx-7.5 的高分辨XPS 譜圖如圖4C和4D 所示。在C 1s XPS 譜圖(圖4C)中, 281.98、284.88 和286.28 eV 處的峰分別歸屬于C—Ti、C—C和C—O 基團[28]。在Cu 2p XPS 譜圖(圖4D)中, 932.4 和952.2 eV 處的峰為Cu0 的特征峰,分別歸屬于Cu 2p3/2 和Cu 2p1/2 軌道,在934.4 和954.2 eV 處的兩個峰分別歸屬于Cu2+的特征峰。上述XPS 結果表明在材料Cu0/Cu2+-Ti3C2Tx-7.5 中Cu 主要以Cu0 和Cu2+的形式存在,與文獻[29]的報道一致。
2.2 Cu0/ Cu2+-Ti3C2Tx的電化學性能分析
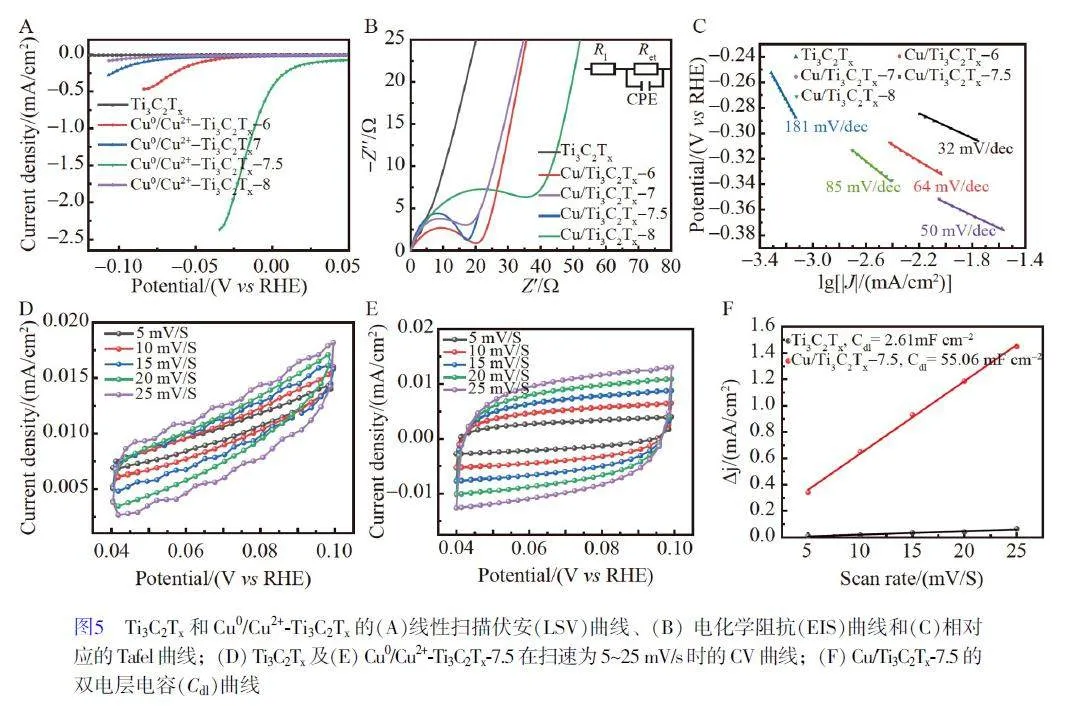
采用常規的三電極體系,在氣密雙室典型的H 型電解池中對Ti3C2Tx 和Cu0/Cu2+-Ti3C2Tx 的電催化性能進行研究。首先采用用線性掃描伏安法(LSV)對材料進行測試,結果如圖5A 所示,隨著電位降低,Ti3C2Tx 的電流密度無明顯變化。通過Cu0 修飾和Cu2+插層的Ti3C2Tx 的極化曲線的起始電位減小,說明Cu2+插層可提高CO2RR 性能,其中, Cu0/Cu2+-Ti3C2Tx-7.5 極化曲線的起始電位最小,當電位增至?0.01 V(vs RHE)時,隨著電位降低,電流開始呈線性增加。但是,當銅的加入量達到8×10?5 mol 即合成材料Cu0/Cu2+-Ti3C2Tx-8 時,其過電位反而增大,這是由于增大銅的加入量使銅在材料表面團聚形成銅團簇。其中各材料的過電位順序為Cu0/Cu2+-Ti3C2Tx-7.5(–0.01 V)Cu0/Cu2+-Ti3C2Tx-6(0.47 mA/cm2)gt;Cu0/Cu2+-Ti3C2Tx-7(0.28 mA/cm2)gt;Cu0/Cu2+-Ti3C2Tx-8(0.19 mA/cm2)gt;Ti3C2Tx(0.08 mA/cm2)。Ti3C2Tx(MXene)的作用是為銅提供一個載體, Cu2+插層可增加Ti3C2Tx 的電化學活性位點并改變其電子結構,引起電導率和載流子密度增加,從而降低電荷轉移的電阻。
為了評估ECR 過程中的電子轉移動力學,在?0.35 V(vs RHE)下進行了電化學阻抗(EIS)測試。圖5B 為樣品的Nyquist 圖,采用帶電荷轉移電阻(Rct)的等效Randles 電路擬合。模型中的電路原件R1 表示溶液的電阻, CPE 表示恒定電位原件, Rct 表示電化學反應電荷轉移電阻。催化劑/電解質界面的電催化動力學決定了Rct, Rct 值越小,表明電子轉移速率越快[30]。如圖5B 所示,經過Cu0 修飾和Cu2+插層的Ti3C2Tx 的Rct 值明顯小于Ti3C2Tx 的Rct 值,而且Cu0/Cu2+-Ti3C2Tx-7.5(Rct=16.9 Ω)
通過對樣品的極化曲線進行分析,得到了各樣品的Tafel 斜率。根據Tafel 方程(η=a+blg| j|,η為過電位, j 為電流密度, b 為Tafel 斜率), b 越小,預示著CO2 還原反應速率越高,并具有良好的催化反應動力學性能。如圖5C 所示, Ti3C2Tx 的b=181 mV/dec,明顯小于Cu0 修飾和Cu2+插層的Ti3C2Tx。Cu0/Cu2+-Ti3C2Tx-7.5(b=32 mV/dec)
有效的電化學活性面積(AECS)也是衡量催化劑性能的一個重要參數,可通過雙電層電容(Cdl)值進行評估,其中AECS 值與Cdl 值成正比。Ti3C2Tx 及Cu0/Cu2+-Ti3C2Tx 分別在掃描速率為5、10、15、20 和25 mV/s 時,在非法拉第電容電流范圍內的CV 曲線如圖5D 和5E 所示,根據CV 曲線中0.07 V(vs RHE)處的電流差值(Δj)計算Cdl 值。電流密度差值與掃速之間的線性關系如圖5F 所示,通過計算得到Cu0/Cu2+-Ti3C2Tx-7.5 的Cdl=55.06 mF/cm2, Ti3C2Tx 的Cdl=2.61 mF/cm2,說明Cu0/Cu2+-Ti3C2Tx-7.5 的AECS 遠大于Ti3C2Tx。
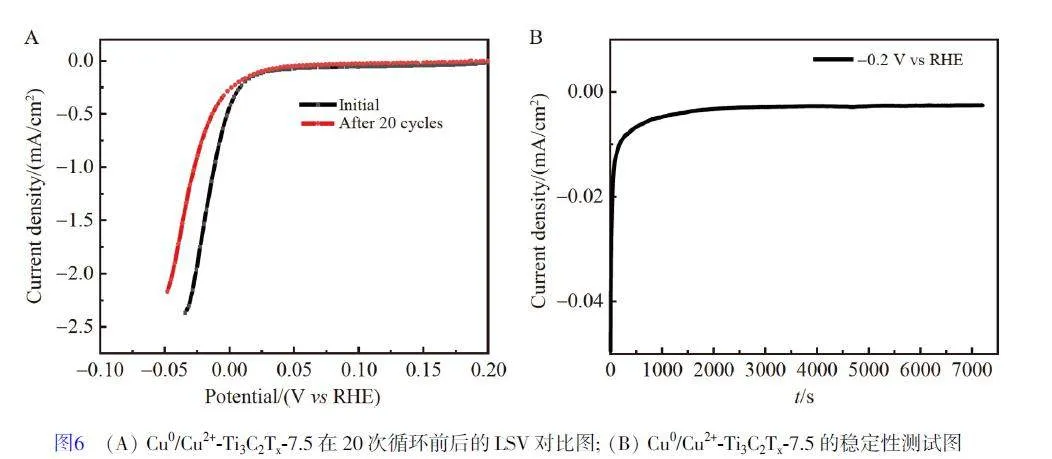
除了高活性外,穩定性也是衡量催化劑性能的一個重要參數,為了考察Cu0/Cu2+-Ti3C2Tx-7.5 在電解質溶液中的穩定性,在偏置電壓為?0.2 V(vs RHE)時測量了陰極電流密度(圖6A),在進行20 個循環周期前后, Cu0/Cu2+-Ti3C2Tx-7.5 電極的極化曲線基本上保持一致。電極連續運行7200 s 后的測試結果如圖6B所示,其電流密度無明顯變化。上述結果表明Cu0/Cu2+-Ti3C2Tx-7.5 的穩定性良好。
雖然此催化劑具有極低的過電位、較大的比表面積、更小的電荷轉移電阻和更大的有效電化學活性面積,但法拉第效率僅為0.16%(詳見電子版文后支持信息),這是由于此材料對乙烯的選擇性不高及存在競爭性析氫反應所致,這也將是后續工作改進的重點。
3 結論
采用一步合成法制備了Cu0 修飾和Cu2+插層的手風琴狀二維催化劑Cu0/Cu2+-Ti3C2Tx,此催化劑具有極低的過電位、較大的比表面積、更小的電荷轉移電阻和更大的有效電化學活性面積,在0.5 mol/L KHCO3電解液中表現出對CO2 的ECR活性。電催化性能測試結果表明,與原始的Ti3C2Tx 相比, Cu0/Cu2+-Ti3C2Tx-7.5的起始電位從0.65 V(vs RHE)降至?0.01 V(vs RHE),接近于標準氫電極電位,這有利于減少電還原過程的能耗。本合成方法未采用有機大分子插層劑,合成過程簡單且環保,為開發電催化CO2 還原制取乙烯的電催化劑提供了新思路。
References
[1] ZOU X, ZHANG Y. Chem. Soc. Rev. , 2015, 44(15): 5148-5180.
[2] CHEN S, ZHANG Z, JIANG W, ZHANG S, ZHU J, WANG L, OU H, ZAMAN S, TAN L, ZHU P, ZHANG E, JIANG P, SU Y, WANG D, LI Y. J. Am. Chem. Soc. , 2022, 144(28): 12807-12815.
[3] ZHANG X, ZHANG Z, LI H, GAO R, XIAO M, ZHU J, FENG M, CHEN Z. Adv. Energy Mater. , 2022, 12(39): 2201461.[4] ZHU Q, DENG Z, XIE H, XING M, ZHANG J. ACS Catal. , 2023, 13(5): 3254-3262.
[5] ZHU J, XIA L, YU R, LU R, LI J, HE R, WU Y, ZHANG W, HONG X, CHEN W, ZHAO Y, ZHOU L, MAI L, WANG Z.J. Am. Chem. Soc. , 2022, 144(34): 15529-15538.
[6] CHEN P, ZHANG P, KANG X, ZHENG L, MO G, WU R, TAI J, HAN B. J. Am. Chem. Soc. , 2022, 144(32): 14769-14777.
[7] ZHAO Y, ZU X, CHEN R, LI X, JIANG Y, WANG Z, WANG S, WU Y, SUN Y, XIE Y. J. Am. Chem. Soc. , 2022, 144(23):10446-10454.
[8] HEENEN H H, SHIN H, KASTLUNGER G, OVERA S, GAUTHIER J A, JIAO F, CHAN K. Energy Environ. Sci. , 2022,15(9): 3978-3990.
[9] ZHU H L, CHEN H Y, HAN Y X, ZHAO Z H, LIAO P Q, CHEN X M. J. Am. Chem. Soc. , 2022, 144(29): 13319-13326.
[10] WANG P, QIAO M, SHAO Q, PI Y, ZHU X, LI Y, HUANG X. Nat. Commun. , 2018, 9(1): 4933.
[11] NGUYEN T N, CHEN Z, ZERAATI A S, SHIRAN H S, SADAF S M, KIBRIA M G, SARGENT E H, DINH C T. J. Am.Chem. Soc. , 2022, 144(29): 13254-13265.
[12] CAO Q, GROTE F, HUΒMANN M, EIGLER S. Nanoscale Adv. , 2021, 3(4): 963-982.
[13] SHUCK C E, SARYCHEVA A, ANAYEE M, LEVITT A, ZHU Y, UZUN S, BALITSKIY V, ZAHORODNA V, GOGOTSI O, GOGOTSI Y. Adv. Eng. Mater. , 2020, 22(3): 1901241.
[14] GEIM A K, NOVOSELOV K S. Nat. Mater. , 2007, 6(3): 183-191.
[15] HALIM J, LUKATSKAYA M R, COOK K M, LU J, SMITH C R, N?SLUND L ?, MAY S J, HULTMAN L, GOGOTSI Y,EKLUND P, BARSOUM M W. Chem. Mater. , 2014, 26(7): 2374-2381.
[16] BAO H, QIU Y, PENG X, WANG J, MI Y, ZHAO S, LIU X, LIU Y, CAO R, ZHUO L, REN J, SUN J, LUO J, SUN X. Nat.Commun. , 2021, 12(1): 238.
[17] DING H M, LI Y B, LI M, CHEN K, LIANG K, CHEN G X, LU J, PALISAITIS J, PERSSON P O ?, EKLUND P,HULTMAN L, DU S Y, CHAI Z F, GOGOTSI Y, HUANG Q J. Science, 2023, 379(6637): 1130-1135.
[18] HO D H, CHOI Y Y, JO S B, MYOUNG J M, CHO J H. Adv. Mater. , 2021, 33(47): 2005846.
[19] GONG Y J, YUAN H T, WU C L, TANG P Z, YANG S Z, YANG A K, LI G D, LIU B F, VAN DE GROEP J,BRONGERSMA M L, CHISHOLM M F, ZHANG S C, ZHOU W, CUI Y. Nat. Nanotechnol. , 2018, 13(4): 294-299.
[20] LIU R, WANG C, LI Y, XIE Y, CHEN Q, CHEN Z, LIU Q. RSC Adv. , 2017, 7(74): 46699-46703.
[21] MOTTER J P, KOSKI K J, CUI Y. Chem. Mater. , 2014, 26(7): 2313-2317.
[22] MUHAMMAD Z, MU K, LV H, WU C, UR REHMAN Z, HABIB M, SUN Z, WU X, SONG L. Nano Res. , 2018, 11(9):4914-4922.
[23] ABBASI-KESBI F, RASHIDI A M, ASTINCHAP B. Appl. Nanosci. , 2018, 8(3): 221-230.
[24] LI T, YAO L, LIU Q, GU J, LUO R, LI J, YAN X, WANG W, LIU P, CHEN B, ZHANG W, ABBAS W, NAZ R, ZHANG D.Angew. Chem. Int. Ed. , 2018, 57(21): 6115-6119.
[25] CHENG G, WALKER A R H. Anal. Bioanal. Chem. , 2010, 396(3): 1057-1069.
[26] JIA Z, LI Z, MA S, ZHANG W, CHEN Y, LUO Y, JIA D, ZHONG B, RAZAL J M, WANG X, KONG L. J. Colloid Interface Sci. , 2021, 584: 1-10.
[27] HOU T Q, WANG B B, MA M L, FENG A L, HUANG Z Y, ZHANG Y, JIA Z, TAN G X, CAO H J, WU G L. Composites,Part B, 2020, 180: 107577.
[28] LU Y, LI D, LIU F. Materials, 2022, 15(1): 307.
[29] YANG Y, HE A, LI H, ZOU Q, LIU Z, TAO C, DU J. ACS Catal. , 2022, 12(20): 12942-12953.
[30] YAO Y, JIN Z, CHEN Y, GAO Z, YAN J, LIU H, WANG J, LI Y, LIU S F. Carbon, 2018, 129: 228-235.
國家自然科學基金項目(Nos. 22265025, 12164037)、寧夏自然科學基金項目(No. 2021AAC05013)和六盤山資源工程技術研究中心項目(No. HGZD22-14)資助。
支持信息
Cu0 /Cu2+修飾Ti3C2Tx 二維材料用于電催化二氧化碳
劉楚存 王亞麗 崔慧娜 姚垚
S1 產物分析
使用Agilent Technoloies 7890A 作為氣相色譜檢測器,通過熱導檢測器(TCD)和氫火焰離子化檢測器(FID)兩種檢測器檢測氣體產物,氣體產物在常溫常壓下直接引入氣相色譜儀在線分析,載氣為高純氬氣。在電解測試前,電解液用高純CO2 (99.99%)鼓泡30 分鐘(PH=7.4),CO2氣體的流速為15 sccm,每次分析取樣1 mL 用于色譜分析。H2 和C2H4 的法拉第效率根據以下公式計算:
FE=(S-1.19893)/7334.4067×μ×(t/60)×10-3/24.01×2×96485/Q
其中,S 為峰面積;μ 為氣體CO2 的流速;t 為電解時間,Q 為電解的庫倫數。
圖1A 所示Cu0/Cu2+-Ti3C2Tx-7.5 的氣相產物以C2H4 為主,通過法拉第效率(FE)計算公式得到,在-1.3 V 電位下,FEC2H4=0.16%,隨著電位的增加,析氫反應逐漸增強。

